文档内容
专练 40 水的电离、溶液的酸碱性及 pH 计算
1.[2022·浙江卷1月]已知25 ℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下
2 a1 a2
列说法正确的是( )
A.在等浓度的NaA、NaHA溶液中,水的电离程度前者小于后者
2
B.向0.1 mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA
2 2
的电离度为0.013%
C.向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D.取pH=a的HA溶液10 mL,加蒸馏水稀释至100 mL,则该溶液pH=a+1
2
2.[2021·浙江卷6月]某同学拟用pH计测定溶液pH以探究某酸HR是否为弱电解质。
下列说法正确的是( )
A.25 ℃时,若测得0.01 mol·L-1 NaR溶液pH=7,则HR是弱酸
B.25 ℃时,若测得0.01 mol·L-1 HR溶液pH>2且pH<7,则HR是弱酸
C.25 ℃时,若测得HR溶液pH=a,取该溶液10.0 mL,加蒸馏水稀释至100.0 mL,
测得pH=b,b-ab,则HR是弱酸
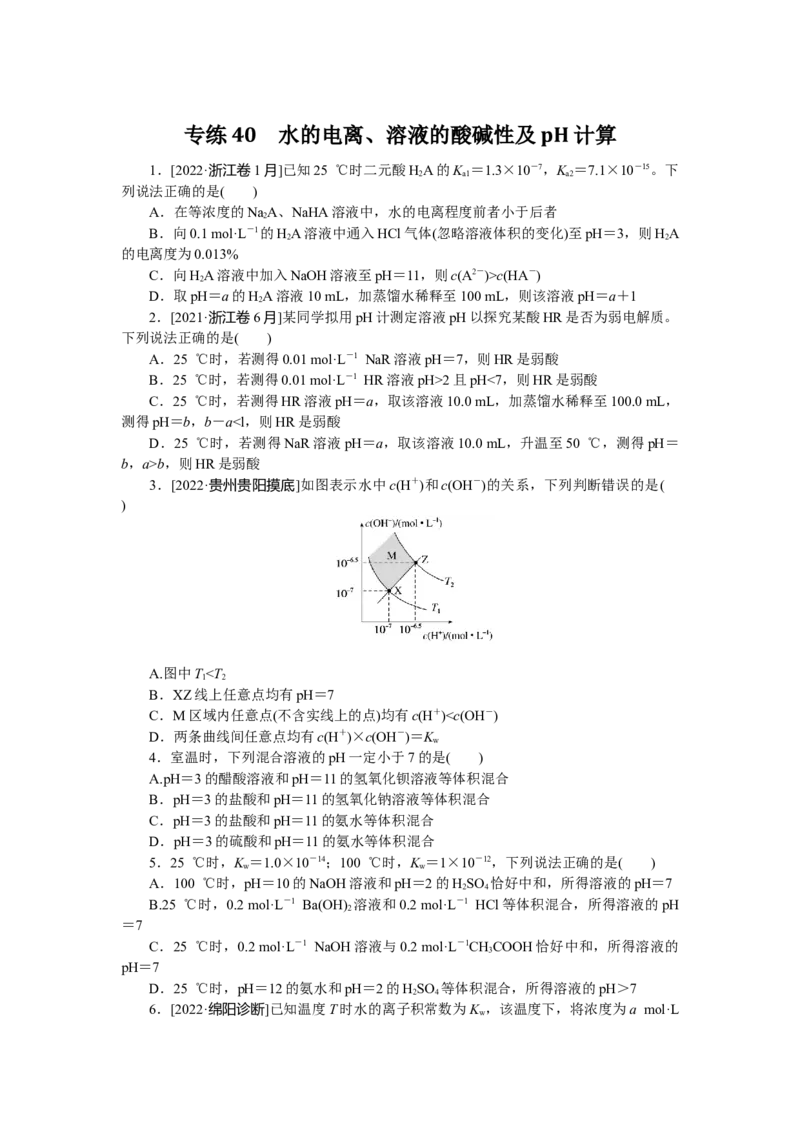
3.[2022·贵州贵阳摸底]如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是(
)
A.图中TT
1 2
B.T 温度时,将pH=10的NaOH溶液与pH=3的HSO 溶液混合,若混合溶液呈中
2 2 4
性,则NaOH溶液与HSO 溶液的体积比为1∶10
2 4
C.b点到c点可以通过温度不变,在水中加入适量的CHCOONa
3
D.图中五个点的K 的关系为b>c>a>d=e
w
10.[2022·牡丹江一中月考]下表是不同温度下水的离子积数据:
温度/℃ 25 t t
1 2
水的离子积(mol2·L-2) 1×10-14 a 1×10-12
试回答以下问题:
(1)若25<t<t,则a________1×10-14(填“>”“<”或“=”)。
1 2(2)25 ℃下,某NaSO 溶液中c(SO)=5×10-4 mol·L-1,取该溶液1 mL加水稀释至10
2 4
mL,则稀释后溶液中c(Na+)∶c(OH-)=________。
(3)在t ℃下,pH=2的稀硫酸溶液中,水电离产生的H+浓度为c(H+) =________。
2 水
(4)t ℃下,将pH=11的苛性钠溶液V L与pH=1的稀硫酸V L(混合体积为原两溶
2 1 2
液体积之和),所得混合溶液的pH=2,则V∶V=________。
1 2
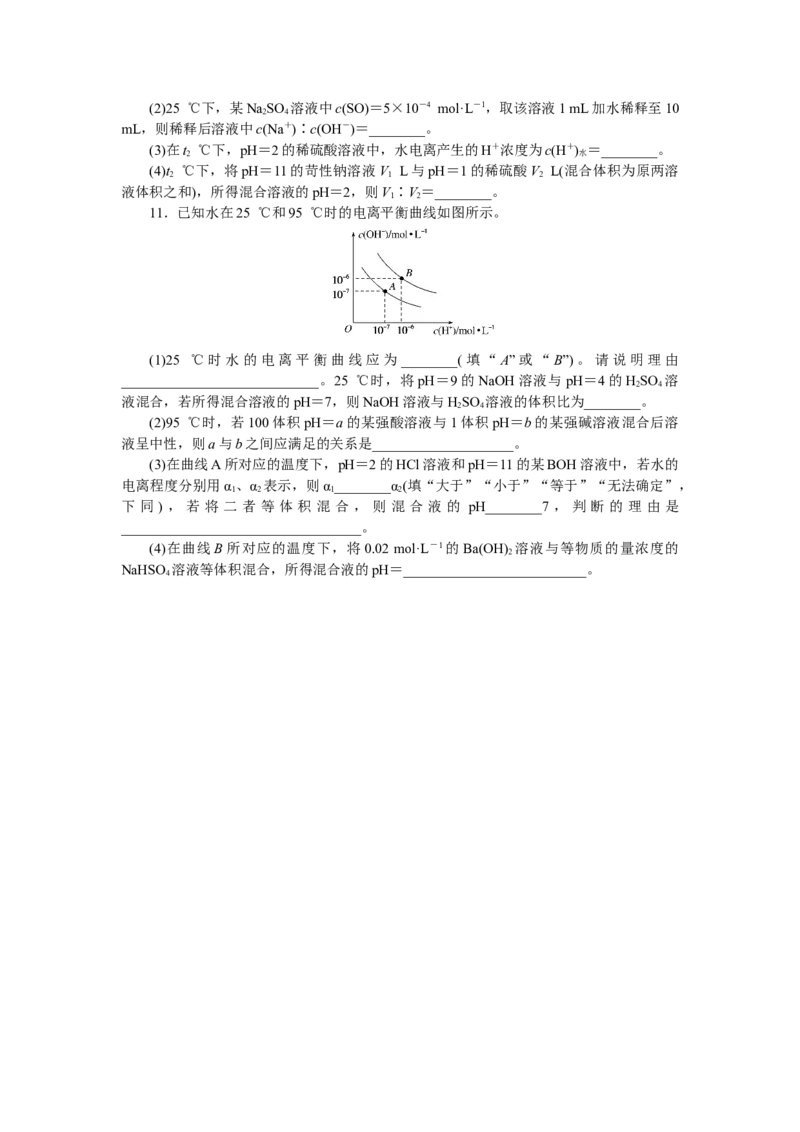
11.已知水在25 ℃和95 ℃时的电离平衡曲线如图所示。
(1)25 ℃时水的电离平衡曲线应为________(填“A”或“B”)。请说明理由
____________________________。25 ℃时,将pH=9的NaOH溶液与pH=4的HSO 溶
2 4
液混合,若所得混合溶液的pH=7,则NaOH溶液与HSO 溶液的体积比为________。
2 4
(2)95 ℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶
液呈中性,则a与b之间应满足的关系是____________________。
(3)在曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的
电离程度分别用α 、α 表示,则α ________α (填“大于”“小于”“等于”“无法确定”,
1 2 1 2
下 同 ) , 若 将 二 者 等 体 积 混 合 , 则 混 合 液 的 pH________7 , 判 断 的 理 由 是
__________________________________。
(4)在曲线B所对应的温度下,将0.02 mol·L-1的Ba(OH) 溶液与等物质的量浓度的
2
NaHSO 溶液等体积混合,所得混合液的pH=__________________________。
4