文档内容
专练 40 水的电离、溶液的酸碱性及 pH 计算
一、单项选择题
1.[2022·全国乙卷]常温下,一元酸HA的K(HA)=1.0×10-3。在某体系中,H+与A-
a
离子不能穿过隔膜,未电离的HA可自由穿过该膜(如图所示)。
设溶液中c (HA)=c(HA)+c(A-),当达到平衡时,下列叙述正确的是 ( )
总
A.溶液Ⅰ中c(H+)=c(OH-)+c(A-)
B.溶液Ⅱ中HA的电离度[]为
C.溶液Ⅰ和Ⅱ中的c(HA)不相等
D.溶液Ⅰ和Ⅱ中的c (HA)之比为10-4
总
2.[2022·辽宁沈阳二中阶段检测]下列滴定反应中,指示剂使用正确的是( )
A.用HO 溶液滴定KI溶液,淀粉作指示剂
2 2
B.用酸性KMnO 标准溶液滴定NaHSO 溶液以测量其浓度,用甲基橙作指示剂
4 3
C.用标准FeCl 溶液滴定KI溶液,用KSCN溶液作指示剂
3
D.用强酸标准溶液滴定并测量某弱碱溶液浓度,用酚酞作指示剂
3.[2022·贵州贵阳摸底]如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是(
)
A.图中THClO
4 2
B.当稀释至pH均为3时,溶液中c(ClO)>c(MnO)
C.在0≤pH≤5时,HMnO 溶液满足pH=lg
4
D.常温下,浓度均为0.1 mol·L-1的NaClO 和NaMnO 溶液的pH:NaMnO >NaClO
2 4 4 2
7.[2022·试题调研]一定温度下,下列溶液的离子浓度关系式正确的是( )
A.pH=5的HS溶液中,c(H+)=c(HS-)=1×10-5 mol·L-1
2
B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C.pH=2的HC O 溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=
2 2 4
c(OH-)+c(HC O)
2
D.pH相同的①CHCOONa ②NaHCO ③NaClO三种溶液的c(Na+):①>②>③
3 3
8.[2022·绵阳诊断]已知温度T时水的离子积常数为K ,该温度下,将浓度为a mol·L
w
-1的一元酸HA与b mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是(
)
A.a=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)= mol·L-1
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
二、不定项选择题
9.[2021·浙江1月]实验测得 10 mL 0.50 mol·L-1 NH Cl溶液、10 mL 0.50 mol·L-1
4
CHCOONa溶液的pH分别随温度与稀释加水量的变化如图所示。已知 25 ℃时CHCOOH
3 3
和NH ·H O的电离常数均为1.8×10-5。下列说法不正确的是 ( )
3 2A.图中实线表示pH随加水量的变化,虚线表示pH随温度的变化
B.将NH Cl溶液加水稀释至浓度为 mol·L-1,溶液pH变化值小于lg x
4
C.随温度升高,K 增大,CHCOONa溶液中c(OH-)减小,c(H+)增大,pH减小
w 3
D.25 ℃时稀释相同倍数的NH Cl溶液与CHCOONa溶液中:c(Na+)-c(CHCOO-)
4 3 3
=c(Cl-)-c(NH)
10.[综合创新]室温下,在实验室中用 0.1 mol·L-1的盐酸滴定10 mL 0.1 mol·L-1的
ROH溶液,滴定曲线如图所示。下列有关叙述错误的是( )
A.K (ROH)的数量级为10-5
b
B.点②对应溶液中:c(R+)+2c(H+)=c(ROH)+2c(OH-)
C.水的电离程度:①<③<④
D.滴加盐酸的过程中保持不变
11.[2022·南阳联考]常温下,向20 mL 0.1 mol·L-1氨水中滴加盐酸,溶液中由水电离
的氢离子浓度随加入盐酸体积的变化如图所示。则下列说法正确的是( )
A.b、d两点为恰好完全反应点
B.c点溶液中c(NH)=c(Cl-)
C.a、b之间的任意一点:c(Cl-)>c(NH),c(H+)>c(OH-)
D.常温下,0.1 mol·L-1氨水的电离常数K 约为1×10-5
a
12.[2022·哈尔滨师大青冈实验中学月考]某温度下K =10-13,在此温度下,将pH=a
w
的NaOH溶液V L与pH=b的HSO 溶液V L混合,下列说法正确的是( )
a 2 4 bA.若所得混合液为中性,且a=12,b=2,则V∶V=1∶10
a b
B.若所得混合液为中性,且a+b=12,则V∶V=100∶1
a b
C.若所得混合液pH=10,且a=12,b=2,则V∶V=1∶9
a b
D.若所得混合液pH=10,且a=12,b=2,则V∶V=101∶99
a b
三、非选择题
13.已知某温度下CHCOOH的电离常数K=1.6×10-5。该温度下,向20 mL 0.01
3
mol·L-1 CHCOOH溶液中逐滴加入0.01 mol·L-1 KOH溶液,其pH变化曲线如图所示(忽
3
略温度变化)。请回答下列有关问题:(已知lg 4=0.6)
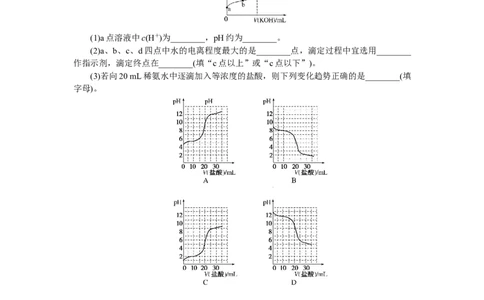
(1)a点溶液中c(H+)为________,pH约为________。
(2)a、b、c、d四点中水的电离程度最大的是________点,滴定过程中宜选用________
作指示剂,滴定终点在________(填“c点以上”或“c点以下”)。
(3)若向20 mL稀氨水中逐滴加入等浓度的盐酸,则下列变化趋势正确的是________(填
字母)。
14.已知水在25 ℃和95 ℃时的电离平衡曲线如图所示。
(1)25 ℃时水的电离平衡曲线应为________(填“A”或“B”)。请说明理由
____________________________________。25 ℃时,将pH=9的NaOH溶液与pH=4的
HSO 溶液混合,若所得混合溶液的 pH=7,则 NaOH 溶液与 HSO 溶液的体积比为
2 4 2 4________。
(2)95 ℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶
液呈中性,则a与b之间应满足的关系是________。
(3)在曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的
电离程度分别用α 、α 表示,则α ________α (填“大于”“小于”“等于”或“无法确
1 2 1 2
定”,下同),若将二者等体积混合,则混合液的 pH________7,判断的理由是
________________________________________________________________________
________________________________________________________________________。
(4)在曲线B所对应的温度下,将0.02 mol·L-1的Ba(OH) 溶液与等物质的量浓度的
2
NaHSO 溶液等体积混合,所得混合液的pH=________。
4