文档内容
专练 57 结构与性质综合应用
1.[2022·全国乙卷]卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答
下列问题:
(1)氟原子激发态的电子排布式有 ,其中能量较高的是 。(填标
号)
a.1s22s22p43s1 b.1s22s22p43d2
c.1s22s12p5 d.1s22s22p33p2
(2)①一氯乙烯(C HCl)分子中,C的一个 杂化轨道与Cl的3p 轨道形成C
2 3 x
—Cl 键,并且Cl的3p 轨道与C的2p 轨道形成3中心4电子的大π键( )。
z z Π4
3
②一氯乙烷(C HCl)、一氯乙烯(C HCl)、一氯乙炔(C HCl)分子中,C—Cl键
2 5 2 3 2
长的顺序是 ,理由:(ⅰ)C的杂化轨道中s成分越多,形
成 的 C—Cl 键 越 强 ; ( ⅱ )
。
(3)卤化物CsICl 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为
2
。 解 释 X 的 熔 点 比 Y 高 的 原 因 _________________________________________
_______________________________________________________________________________。
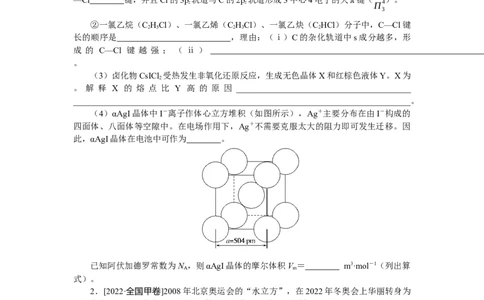
(4)αAgI晶体中I-离子作体心立方堆积(如图所示),Ag+主要分布在由I-构成的
四面体、八面体等空隙中。在电场作用下,Ag+不需要克服太大的阻力即可发生迁移。因
此,αAgI晶体在电池中可作为 。
已知阿伏加德罗常数为N ,则αAgI晶体的摩尔体积V = m3·mol-1(列出算
A m
式)。
2.[2022·全国甲卷]2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为
“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH===CH )与
2 2
四氟乙烯(CF===CF )的共聚物(ETFE)制成。回答下列问题:
2 2
(1)基态F原子的价电子排布图(轨道表示式)为 。
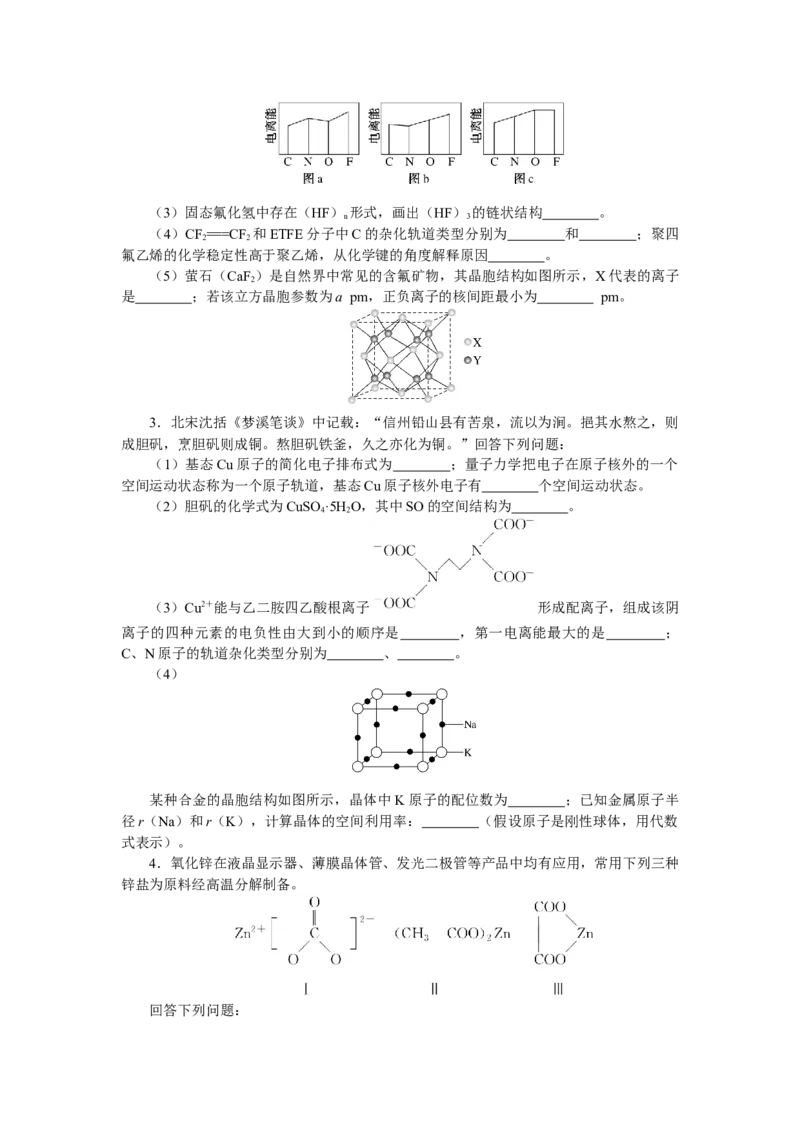
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不
同 ) 。 第 一 电 离 能 的 变 化 图 是 ( 填 标 号 ) , 判 断 的 根 据 是
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________;
第三电离能的变化图是 (填标号)。(3)固态氟化氢中存在(HF) 形式,画出(HF) 的链状结构 。
n 3
(4)CF===CF 和ETFE分子中C的杂化轨道类型分别为 和 ;聚四
2 2
氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因 。
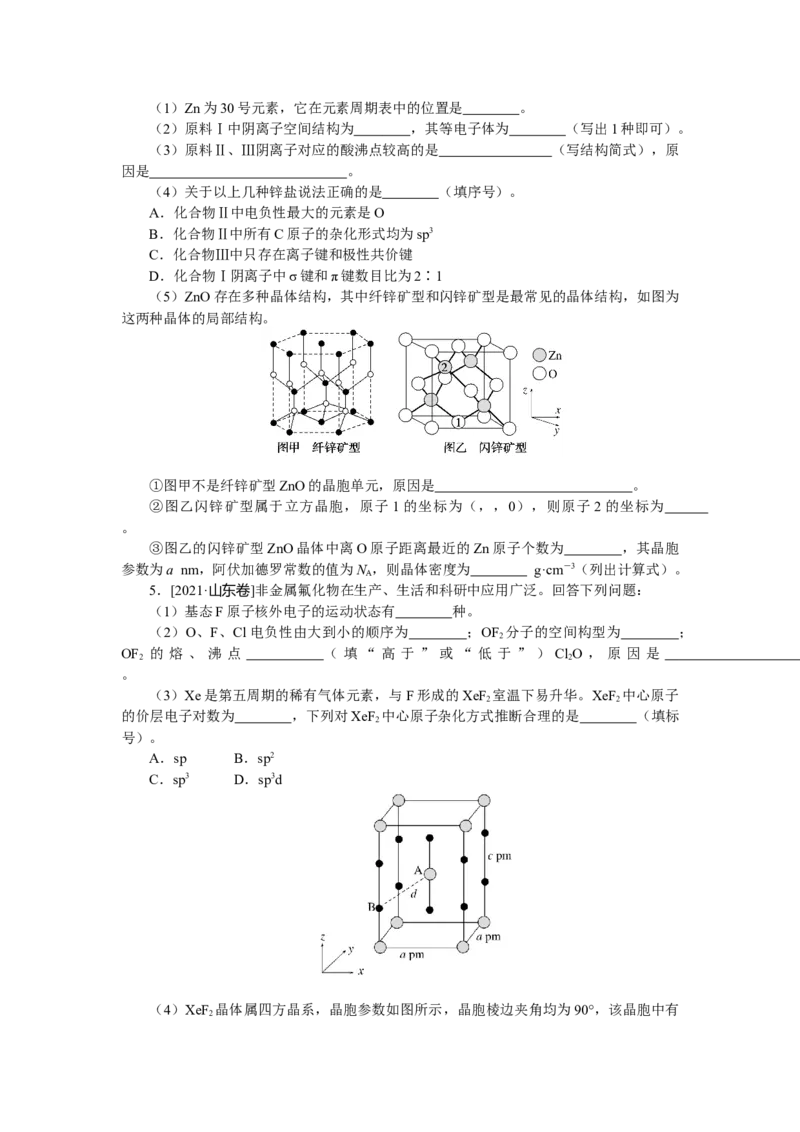
(5)萤石(CaF )是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子
2
是 ;若该立方晶胞参数为a pm,正负离子的核间距最小为 pm。
3.北宋沈括《梦溪笔谈》中记载:“信州铅山县有苦泉,流以为涧。挹其水熬之,则
成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之亦化为铜。”回答下列问题:
(1)基态Cu原子的简化电子排布式为 ;量子力学把电子在原子核外的一个
空间运动状态称为一个原子轨道,基态Cu原子核外电子有 个空间运动状态。
(2)胆矾的化学式为CuSO ·5H O,其中SO的空间结构为 。
4 2
(3)Cu2+能与乙二胺四乙酸根离子 形成配离子,组成该阴
离子的四种元素的电负性由大到小的顺序是 ,第一电离能最大的是 ;
C、N原子的轨道杂化类型分别为 、 。
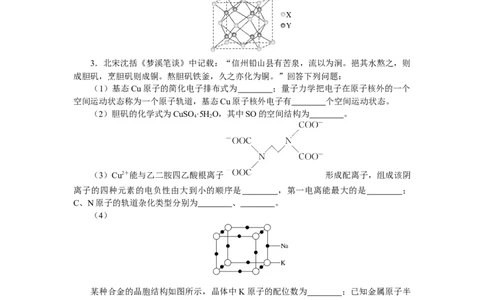
(4)
某种合金的晶胞结构如图所示,晶体中K原子的配位数为 ;已知金属原子半
径r(Na)和r(K),计算晶体的空间利用率: (假设原子是刚性球体,用代数
式表示)。
4.氧化锌在液晶显示器、薄膜晶体管、发光二极管等产品中均有应用,常用下列三种
锌盐为原料经高温分解制备。
回答下列问题:(1)Zn为30号元素,它在元素周期表中的位置是 。
(2)原料Ⅰ中阴离子空间结构为 ,其等电子体为 (写出1种即可)。
(3)原料Ⅱ、Ⅲ阴离子对应的酸沸点较高的是 (写结构简式),原
因是 。
(4)关于以上几种锌盐说法正确的是 (填序号)。
A.化合物Ⅱ中电负性最大的元素是O
B.化合物Ⅱ中所有C原子的杂化形式均为sp3
C.化合物Ⅲ中只存在离子键和极性共价键
D.化合物Ⅰ阴离子中σ键和π键数目比为2∶1
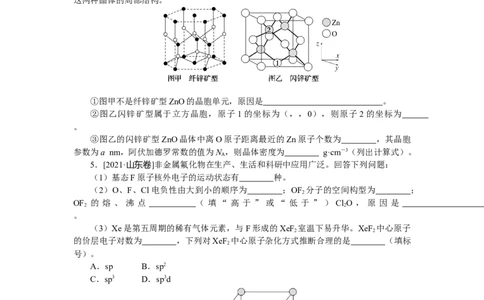
(5)ZnO存在多种晶体结构,其中纤锌矿型和闪锌矿型是最常见的晶体结构,如图为
这两种晶体的局部结构。
①图甲不是纤锌矿型ZnO的晶胞单元,原因是 。
②图乙闪锌矿型属于立方晶胞,原子 1的坐标为(,,0),则原子2的坐标为
。
③图乙的闪锌矿型ZnO晶体中离O原子距离最近的Zn原子个数为 ,其晶胞
参数为a nm,阿伏加德罗常数的值为N ,则晶体密度为 g·cm-3(列出计算式)。
A
5.[2021·山东卷]非金属氟化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态F原子核外电子的运动状态有 种。
(2)O、F、Cl电负性由大到小的顺序为 ;OF 分子的空间构型为 ;
2
OF 的 熔 、 沸 点 ( 填 “ 高 于 ” 或 “ 低 于 ” ) ClO , 原 因 是
2 2
。
(3)Xe是第五周期的稀有气体元素,与F形成的XeF 室温下易升华。XeF 中心原子
2 2
的价层电子对数为 ,下列对XeF 中心原子杂化方式推断合理的是 (填标
2
号)。
A.sp B.sp2
C.sp3 D.sp3d
(4)XeF 晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有
2个XeF 分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原
2
子的分数坐标,如A点原子的分数坐标为(,,)。已知Xe—F键长为r pm,则B点原
子的分数坐标为 ;晶胞中A、B间距离d= pm。