文档内容
专练 57 结构与性质综合应用
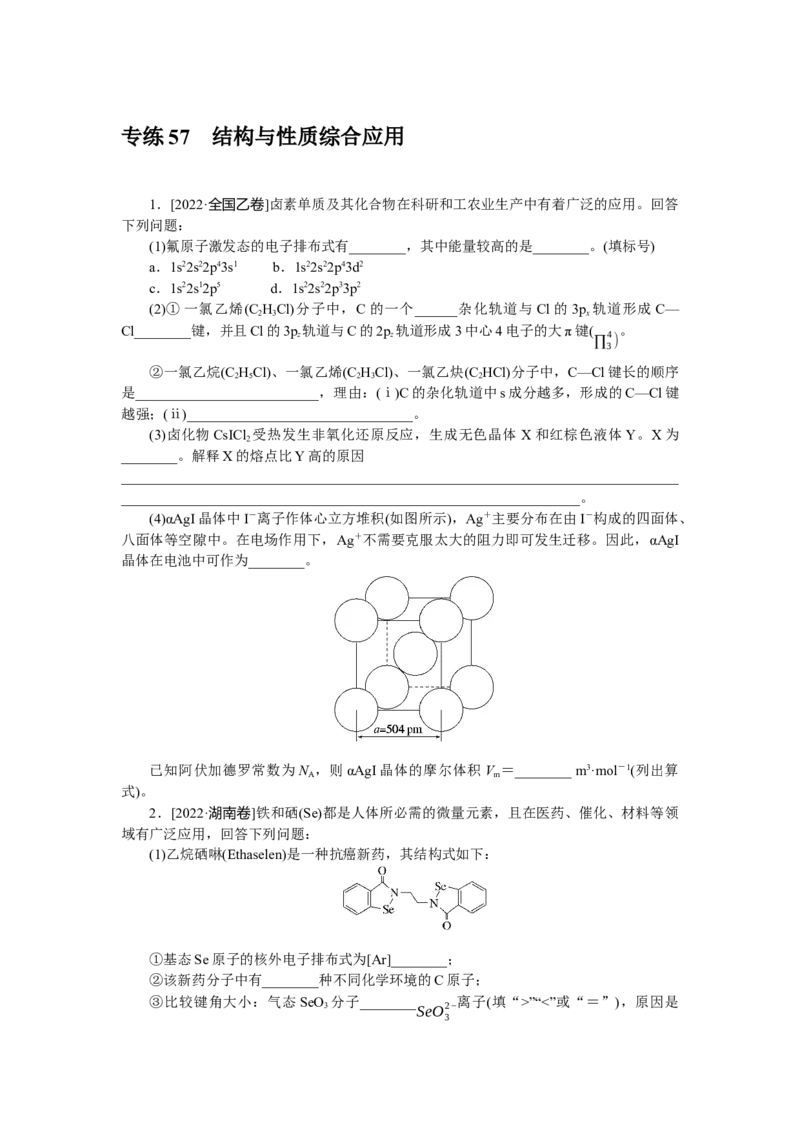
1.[2022·全国乙卷]卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答
下列问题:
(1)氟原子激发态的电子排布式有________,其中能量较高的是________。(填标号)
a.1s22s22p43s1 b.1s22s22p43d2
c.1s22s12p5 d.1s22s22p33p2
(2)①一氯乙烯(C HCl)分子中,C的一个______杂化轨道与 Cl的3p 轨道形成C—
2 3 x
Cl________键,并且Cl的3p 轨道与C的2p 轨道形成3中心4电子的大π键( 。
z z ∏4 )
3
②一氯乙烷(C HCl)、一氯乙烯(C HCl)、一氯乙炔(C HCl)分子中,C—Cl键长的顺序
2 5 2 3 2
是__________________________,理由:(ⅰ)C的杂化轨道中s成分越多,形成的C—Cl键
越强;(ⅱ)________________________________。
(3)卤化物CsICl 受热发生非氧化还原反应,生成无色晶体 X和红棕色液体Y。X为
2
________。解释X的熔点比Y高的原因
_______________________________________________________________________________
_________________________________________________________________。
(4)αAgI晶体中I-离子作体心立方堆积(如图所示),Ag+主要分布在由I-构成的四面体、
八面体等空隙中。在电场作用下,Ag+不需要克服太大的阻力即可发生迁移。因此,αAgI
晶体在电池中可作为________。
已知阿伏加德罗常数为N ,则αAgI晶体的摩尔体积V =________ m3·mol-1(列出算
A m
式)。
2.[2022·湖南卷]铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料等领
域有广泛应用,回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:
①基态Se原子的核外电子排布式为[Ar]________;
②该新药分子中有________种不同化学环境的C原子;
③比较键角大小:气态SeO 分子________ 离子(填“>”“<”或“=”),原因是
3 SeO2−
3____________________________________。
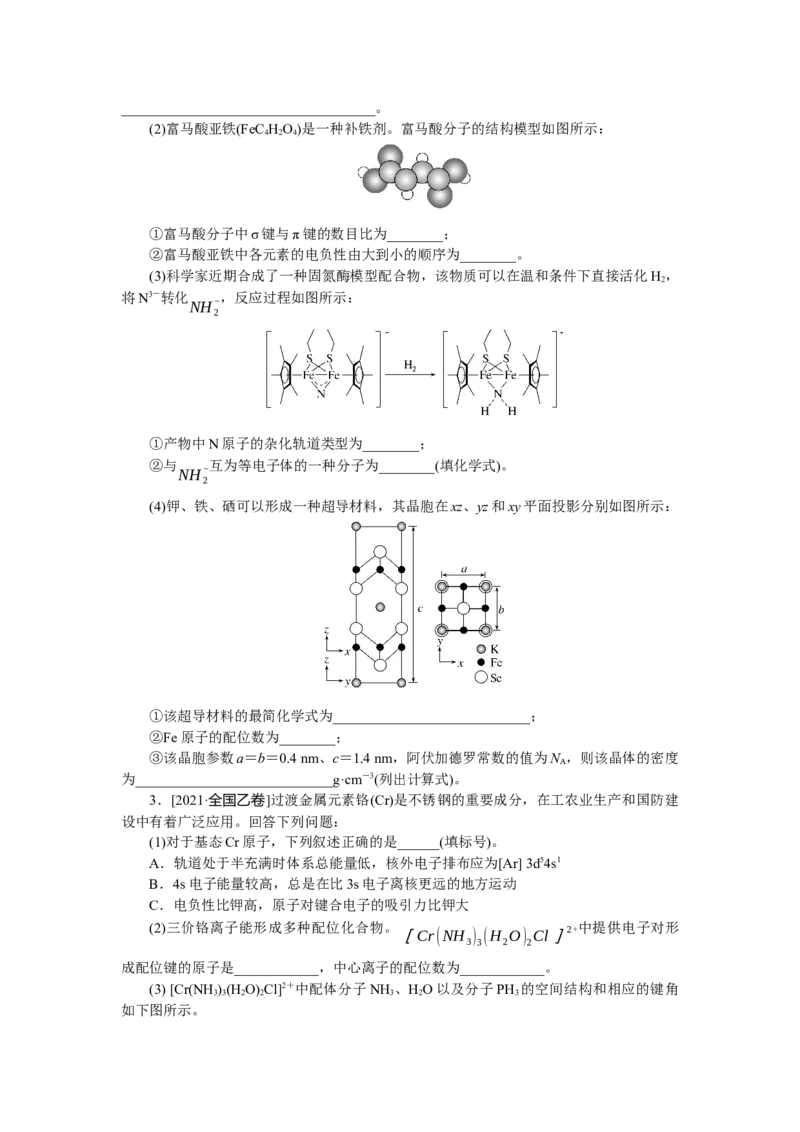
(2)富马酸亚铁(FeC HO)是一种补铁剂。富马酸分子的结构模型如图所示:
4 2 4
①富马酸分子中σ键与π键的数目比为________;
②富马酸亚铁中各元素的电负性由大到小的顺序为________。
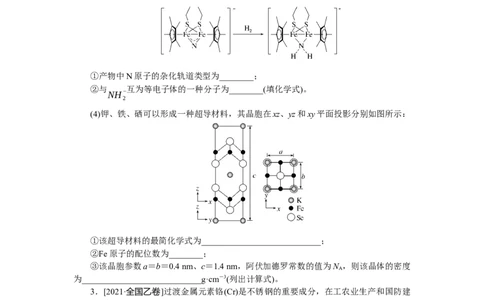
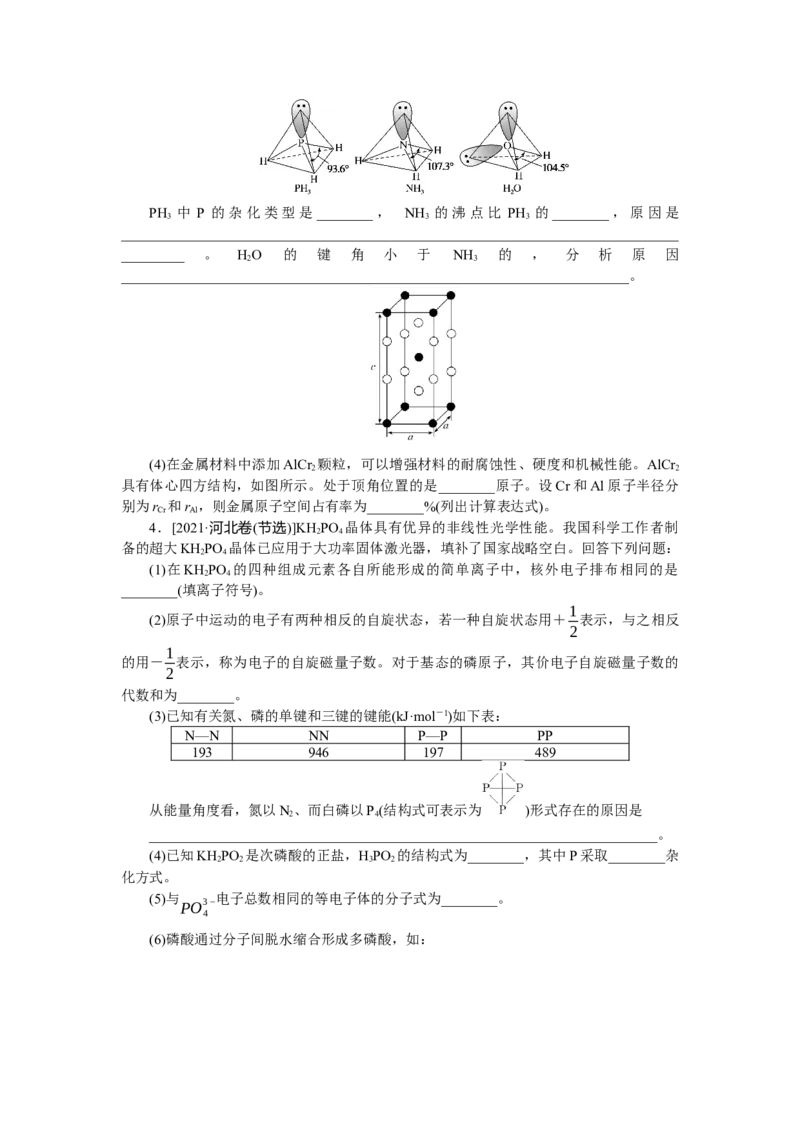
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H ,
2
将N3-转化 ,反应过程如图所示:
NH−
2
①产物中N原子的杂化轨道类型为________;
②与 互为等电子体的一种分子为________(填化学式)。
NH−
2
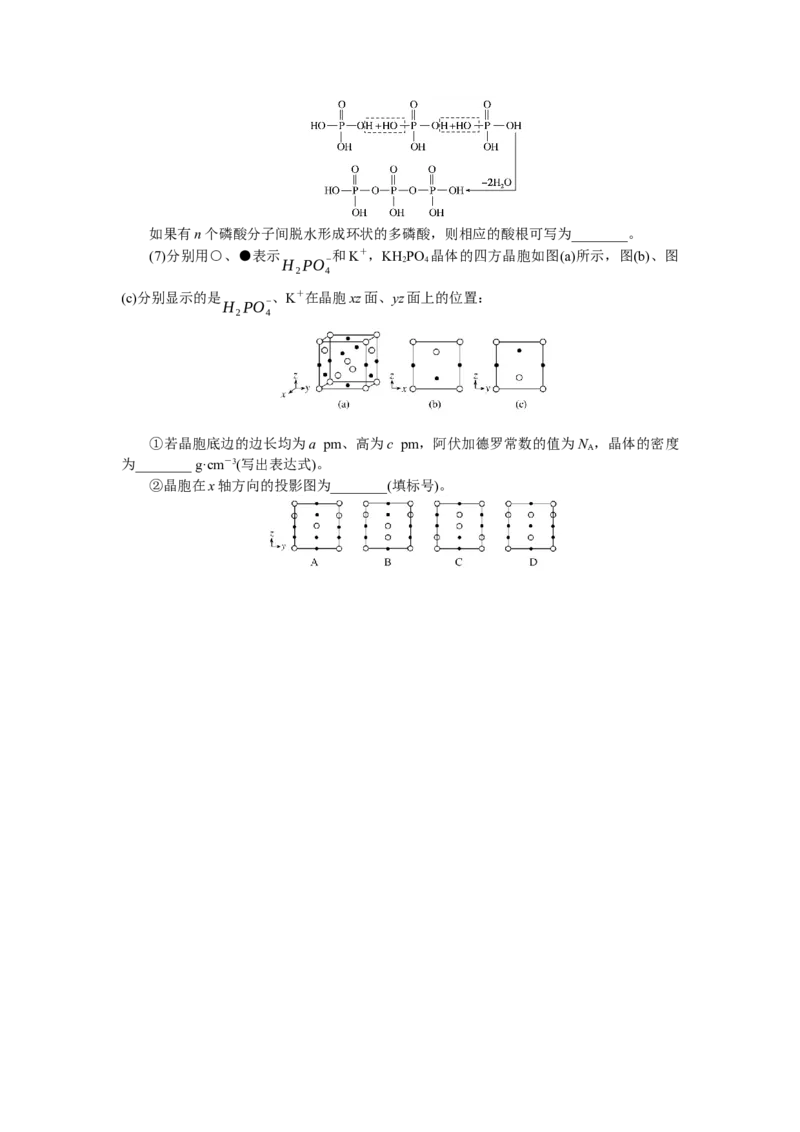
(4)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:
①该超导材料的最简化学式为____________________________;
②Fe原子的配位数为________;
③该晶胞参数a=b=0.4 nm、c=1.4 nm,阿伏加德罗常数的值为N ,则该晶体的密度
A
为____________________________g·cm-3(列出计算式)。
3.[2021·全国乙卷]过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建
设中有着广泛应用。回答下列问题:
(1)对于基态Cr原子,下列叙述正确的是______(填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar] 3d54s1
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。
[Cr(NH ) (H O) Cl]
2+中提供电子对形
3 3 2 2
成配位键的原子是____________,中心离子的配位数为____________。
(3) [Cr(NH )(H O) Cl]2+中配体分子NH 、HO以及分子PH 的空间结构和相应的键角
3 3 2 2 3 2 3
如下图所示。PH 中 P 的杂化类型是________, NH 的沸点比 PH 的________,原因是
3 3 3
_______________________________________________________________________________
_________ 。 HO 的 键 角 小 于 NH 的 , 分 析 原 因
2 3
________________________________________________________________________。
(4)在金属材料中添加AlCr 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr
2 2
具有体心四方结构,如图所示。处于顶角位置的是________原子。设Cr和Al原子半径分
别为r 和r ,则金属原子空间占有率为________%(列出计算表达式)。
Cr Al
4.[2021·河北卷(节选)]KH PO 晶体具有优异的非线性光学性能。我国科学工作者制
2 4
备的超大KH PO 晶体已应用于大功率固体激光器,填补了国家战略空白。回答下列问题:
2 4
(1)在KH PO 的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是
2 4
________(填离子符号)。
1
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反
2
1
的用- 表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的
2
代数和为________。
(3)已知有关氮、磷的单键和三键的键能(kJ·mol-1)如下表:
N—N NN P—P PP
193 946 197 489
从能量角度看,氮以N、而白磷以P(结构式可表示为 )形式存在的原因是
2 4
________________________________________________________________________。
(4)已知KH PO 是次磷酸的正盐,HPO 的结构式为________,其中P采取________杂
2 2 3 2
化方式。
(5)与 电子总数相同的等电子体的分子式为________。
PO3−
4
(6)磷酸通过分子间脱水缩合形成多磷酸,如:如果有n个磷酸分子间脱水形成环状的多磷酸,则相应的酸根可写为________。
(7)分别用○、●表示 和K+,KH PO 晶体的四方晶胞如图(a)所示,图(b)、图
H PO− 2 4
2 4
(c)分别显示的是 、K+在晶胞xz面、yz面上的位置:
H PO−
2 4
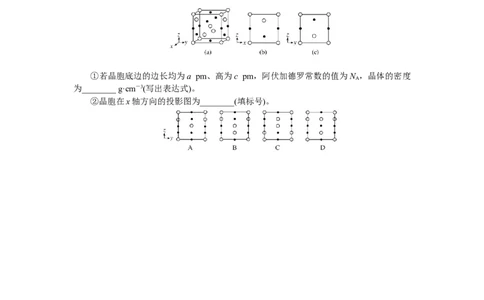
①若晶胞底边的边长均为a pm、高为c pm,阿伏加德罗常数的值为N ,晶体的密度
A
为________ g·cm-3(写出表达式)。
②晶胞在x轴方向的投影图为________(填标号)。