文档内容
第 24 讲 原电池的工作原理
知识导航
小杨老师 15521324728 侵权必究
知识精讲
小杨老师 15521324728 侵权必究
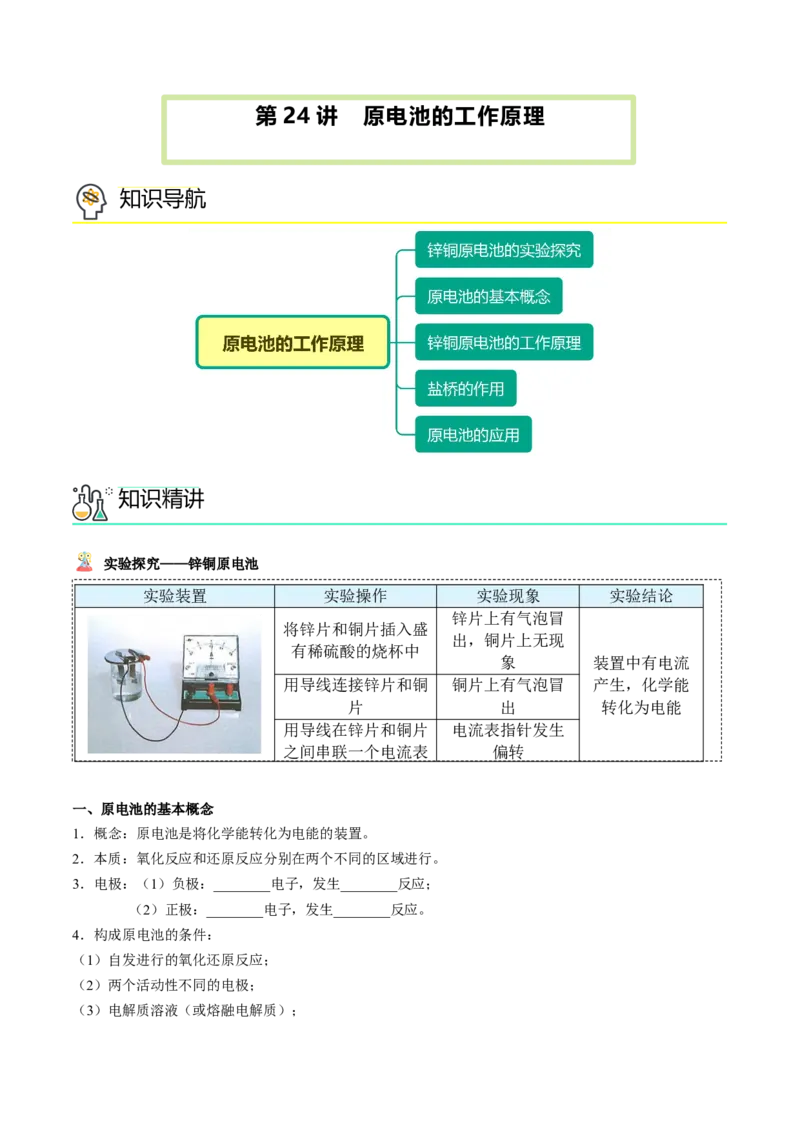
实验探究——锌铜原电池
实验装置 实验操作 实验现象 实验结论
锌片上有气泡冒
将锌片和铜片插入盛
出,铜片上无现
有稀硫酸的烧杯中
象 装置中有电流
用导线连接锌片和铜 铜片上有气泡冒 产生,化学能
片 出 转化为电能
用导线在锌片和铜片 电流表指针发生
之间串联一个电流表 偏转
一、原电池的基本概念
1.概念:原电池是将化学能转化为电能的装置。
杨sir化学,侵权必究
2.本质:氧化反应和还原反应分别在两个不同的区域进行。
3.电极:(1)负极:________电子,发生________反应;
(2)正极:________电子,发生________反应。
4.构成原电池的条件:
(1)自发进行的氧化还原反应;
(2)两个活动性不同的电极;
(3)电解质溶液(或熔融电解质);(4)形成闭合回路。
二、锌铜原电池的工作原理
杨sir化学,侵权必究
负 极
(Zn)
工作原理 正 极
(反应方程式) (Cu)
总 反 应 离 子 方 程 式 :
。
电子移动方向 由 极经导线流向 极(电流方向相反)。
离子移动方向 阳离子向 极移动,阴离子向 极移动。
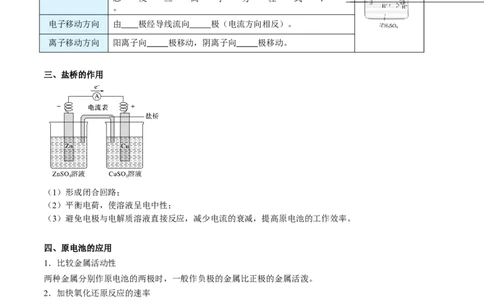
三、盐桥的作用
(1)形成闭合回路;
(2)平衡电荷,使溶液呈电中性;
(3)避免电极与电解质溶液直接反应,减少电流的衰减,提高原电池的工作效率。
杨sir化学,侵权必究
四、原电池的应用
1.比较金属活动性
两种金属分别作原电池的两极时,一般作负极的金属比正极的金属活泼。
杨sir化学,侵权必究
2.加快氧化还原反应的速率
一个氧化还原反应,构成原电池时的反应速率比直接接触的反应速率快。
3.设计原电池
理论上,任何一个自发的氧化还原反应,都可以设计成原电池。利用原电池原理设计和制造原电池,可以
将化学能直接转化为电能。
杨sir化学,侵权必究
对点训练
小杨老师 15521324728 侵权必究
题型一:原电池的工作原理
杨sir化学,侵权必究【例1】由U形管、质量为 的铁棒、质量为 的碳棒和 溶液组成的装置如图所示,
下列说法正确的是
A.闭合K,电子通过电解质溶液移到碳棒上
B.闭合K,铁棒上有紫红色固体析出
C.闭合K,当电路中有 个电子通过时,理论上碳棒与铁棒的质量差为
D.闭合K,铁棒表面发生的电极反应为
【变1-2】如图所示是 和 形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下。则
卡片上的描述合理的是
2021.6.18,实验后的记录:
① 为正极, 为负极
② 极上有气泡产生,发生还原反应
③ 向 极移动
④若有0.5 电子流经导线,则可产生0.25 气体
⑤电子的流向是:
⑥正极反应式: ,发生氧化反应
A.①②④ B.②④ C.②③④ D.③④⑤
杨sir化学,侵权必究
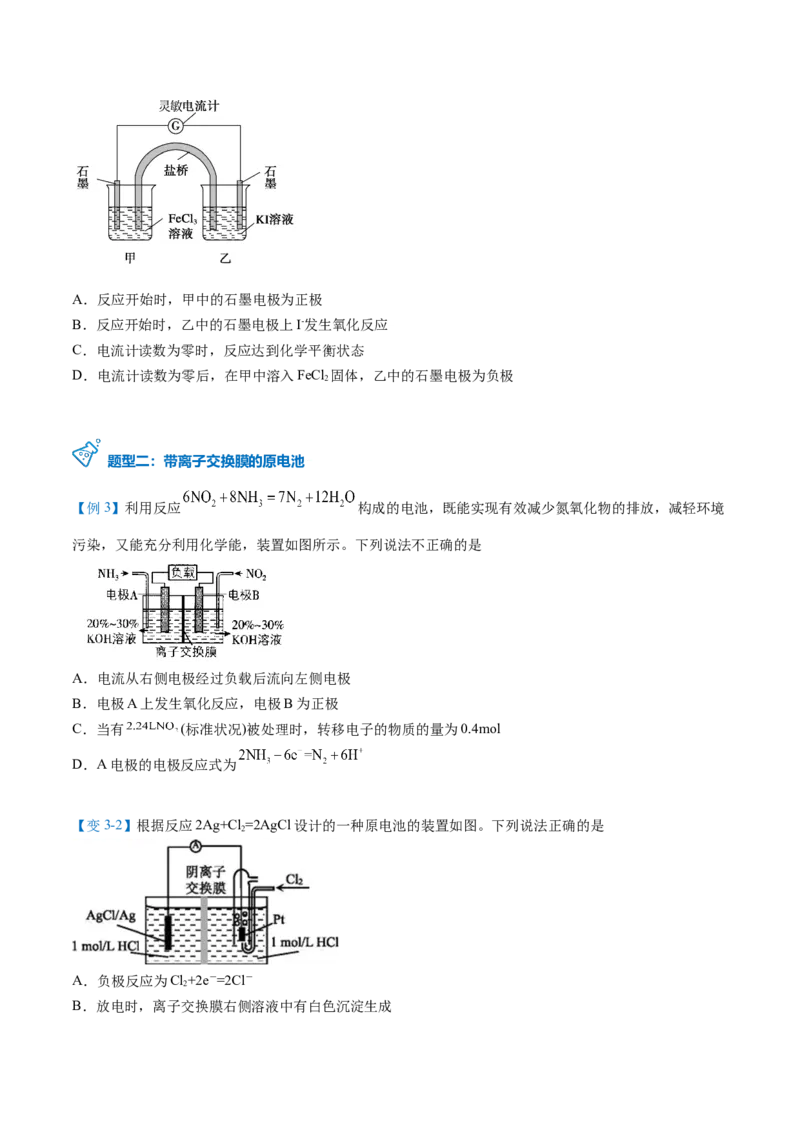
【变2】控制适合的条件,将反应2Fe3++2I- 2Fe2++I 设计成如下图所示的原电池。下列判断错误的
2
是A.反应开始时,甲中的石墨电极为正极
B.反应开始时,乙中的石墨电极上I-发生氧化反应
杨sir化学,侵权必究
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl 固体,乙中的石墨电极为负极
2
题型二:带离子交换膜的原电池
杨sir化学,侵权必究
【例3】利用反应 构成的电池,既能实现有效减少氮氧化物的排放,减轻环境
污染,又能充分利用化学能,装置如图所示。下列说法不正确的是
A.电流从右侧电极经过负载后流向左侧电极
B.电极A上发生氧化反应,电极B为正极
C.当有 (标准状况)被处理时,转移电子的物质的量为0.4mol
D.A电极的电极反应式为
【变3-2】根据反应2Ag+Cl =2AgCl设计的一种原电池的装置如图。下列说法正确的是
2
A.负极反应为Cl+2e-=2Cl-
2
B.放电时,离子交换膜右侧溶液中有白色沉淀生成C.理论上,可以用NaCl溶液代替盐酸
D.当电路中有0.01 mole-转移时,交换膜左侧溶液中约减少0.02 mol离子
杨sir化学,侵权必究
题型三:原电池的应用
杨sir化学,侵权必究
【例4】有abcd四个金属电极,有关的反应装置及部分反应现象见表,由此可判断这四种金属的活动性顺
序是
实验
装置
部分实 a极质量减小,b极 b极有气体产生,c d极溶解,c极有气 电流计指示,导线中电流
验现象 质量增加 极无变化 体产生 从a极流向d极
A.a>b>c>d B.b>c>d>a C.d>a>b>c D.a>b>d>c
【例5】3.25 g锌与100 mL 1 mol·L-1的稀硫酸反应,为了加快反应速率而不改变H 的产量,可采取的措施
2
是
A.滴加几滴浓盐酸 B.滴加几滴浓硝酸
C.滴加几滴硫酸铜溶液 D.加入少量锌粒
【变6】设计原电池装置证明Fe3+的氧化性比Cu2+强。
(1)写出能说明氧化性Fe3+大于Cu2+的离子方程式:___________。
(2)若要将上述反应设计成原电池,电极反应式分别是:
①负极:___________
②正极:___________。
(3)画出装置图,指出电极材料和电解质溶液:
①不含盐桥 ②含盐桥
题型四:原电池综合考查
杨sir化学,侵权必究
【例8】某研究性学习小组根据反应设计如图原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为 ,溶液的体积均为200mL,盐
桥中装有饱和 溶液。
回答下列问题:
(1)此原电池的负极是石墨_____(填“a”或“b”),电池工作时,盐桥中的 移向_____(填“甲”或“乙”)烧
杯。
(2)正极反应式为:_______。
(3)若不考虑溶液的体积变化, 浓度变为 ,则反应中转移的电子为_______mol。
提分特训
小杨老师 15521324728 侵权必究
【题1】下图为番茄电池装置示意图,下列说法正确的是
A.铜片上发生氧化反应 B.锌片质量减小,发生还原反应
C.电子由锌片通过导线流向铜片 D.该装置可将电能转化为化学能
【题2】下列关于下图装置(该盐桥为含KNO 的琼脂)的说法正确的是
3
A.银电极是负极B.铜电极上发生的反应为Cu-2e-=Cu2+
C.外电路中的电子是从银电极流向铜电极
D.盐桥中K+移向CuSO 溶液
4
【题4】利用反应NO +NH→N+H O(未配平)消除NO 的简易装置如图所示。下列说法正确的是
2 3 2 2 2
A.a电极反应式是2NH -6e-+6OH-=N +6H O
3 2 2
B.消耗4.48 LNH 时,被消除的NO 的物质的量为0.15 mol
3 2
C.若离子交换膜是阳离子交换摸,装置右室中溶液的碱性减弱
D.整个装置中NaOH的物质的量不断减少
【题5】欲提高Cu粉与1.2 mol/L的HNO 溶液的反应速度,可加入下列什么试剂( )
3
A.蒸馏水 B.碳酸钠固体 C.食盐水 D.AgNO 溶液(少量)
3
【题6】写出Fe和Cu、浓硝酸构成的原电池的电极反应式及电池反应式。
负极反应式:___________;正极反应式:___________。电池反应式:___________。
【题8】反应Fe+H SO =FeSO+H ,请回答下列问题。
2 4 4 2
(1)若要使该反应的反应速率加快,下列措施可行的是___(填字母)。
A.将铁粉改为铁片 B.加入少量醋酸钠固体
C.滴加少量CuSO D.将稀硫酸改为98%的浓硫酸
4
(2)若将上述反应设计成原电池,石墨棒为原电池某一极材料,则石墨棒为___极(填“正”或“负”)。石墨棒
上产生的现象为___,该极上发生的电极反应为___,原电池工作时溶液中的SO 移向___极(填正或负),
若反应产生3.36L气体(已换算成标况下),则理论上消耗铁的质量是__ 。
(3)实验后同学们经过充分讨论,认为符合某些要求的化学反应都可以设计成原电池。下列化学反应在
理论上可以设计成原电池的是___。
A.AgNO+HCl=AgCl+HNO B.NaOH+HCl=NaCl+H O
3 3 2
C.C(s)+HO(g)=CO(g)+H (g) D.Pb+PbO+2H SO =2PbSO+2H O
2 2 2 2 4 4 2
在所选反应中选择其中某个反应设计成原电池,该电池负极反应为:___。
杨sir化学,侵权必究提分作业
小杨老师 15521324728 侵权必究
【练1】化学电源应用广泛。某原电池装置如图所示,下列说法正确的是
A.锌电极发生氧化反应
B.锌片和铜片都有O 产生
2
C.电子由铜电极经导线流向锌电极
D.原电池工作一段时间后溶液的c(H+)不变
【练2】关于如图所示的原电池,下列说法正确的是
A.盐桥中的阳离子向硫酸铜溶液中迁移
B.可以用铜导线替代图中的盐桥
C.铜电极发生氧化反应,其电极反应是
杨sir化学,侵权必究
D.取出盐桥后,电流表仍会偏转,锌电极在反应后质量减少
【练3】在下图所示的柠檬水果电池中,外电路上的电子从电极Y流向电极X。若X为铅电极,则Y可能
是
A.锌 B.银 C.石墨 D.铜
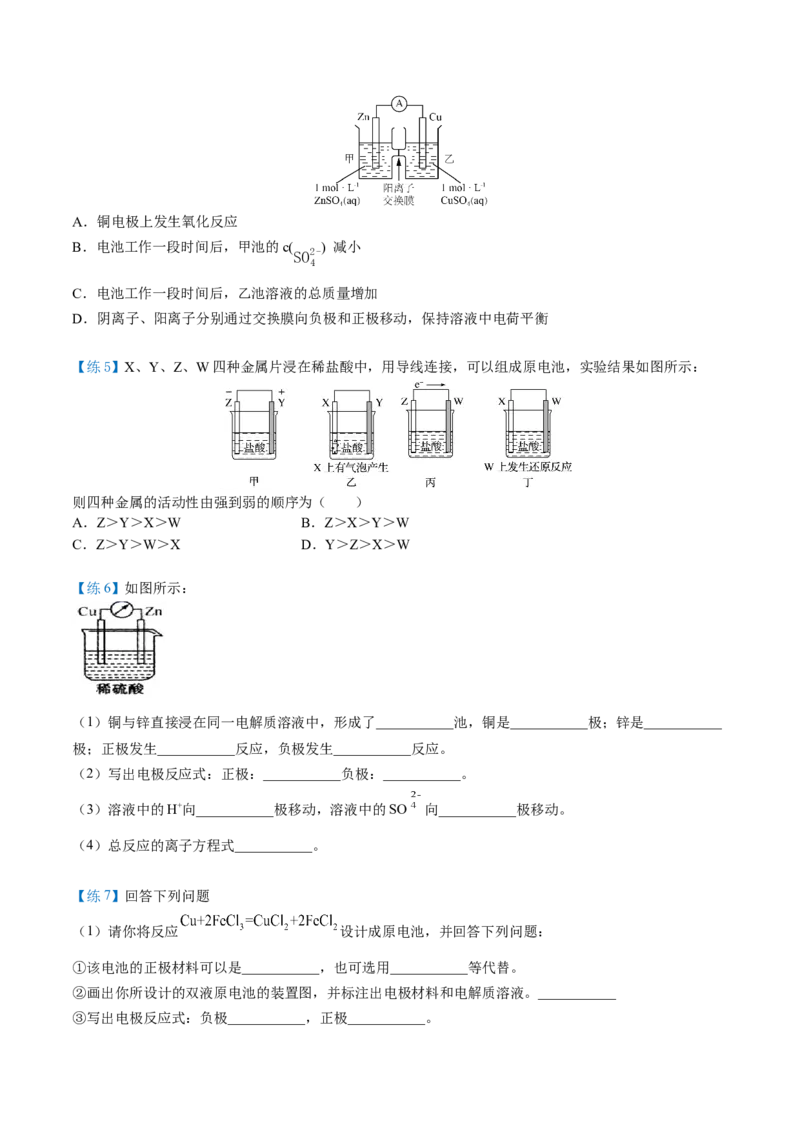
【练4】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是(
)A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的c( ) 减小
SO2-
4
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴离子、阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
【练5】X、Y、Z、W四种金属片浸在稀盐酸中,用导线连接,可以组成原电池,实验结果如图所示:
则四种金属的活动性由强到弱的顺序为( )
A.Z>Y>X>W B.Z>X>Y>W
C.Z>Y>W>X D.Y>Z>X>W
【练6】如图所示:
(1)铜与锌直接浸在同一电解质溶液中,形成了___________池,铜是___________极;锌是___________
极;正极发生___________反应,负极发生___________反应。
(2)写出电极反应式:正极:___________负极:___________。
(3)溶液中的H+向___________极移动,溶液中的SO 向___________极移动。
杨sir化学,侵权必究
(4)总反应的离子方程式___________。
【练7】回答下列问题
(1)请你将反应 设计成原电池,并回答下列问题:
①该电池的正极材料可以是___________,也可选用___________等代替。
②画出你所设计的双液原电池的装置图,并标注出电极材料和电解质溶液。___________
③写出电极反应式:负极___________,正极___________。④该电池负极材料质量减重3.2g,则电路中通过的电子的数目为___________。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育