文档内容
专项 08 化学反应速率与化学平衡
该专题分为两个板块
【1】知识清单
一、化学反应速率与速率常数
1. 化学反应速率的计算
2. 外界条件对化学反应速率的影响
3. 化学反应速率常数及应用
二、化学平衡常数与平衡移动
1. 化学平衡常数
2. 化学平衡移动的判断方法
三、化学平衡图像
1. 两种典型的图像
2. 解答化学平衡图像题四步骤
【2】专项练习
【1】知识清单
一、化学反应速率与速率常数
1.化学反应速率的计算
2.外界条件对化学反应速率的影响
3.化学反应速率常数及应用(1)基元反应
研究表明,氢气和氧气混合在点燃或有催化剂存在的条件下,主要发生以下四步反应:
H――→2H·
2
H·+O―→·OH+O·,
2
O·+H―→·OH+H·,
2
·OH+H―→HO+H·。
2 2
反应总方程式为2H+O=====2HO。
2 2 2
大多数化学反应都是分几步完成的,其中的每一步反应称为基元反应。例如:H·+O―→·OH+O·,即为
2
氢气与氧气生成水的反应中的一个基元反应。
(2)速率方程与速率常数
①速率方程
基元反应的化学反应速率与反应物的浓度数值相应幂次的乘积成正比,其方次即为各物质前面系数。即对
于基元反应:aA(g)+bB(g) gG(g)+hH(g),则v =k ca(A)·cb(B)(其中k正为正反应的速率常数),v
正 正 逆
=k cg(G)·ch(H)(其中k逆为逆反应的速率常数)。
逆
如:2NO (g) 2NO(g)+O(g)
2 2
v =k ·c2(NO)·c(O)
逆 逆 2
2H(g)+2NO(g) N(g)+2HO(g)
2 2 2
v =k ·c2(H )·c2(NO)。
正 正 2
②速率常数
a.速率常数(k)是指在给定温度下,反应物浓度皆为1 mol·L-1时的反应速率。在相同的浓度条件下,可用速
率常数大小来比较化学反应的反应速率。反应物浓度改变,但速率常数不变。因此可以应用速率方程求出
该温度下任意浓度时的反应速率。
b.影响因素
速率常数是温度的函数,同一反应,温度不同,速率常数将有不同的值,温度相同,速率常数(k)相同。浓
度不影响速率常数。
(3)速率常数与化学平衡常数之间的关系
一定温度下,可逆反应:aA(g)+bB(g) gG(g)+hH(g),达到平衡状态时,v =k ca(A)·cb(B),v =k
正 正 逆
·cg(G)·ch(H),因平衡时v =v ,则k ca(A)·cb(B)=k ·cg(G)·ch(H),则K=k /k =
逆 正 逆 正 逆 正 逆
二、化学平衡常数与平衡移动
1.化学平衡常数
(1)对于可逆反应mA(g)+nB(g) pC(g)+qD(g)在一定温度下达到化学平衡时,K=。
(2)化学平衡常数是指某一个具体反应的平衡常数,当化学反应方向改变或化学计量数改变时,化学平衡常
数也发生改变。化学方程式 平衡常数表达式
2SO (g)+O(g) 2SO (g) K =
2 2 3 1
K=
1
2SO (g) 2SO (g)+O(g) K =
3 2 2 2
K=K1
3
SO (g)+O(g) SO (g) K =
2 2 3 3
如已知某温度下,H(g)+S(s) HS(g) K,
2 2 1
S(s)+O(g) SO (g) K
2 2 2
则该温度下反应H(g)+SO (g) HS(g)+O(g)的平衡常数K=K/K 。
2 2 2 2 1 2
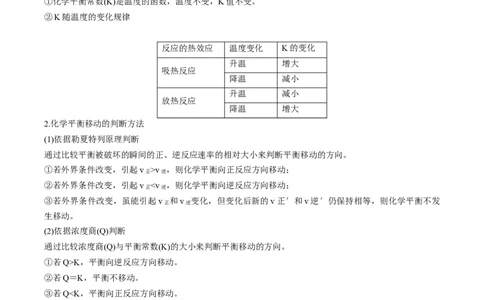
(3)化学平衡常数与温度的关系
①化学平衡常数(K)是温度的函数,温度不变,K值不变。
②K随温度的变化规律
反应的热效应 温度变化 K的变化
升温 增大
吸热反应
降温 减小
升温 减小
放热反应
降温 增大
2.化学平衡移动的判断方法
(1)依据勒夏特列原理判断
通过比较平衡被破坏的瞬间的正、逆反应速率的相对大小来判断平衡移动的方向。
①若外界条件改变,引起v >v ,则化学平衡向正反应方向移动;
正 逆
②若外界条件改变,引起v K,平衡向逆反应方向移动。
②若Q=K,平衡不移动。
③若QK(a)>K(b)
B.a点和d点容器内的压强相等
C.a点:每断裂2 mol C=O键,同时断裂2 mol O-H键
D.若c点时总压强为p,T 温度下该反应以分压表示的平衡常数
5
3.(辽宁省沈阳市2021-2022学年高三上学期教学质量检测(一)化学试卷)由γ一羟基丁酸
(HOCHCHCHCOOH)生成γ-丁内酯( )的反应如下:HOCH CHCHCOOH
2 2 2 2 2 2
+H O。在25°C时,溶液中γ一羟基丁酸初始浓度为0.180mol/L,随着反应的进行,测得γ一丁内酯的浓度
2
随时间的变化如下表所示。下列说法中错误的是
t/min 21 50 80 100 120 160 220 ∞
c/(mol/L) 0.024 0.050 0.071 0.081 0.090 0.104 0.116 0.132
A.在120min时,γ一羟基丁酸的转化率为50%
B.在50~80min内,以γ一丁内酯的浓度变化表示的反应速率为0.07mol/(L·min)
C.在25°C时,该反应的平衡常数为K=2.75
D.为提高平衡时γ一羟基丁酸的转化率,可采取的措施是移出γ一丁内酯
4.(山东新高考质量测评联盟2021届高三4月联考化学试题)MTP是一类重要的药物中间体,可以由
TOME经环化后合成。其反应式为:
+CH OH
3
为了提高TOME的转化率,反应进行时需及时从溶液体系中移出部分甲醇。TOME的转化率随反应时间的
变化如图所示。设TOME的初始浓度为a ,反应过程中液体体积变化忽略不计。下列说法正确的是
A.X、Y两点温度不同,MTP的物质的量浓度不相等
B.X、Z两点的瞬时速率大小为
C.若Z点处于化学平衡,则210 时反应的平衡常数
D.190 时,0~150min之间的MTP的平均反应速率为
5.(重庆市育才中学2022届高三高考适应性考试(一)化学试题)在一密闭容器中加入 和 发生
反应: 。测得 的平衡转化率与压强、温度之间的关系如图
所示。下列说法错误的是
A.
B.温度升高,该反应的平衡常数减小
C.增加 或移走 既能提高原料的平衡转化率又能加快反应速率
D.保持温度和容器体积不变,往平衡体系中再充入一定量的 ,再次平衡时, 的体积分数减小
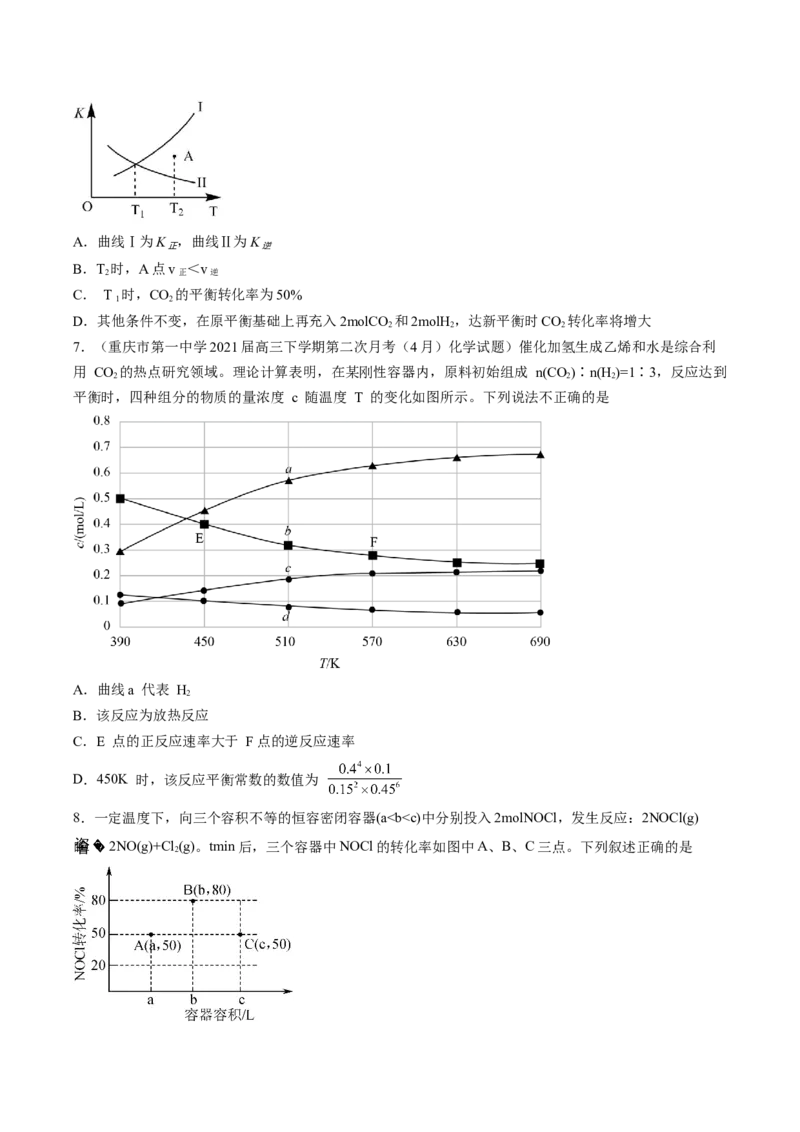
6.(重庆市西南大学附属中学校高2021届高三第二次月考化学试题)在恒容密闭容器中充入1molCO 和
2
2molH 发生如下反应:CO(g)+H(g) CO(g)+HO(g)ΔH>0。如图所示为该反应正反应的平衡常数K
2 2 2 2 正
和逆反应的平衡常数K 随温度变化的曲线。下列分析正确的是
逆A.曲线Ⅰ为K ,曲线Ⅱ为K
正 逆
B.T 时,A点v <v
2 正 逆
C. T 时,CO 的平衡转化率为50%
1 2
D.其他条件不变,在原平衡基础上再充入2molCO 和2molH ,达新平衡时CO 转化率将增大
2 2 2
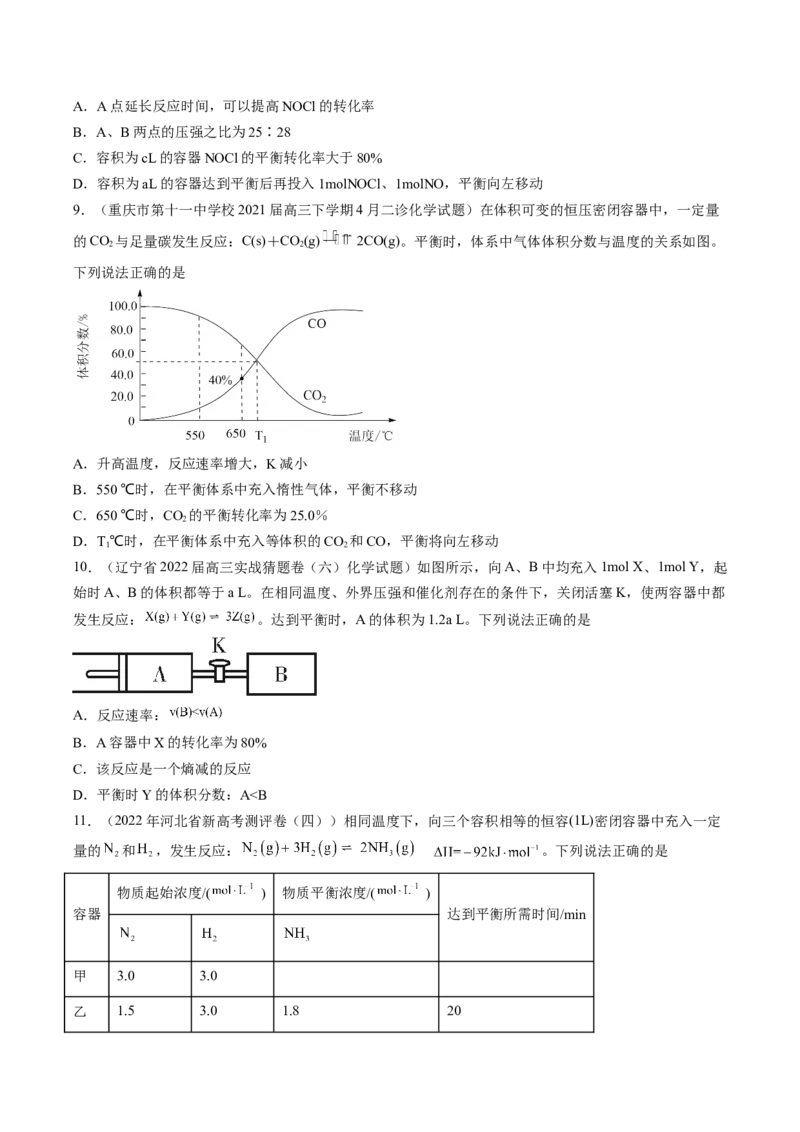
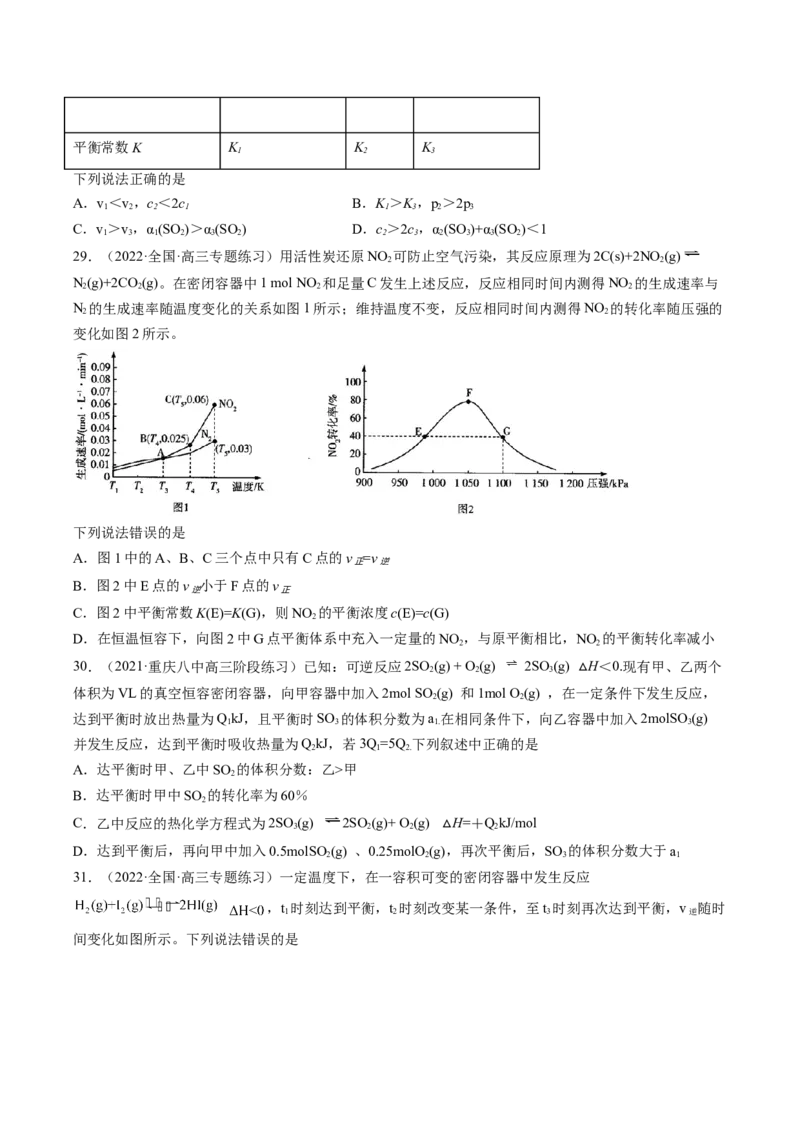
7.(重庆市第一中学2021届高三下学期第二次月考(4月)化学试题)催化加氢生成乙烯和水是综合利
用 CO 的热点研究领域。理论计算表明,在某刚性容器内,原料初始组成 n(CO)∶n(H )=1∶3,反应达到
2 2 2
平衡时,四种组分的物质的量浓度 c 随温度 T 的变化如图所示。下列说法不正确的是
A.曲线a 代表 H
2
B.该反应为放热反应
C.E 点的正反应速率大于 F点的逆反应速率
D.450K 时,该反应平衡常数的数值为
8.一定温度下,向三个容积不等的恒容密闭容器(a0 C.v >v D.K >K
M(正) N(逆) M N
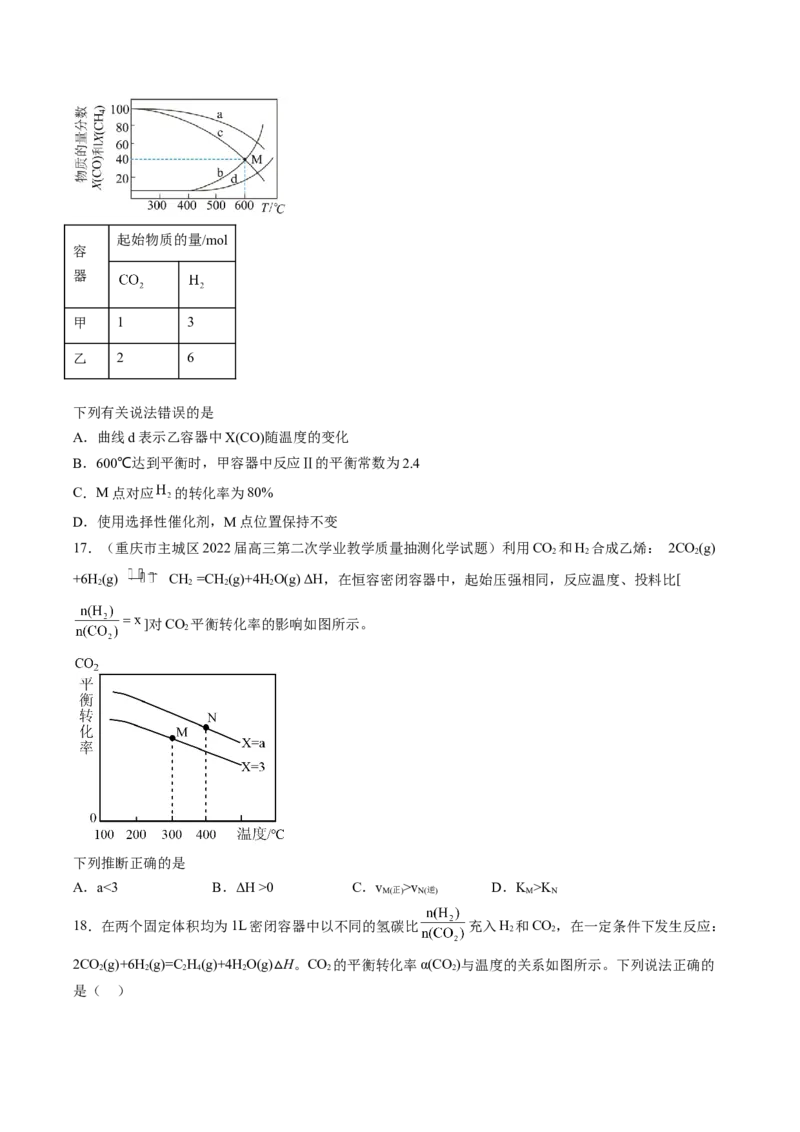
18.在两个固定体积均为1L密闭容器中以不同的氢碳比 充入H 和CO,在一定条件下发生反应:
2 2
2CO(g)+6H(g)=C H(g)+4HO(g) H。CO 的平衡转化率α(CO)与温度的关系如图所示。下列说法正确的
2 2 2 4 2 2 2
是( )
△A.该反应在常温下不可能自发进行
B.X的氢碳比X>2.0,在氢碳比为2.0时Q点v (H )>P点v (H )
逆 2 逆 2
C.若起始时CO、H 浓度分别为0.5mol/L、1.0mol/L,则可得P点对应温度的平衡常数的值为512
2 2
D.向处于P点状态的容器中,按2:4:1:4的比例再充入CO、H、C H、HO,再次平衡后α(CO)减
2 2 2 4 2 2
小
19.已知: ,速率方程为 ,其中k为反应速率常数且只与温度
有关,该反应平衡常数与温度的关系为 (式中R、C为常数,且R>0。T为温度,单位为K)。下
列说法正确的是
A.恒温恒容条件下再充入CO,c(CO)增大, 增大
B.向一容积不变的容器中充入一定量的CO(g)和 (g),一定温度下发生反应,压强不再变化时,该反
应达到平衡
C.恒温恒压条件下充入He,有利于提高 的平衡转化率
D.降低温度,有利于提高 平衡转化率
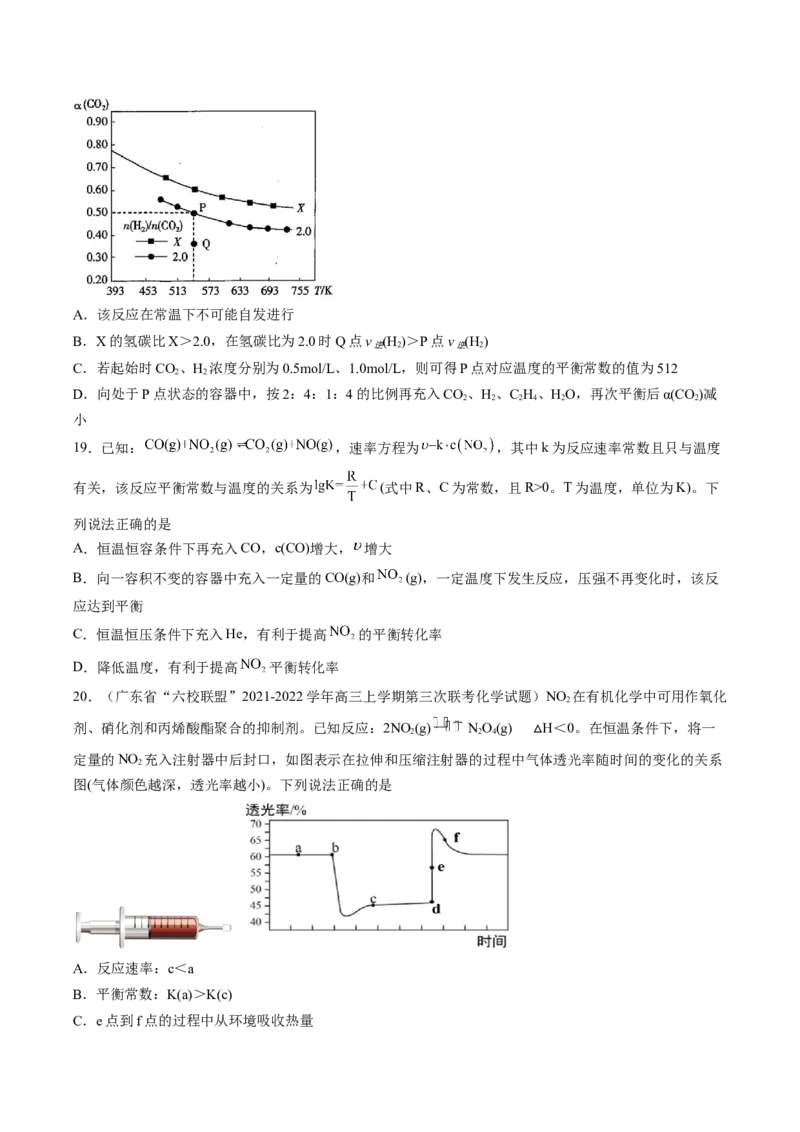
20.(广东省“六校联盟”2021-2022学年高三上学期第三次联考化学试题)NO 在有机化学中可用作氧化
2
剂、硝化剂和丙烯酸酯聚合的抑制剂。已知反应:2NO (g) NO(g) H<0。在恒温条件下,将一
2 2 4
定量的NO 充入注射器中后封口,如图表示在拉伸和压缩注射器的过程中气△体透光率随时间的变化的关系
2
图(气体颜色越深,透光率越小)。下列说法正确的是
A.反应速率:c<a
B.平衡常数:K(a)>K(c)
C.e点到f点的过程中从环境吸收热量D.d点到e点的变化可以用勒夏特列原理解释
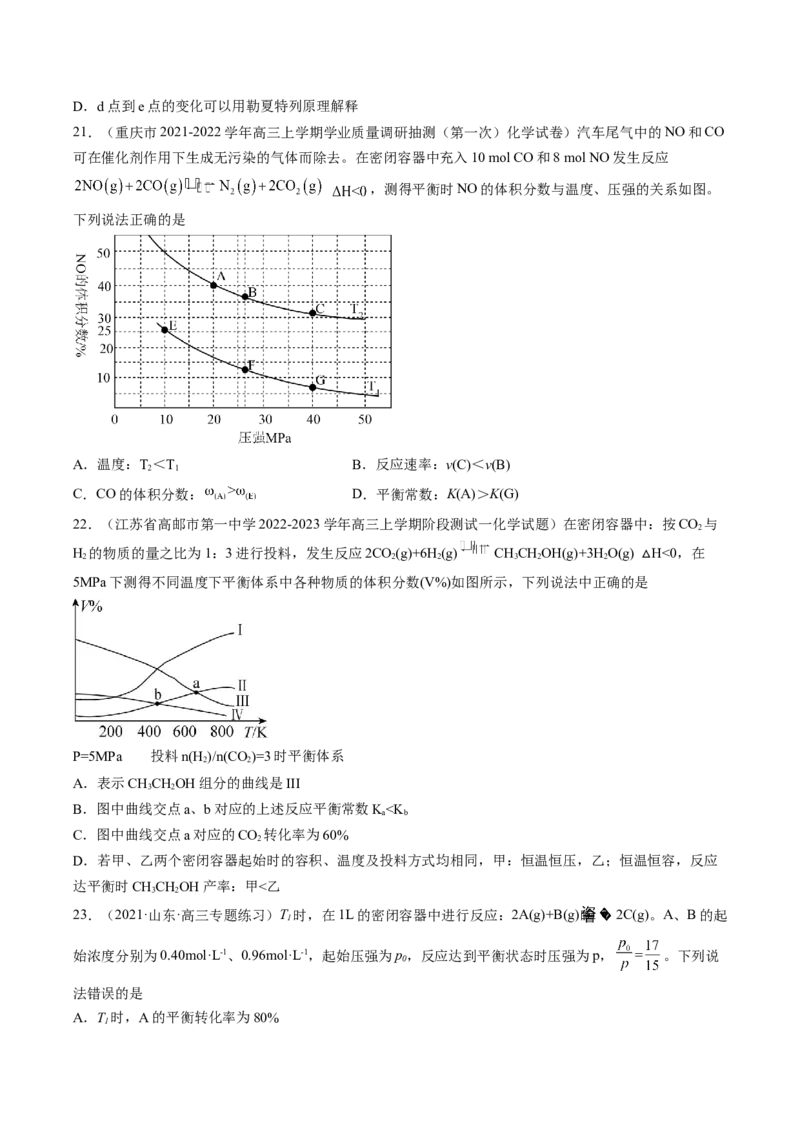
21.(重庆市2021-2022学年高三上学期学业质量调研抽测(第一次)化学试卷)汽车尾气中的NO和CO
可在催化剂作用下生成无污染的气体而除去。在密闭容器中充入10 mol CO和8 mol NO发生反应
,测得平衡时NO的体积分数与温度、压强的关系如图。
下列说法正确的是
A.温度:T<T B.反应速率:v(C)<v(B)
2 1
C.CO的体积分数: D.平衡常数:K(A)>K(G)
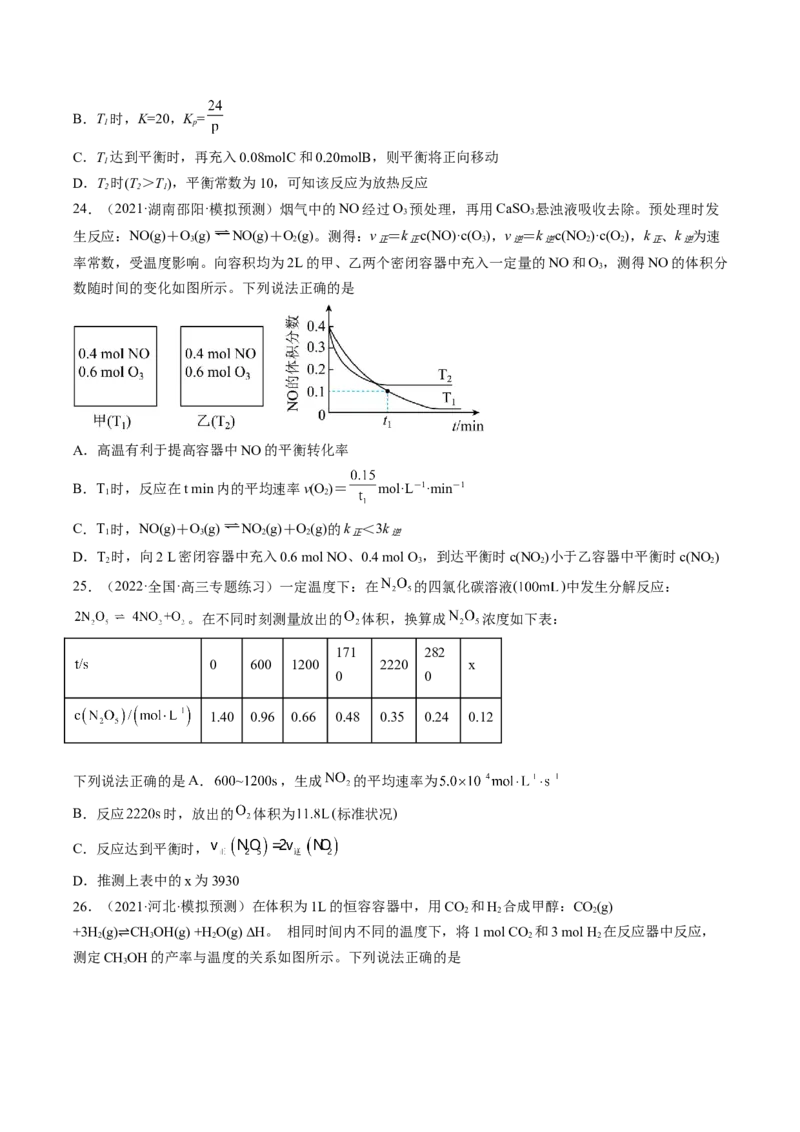
22.(江苏省高邮市第一中学2022-2023学年高三上学期阶段测试一化学试题)在密闭容器中:按CO 与
2
H 的物质的量之比为1:3进行投料,发生反应2CO(g)+6H(g) CHCHOH(g)+3H O(g) H<0,在
2 2 2 3 2 2
5MPa下测得不同温度下平衡体系中各种物质的体积分数(V%)如图所示,下列说法中正确的是△
P=5MPa 投料n(H )/n(CO)=3时平衡体系
2 2
A.表示CHCHOH组分的曲线是III
3 2
B.图中曲线交点a、b对应的上述反应平衡常数Kv(逆)
B.图中P点所示条件下,延长反应时间不能提高CHOH的产率
3
C.该反应的 ∆H>0
D.520K下,X点所对应甲醇的产率为50%,则平衡常数K=
27.(2021·全国·高三专题练习)某温度下2 L密闭容器中3种气体起始状态和平衡状态时的物质的量(n)
如表所示,下列说法正确的是
A.该温度下,此反应的平衡常数表达式是K=
B.其他条件不变,升高温度,若W的体积分数减小,则此反应ΔH<0
C.其他条件不变,使用催化剂,正、逆反应速率和平衡常数均增大,平衡不移动
D.其他条件不变,当密闭容器中混合气体密度不变时,表明反应已达到平衡
28.(2021·全国·高三专题练习)一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,
发生反应2SO (g)+O(g) 2SO (g)(正反应放热),测得反应的相关数据如下:
2 2 3
容器1 容器2 容器3
反应温度T/K 700 700 800
反应物投入量 2molSO 、1molO 4molSO 2molSO 、1molO
2 2 3 2 2
平衡v (SO )/mol/(L·s) v v v
正 2 1 2 3
平衡c(SO )mol/L c c c
3 1 2 3
平衡体系总压强p/Pa p p p
1 2 3
物质的平衡转化率/α α (SO ) α (SO ) α (SO )
1 2 2 3 3 2平衡常数K K K K
1 2 3
下列说法正确的是
A.v<v,c<2c B.K >K ,p>2p
1 2 2 1 1 3 2 3
C.v>v,α (SO )>α (SO ) D.c>2c,α (SO )+α (SO )<1
1 3 1 2 3 2 2 3 2 3 3 2
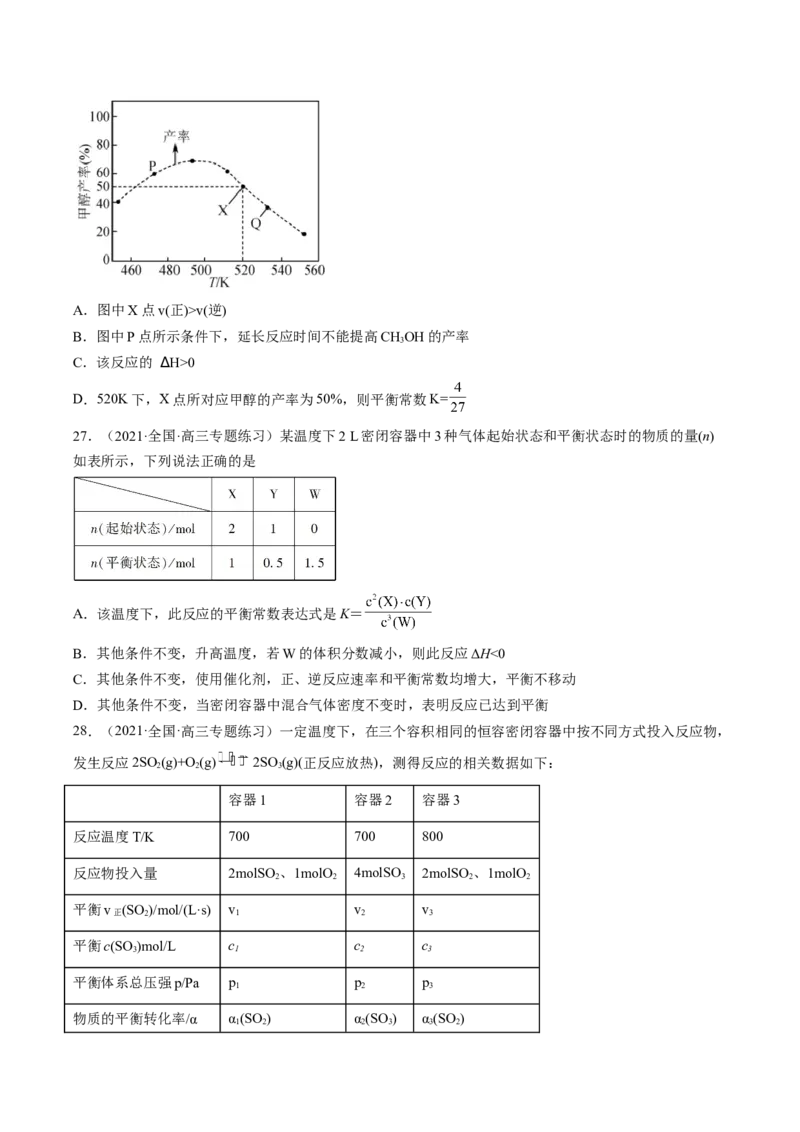
29.(2022·全国·高三专题练习)用活性炭还原NO 可防止空气污染,其反应原理为2C(s)+2NO (g)
2 2
N(g)+2CO (g)。在密闭容器中1 mol NO 和足量C发生上述反应,反应相同时间内测得NO 的生成速率与
2 2 2 2
N 的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内测得NO 的转化率随压强的
2 2
变化如图2所示。
下列说法错误的是
A.图1中的A、B、C三个点中只有C点的v =v
正 逆
B.图2中E点的v 小于F点的v
逆 正
C.图2中平衡常数K(E)=K(G),则NO 的平衡浓度c(E)=c(G)
2
D.在恒温恒容下,向图2中G点平衡体系中充入一定量的NO ,与原平衡相比,NO 的平衡转化率减小
2 2
30.(2021·重庆八中高三阶段练习)已知:可逆反应2SO (g) + O(g) 2SO (g) H<0.现有甲、乙两个
2 2 3
体积为VL的真空恒容密闭容器,向甲容器中加入2mol SO (g) 和1mol O(g) ,在一定条件下发生反应,
2 2 △
达到平衡时放出热量为QkJ,且平衡时SO 的体积分数为a 在相同条件下,向乙容器中加入2molSO (g)
1 3 1. 3
并发生反应,达到平衡时吸收热量为QkJ,若3Q=5Q 下列叙述中正确的是
2 1 2.
A.达平衡时甲、乙中SO 的体积分数:乙>甲
2
B.达平衡时甲中SO 的转化率为60%
2
C.乙中反应的热化学方程式为2SO (g) 2SO (g)+ O (g) H=+QkJ/mol
3 2 2 2
D.达到平衡后,再向甲中加入0.5molSO
2
(g) 、0.25molO
2
(g)△ ,再次平衡后,SO
3
的体积分数大于a
1
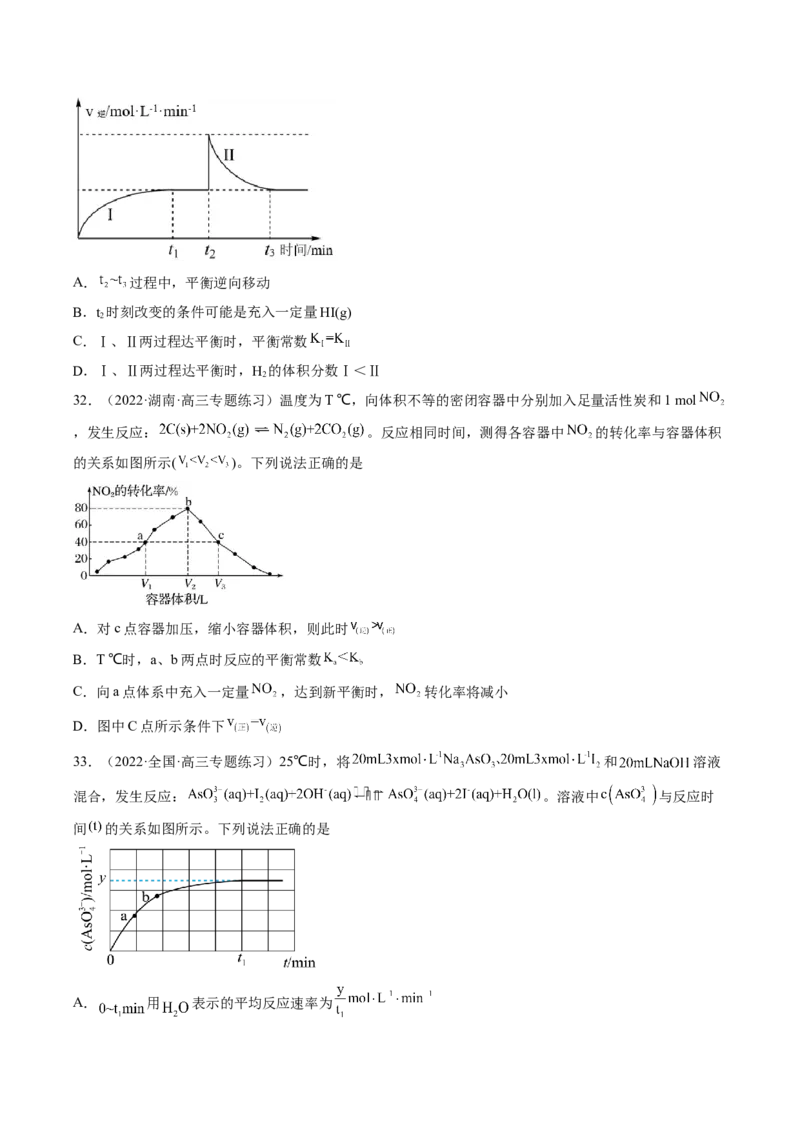
31.(2022·全国·高三专题练习)一定温度下,在一容积可变的密闭容器中发生反应
,t 时刻达到平衡,t 时刻改变某一条件,至t 时刻再次达到平衡,v 随时
1 2 3 逆
间变化如图所示。下列说法错误的是A. 过程中,平衡逆向移动
B.t 时刻改变的条件可能是充入一定量HI(g)
2
C.Ⅰ、Ⅱ两过程达平衡时,平衡常数
D.Ⅰ、Ⅱ两过程达平衡时,H 的体积分数Ⅰ<Ⅱ
2
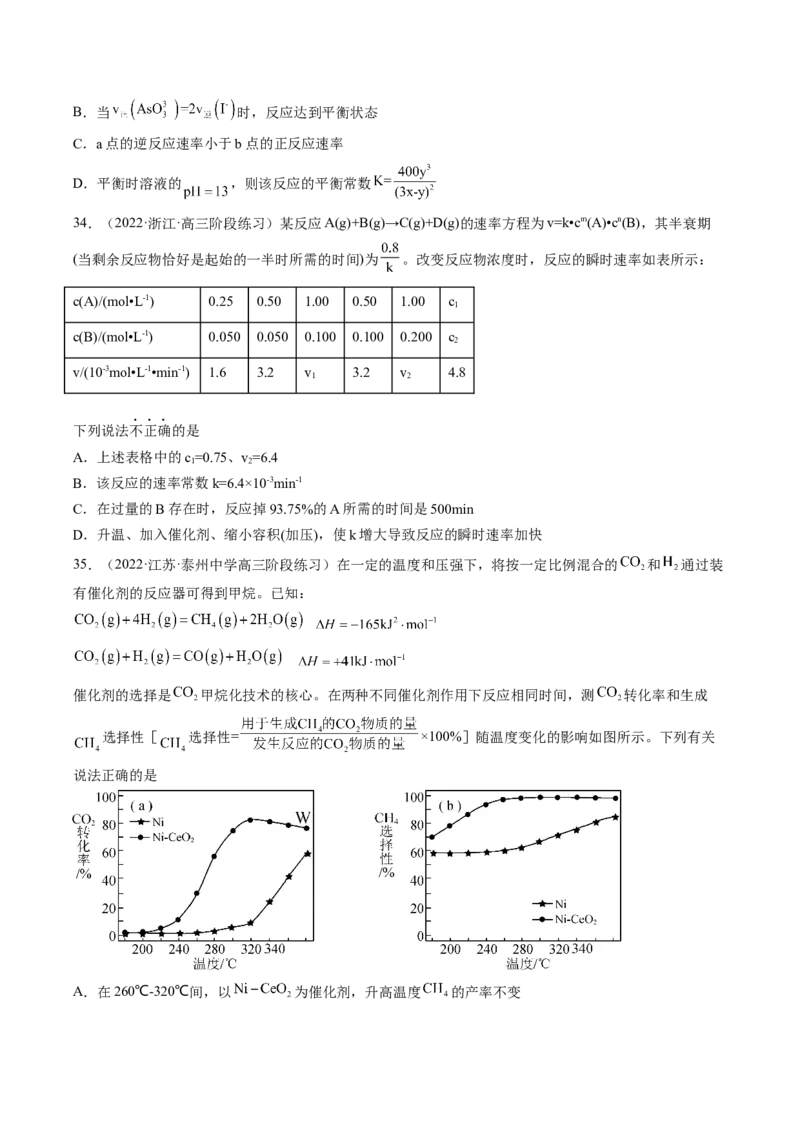
32.(2022·湖南·高三专题练习)温度为T ℃,向体积不等的密闭容器中分别加入足量活性炭和1 mol
,发生反应: 。反应相同时间,测得各容器中 的转化率与容器体积
的关系如图所示( )。下列说法正确的是
A.对c点容器加压,缩小容器体积,则此时
B.T ℃时,a、b两点时反应的平衡常数
C.向a点体系中充入一定量 ,达到新平衡时, 转化率将减小
D.图中C点所示条件下
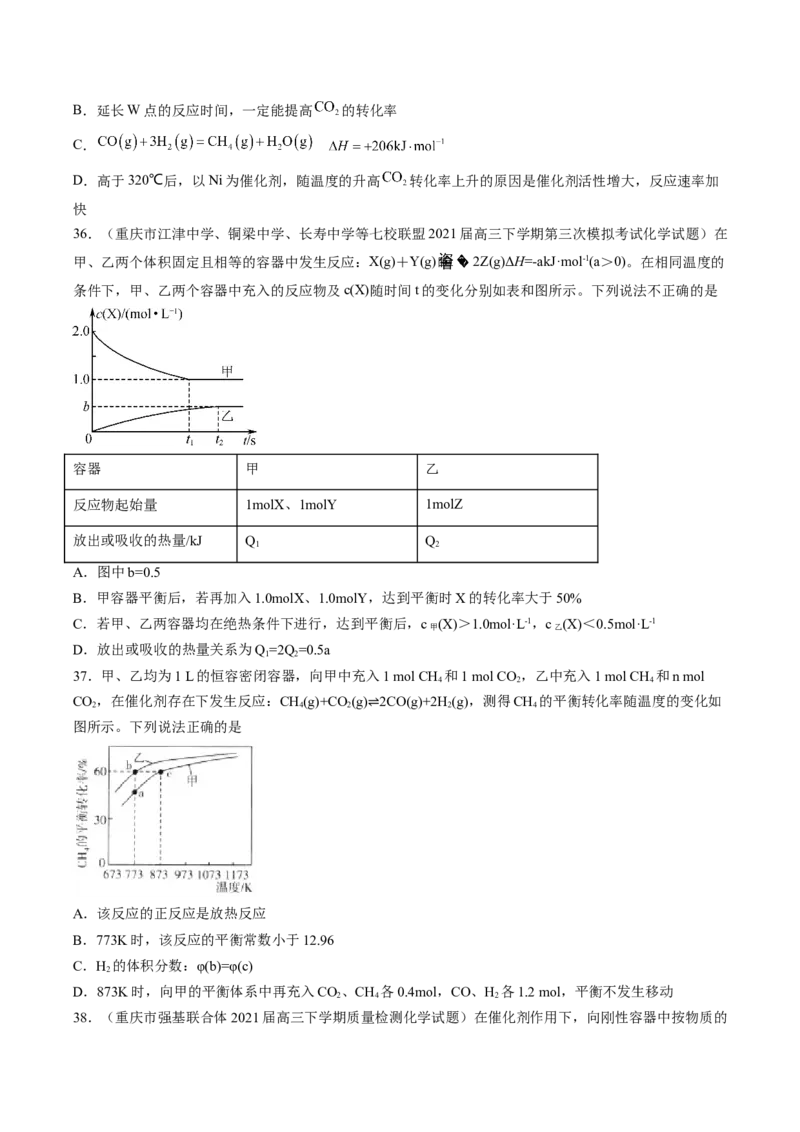
33.(2022·全国·高三专题练习)25℃时,将 和 溶液
混合,发生反应: 。溶液中 与反应时
间 的关系如图所示。下列说法正确的是
A. 用 表示的平均反应速率为B.当 时,反应达到平衡状态
C.a点的逆反应速率小于b点的正反应速率
D.平衡时溶液的 ,则该反应的平衡常数
34.(2022·浙江·高三阶段练习)某反应A(g)+B(g)→C(g)+D(g)的速率方程为v=k•cm(A)•cn(B),其半衰期
(当剩余反应物恰好是起始的一半时所需的时间)为 。改变反应物浓度时,反应的瞬时速率如表所示:
c(A)/(mol•L-1) 0.25 0.50 1.00 0.50 1.00 c
1
c(B)/(mol•L-1) 0.050 0.050 0.100 0.100 0.200 c
2
v/(10-3mol•L-1•min-1) 1.6 3.2 v 3.2 v 4.8
1 2
下列说法不正确的是
A.上述表格中的c=0.75、v=6.4
1 2
B.该反应的速率常数k=6.4×10-3min-1
C.在过量的B存在时,反应掉93.75%的A所需的时间是500min
D.升温、加入催化剂、缩小容积(加压),使k增大导致反应的瞬时速率加快
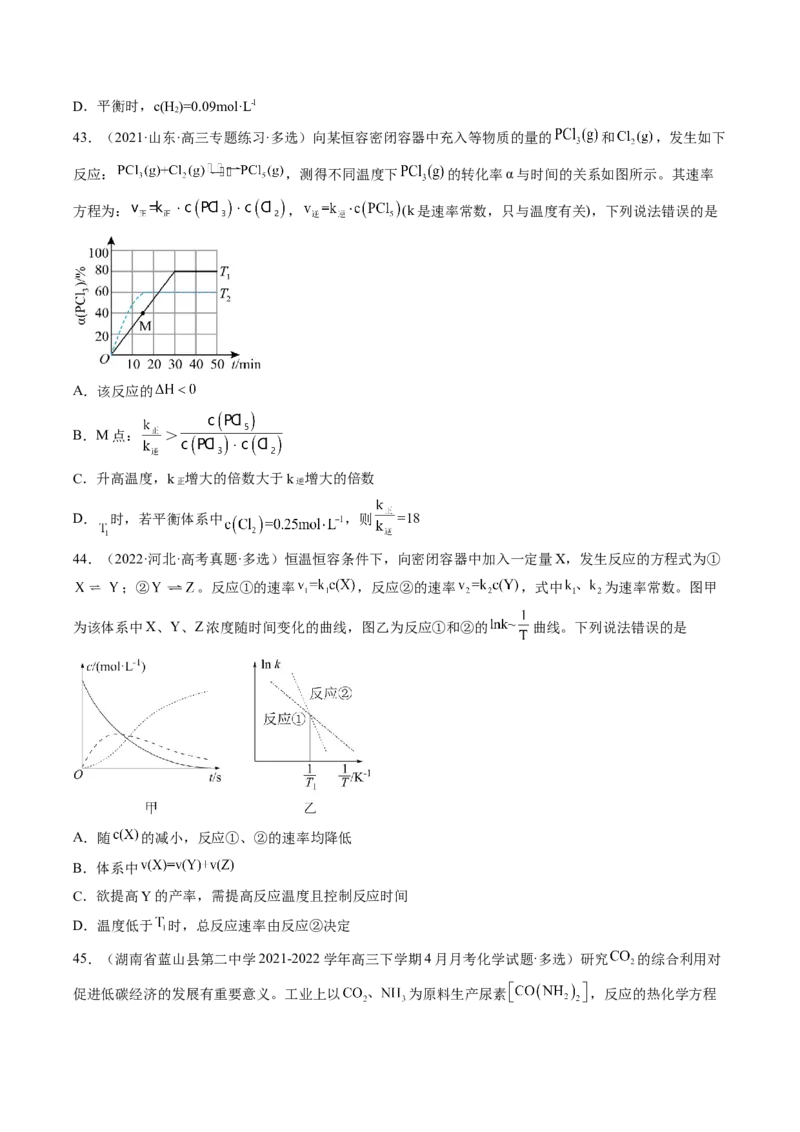
35.(2022·江苏·泰州中学高三阶段练习)在一定的温度和压强下,将按一定比例混合的 和 通过装
有催化剂的反应器可得到甲烷。已知:
催化剂的选择是 甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测 转化率和生成
选择性[ 选择性= ×100%]随温度变化的影响如图所示。下列有关
说法正确的是
A.在260℃-320℃间,以 为催化剂,升高温度 的产率不变B.延长W点的反应时间,一定能提高 的转化率
C.
D.高于320℃后,以Ni为催化剂,随温度的升高 转化率上升的原因是催化剂活性增大,反应速率加
快
36.(重庆市江津中学、铜梁中学、长寿中学等七校联盟2021届高三下学期第三次模拟考试化学试题)在
甲、乙两个体积固定且相等的容器中发生反应:X(g)+Y(g) 2Z(g)ΔH=-akJ·mol-1(a>0)。在相同温度的
条件下,甲、乙两个容器中充入的反应物及c(X)随时间t的变化分别如表和图所示。下列说法不正确的是
容器 甲 乙
反应物起始量 1molX、1molY 1molZ
放出或吸收的热量/kJ Q Q
1 2
A.图中b=0.5
B.甲容器平衡后,若再加入1.0molX、1.0molY,达到平衡时X的转化率大于50%
C.若甲、乙两容器均在绝热条件下进行,达到平衡后,c (X)>1.0mol·L-1,c (X)<0.5mol·L-1
甲 乙
D.放出或吸收的热量关系为Q=2Q =0.5a
1 2
37.甲、乙均为1 L的恒容密闭容器,向甲中充入1 mol CH 和1 mol CO ,乙中充入1 mol CH 和n mol
4 2 4
CO,在催化剂存在下发生反应:CH(g)+CO (g) 2CO(g)+2H(g),测得CH 的平衡转化率随温度的变化如
2 4 2 2 4
图所示。下列说法正确的是
⇌
A.该反应的正反应是放热反应
B.773K时,该反应的平衡常数小于12.96
C.H 的体积分数:φ(b)=φ(c)
2
D.873K时,向甲的平衡体系中再充入CO、CH 各0.4mol,CO、H 各1.2 mol,平衡不发生移动
2 4 2
38.(重庆市强基联合体2021届高三下学期质量检测化学试题)在催化剂作用下,向刚性容器中按物质的量比1︰1充入甲醇和异丁烯(用R表示),分别在T 和T 两个温度下发生反应生成有机物W:CHOH(g)+
1 2 3
R(g) W(g) ΔH。异丁烯的转化率随时间的变化关系如图所示。下列说法正确的是
⇌
A.T>T,ΔH>0
1 2
B.v =v >v
M正 B正 A逆
C.维持T 不变,再向容器中充入1 mol W,新平衡时W的百分含量减小
2
D.T 时,容器内起始总压为p kPa,则用分压表示的该反应的平衡常数K= kPa-1
1 0 p
39.(重庆市普通高中学业水平选择性考试2021届高三第三次联合诊断检测化学试题)利用活性炭可以处
理NO的污染,其原理为: 。现向某容积固定的密闭容器加入一
定量的活性炭和一定量的NO,在T℃时,各物质的量浓度随时间变化如图所示,下列说法正确的是
1
A.0~10min的平均速率v(CO)=0.1mol·L-1·min-1
2
B.50min时改变的条件是升温
C.若原平衡态压强为100kPa,维持体积不变,再通入一定量的CO(g),达到平衡后压强变为150kPa,则
2
平衡时NO转化了
D.50min时改变的条件是加入高效的催化剂
40.(江苏省徐州市2021届高三年级5月考前模拟化学试题)CH 与CO 重整可以同时利用两种温室气体,
4 2
其工艺过程中涉及如下反应:
反应①:CH(g)+CO (g) 2CO(g)+2H(g) ΔH =+247.4kJ·mol-1
4 2 2 1
反应②:CO(g)+H(g) CO(g)+HO(g) ΔH=+41.2kJ·mol-1
2 2 ⇌ 2 2
⇌
反应③:CH(g)+ O(g) CO(g)+2H(g) ΔH = -35.6kJ·mol-1
4 2 2 3
⇌
一定条件下,向体积为VL的密闭容器中通入CH、CO 各1.0mol及少量O,测得不同温度下反应平衡时
4 2 2
各产物产量如图所示,下列说法正确的是A.2CO(g)+O(g)=2CO (g) ΔH=-283kJ·mol-1
2 2
B.图中曲线a和b分别代表产物CO和H
2
C.温度高于900K时,HO的含量下降的原因之一是反应③向逆向进行
2
D.升高温度和增加压强均能使CO的产量增加
41.(重庆市第一中学2021-2022学年高三上学期第三次月考化学试题)我国科学家在全球首次实现二氧
化碳到淀粉的合成,其第一阶段是将二氧化碳催化加氢制得甲醇,反应方程式如下:
Ⅰ:
Ⅱ:
Ⅲ:
向容积为 的密闭装置中充入 和 ,在t℃下反应, 后达平衡状态.测得容器内
, , ,下列说法错误的是
A.可以通过监测容器内的总压来判断反应Ⅰ是否达到平衡
B.达平衡时,用 表示的反应Ⅰ的平均反应速率为
C.t℃下,反应Ⅱ的平衡常数为
D.向容器内再投入 和 ,再次平衡后,
42.(湖南省长沙市明德中学2021届高三第一次模拟考试化学试题·多选)一定温度下,在5L恒容密闭容
器中发生反应CH(g)+HO(g) CO(g)+3H(g),反应过程中的部分数据如下表所示:
4 2 2
n(CH)/mol n(H O)/mol n(CO)/mol n(H )/mol
4 2 2
0 0.2 1.0 0 0
t/min 0.05
1
t/min 0.45
2
t min 0.85
3/
下列说法正确的是
A.0-t 时刻用H 表示的平均反应速率为0.03/t mol·L-1·min-1
1 2 1
B.该反应从t 时刻开始达到平衡状态
2
C.CH 的平衡转化率为15%
4D.平衡时,c(H)=0.09mol·L-l
2
43.(2021·山东·高三专题练习·多选)向某恒容密闭容器中充入等物质的量的 和 ,发生如下
反应: ,测得不同温度下 的转化率α与时间的关系如图所示。其速率
方程为: , (k是速率常数,只与温度有关),下列说法错误的是
A.该反应的
B.M点: >
C.升高温度,k 增大的倍数大于k 增大的倍数
正 逆
D. 时,若平衡体系中 ,则 =18
44.(2022·河北·高考真题·多选)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为①
;② 。反应①的速率 ,反应②的速率 ,式中 为速率常数。图甲
为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的 曲线。下列说法错误的是
A.随 的减小,反应①、②的速率均降低
B.体系中
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于 时,总反应速率由反应②决定
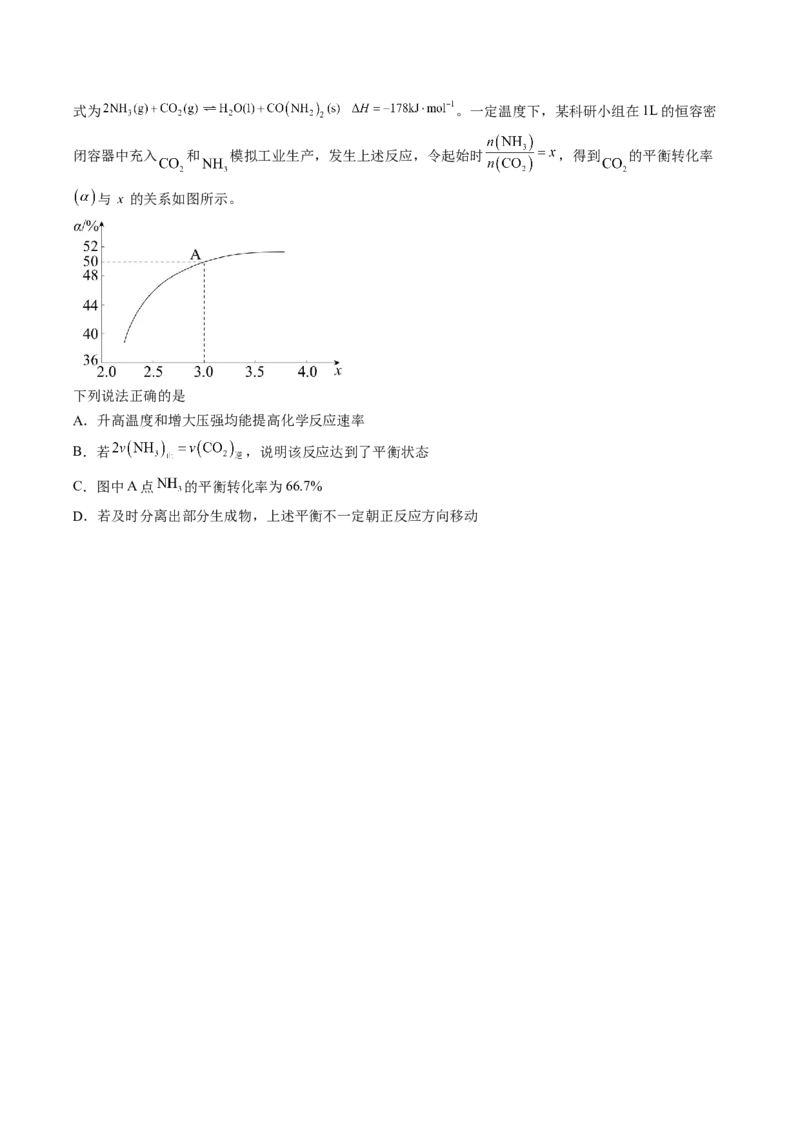
45.(湖南省蓝山县第二中学2021-2022学年高三下学期4月月考化学试题·多选)研究 的综合利用对
促进低碳经济的发展有重要意义。工业上以 为原料生产尿素 ,反应的热化学方程式为 。一定温度下,某科研小组在1L的恒容密
闭容器中充入 和 模拟工业生产,发生上述反应,令起始时 ,得到 的平衡转化率
与 的关系如图所示。
下列说法正确的是
A.升高温度和增大压强均能提高化学反应速率
B.若 ,说明该反应达到了平衡状态
C.图中A点 的平衡转化率为66.7%
D.若及时分离出部分生成物,上述平衡不一定朝正反应方向移动