文档内容
第三篇 化学反应与能量
专项 18 利用键能计算反应热
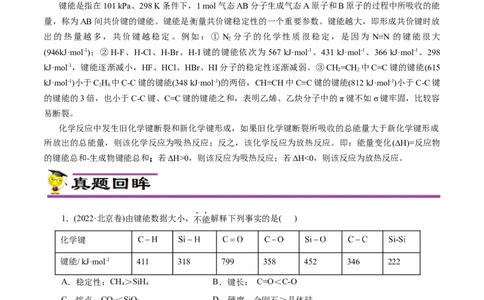
键能是指在101 kPa、298 K条件下,1 mol气态AB分子生成气态A原子和B原子的过程中所吸收的能
量,称为AB间共价键的键能。键能是衡量共价键稳定性的一个重要参数。键能越大,即形成共价键时放
出的热量越多,共价键越稳定。例如:① N 分子的化学性质很稳定,是因为 N≡N 的键能很大
2
(946kJ·mol-1);②H-F、H-Cl、H-Br、H-I键的键能依次为567 kJ·mol-1、431 kJ·mol-1、366 kJ·mol-1、298
kJ·mol-1,键能逐渐减小,HF、HCl、HBr、HI分子的稳定性逐渐减弱。③CH=CH 中C=C键的键能(615
2 2
kJ·mol-1)小于C H 中C-C键的键能(348 kJ·mol-1)的两倍,CH≡CH中C≡C键的键能(812 kJ·mol-1)小于C-C键
2 6
的键能的3倍,也小于C-C键、C=C键的键能之和,表明乙烯、乙炔分子中的π键不如σ键牢固,比较容
易断裂。
化学反应中发生旧化学键断裂和新化学键形成,如果旧化学键断裂所吸收的总能量大于新化学键形成
所放出的总能量,则该化学反应为吸热反应;反之,该化学反应为放热反应。即:能量变化(ΔH)=反应物
的键能总和-生成物键能总和;若ΔH>0,则该反应为吸热反应;若ΔH<0,则该反应为放热反应。
1.(2022·北京卷)由键能数据大小,不能解释下列事实的是( )
化学键
键能/ kJ·mol-1 411 318 799 358 452 346 222
A.稳定性:CH>SiH B.键长: C=O<C-O
4 4
C.熔点:CO<SiO D.硬度:金刚石>晶体硅
2 2
【答案】C
【解析】A项,键能越大越稳定,C-H键能大于Si-H,所以稳定性:CH>SiH,故不选A;B项,键
4 4
能越大,键长越短,C=O键能大于C-O,所以键长:C=O<C-O,故不选B;C项,CO 是分子晶体,熔点
2
由分子间作用力决定,SiO 是共价晶体,所以熔点CO<SiO,不能用键能解释熔点CO<SiO,故选C;
2 2 2 2 2
D项,金刚石、晶体硅都是共价晶体,共价晶体中键能越大,晶体的硬度越大,C-C的键能大于Si-Si,所
以硬度:金刚石>晶体硅,故不选D;故选C。
1
原创精品资源学科网独家享有版权,侵权必究!
1
学科网(北京)股份有限公司2.(2022·浙江省6月选考)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O HO HO
2 2 2 2 2
能量/ kJ·mol-l 249 218 39 10 0 0
可根据HO(g)+HO(g)= H O(g)计算出HO 中氧氧单键的键能为214 kJ·mol-l。下列说法不正确的是(
2 2 2 2
)
A.H 的键能为436 kJ·mol-l
2
B.O 的键能大于HO 中氧氧单键的键能的两倍
2 2 2
C.解离氧氧单键所需能量: HOO<HO
2 2
D.HO(g)+O(g)= H O(g) ΔH=-143kJ·mol−1
2 2 2
【答案】C
【解析】A项,根据表格中的数据可知,H 的键能为218×2=436 kJ·mol-l,A正确;
2
B项,由表格中的数据可知O 的键能为:249×2=498 kJ·mol-l,由题中信息可知HO 中氧氧单键的键能为
2 2 2
214 kJ·mol-l,则O 的键能大于HO 中氧氧单键的键能的两倍,B正确;C项,由表格中的数据可知
2 2 2
HOO=HO+O,解离其中氧氧单键需要的能量为249+39-10=278 kJ·mol-l,HO 中氧氧单键的键能为214
2 2
kJ·mol-l,C错误;D项,由表中的数据可知HO(g)+O(g)= H O(g)的 ,D
2 2 2
正确;故选C。
3.(2021•浙江1月选考)已知共价键的键能与热化学方程式信息如下表:
共价键 H- H H-O
键能/(kJ·mol-1) 436 463
热化学方程式 2H(g) + O (g)=2HO(g) ΔH= -482kJ·mol-1
2 2 2
则2O(g)=O (g)的ΔH为( )
2
A.428 kJ·mol-1 B.-428 kJ·mol-1 C.498 kJ·mol-1 D.-498 kJ·mol-1
【答案】D
【解析】反应的ΔH=2(H-H)+(O-O)-4(H-O);-482kJ/mol=2×436kJ/mol+(O-O)-4×463kJ/mol,解得O-O
键的键能为498kJ/mol,2个氧原子结合生成氧气的过程需要释放能量,因此2O(g)=O (g)的ΔH=-498kJ/
2
mol。
4.(2018•天津卷节选)CO 与CH 经催化重整,制得合成气:
2 4
2
原创精品资源学科网独家享有版权,侵权必究!
2
学科网(北京)股份有限公司CH(g)+CO (g) 2CO(g)+2H(g)
4 2 2
已知上述反应中相关的化学键键能数据如下:
化学键 C—H H—H C← O(CO)
键能/(kJ·mol-1) 413 745 436 1 075
则该反应的ΔH= 。
分别在v L恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH 和CO 各1 mol的混合气体。两
4 2
容器中反应达平衡后放出或吸收的热量较多的是 (填“A”或“B”)。
【答案】 +120 kJ·mol-1 B
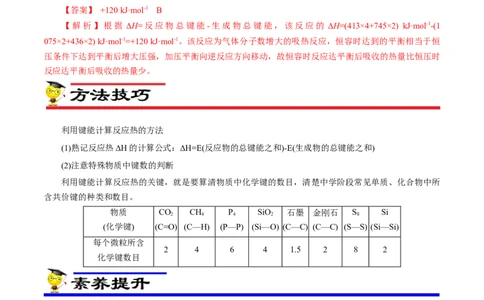
【解析】根据 ΔH=反应物总键能-生成物总键能,该反应的 ΔH=(413×4+745×2) kJ·mol-1-(1
075×2+436×2) kJ·mol-1=+120 kJ·mol-1。该反应为气体分子数增大的吸热反应,恒容时达到的平衡相当于恒
压条件下达到平衡后增大压强,加压平衡向逆反应方向移动,故恒容时反应达平衡后吸收的热量比恒压时
反应达平衡后吸收的热量少。
利用键能计算反应热的方法
(1)熟记反应热ΔH的计算公式:ΔH=E(反应物的总键能之和)-E(生成物的总键能之和)
(2)注意特殊物质中键数的判断
利用键能计算反应热的关键,就是要算清物质中化学键的数目,清楚中学阶段常见单质、化合物中所
含共价键的种类和数目。
物质 CO CH P SiO 石墨 金刚石 S Si
2 4 4 2 8
(化学键) (C=O) (C—H) (P—P) (Si—O) (C—C) (C—C) (S—S) (Si—Si)
每个微粒所含
2 4 6 4 1.5 2 8 2
化学键数目
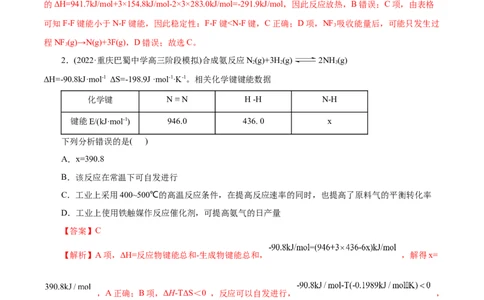
1.(2022·陕西省子洲中学质检)生产液晶显示器的过程中使用的化学清洗剂NF 是一种温室气体,在大
3
气中寿命可达740年之久。键能是指破坏(或生成)1mol化学键所需要吸收(或放出)的能量。结合表中信息,
下列说法正确的是( )
化学键 N≡N F-F N-F
键能(kJ/mol) 941.7 154.8 283.0
3
原创精品资源学科网独家享有版权,侵权必究!
3
学科网(北京)股份有限公司A.过程N(g)→2N(g)放出能量
2
B.反应N(g)+3F (g)=2NF (g)是吸热反应
2 2 3
C.稳定性:F-F键0
4 2 2 1
反应Ⅱ CH(g) +2H O(g) CO(g) +4H (g) ΔH>0
4 2 2 2 2
反应ⅢCO(g) +H O(g) CO(g) +H (g) ΔH
2 2 2 3
已知部分化学键的键能数据如下表:
9
原创精品资源学科网独家享有版权,侵权必究!
9
学科网(北京)股份有限公司化学键 O-H H-H C=O C≡O( CO)
键能/(kJ·mol -1) 463 436 803 1075
则ΔH=_______,若反应Ⅲ的正反应活化能E(正) =83 kJ· mol-1,则逆反应活化能E(逆)=
3 a a
_______kJ·mol-1。
【答案】-41kJ/mol 124
【解析】由ΔH=反应物总键能-生成物总键能,ΔH=1075kJ/mol+2×463kJ/mol-(2×803kJ/mol+436kJ/
3
mol)=-41kJ/mol;根据ΔH= E(正)- E(逆),则E(逆)= E(正)- ΔH =83kJ/mol-(-41kJ/mol)=124 kJ·mol-1。
a a a a 3
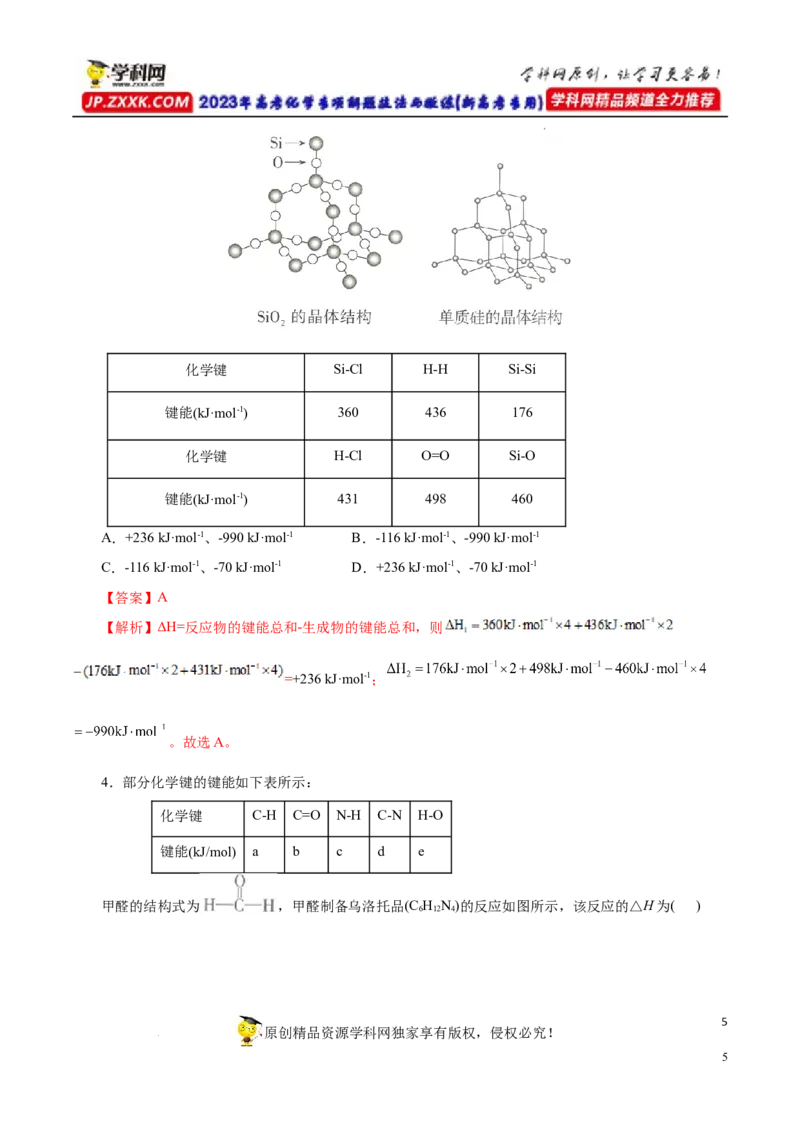
14.参考以下表格中的键能数据,回答下列问题:
化学键 Si—O Si—Cl H—H H—Cl Si—Si Si—C
键能/kJ·mo1-1 460 360 436 431 176 347
(2)比较下列两组物质的熔点高低(填“>”或“<”):SiC_______Si;SiCl _______SiO。
4 2
(3)能不能根据键能的数据判断晶体硅和化合物SiCl 的熔点高低?_______(填“能”或“不能”),理
4
由是_______。
(4)工业上高纯硅可通过下列反应制取:SiCl (g)+2H(g)=Si(s)+4HCl(g)。计算该反应的反应热△H为
4 2
_______kJ/mol。
【答案】(1) > <
(2)不能 晶体硅是原子晶体,它的熔点与共价键的强度有直接关系,而四氯化碳是分子晶体,
它的熔点与分子间作用力的大小有关,所以不能用键能比较它们熔点的高低
(3)236
【解析】(1)碳化硅和硅都是原子晶体,晶体类型相同的物质其熔点与键长成正比,键长越长,键能越
小,熔点越低,碳化硅的键长小于硅硅键长,所以碳化硅的熔点比硅的高;二氧化硅是原子晶体,氯化硅
是分子晶体,原子晶体的熔点高于分子晶体,所以二氧化硅的熔点比氯化硅的高;(2)物质熔点高低由构成
物质的微粒间作用力决定,单质Si属于原子晶体,原子间作用力是共价键;SiCl 属于分子晶体,分子间作
4
用力是范德华力,比共价键弱得多.因此不能都根据键能来判断物质的熔点高低;物质熔点高低由构成物
质的微粒间作用力决定,单质Si属于原子晶体,原子间作用力是共价键;SiCl 属于分子晶体,分子间作用
4
力是范德华力,比共价键弱得多,因此不能都根据键能来判断物质的熔点高低。(3)化学反应方程式中的反
应热=反应物的键能之和-生成物的键能之和,因此ΔH=360kJ/mol×4+436kJ/mol×2-176kJ/mol×2-431kJ/
10
原创精品资源学科网独家享有版权,侵权必究!
10
学科网(北京)股份有限公司mol×4=+236 kJ/mol。
11
原创精品资源学科网独家享有版权,侵权必究!
11
学科网(北京)股份有限公司12
原创精品资源学科网独家享有版权,侵权必究!
12
学科网(北京)股份有限公司