文档内容
第五篇 水溶液中的离子反应与平衡
专项 32 分布系数图象
随着新高考的全面实施,分布系数图象已成为水溶液中的离子平衡的高考新宠。分布系数图象简称分
布曲线,是指以pH为横坐标,分布系数即组分的平衡浓度占总浓度的分数为纵坐标,分布系数与溶液 pH
之间的关系曲线。命题设计新颖灵活,综合性强,难度较大。涉及内容主要有:电解质相对强弱的判断,
离子浓度的变化或定量计算,pH的计算,水解平衡的强弱判断或粒子浓度大小比较等。题目注重考查考生
的读图识表能力、逻辑推理能力以及分析问题和解决问题的能力。
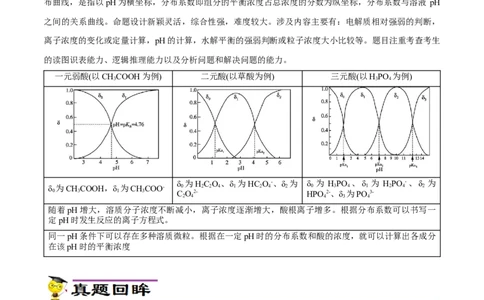
一元弱酸(以CHCOOH为例) 二元酸(以草酸为例) 三元酸(以HPO 为例)
3 3 4
δ 为HC O 、δ 为HC O-、δ 为 δ 为 HPO 、δ 为 HPO -、δ 为
δ 为CHCOOH,δ 为CHCOO- 0 2 2 4 1 2 4 2 0 3 4 1 2 4 2
0 3 1 3 C O2- HPO 2-、δ 为PO 3-
2 4 4 3 4
随着pH增大,溶质分子浓度不断减小,离子浓度逐渐增大,酸根离子增多。根据分布系数可以书写一
定pH时发生反应的离子方程式。
同一pH条件下可以存在多种溶质微粒。根据在一定pH时的分布系数和酸的浓度,就可以计算出各成分
在该pH时的平衡浓度
1.(2022•辽宁省选择性考试)甘氨酸(NH CHCOOH)是人体必需氨基酸之一、在 时,
2 2
NH +CHCOOH、NH +CHCOO-和NH CHCOO-的分布分数【如 】与溶液
3 2 3 2 2 2
关系如图。下列说法错误的是( )A.甘氨酸具有两性
B.曲线c代表NH CHCOO-
2 2
C.NH +CHCOO-+H O NH +CHCOOH+OH-的平衡常数K=10-11.65
3 2 2 3 2
D.c 2(NH +CHCOO-)<c(NH +CHCOOH) · c(NH2CHCOO-)
3 2 3 2 2
【答案】D
【解析】A项,NH CHCOOH中存在-NH 和-COOH,所以溶液既有酸性又有碱性,故A正确;B项,
2 2 2
氨基具有碱性,在酸性较强时会结合氢离子,羧基具有酸性,在碱性较强时与氢氧根离子反应,故曲线a
表示NH +CHCOOH的分布分数随溶液pH的变化,曲b表示NH +CHCOO-的分布分数随溶液pH的变化,
3 2 3 2
曲线c表示NH CHCOO-的分布分数随溶液pH的变化,故B正确;C项,NH +CHCOO-+H O
2 2 3 2 2
NH +CHCOOH+OH-的平衡常数 , 时,根据a,b曲线交点坐标(2.35,
3 2
0.50)可知,pH=2.35时,c(NH +CHCOO-)=c(NH +CHCOOH),则 ,故C正确;
3 2 3 2
D项,由C项分析可知, ,根据b,c曲线交点坐标坐标(9.78,0.50)分析可得电离
平衡NH +CHCOO- NH CHCOO-+H+的电离常数为K=10-9.78, ,
3 2 2 2 1则 ,即c 2(NH +CHCOO-)>c(NH +CHCOOH) ·
3 2 3 2
c(NH CHCOO-),故D错误;故选D。
2 2
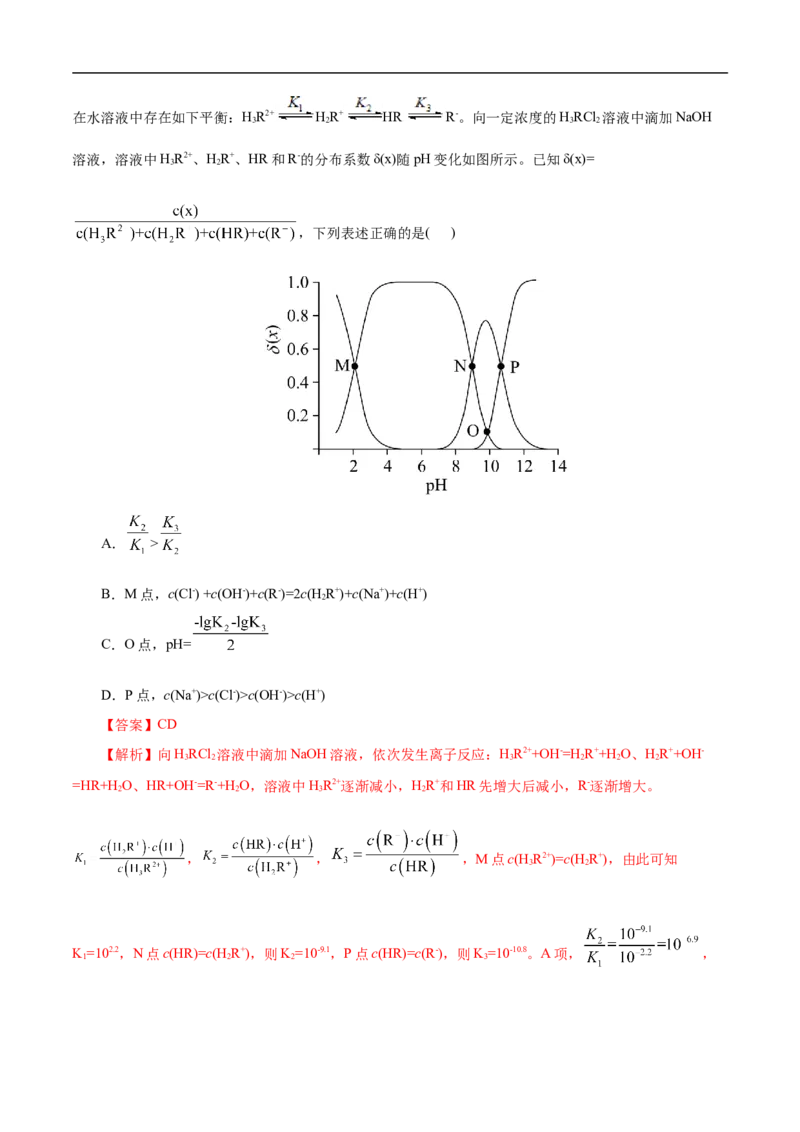
2.(2021•浙江6月选考)取两份10mL 0.05mol·Lˉ1的NaHCO 溶液,一份滴加0.05mol·Lˉ1的盐酸,另
3
一份滴加0.05mol·Lˉ1 NaOH溶液,溶液的pH随加入酸(或碱)体积的变化如图。
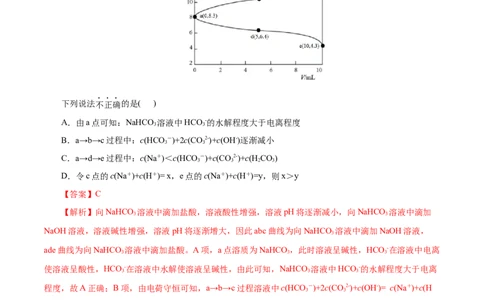
下列说法不正确的是( )
A.由a点可知:NaHCO 溶液中HCO -的水解程度大于电离程度
3 3
B.a→b→c过程中:c(HCO -)+2c(CO2-)+c(OH-)逐渐减小
3 3
C.a→d→e过程中:c(Na+)<c(HCO -)+c(CO2-)+c(H CO)
3 3 2 3
D.令c点的c(Na+)+c(H+)= x,e点的c(Na+)+c(H+)=y,则x>y
【答案】C
【解析】向NaHCO 溶液中滴加盐酸,溶液酸性增强,溶液pH将逐渐减小,向NaHCO 溶液中滴加
3 3
NaOH溶液,溶液碱性增强,溶液pH将逐渐增大,因此abc曲线为向NaHCO 溶液中滴加NaOH溶液,
3
ade曲线为向NaHCO 溶液中滴加盐酸。A项,a点溶质为NaHCO ,此时溶液呈碱性,HCO -在溶液中电离
3 3 3
使溶液呈酸性,HCO -在溶液中水解使溶液呈碱性,由此可知,NaHCO 溶液中HCO -的水解程度大于电离
3 3 3
程度,故A正确;B项,由电荷守恒可知,a→b→c过程溶液中c(HCO -)+2c(CO2-)+c(OH-)= c(Na+)+c(H
3 3
+),滴加NaOH溶液的过程中c(Na+)保持不变,c(H+)逐渐减小,因此c(HCO -)+2c(CO2-)+c(OH-)逐渐减小,
3 3
故B正确;C项,由物料守恒可知,a点溶液中c(Na+)=c(HCO -)+c(CO2-)+c(H CO),向NaHCO 溶液中滴
3 3 2 3 3
加盐酸过程中有CO 逸出,因此a→d→e过程中c(Na+)>c(HCO -)+c(CO2-)+c(H CO),故C错误;D项,
2 3 3 2 3
c点溶液中c(Na+)+c(H+)=(0.05+10-11.3)mol/L,e点溶液体积增大1倍,此时溶液中c(Na+)+c(H+)=(0.025+10-
4)mol/L,因此x>y,故D正确;故选C。
3.(2021•山东卷)赖氨酸[H N+(CH)CH(NH)COO-,用HR表示]是人体必需氨基酸,其盐酸盐(H RCl )
3 2 4 2 3 2在水溶液中存在如下平衡:HR2+ HR+ HR R-。向一定浓度的HRCl 溶液中滴加NaOH
3 2 3 2
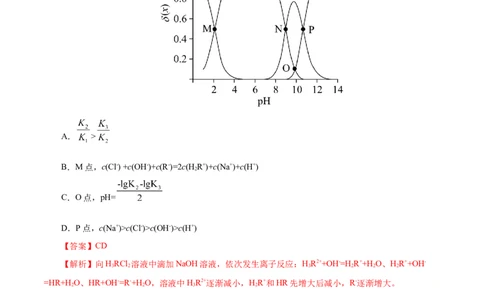
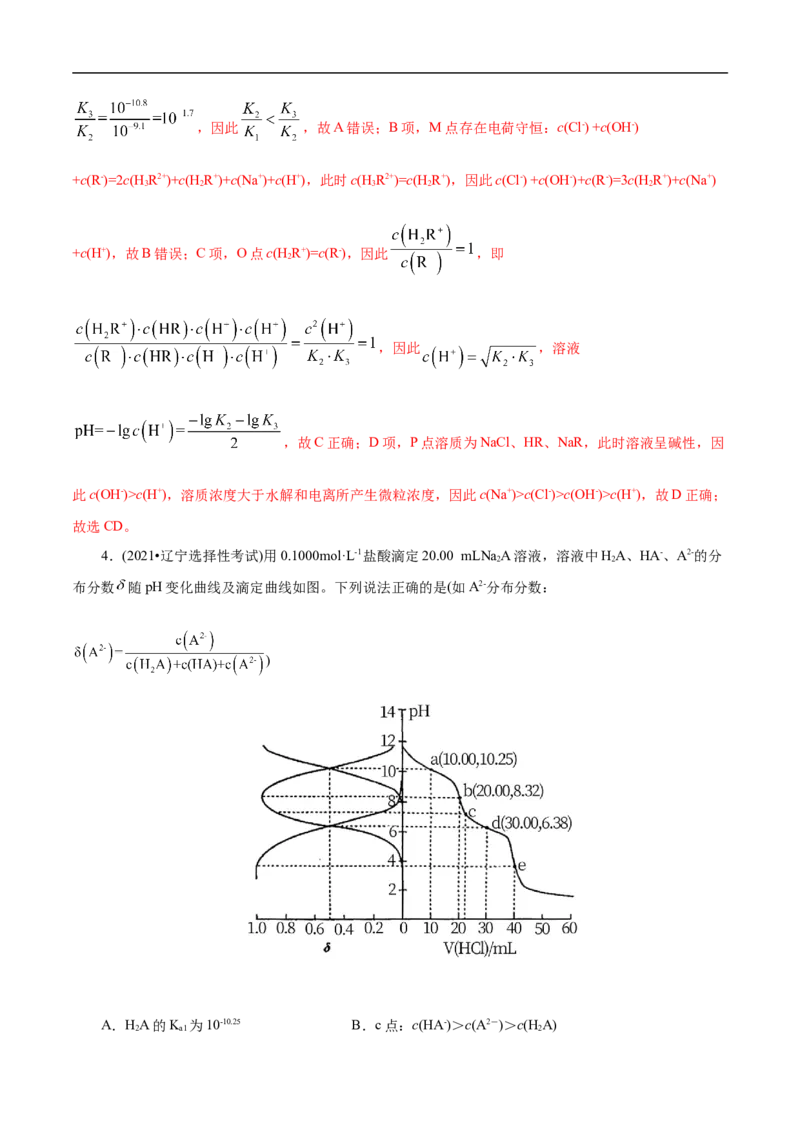
溶液,溶液中HR2+、HR+、HR和R-的分布系数δ(x)随pH变化如图所示。已知δ(x)=
3 2
,下列表述正确的是( )
A. >
B.M点,c(Cl-) +c(OH-)+c(R-)=2c(H R+)+c(Na+)+c(H+)
2
C.O点,pH=
D.P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
【答案】CD
【解析】向HRCl 溶液中滴加NaOH溶液,依次发生离子反应:HR2++OH-=H R++H O、HR++OH-
3 2 3 2 2 2
=HR+H O、HR+OH-=R-+H O,溶液中HR2+逐渐减小,HR+和HR先增大后减小,R-逐渐增大。
2 2 3 2
, , ,M点c(H R2+)=c(H R+),由此可知
3 2
K=102.2,N点c(HR)=c(H R+),则K=10-9.1,P点c(HR)=c(R-),则K=10-10.8。A项, ,
1 2 2 3,因此 ,故A错误;B项,M点存在电荷守恒:c(Cl-) +c(OH-)
+c(R-)=2c(H R2+)+c(H R+)+c(Na+)+c(H+),此时c(H R2+)=c(H R+),因此c(Cl-) +c(OH-)+c(R-)=3c(H R+)+c(Na+)
3 2 3 2 2
+c(H+),故B错误;C项,O点c(H R+)=c(R-),因此 ,即
2
,因此 ,溶液
,故C正确;D项,P点溶质为NaCl、HR、NaR,此时溶液呈碱性,因
此c(OH-)>c(H+),溶质浓度大于水解和电离所产生微粒浓度,因此c(Na+)>c(Cl-)>c(OH-)>c(H+),故D正确;
故选CD。
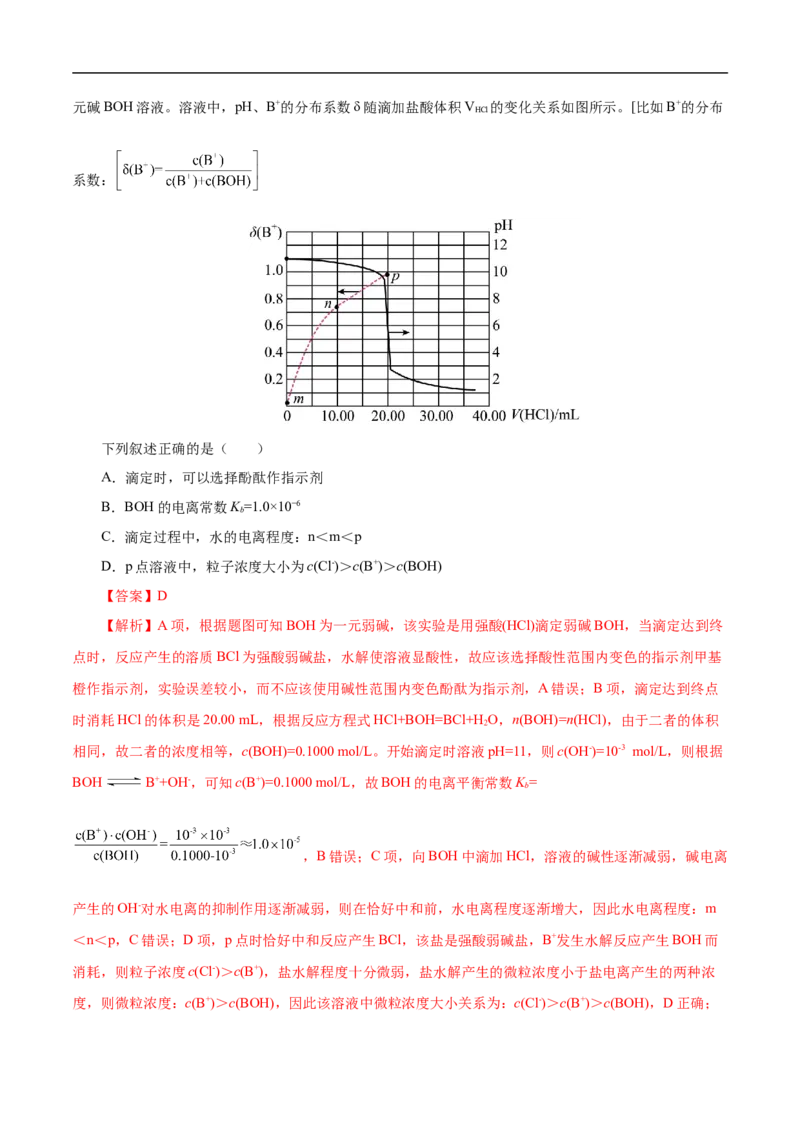
4.(2021•辽宁选择性考试)用0.1000mol·L-1盐酸滴定20.00 mLNa A溶液,溶液中HA、HA-、A2-的分
2 2
布分数 随pH变化曲线及滴定曲线如图。下列说法正确的是(如A2-分布分数:
)
A.HA的K 为10-10.25 B.c点:c(HA-)>c(A2-)>c(H A)
2 a1 2C.第一次突变,可选酚酞作指示剂 D.c (NaA)= 0.2000mol·L-1
2
【答案】C
【解析】用0.1000mol·L-1盐酸滴定20.00 mLNa A溶液,pH较大时A2-的分布分数 最大,随着pH的
2
减小,A2-的分布分数 逐渐减小,HA-的分布分数 逐渐增大,恰好生成NaHA之后,HA-的分布分数 逐
渐减小,HA的分布分数 逐渐增大,表示HA、HA-、A2-的分布分数 的曲线如图所示,
2 2
。A项,HA的 ,根据上图交点
2
1计算可知K =10-6.38,A错误;B项,根据图像可知c点中c(HA-)>c(H A)>c(A2-),B错误;C项,根据
a1 2
图像可知第一次滴定突跃溶液呈碱性,所以可以选择酚酞做指示剂,C正确;D项,根据图像e点可知,
当加入盐酸40mL时,全部生成HA,根据NaA+2HCl=2NaCl+H A计算可知c (Na A)= 0.1000mol·L-1,D
2 2 2 2
错误;故选C。
分布系数图像
分布曲线是指以pH为横坐标,分布系数即组分的平衡浓度占总浓度的分数为纵坐标,分布系数与溶
液pH之间的关系曲线。
举例 一元弱酸(以CHCOOH为例) 二元酸(以草酸为例) 三元酸(以HPO 为例)
3 3 4弱电解质分布
系数图
δ 为HPO 分布系数、δ 为
0 3 4 1
δ 为HC O 分布系数、
0 2 2 4
δ、δ 分别为CHCOOH、 HPO分布系数、δ 为HPO
0 1 3 2 2
δ δ 为HC O分布系数、δ
1 2 2
CHCOO-分布系数 分布系数、δ 为PO分布系
3 3
为C O分布系数
2
数
当溶液的pH=2时δ=δ,
0 1
当pH<pK 时,主要存在形 当溶液的pH=1.2时δ= pH=7.1时δ=δ,pH=
a 0 1 2
式是CHCOOH;当pH>pK δ,pH=4.2时δ=δ; 12.2时δ=δ;当pH<2
3 a 1 1 2 2 3
时,主要存在形式是 当pH<1.2时,HC O 时,HPO 占优势;在2<
2 2 4 3 4
含义 CHCOO-。 占优势;在1.2<pH< pH<7.1区间,HPO占优
3 2
δ 与δ 曲线相交在δ=δ= 4.2区间,HC O占优 势;在7.1<pH<12.2区
0 1 0 1 2
0.5处,此时c(CHCOOH)= 势;而当pH>4.2时, 间,HPO占优势;而当pH
3
c(CHCOO-),即pH=pK C O为主要存在形式 >12.2时,PO为主要存在
3 a 2
形式
pH由2到6发生反应的离子 pH由4到6发生反应的 pH由11到14发生反应的
离子方程式 方程式:CHCOOH+OH- 离子方程式:HC O+OH 离子方程式:HPO+OH-
3 2
===CH COO-+HO -===C O+HO ===PO+HO
3 2 2 2 2
K(CHCOOH)=,
3
K (H PO )=,从图可知,
3 3 4
从图可知,c(CHCOO-)= K (H C O)=,从图可
3 2 2 2 4
c(HPO)=c(PO)时pH=
c(CHCOOH)时pH=pK= 知,c(C O)=c(HC O)时
3 2 2
求lgK 12.2,K =c(H+)=10-12.2,
3
4.76。K(CHCOOH)=c(H+) pH=4.2,K =c(H+)=10
3 2
lg K
a
=10-4.76,lg K(CHCOOH)= -4.2,lg K =-4.2
3 2
=-12.2
-4.76
1.(2023届·辽宁省六校高三开学考试)常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的一元碱BOH溶液。溶液中,pH、B+的分布系数δ随滴加盐酸体积V 的变化关系如图所示。[比如B+的分布
HCl
系数:
下列叙述正确的是( )
A.滴定时,可以选择酚酞作指示剂
B.BOH的电离常数K =1.0×10−6
b
C.滴定过程中,水的电离程度:n<m<p
D.p点溶液中,粒子浓度大小为c(Cl-)>c(B+)>c(BOH)
【答案】D
【解析】A项,根据题图可知BOH为一元弱碱,该实验是用强酸(HCl)滴定弱碱BOH,当滴定达到终
点时,反应产生的溶质BCl为强酸弱碱盐,水解使溶液显酸性,故应该选择酸性范围内变色的指示剂甲基
橙作指示剂,实验误差较小,而不应该使用碱性范围内变色酚酞为指示剂,A错误;B项,滴定达到终点
时消耗HCl的体积是20.00 mL,根据反应方程式HCl+BOH=BCl+H O,n(BOH)=n(HCl),由于二者的体积
2
相同,故二者的浓度相等,c(BOH)=0.1000 mol/L。开始滴定时溶液pH=11,则c(OH-)=10-3 mol/L,则根据
BOH B++OH-,可知c(B+)=0.1000 mol/L,故BOH的电离平衡常数K =
b
,B错误;C项,向BOH中滴加HCl,溶液的碱性逐渐减弱,碱电离
产生的OH-对水电离的抑制作用逐渐减弱,则在恰好中和前,水电离程度逐渐增大,因此水电离程度:m
<n<p,C错误;D项,p点时恰好中和反应产生BCl,该盐是强酸弱碱盐,B+发生水解反应产生BOH而
消耗,则粒子浓度c(Cl-)>c(B+),盐水解程度十分微弱,盐水解产生的微粒浓度小于盐电离产生的两种浓
度,则微粒浓度:c(B+)>c(BOH),因此该溶液中微粒浓度大小关系为:c(Cl-)>c(B+)>c(BOH),D正确;故选D。
2.(2022·福建省漳州市高毕业班一模)边搅拌边向NaCO 溶液中通入SO 制备NaHSO 溶液,水溶液
2 3 2 3
中HSO 、HSO -、SO 2-的分布系数δ随pH的变化关系如图所示。[比如HSO 的分布系数: δ (H SO ) =
2 3 3 3 2 3 2 3
],下列有关叙述错误的是( )
A.当溶液pH范围为4~5时,停止通入SO
2
B.根据曲线数据计算可知K (H SO )的数量级为10-7
a2 2 3
C.a点的溶液中c(H+)+c(Na+)=c(OH—)+c( HSO -)+2c(SO 2-)+c( HCO-) +2c(CO2-)
3 3 3 3
D.pH=3的溶液中,c(Na+)<c(HSO -)+c(H SO )
3 2 3
【答案】B
【解析】A项,由图可知,当溶液pH范围为4~5时,二氧化硫与碳酸钠恰好反应生成亚硫酸氢钠,
则当溶液pH范围为4~5时,停止通入二氧化硫,故A正确;B项,由图可知,当溶液中c(HSO -)=c(SO 2-)
3 3
时,溶液pH为7.2,则K (H SO )= = c(H+)=10—7.2,则K (H SO )的数量级为10-8,故B错
a2 2 3 a2 2 3
误;C项,由图可知,a点为亚硫酸氢钠、亚硫酸和碳酸的混合溶液,溶液中存在电荷守恒关系c(H+)
+c(Na+)=c(OH—)+c( HSO -)+2c(SO 2-)+c( HCO-) +2c(CO2-),故C正确;D项,由图可知,pH=3的溶液为亚
3 3 3 3
硫酸氢钠、亚硫酸和碳酸的混合溶液,由物料守恒可知,溶液中c(Na+)<c(HSO -)+c(H SO ),故D正确;
3 2 3
故选B。
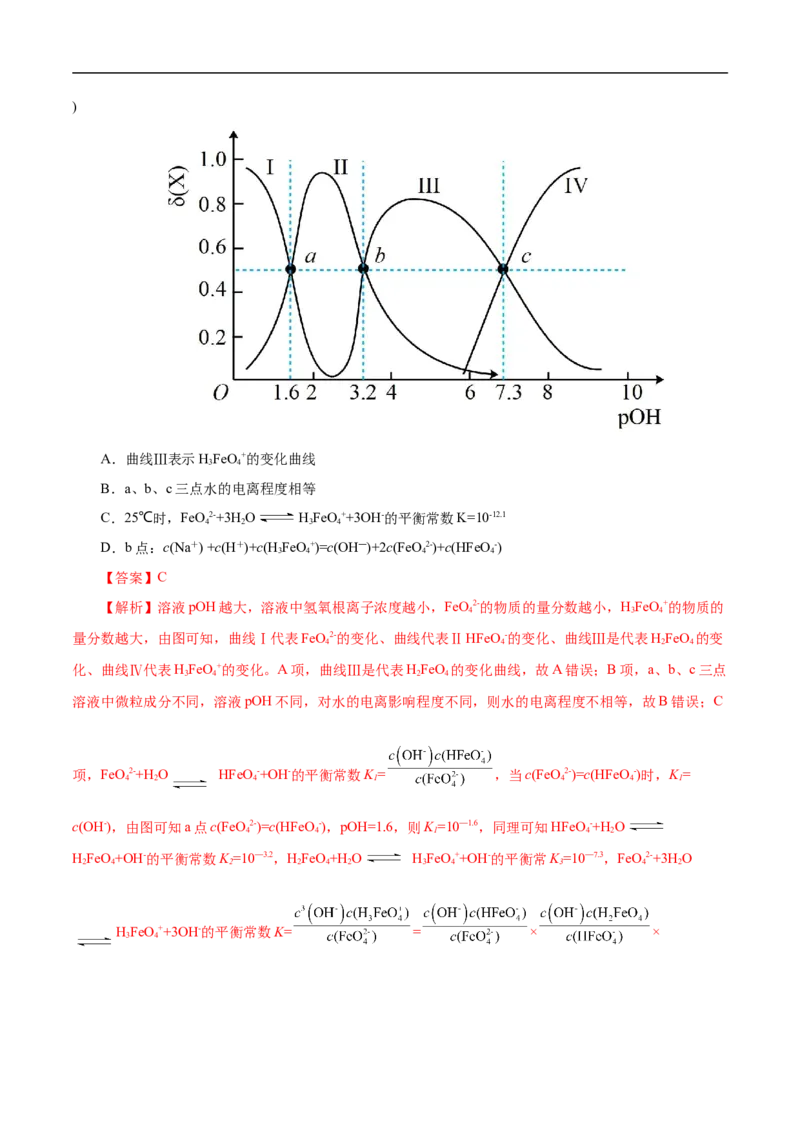
3.(2022·辽宁省实验中学模拟预测)常温下,将一定量稀硫酸滴入高铁酸钠(Na FeO)溶液中,溶液中
2 4
含铁微粒FeO2-、HFeO -、HFeO、HFeO+的物质的量分数 随pOH的变化如图。下列说法正确的是(
4 4 2 4 3 4)
A.曲线Ⅲ表示HFeO+的变化曲线
3 4
B.a、b、c三点水的电离程度相等
C.25℃时,FeO2-+3H O HFeO++3OH-的平衡常数K=10-12.1
4 2 3 4
D.b点:c(Na+) +c(H+)+c(H FeO+)=c(OH―)+2c(FeO 2-)+c(HFeO -)
3 4 4 4
【答案】C
【解析】溶液pOH越大,溶液中氢氧根离子浓度越小,FeO2-的物质的量分数越小,HFeO+的物质的
4 3 4
量分数越大,由图可知,曲线Ⅰ代表FeO2-的变化、曲线代表ⅡHFeO -的变化、曲线Ⅲ是代表HFeO 的变
4 4 2 4
化、曲线Ⅳ代表HFeO+的变化。A项,曲线Ⅲ是代表HFeO 的变化曲线,故A错误;B项,a、b、c三点
3 4 2 4
溶液中微粒成分不同,溶液pOH不同,对水的电离影响程度不同,则水的电离程度不相等,故B错误;C
项,FeO2-+H O HFeO -+OH-的平衡常数K = ,当c(FeO 2-)=c(HFeO -)时,K =
4 2 4 1 4 4 1
c(OH-),由图可知a点c(FeO 2-)=c(HFeO -),pOH=1.6,则K =10—1.6,同理可知HFeO -+H O
4 4 1 4 2
HFeO+OH-的平衡常数K =10—3.2,HFeO+H O HFeO++OH-的平衡常K =10—7.3,FeO2-+3H O
2 4 2 2 4 2 3 4 3 4 2
HFeO++3OH-的平衡常数K= = × ×
3 4= K ×K ×K =10-12.1,故C正确;D项,b点溶液中c(HFeO -)= c(H FeO),溶液中存在电
1 2 3 4 2 4
荷守恒关系c(Na+)+c(H+)+c(H FeO+)=c(OH-)+2c(FeO 2-)+c(HFeO -) +2c(SO 2-),溶液中c(SO 2-)≠c(HFeO -),则
3 4 4 4 4 4 4
b点溶液中c(Na+)+c(H+)+c(H FeO+)≠c(OH-)+2c(FeO 2-)+3c(HFeO -),故D错误;故选C。
3 4 4 4
4.(2022·浙江省五校高三联考)室温下,向1.00L0.100mol/LNHHCO 溶液中加入NaOH稀溶液,溶
4 3
液中主要型体的分布系数[比如A2-的分布系数δ(A2-)= ]以及pH随n(NaOH)变化如图。
下列说法不正确的是( )
A.0.100mol/LNH HCO 溶液中 >1,水的电离受到促进
4 3
B.加入NaOH稀溶液过程中,溶液满足关系式c(NH +)+c(NH•H O)=c(CO2-)+c(HCO-)+c(H CO)
4 3 2 3 3 2 3
C.K (H CO)K (NH •H O)>K
a2 2 3 b 3 2 w
D.加入少量NaOH时,OH-主要先与NH 反应
【答案】C
【解析】A项,NH HCO =NH++HCO-,NH +和HCO -分别发生水解,HCO -+H O
4 3 4 3 4 3 3 2
HCO+OH-,NH ++H O NH ·H O+H+,因为 ,所以c(OH―)>c(H+),则说明HCO -水解程
2 3 4 2 3 2 3
度大,使水电离受到促进,故A正确;B项,NH HCO =NH++HCO-,NH +和HCO -分别发生水解,HCO -
4 3 4 3 4 3 3
+H O HCO+OH-,NH ++H O NH ·H O+H+,则由物料守恒得c(NH +)+c(NH•H O)=c(CO2-)
2 2 3 4 2 3 2 4 3 2 3+c(HCO-)+c(H CO),故B正确;C项,
3 2 3
,图中
时, ,所以 ,因此
,故C错误;D项,加入少量NaOH时,HCO -浓度基本不变,而
3
NH +浓度快速减小,所以OH-先与NH +发生主要反应,故D正确;故选C。
4 4
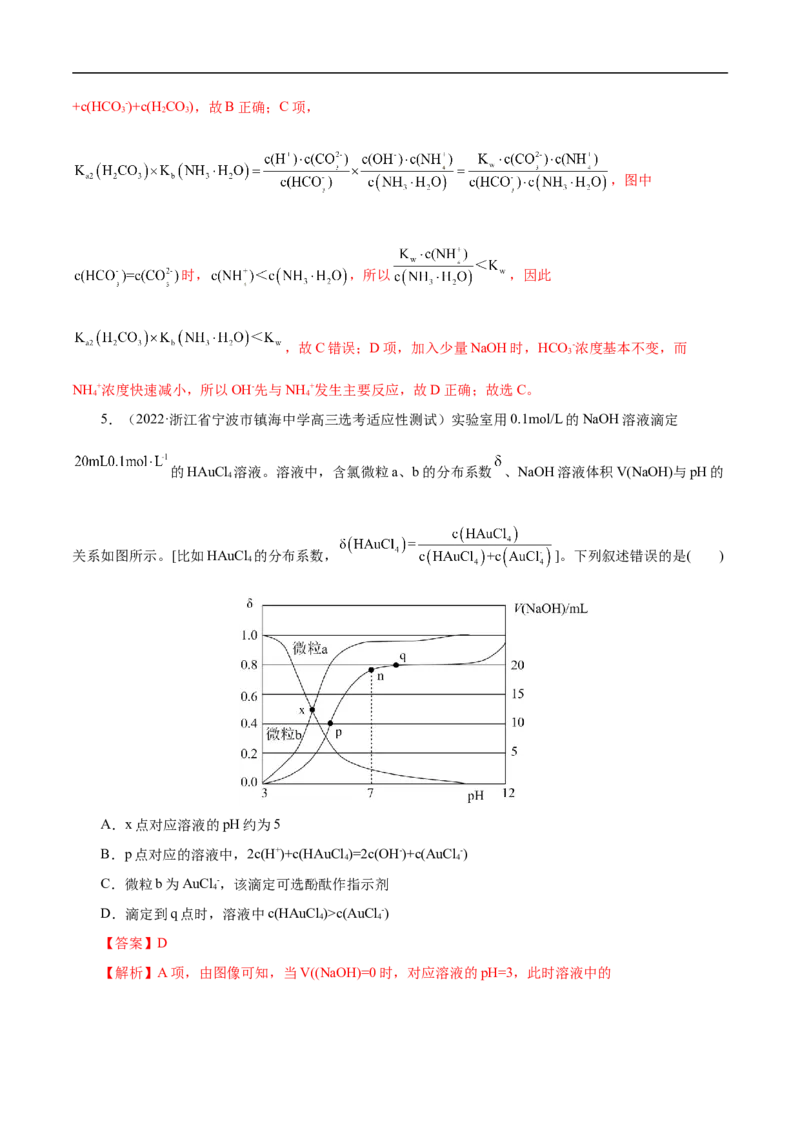
5.(2022·浙江省宁波市镇海中学高三选考适应性测试)实验室用0.1mol/L的NaOH溶液滴定
的HAuCl 溶液。溶液中,含氯微粒a、b的分布系数 、NaOH溶液体积V(NaOH)与pH的
4
关系如图所示。[比如HAuCl 的分布系数, ]。下列叙述错误的是( )
4
A.x点对应溶液的pH约为5
B.p点对应的溶液中,2c(H+)+c(HAuCl )=2c(OH-)+c(AuCl -)
4 4
C.微粒b为AuCl -,该滴定可选酚酞作指示剂
4
D.滴定到q点时,溶液中c(HAuCl )>c(AuCl -)
4 4
【答案】D
【解析】A项,由图像可知,当V((NaOH)=0时,对应溶液的pH=3,此时溶液中的c(H+)=0.001mol·L-1, ,x点时,根据图像有c(HAuCl )= c(AuCl -),
4 4
则此时的 , ,A正确;B项,p点时,V((NaOH)=10mL,根据电荷守
恒有:c(H+)+c(Na+)= c(OH-)+ c(AuCl -),根据物料守恒有:2c(Na+)= c(HAuCl )+ c(AuCl -),两式联立方程消
4 4 4
去c(Na+),解得:2c(H+)+c(HAuCl )=2c(OH-)+c(AuCl -),B正确;C项,随着NaOH的加入,HAuCl 逐渐减
4 4 4
少,AuCl -逐渐增多,结合图像可知,微粒a为HAuCl ,微粒b为AuCl -,滴定到q点时,
4 4 4
V((NaOH)=20mL,两者恰好完全反应,生成NaAuCl 溶液,此时溶液呈碱性,所以选酚酞作指示剂,C正
4
确;D项,滴定到q点时,V((NaOH)=20mL,由图可知c(AuCl -)>c(HAuCl ),D错误;故选D。
4 4
6.(2022·浙江省温州市普通高中高三适应性测试三模考试)1L0.10mol·L-1HRO 溶液pH<1,向其中
3 3
加入NaOH固体(忽略体积变化),测得溶液中各种含R微粒的物质的量分数(δ)与溶液pH的关系如图所示。
下列有关说法不正确的是( )
A.当加入0.1molNaOH时:c(Na+)=c(H RO-)+c(HRO2-)+c(RO 3-)
2 3 3 3
B.当加入0.2molNaOH时:(RO3-)>c(H RO-)
3 2 3
C.曲线δ 是指微粒HRO-的变化趋势
1 2 3
D.N点,c(HRO 2-)=c(RO 3-)=0.05mol·L-1
3 3
【答案】D
【解析】0.10mol·L-1HRO 溶液pH<1,说明其一级电离为完全电离,随着pH的增大HRO-逐渐减少,
3 3 2 3
HRO 2-逐渐增多,故δ 代表HRO-,δ 代表HRO 2-,当HRO 2-达到最大值后,浓度逐渐降低,RO3-逐渐增
3 1 2 3 2 3 3 3
加,故δ 代表RO3-。A项,当加入0.1molNaOH时,溶液为NaH RO 溶液,根据物料守恒可知,
3 3 2 3
c(Na+)=c(H RO-)+c(HRO2-)+c(RO 3-),A正确;B项,当加入0.2molNaOH时,溶液为NaHRO 溶液,由分
2 3 3 3 2 3
析可知δ 代表HRO 2-,当其为最大值时,溶液显酸性,说明HRO 2-的电离大于水解,故
2 3 3
(RO3-)>c(H RO-),B正确;C项,曲线δ 是指微粒HRO-的变化趋势,C正确;D项,最初HRO 溶液浓
3 2 3 1 2 3 3 3
度为0.10mol·L-1,由分析可知,虽然N点c(HRO 2-)=c(RO 3-),但是HRO 的二级电离和三级电离都是微弱
3 3 3 3
的,即溶液中随时都存在HRO-,故c(HRO 2-)=c(RO 3-)<0.05mol·L-1,D错误;故选D。
2 3 3 3
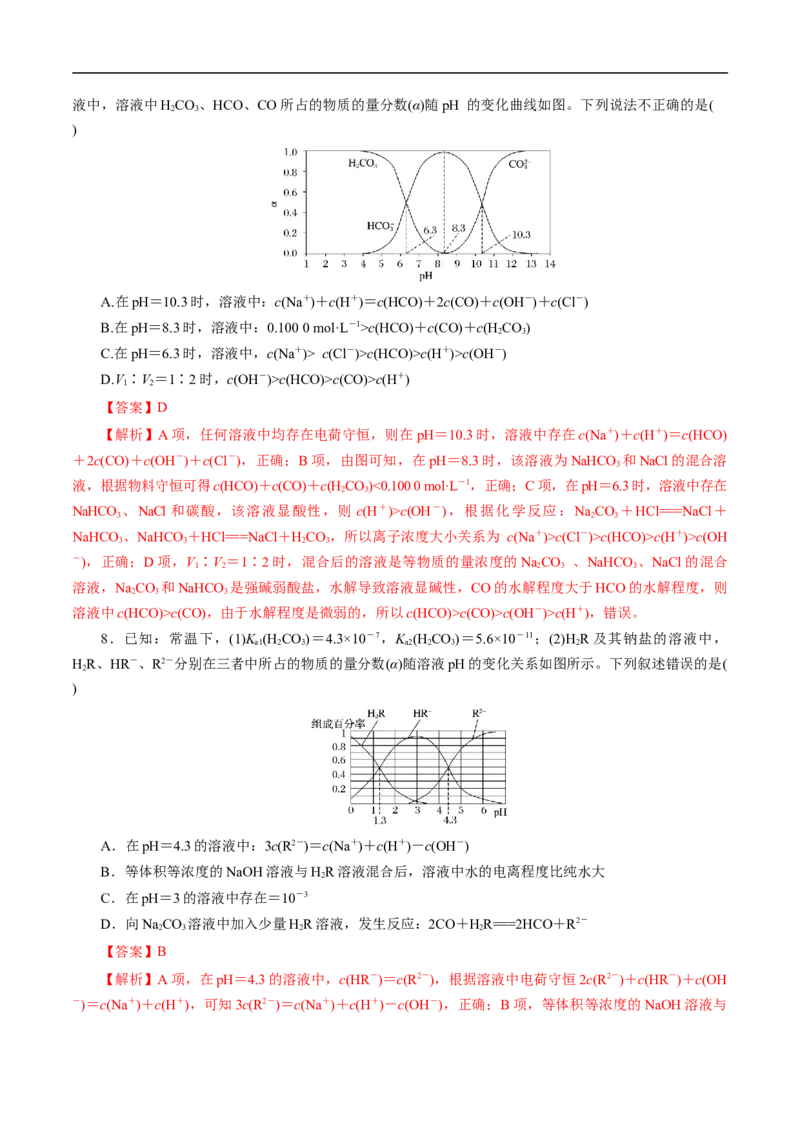
7.常温下,将体积为V 的 0.100 0 mol·L-1 HCl溶液逐滴加入体积为V 的0.100 0 mol·L-1 Na CO 溶
1 2 2 3液中,溶液中HCO 、HCO、CO所占的物质的量分数(α)随pH 的变化曲线如图。下列说法不正确的是(
2 3
)
A.在pH=10.3时,溶液中:c(Na+)+c(H+)=c(HCO)+2c(CO)+c(OH-)+c(Cl-)
B.在pH=8.3时,溶液中:0.100 0 mol·L-1>c(HCO)+c(CO)+c(H CO)
2 3
C.在pH=6.3时,溶液中,c(Na+)> c(Cl-)>c(HCO)>c(H+)>c(OH-)
D.V∶V=1∶2时,c(OH-)>c(HCO)>c(CO)>c(H+)
1 2
【答案】D
【解析】A项,任何溶液中均存在电荷守恒,则在pH=10.3时,溶液中存在c(Na+)+c(H+)=c(HCO)
+2c(CO)+c(OH-)+c(Cl-),正确;B项,由图可知,在pH=8.3时,该溶液为NaHCO 和NaCl的混合溶
3
液,根据物料守恒可得c(HCO)+c(CO)+c(H CO)<0.100 0 mol·L-1,正确;C项,在pH=6.3时,溶液中存在
2 3
NaHCO 、NaCl 和碳酸,该溶液显酸性,则 c(H+)>c(OH-),根据化学反应:NaCO +HCl===NaCl+
3 2 3
NaHCO 、NaHCO +HCl===NaCl+HCO ,所以离子浓度大小关系为 c(Na+)>c(Cl-)>c(HCO)>c(H+)>c(OH
3 3 2 3
-),正确;D项,V∶V =1∶2时,混合后的溶液是等物质的量浓度的NaCO 、NaHCO 、NaCl的混合
1 2 2 3 3
溶液,NaCO 和NaHCO 是强碱弱酸盐,水解导致溶液显碱性,CO的水解程度大于HCO的水解程度,则
2 3 3
溶液中c(HCO)>c(CO),由于水解程度是微弱的,所以c(HCO)>c(CO)>c(OH-)>c(H+),错误。
8.已知:常温下,(1)K (H CO)=4.3×10-7,K (H CO)=5.6×10-11;(2)H R及其钠盐的溶液中,
a1 2 3 a2 2 3 2
HR、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH的变化关系如图所示。下列叙述错误的是(
2
)
A.在pH=4.3的溶液中:3c(R2-)=c(Na+)+c(H+)-c(OH-)
B.等体积等浓度的NaOH溶液与HR溶液混合后,溶液中水的电离程度比纯水大
2
C.在pH=3的溶液中存在=10-3
D.向NaCO 溶液中加入少量HR溶液,发生反应:2CO+HR===2HCO+R2-
2 3 2 2
【答案】B
【解析】A项,在pH=4.3的溶液中,c(HR-)=c(R2-),根据溶液中电荷守恒2c(R2-)+c(HR-)+c(OH
-)=c(Na+)+c(H+),可知3c(R2-)=c(Na+)+c(H+)-c(OH-),正确;B项,等体积等浓度的NaOH溶液与HR溶液混合生成NaHR,此时HR-含量最高,HR和R2-含量接近于0,由题图可知,此时pH接近于3,
2 2
溶液显酸性,对水的电离起到抑制作用,所以溶液中水的电离程度比纯水小,错误;C项,当溶液pH=
1.3时,c(H R)=c(HR-),则K ==10-1.3,当溶液pH=4.3时,c(R2-)=c(HR-),则K ==10-4.3,===
2 a1 a2
10-3,正确;D项,由C选项分析可知,HR的电离常数K 大于HCO 的K ,即酸性:HR->HCO,所
2 a2 2 3 a2
以向NaCO 溶液中加入少量HR溶液,发生反应:2CO+HR===2HCO+R2-,正确。
2 3 2 2
9.(2022·江苏省如皋中学三模)水体中的As(V)可转化为Ca (AsO) 沉淀除去, As(Ⅲ)可用碘水氧
3 4 2
化为As(Ⅴ)后,再转化为Ca (AsO) 沉淀除去,已知Ksp[Ca (AsO)]=1×10-21.2、Ksp[Ca(CO )]=1×10-8.6;
3 4 2 3 4 2 3
HAsO 水溶液中含砷的各物种的分布分数与pH的关系分别如下图所示。下列说法正确的是
3 4
A.0.1mol-1NaHA O 溶液中存在:2c(Na+)=c(H A O)+c(H A O )+c(HA O )+c(A O )
2 S 4 3 S 4 2 S S S
B.用0.1mol·L-1NaCO 溶液浸泡Ca (A O) 沉淀,无CaCO 沉淀转化生成
2 3 3 S 4 2 3
C.
D.pH>13时,向NaAsO 溶液中滴加少量碘水时发生反应的离子方程式为:
2 3
【答案】C
【解析】如图所示,当 时,HAsO 的 ,同
3 4
理 , 。A项,0.1mol-1NaHA O 溶
2 S 4
液中存在物料守恒:c(Na+)=2[c(H A O)+c(H A O-)+c(HA O2-)+c(A O3-)],A错误;B项,Ca (A O) 沉淀
3 S 4 2 S 4 S 4 S 4 3 S 4 2
在溶液中存在沉淀溶解平衡:Ca (A O) 3Ca2++2A O3-,
3 S 4 2 S 4,
,用0.1mol·L-1NaCO 溶液浸泡Ca (A O) 沉淀,
2 3 3 S 4 2
,故有CaCO 沉淀转化生成,B错误;
3
C项, ,C正确;D项,pH>13时,向
NaAsO 溶液中滴加少量碘水时会发生反应:A O3-+I +H O= A O3-+2I-+2H+,但由于NaAsO 溶液过量,
2 3 S 3 2 2 S 4 2 3
生成的氢离子继续与NaAsO 反应生成HA O2-,D错误;故选C。
2 3 S 4
10.(2022·山东省济宁市三模)工业上利用NaClO将废水中的As(III)氧化为As(V),然后经吸附、沉
降而除去。As(III)和As(V)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分
数)与pH的关系如图所示。一般把10-1>K >10-4的酸称为中强酸,把K <10-4的酸称为弱酸,下列说法不正
a a
确的是( )
A.HAsO 、HAsO 都是弱酸
3 4 3 3
B.pH=10时,NaClO将As(III)氧化为As(V)的离子方程式:HAsO -+ClO-+OH-=HAsO 2-+Cl-+H O
2 3 4 2
C.HAsO -+H AsO - HAsO2-+H AsO K=102.4
2 4 2 3 4 3 3
D.相同温度下,同浓度的NaAsO 溶液与NaHAsO 溶液,前者碱性强
3 4 2 3
【答案】D
【解析】根据As(III)水溶液中含砷的各物质的分布分数知,当HAsO 与HAsO -相等时溶液的
3 3 2 3
pH=9.2,则HAsO 的K = =10-9.2;根据As(V)水溶液中含砷的各物质的分布分数知,当
3 3 a1HAsO 与HAsO -相等时溶液的pH在2~3之间,HAsO -与HAsO2-相等时溶液的pH=6.8,则HAsO 的
3 4 2 4 2 4 4 3 3
K = >10-3、K = =10-6.8。A项,一般把10-1>K >10-4的酸称为中强酸,
a1 a2 a
把K <10-4的酸称为弱酸,HAsO 的K =10-9.2<10-4,HAsO 是弱酸,A项正确;B项,pH=10时,As(III)
a 3 3 a1 3 3
主要以HAsO -形式存在,As(V)主要以HAsO2-形式存在,NaClO将HAsO -氧化成HAsO2-,自身被还原
2 3 4 2 3 4
成Cl-,根据得失电子守恒、原子守恒和电荷守恒,反应的离子方程式:HAsO -+ClO-+OH-= HAsO 2-+Cl-
2 3 4
+H O,B项正确;C项,HAsO -+ H AsO - HAsO2-+H AsO 的K= =
2 2 4 2 3 4 3 3
= = =102.4,C项正确;D.根据As(III)水溶液中含砷的各物
质的分布分数知,当HAsO -与HAsO2-相等时溶液的pH>12,HAsO 的K <10-12,根据As(V)水溶液中
2 3 3 3 3 a2
含砷的各物质的分布分数知,当HAsO2-与AsO 3-相等时溶液的pH在11~12之间,HAsO 的K >10-12>
4 4 3 4 a3
K (H AsO ),故相同温度下同浓度的NaAsO 溶液与NaHAsO 溶液,AsO 3-的水解程度小于HAsO2-的水
a2 3 3 3 4 2 3 4 3
解程度,后者碱性强,D项错误;故选D。
11.(2022·湖南省邵东市第三中学高三阶段练习)常温下,铜离子与氨分子能形成多种配合物
[Cu(NH )]2+其中配位数x=1,2,…。向一定浓度的硫酸铜溶液中加入不同量的NH 后可绘制出下图分布曲
3 x 3
线。图中横坐标为c(NH )的对数,纵坐标δ为含铜物种的分布系数(如: ,Σ
3
表示加和), 表示溶液中x的平均值。根据以上信息,下列说法错误的是A.图中曲线③为[Cu(NH )]2+的分布曲线
3 4
B.当c(NH )=10-3mol/L时, =2,说明此时溶液中的溶质为[Cu(NH )]2+
3 3 2
C.溶液始终存在c(Cu2+)+Σ c[Cu(NH )2+]=c(SO2-)
3 x 4
D.氨水与Cu2+反应得不到单一产物,故不能利用已知浓度的氨水滴定未知浓度的Cu2+
【答案】B
【解析】A项,随着lgc(NH)的增大,Cu2+浓度降低,曲线①为[Cu(NH )]2+的分布曲线,依此类推,曲
3 3
线③为[Cu(NH )]2+的分布曲线,A正确;B项,当c(NH )=10-3mol/L时,lgc(NH)=-3,根据图中曲线可知,
3 4 3 3
此时溶液中的溶质主要为[Cu(NH )]2+,而[Cu(NH )]2+与[Cu(NH )]2+相等,故 =2,只是说明
3 2 3 3 3
中的x为2,B错误;C项,根据物料守恒有c(Cu2+)+ [Cu(NH )]2++[Cu(NH)]2++[Cu(NH)]2+
3 3 2 3 3
+[Cu(NH)]2+= c(SO 2-),而Σ c[Cu(NH )2+]= [Cu(NH )]2++[Cu(NH)]2++[Cu(NH)]2++[Cu(NH)]2+,故溶液始
3 4 4 3 x 3 3 2 3 3 3 4
终存在c(Cu2+)+Σ c[Cu(NH )2+]=c(SO2-),C正确;D项,氨水与Cu2+反应可得到Cu(OH) 、[Cu(NH )]2+、
3 x 4 2 3
[Cu(NH )]2+、[Cu(NH )]2+、[Cu(NH )]2+等,得不到单一产物,故不能利用已知浓度的氨水滴定未知浓度的
3 2 3 3 3 4
Cu2+,D正确;故选B。
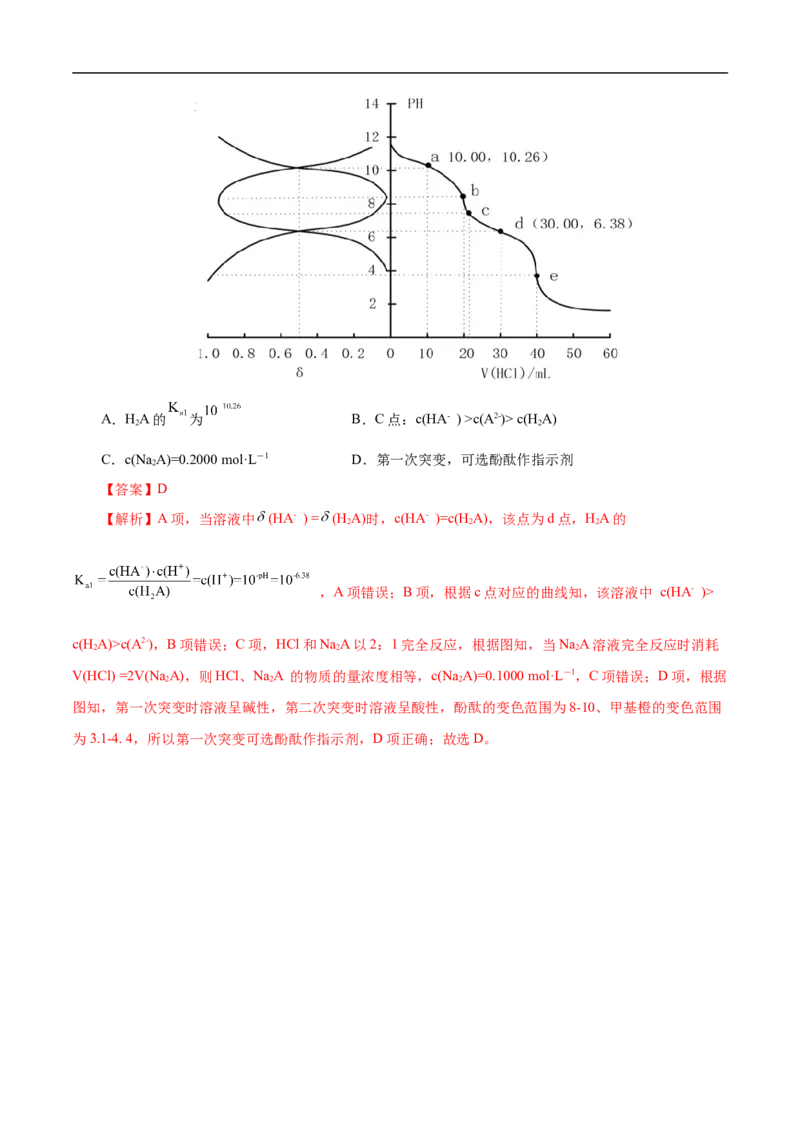
12.(2022·浙江省东阳市高三选考模拟考试)用0.1000 盐酸滴定20.00 NaA溶液,溶液中
2
HA、HA-、A2-的分布分数 随pH变化曲线及滴定曲线如图。下列说法正确的是( )
2A.HA的 为 B.C点:c(HA- ) >c(A2-)> c(HA)
2 2
C.c(Na A)=0.2000 mol·L-1 D.第一次突变,可选酚酞作指示剂
2
【答案】D
【解析】A项,当溶液中 (HA- ) = (H A)时,c(HA- )=c(H A),该点为d点,HA的
2 2 2
,A项错误;B项,根据c点对应的曲线知,该溶液中 c(HA- )>
c(HA)>c(A2-),B项错误;C项,HCl和NaA以2:1完全反应,根据图知,当NaA溶液完全反应时消耗
2 2 2
V(HCl) =2V(Na A),则HCl、NaA 的物质的量浓度相等,c(Na A)=0.1000 mol·L-1,C项错误;D项,根据
2 2 2
图知,第一次突变时溶液呈碱性,第二次突变时溶液呈酸性,酚酞的变色范围为8-10、甲基橙的变色范围
为3.1-4. 4,所以第一次突变可选酚酞作指示剂,D项正确;故选D。