文档内容
第六篇 物质结构与性质
专项 41 螯合物
为了考查考生的迁移能力,近年来试题中常出现螯合物,此类题起点高,落点低,加大获取信息和信
息转换能力的考查力度,能有效缩短现代科技成就与教材呈现知识之间的距离,拓展了命题空间。螯合物
是具有环状结构的配合物,是通过两个或多个配位体与同一金属离子形成螯合环的螯合作用而得到。螯合
物是配合物的一种,在螯合物的结构中,一定有一个或多个多齿配体提供多对电子与中心体形成配位
键。"螯"指螃蟹的大钳,此名称比喻多齿配体像螃蟹一样用两只大钳紧紧夹住中心体。螯合物通常比一般
配合物要稳定。从配合物的研究可知,具有五元环或六元环的螯合物很稳定,而且所形成的环越多,螯合
物越稳定。
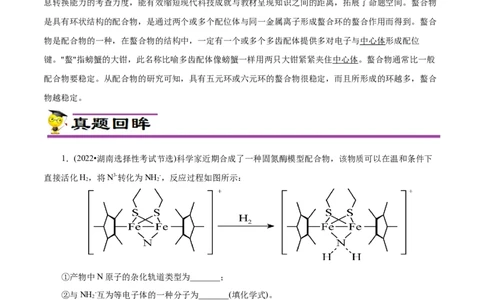
1.(2022•湖南选择性考试节选)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下
直接活化H,将N3-转化为NH -,反应过程如图所示:
2 2
①产物中N原子的杂化轨道类型为_______;
②与NH -互为等电子体的一种分子为_______(填化学式)。
2
【答案】 sp3杂化 HO
2
【解析】①由结构简式可知,产物中氮原子的价层电子对数为4,原子的杂化方式为sp3杂化;②水分
子和氨基阴离子的原子个数都为3、价电子数都为8,互为等电子体。
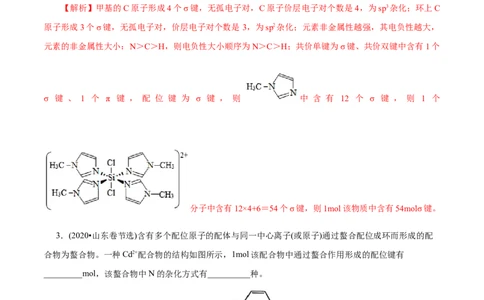
2.(2021•湖南选择性考试节选)SiCl 与N﹣甲基咪唑( )反应可以得到M2+,其结构如图所
4
示:N﹣甲基咪唑分子中碳原子的杂化轨道类型为 ,H、C、N的电负性由大到小的顺序为
,1个M2+中含有 个σ键;
【答案】sp2、sp3 N>C>H 54
【解析】甲基的C原子形成4个σ键,无孤电子对,C原子价层电子对个数是4,为sp3杂化;环上C
原子形成3个σ键,无孤电子对,价层电子对个数是 3,为sp2杂化;元素非金属性越强,其电负性越大,
元素的非金属性大小:N>C>H,则电负性大小顺序为N>C>H;共价单键为σ键、共价双键中含有1个
σ 键 、 1 个 π 键 , 配 位 键 为 σ 键 , 则 中 含 有 12 个 σ 键 , 则 1 个
分子中含有12×4+6=54个σ键,则1mol该物质中含有54molσ键。
3.(2020•山东卷节选)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配
合物为螯合物。一种Cd2+配合物的结构如图所示,1mol该配合物中通过螯合作用形成的配位键有
_________mol,该螯合物中N的杂化方式有__________种。
【答案】6 1
【解析】由该物质的结构简式和分析,根据题意“含有多个配位原子的配体与同一中心离子或原子通过螯合配位成环而形成的配合物为螯合物”,故该配合物中通过螯合作用形成的配位键有6mol,Cd—NO 那
2
个不算;该螯合物中N原子的杂化方式都是sp2杂化,故该物质中N的杂化方式有1种。
①认真阅读题干,沟通新旧知识;②针对问题,全力寻找突破口;③积极联想类比,实现知识迁移。
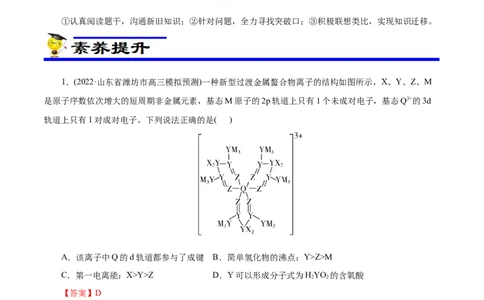
1.(2022·山东省潍坊市高三模拟预测)一种新型过渡金属螯合物离子的结构如图所示,X、Y、Z、M
是原子序数依次增大的短周期非金属元素,基态M原子的2p轨道上只有1个未成对电子,基态Q3+的3d
轨道上只有1对成对电子。下列说法正确的是( )
A.该离子中Q的d轨道都参与了成键 B.简单氢化物的沸点:Y>Z>M
C.第一电离能:X>Y>Z D.Y可以形成分子式为HYO 的含氧酸
2 2
【答案】D
【解析】X、Y、Z、M是原子序数依次增大的短周期非金属元素,基态M原子的2p轨道上只有1个
未成对电子,离子结构中M只形成1个共价键,M为F;基态Q3+的3d轨道上只有1对成对电子,Q为
Co;X只形成1个共价键,X为H;Y形成4个共价键,Y为C;Z形成3个共价键,Z为N,综上分析,
X、Y、Z、M、Q分别为H、C、N、F、Co。A项,Co3+的价电子排布为3d6,其d轨道并没有全部参与成
键,还有空的s轨道、p轨道参与成键,A错误;B项,Y、Z、M分别为C、N、F,简单氢化物分别为
CH、NH 、HF,氨气和氟化氢都存在分子间氢键,F的电负性强于N,甲烷分子间不存在分子间氢键,因
4 3
此简单氢化物沸点:HF>NH >CH ,B错误;C项,X、Y、Z分别为H、C、N,其第一电离能由高到低顺
3 4序为:N>C>H,C错误;D项,Y为C,可形成含氧酸甲酸(HCOOH),其分子式为:HCO,D正确;故
2 2
选D。
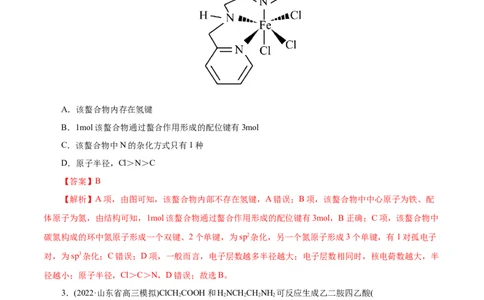
2.(2022·湖北省八市高三联考模拟)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成
环而形成的配合物为螯合物,一种 配合物的结构如图所示,下列说法正确的是
A.该螯合物内存在氢键
B.1mol该螯合物通过螯合作用形成的配位键有3mol
C.该螯合物中N的杂化方式只有1种
D.原子半径,Cl>N>C
【答案】B
【解析】A项,由图可知,该螯合物内部不存在氢键,A错误;B项,该螯合物中中心原子为铁、配
体原子为氮,由结构可知,1mol该螯合物通过螯合作用形成的配位键有3mol,B正确;C项,该螯合物中
碳氮构成的环中氮原子形成一个双键、2个单键,为sp2杂化,另一个氮原子形成3个单键,有1对孤电子
对,为sp3杂化;C错误;D项,一般而言,电子层数越多半径越大;电子层数相同时,核电荷数越大,半
径越小;原子半径,Cl>C>N,D错误;故选B。
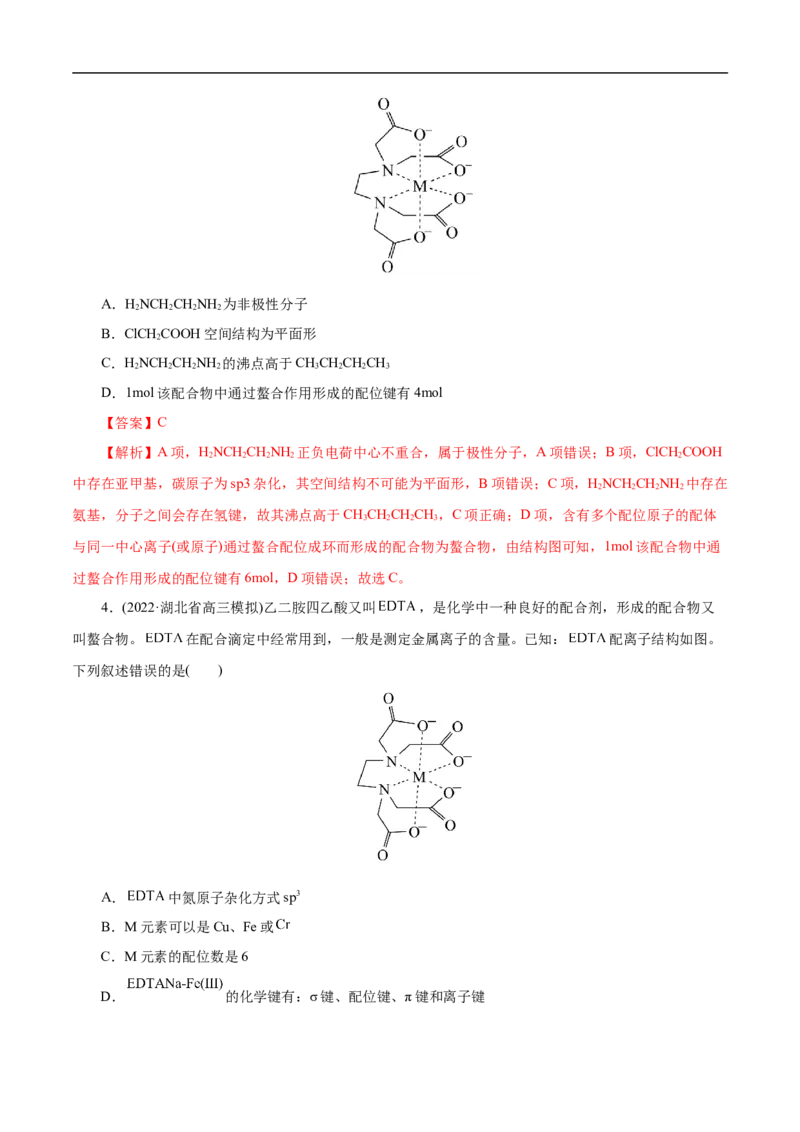
3.(2022·山东省高三模拟)ClCHCOOH和HNCH CHNH 可反应生成乙二胺四乙酸(
2 2 2 2 2
),乙二胺四乙酸与金属阳离子形成配合物的结构如图所示。已知含有
多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。下列说法正确
的是( )A.HNCH CHNH 为非极性分子
2 2 2 2
B.ClCHCOOH空间结构为平面形
2
C.HNCH CHNH 的沸点高于CHCHCHCH
2 2 2 2 3 2 2 3
D.1mol该配合物中通过螯合作用形成的配位键有4mol
【答案】C
【解析】A项,HNCH CHNH 正负电荷中心不重合,属于极性分子,A项错误;B项,ClCHCOOH
2 2 2 2 2
中存在亚甲基,碳原子为sp3杂化,其空间结构不可能为平面形,B项错误;C项,HNCH CHNH 中存在
2 2 2 2
氨基,分子之间会存在氢键,故其沸点高于CHCHCHCH,C项正确;D项,含有多个配位原子的配体
3 2 2 3
与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物,由结构图可知,1mol该配合物中通
过螯合作用形成的配位键有6mol,D项错误;故选C。
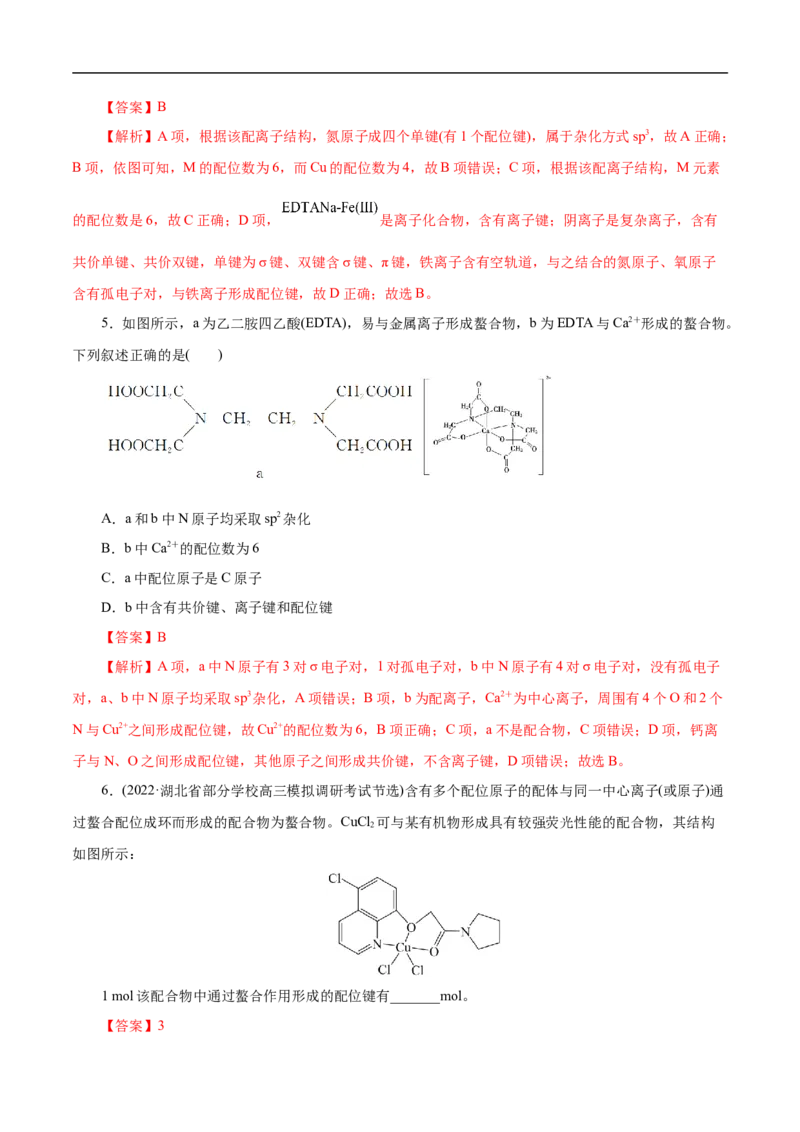
4.(2022·湖北省高三模拟)乙二胺四乙酸又叫 ,是化学中一种良好的配合剂,形成的配合物又
叫螯合物。 在配合滴定中经常用到,一般是测定金属离子的含量。已知: 配离子结构如图。
下列叙述错误的是( )
A. 中氮原子杂化方式sp3
B.M元素可以是Cu、Fe或
C.M元素的配位数是6
D. 的化学键有:σ键、配位键、π键和离子键【答案】B
【解析】A项,根据该配离子结构,氮原子成四个单键(有1个配位键),属于杂化方式sp3,故A正确;
B项,依图可知,M的配位数为6,而Cu的配位数为4,故B项错误;C项,根据该配离子结构,M元素
的配位数是6,故C正确;D项, 是离子化合物,含有离子键;阴离子是复杂离子,含有
共价单键、共价双键,单键为σ键、双键含σ键、π键,铁离子含有空轨道,与之结合的氮原子、氧原子
含有孤电子对,与铁离子形成配位键,故D正确;故选B。
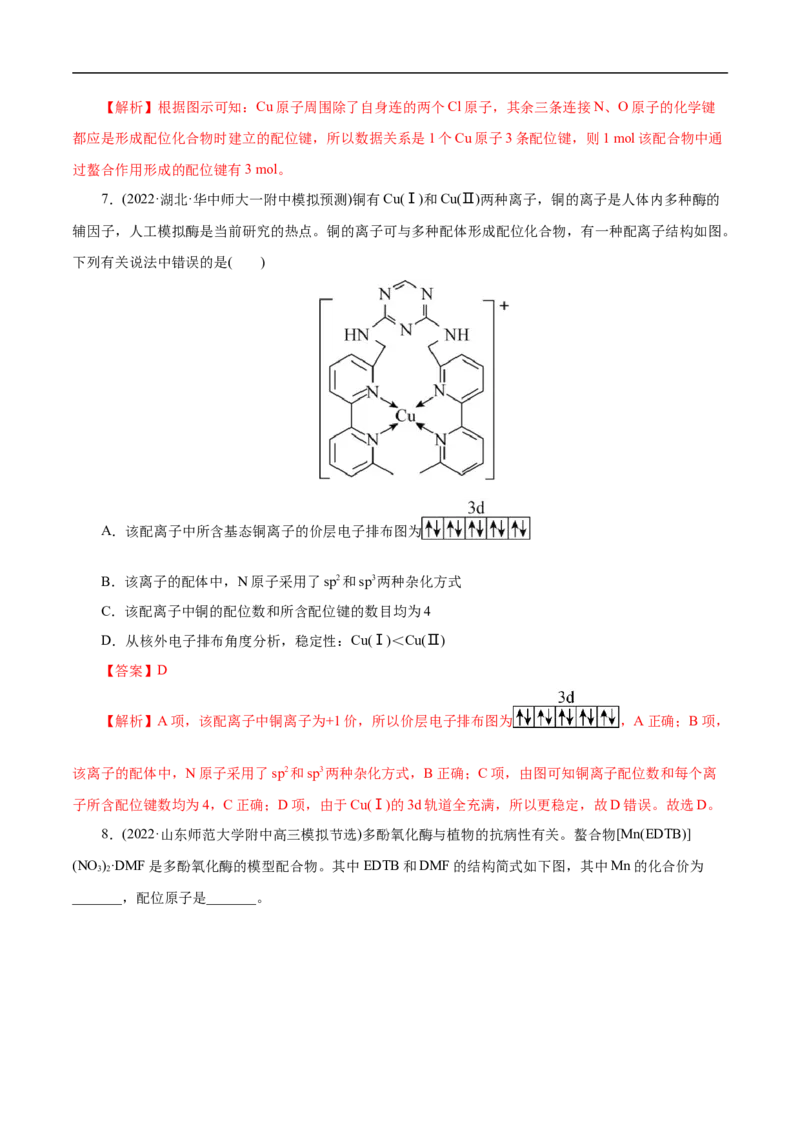
5.如图所示,a为乙二胺四乙酸(EDTA),易与金属离子形成螯合物,b为EDTA与Ca2+形成的螯合物。
下列叙述正确的是( )
A.a和b中N原子均采取sp2杂化
B.b中Ca2+的配位数为6
C.a中配位原子是C原子
D.b中含有共价键、离子键和配位键
【答案】B
【解析】A项,a中N原子有3对σ电子对,1对孤电子对,b中N原子有4对σ电子对,没有孤电子
对,a、b中N原子均采取sp3杂化,A项错误;B项,b为配离子,Ca2+为中心离子,周围有4个O和2个
N与Cu2+之间形成配位键,故Cu2+的配位数为6,B项正确;C项,a不是配合物,C项错误;D项,钙离
子与N、O之间形成配位键,其他原子之间形成共价键,不含离子键,D项错误;故选B。
6.(2022·湖北省部分学校高三模拟调研考试节选)含有多个配位原子的配体与同一中心离子(或原子)通
过螯合配位成环而形成的配合物为螯合物。CuCl 可与某有机物形成具有较强荧光性能的配合物,其结构
2
如图所示:
1 mol该配合物中通过螯合作用形成的配位键有_______mol。
【答案】3【解析】根据图示可知:Cu原子周围除了自身连的两个Cl原子,其余三条连接N、O原子的化学键
都应是形成配位化合物时建立的配位键,所以数据关系是1个Cu原子3条配位键,则1 mol该配合物中通
过螯合作用形成的配位键有3 mol。
7.(2022·湖北·华中师大一附中模拟预测)铜有Cu(Ⅰ)和Cu(Ⅱ)两种离子,铜的离子是人体内多种酶的
辅因子,人工模拟酶是当前研究的热点。铜的离子可与多种配体形成配位化合物,有一种配离子结构如图。
下列有关说法中错误的是( )
A.该配离子中所含基态铜离子的价层电子排布图为
B.该离子的配体中,N原子采用了sp2和sp3两种杂化方式
C.该配离子中铜的配位数和所含配位键的数目均为4
D.从核外电子排布角度分析,稳定性:Cu(Ⅰ)<Cu(Ⅱ)
【答案】D
【解析】A项,该配离子中铜离子为+1价,所以价层电子排布图为 ,A正确;B项,
该离子的配体中,N原子采用了sp2和sp3两种杂化方式,B正确;C项,由图可知铜离子配位数和每个离
子所含配位键数均为4,C正确;D项,由于Cu(Ⅰ)的3d轨道全充满,所以更稳定,故D错误。故选D。
8.(2022·山东师范大学附中高三模拟节选)多酚氧化酶与植物的抗病性有关。螯合物[Mn(EDTB)]
(NO )·DMF是多酚氧化酶的模型配合物。其中EDTB和DMF的结构简式如下图,其中Mn的化合价为
3 2
_______,配位原子是_______。【答案】 +2 N
【解析】由配合物的化学式和化合价代数和为0可知,配合物中锰元素的化合价为+2价,具有空轨道
的锰两者与EDTB中具有孤对电子的氮原子形成配位键。
9.(2022·广东省广州市七区教学质量监测节选)螯合物是具有环状结构的配合物,铜的一种整合物结
构如图,该配合物中Cu2+的配位数为____,其中C、N、О按电负性由小到大的顺序排列为____。该配合
物中碳原子的杂化方式有____。
【答案】4 C<N<O sp2、sp3
、【解析】该配合物中Cu2+的配位数为4,同周期元素从左到右电负性依次增大,其中C、N、О按电
负性由小到大的顺序排列为C<N<O。该配合物中碳原子成四个σ键或三个σ键,该配合物中碳原子的杂
化方式有sp2、sp3。
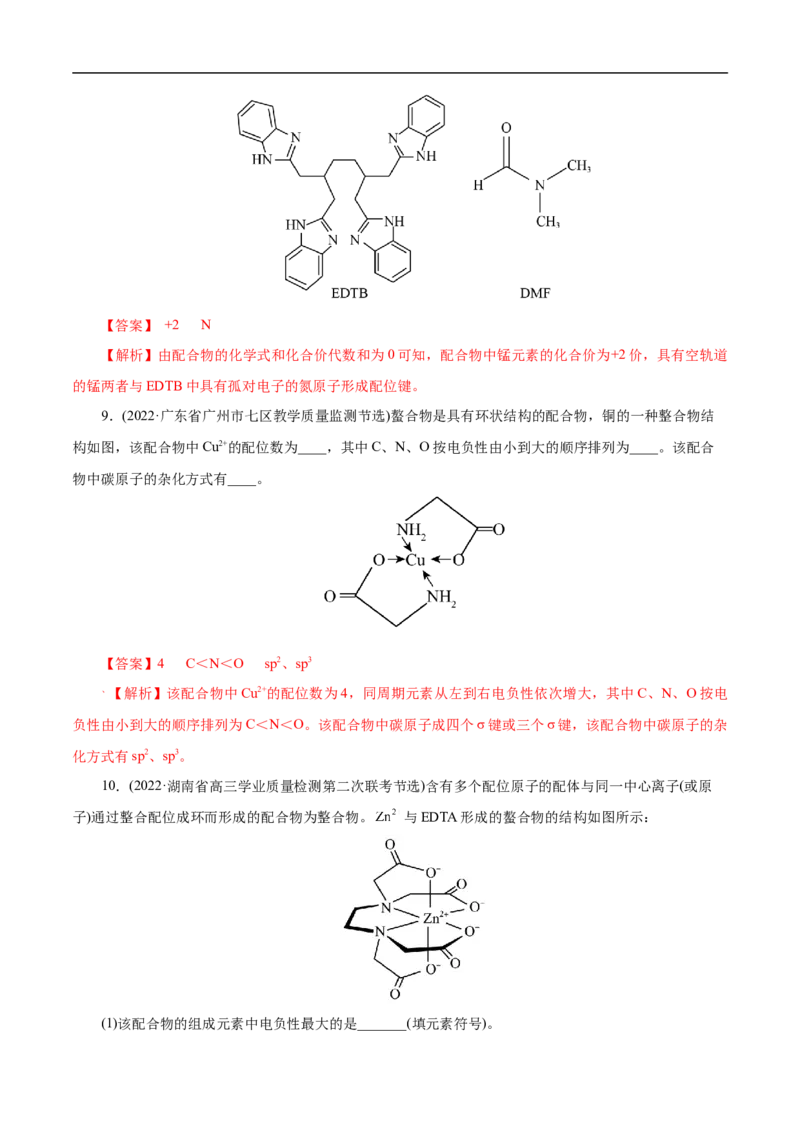
10.(2022·湖南省高三学业质量检测第二次联考节选)含有多个配位原子的配体与同一中心离子(或原
子)通过整合配位成环而形成的配合物为整合物。 与EDTA形成的螯合物的结构如图所示:
(1)该配合物的组成元素中电负性最大的是_______(填元素符号)。(2)1个该配合物分子中通过螯合作用形成的配位键有_______个,该配合物中碳原子的杂化方式为
_______。
【答案】(1) O (2)6 sp2、sp3
【解析】(1)该配合物的组成元素有H、C、N、O、Zn,非金属性越强电负性越大,故氧元素的电负性
最大。(2)只有成环的配位键才能起到螯合作用,由配合物结构图可知,提供孤对电子的原子为N、O,1
个该配合物分子中通过螯合作用形成的配位键有6个;该配合物的碳氧双键中碳原子为sp2杂化,其他碳原
子为sp3杂化。
11.(2023届·湖南省邵阳市第二中学高三开学考试节选)L-赖氨酸锌螯合物X (结构为如图)易被人体吸
收。
(1)X中元素(除H外)的第一电离能由小到大的顺序为_______,加“*”氧原子的杂化方式为_______。
(2)X的晶体中存在的微粒间作用力有._______。
A.离子键 B.π键 C.金属键 D.配位
键 E.非极性键
(3)L-赖氨酸易溶于水主要原因是_______。
【答案】(1)Zn、C、O、N sp3杂化 (2)B、D、E
(3)L-赖氨酸分子与水分子形成分子间氢键
【解析】(1)X中元素(除H外)还有C、N、O、Zn,非金属的第一电离能大于金属,故Zn的第一电离
能最小,C、N、O位于同一周期,从左往右呈增大趋势,N为半满结构,第一电离能最大,故第一电离能
由小到大的顺序为Zn、C、O、N;加“*”氧原子有两个单键和两个孤电子对,杂化方式为sp3杂化;(2)X
晶体中酯基中存在π键,Zn与O之间是配位键,C-C之间为非极性键,故选B、D、E;(3)L-赖氨酸易溶
于水主要原因是L-赖氨酸分子与水分子形成分子间氢键。
12.(2022·四川省巴中高三模拟节选)Fe、Ni元素性质非常相似,属于铁系元素,得到广泛应用,请回
答下列问题:
(1)Fe元素属于元素周期表的_______ 区(填分区)
(2)基态Ni2+核外电子排布式为________________。
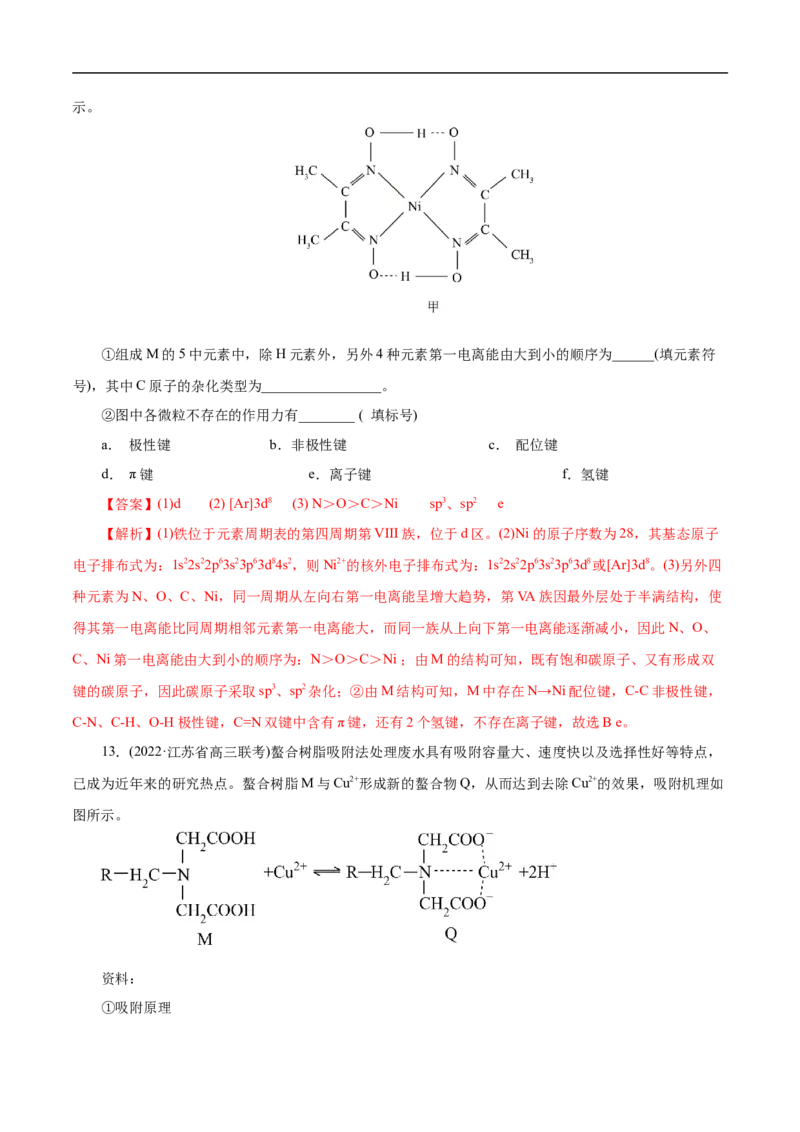
(3)鉴定Ni2+的特征反应是将丁二酮肟加入Ni2+盐溶液中,生成鲜红色的螯合物M,M的结构如图甲所示。
①组成M的5中元素中,除H元素外,另外4种元素第一电离能由大到小的顺序为______(填元素符
号),其中C原子的杂化类型为_________________。
②图中各微粒不存在的作用力有________ ( 填标号)
a. 极性键 b.非极性键 c. 配位键
d. π键 e.离子键 f.氢键
【答案】(1)d (2) [Ar]3d8 (3) N>O>C>Ni sp3、sp2 e
【解析】(1)铁位于元素周期表的第四周期第VIII族,位于d区。(2)Ni的原子序数为28,其基态原子
电子排布式为:1s22s22p63s23p63d84s2,则Ni2+的核外电子排布式为:1s22s22p63s23p63d8或[Ar]3d8。(3)另外四
种元素为N、O、C、Ni,同一周期从左向右第一电离能呈增大趋势,第VA族因最外层处于半满结构,使
得其第一电离能比同周期相邻元素第一电离能大,而同一族从上向下第一电离能逐渐减小,因此N、O、
C、Ni第一电离能由大到小的顺序为:N>O>C>Ni ;由M的结构可知,既有饱和碳原子、又有形成双
键的碳原子,因此碳原子采取sp3、sp2杂化;②由M结构可知,M中存在N→Ni配位键,C-C非极性键,
C-N、C-H、O-H极性键,C=N双键中含有π键,还有2个氢键,不存在离子键,故选B e。
13.(2022·江苏省高三联考)螯合树脂吸附法处理废水具有吸附容量大、速度快以及选择性好等特点,
已成为近年来的研究热点。螯合树脂M与Cu2+形成新的螯合物Q,从而达到去除Cu2+的效果,吸附机理如
图所示。
资料:
①吸附原理螯合树脂M中的—OH解离出H+,变成—COO-,而且树脂中含有N原子,在与Cu2+接触时,树脂中
的—COO-、N原子与Cu2+形成配位键,形成新的螯合物Q,从而达到去除Cu2+的目的。
②在体系酸性较强情况下,氮原子与氢离子具有较强的配位能力。
(1)基态Cu的价层电子排布的轨道表示式是____。
(2)M中四种元素电负性由大到小的顺序为(用元素符号表示)____。
(3)M中N原子的杂化轨道类型为____。
(4)Q中存在配位键,其中提供空轨道的是____。
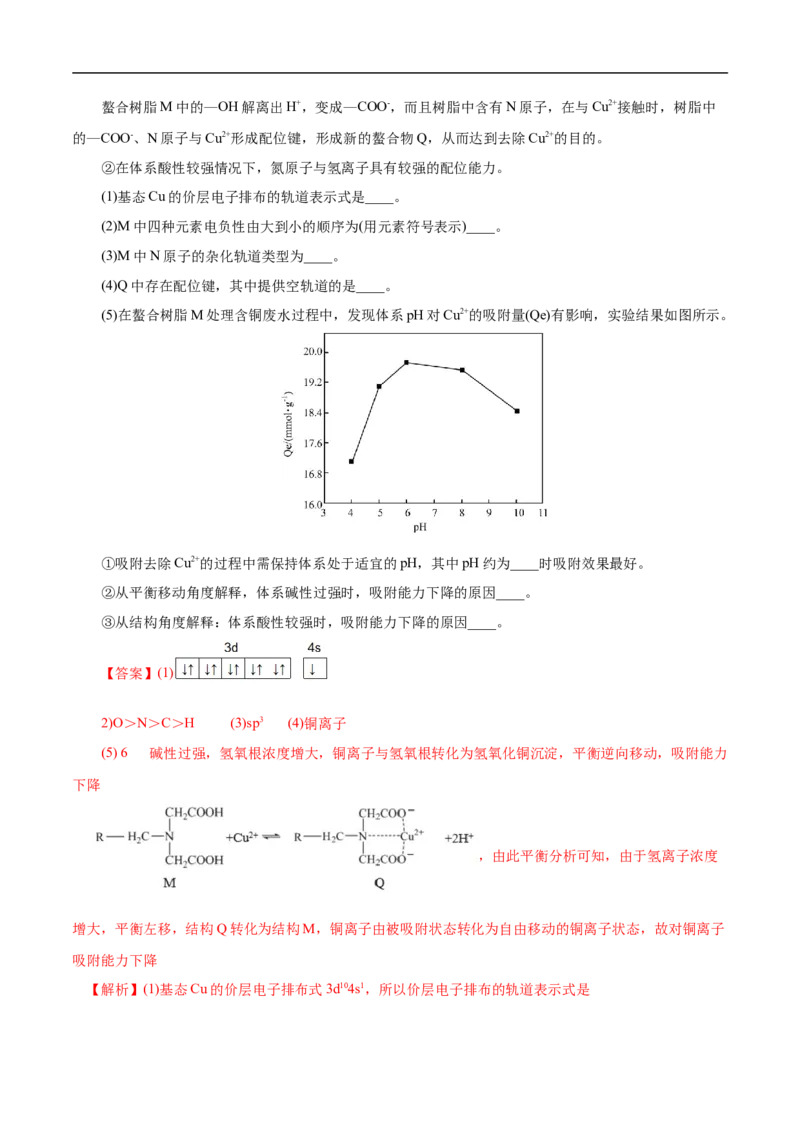
(5)在螯合树脂M处理含铜废水过程中,发现体系pH对Cu2+的吸附量(Qe)有影响,实验结果如图所示。
①吸附去除Cu2+的过程中需保持体系处于适宜的pH,其中pH约为____时吸附效果最好。
②从平衡移动角度解释,体系碱性过强时,吸附能力下降的原因____。
③从结构角度解释:体系酸性较强时,吸附能力下降的原因____。
【答案】(1)
2)O>N>C>H (3)sp3 (4)铜离子
(5) 6 碱性过强,氢氧根浓度增大,铜离子与氢氧根转化为氢氧化铜沉淀,平衡逆向移动,吸附能力
下降
,由此平衡分析可知,由于氢离子浓度
增大,平衡左移,结构Q转化为结构M,铜离子由被吸附状态转化为自由移动的铜离子状态,故对铜离子
吸附能力下降
【解析】(1)基态Cu的价层电子排布式3d104s1,所以价层电子排布的轨道表示式是;(2)元素周期表从下往上,从左往右,得电子能力越来越强,电负性越来越大,
所以M中四种元素电负性由大到小的顺序为O>N>C>H;(3)M中N原子形成三条σ键,含有一个孤电
子对,价层电子对为4,,所以杂化方式为sp3;(4)Q中铜离子和O原子形成配位键,其中O原子提供孤电
子对,铜离子提供空轨道;(5)①分析图示可知,pH为6,吸附效果最好;②碱性过强,氢氧根浓度增大,
铜离子与氢氧根转化为氢氧化铜沉淀,平衡逆向移动,吸附能力下降;③从结构角度解释:体系酸性较强
时,吸附能力下降的原因在于存在以下反应平衡
,由此平衡分析可知,由于氢离子浓度增大,
平衡左移,结构Q转化为结构M,铜离子由被吸附状态转化为自由移动的铜离子状态,故对铜离子吸附能
力下降。
14.(2022·河南省高三百校大联考)铁及其化合物是日常生活生产中应用广泛的材料。请回答下列问题:
(1)基态铁原子中,最高能层电子的电子云的形状为____,原子中未成对的电子数为____。
(2)铁的常见氧化物中氧化铁比氧化亚铁稳定,试从原子结构角度解释原因:____。
(3)铁作为过渡金属,能形成多种配位化合物。赤血盐{K [Fe(CN) ]}为红色晶体,其配离子中提供空轨
3 6
道的为____ (填微粒符号),配位原子是____ (填元素符号);Fe2+与1,10—邻二氮菲(phen)在水溶液中能形
成稳定的螯合物,其结构如图,该螯合物中各元素的电负性由大到小的顺序为____,N的杂化方式为____ ,
Fe2+的配位数为____。(4)无水三氯化铁(FeCl )为棕黑色,共价性较强,熔点为307.6℃,沸点约为316℃,易升华,400℃以
3
下的气态FeCl 的相对分子质量测定值约为325,其原因是____。
3
(5)一种铁、碳形成的间腺化合物的晶体结构如图1所示,其晶胞为长方体,结构如图2所示(晶胞中部
分铁原子未标出)。
①该晶体的化学式为____。
②与碳原子紧邻的铁原子构成的空间构型为____。
③则该晶体的密度为____g·cm-3(用N 表示阿伏加德罗常数的值,用含a、b、c、N 的式子表示)。
A A
【答案】(1)球形 4
(2)Fe2+的价电子排布式为3d6,Fe3+的价电子排布式为3d5,3d能级处于半充满的稳定状态,故氧化铁
比氧化亚铁稳定
(3) Fe3+ C N>C>H>Fe sp2 6
(4)气态FeCl 主要以二聚体形式存在
3
(5) Fe C 正八面体
3
【解析】(1)基态铁原子的电子排布式为1s22s22p63s23p63d64s2,其最高能层为第N能层,其电子的电子
云形状为球形,原子中未成对的电子数为4;(2)Fe2+的价电子排布式为3d6,Fe3+的价电子排布式为3d5,3d
能级处于半充满的稳定状态,故氧化铁比氧化亚铁稳定;(3){K [Fe(CN) ]}的配离子为[Fe(CN) ]3-,提供空
3 6 6
轨道的为中心离子Fe3+,C的电负性比N的电负性弱,更易提供孤电子对形成配位键,故配位原子是C;
该螯合物中各元素的电负性由大到小的顺序为N>C>H>Fe,N原子形成3个σ键,无孤电子对,故价层电
子对数为3,故N的杂化方式为sp2,Fe2+与6个N原子形成配位键,故Fe2+的配位数为6;(4)400°C以下的气态FeCl 的相对分子质量测定值约为325的原因是气态FeCl 主要以二聚体形式存在;(5)①由结构图可知,
3 3
碳原子位于铁原子形成的正八面体的中心,每个铁原子又为两个正八面体共用,则根据均摊法可知,C的
个数为1个,Fe的个数为 ,该晶体的化学式为Fe C;②与碳原子紧邻的铁原子构成的空间构型为
3
正八面体;③由晶胞结构图可知,一个晶胞中含有的C原子数为 则该晶体的密度为
。
15.(2022·广东省高三模拟)如图,铜离子与有机物HA可形成一种螯合物CuA,从而萃取水中的铜离
2
子。
回答下列问题:
(1)基态铜原子价电子排布式为_______。
(2)有机物HA中,C、N、O三种元素的电负性由大到小的顺序是_______。
(3)螯合物CuA 中的氮原子、氧原子的杂化方式分别为_______。
2
(4)下列关于螯合物CuA 的说法中,正确的是_______(填序号)。
2
①CuA 中O的配位能力比N强 ②与Cu2+配位的4个原子可能呈平面构型
2
③CuA 既溶于水又溶于有机溶剂 ④每个CuA 中含2个氢键、2个π键
2 2
(5)萃取后,铜离子进入有机相中,反萃取时,螯合物释放出铜离子,铜离子进入水相,可用于铜离子
的富集及提纯,则反萃取时常加入的试剂是_______。
(6)金属铜与铝可形成多种组成不同的合金,其中一种合金的晶胞如图甲所示,晶胞参数α=β=γ=90°,
a=b=0.41 nm,c=0.58 nm,按图甲中阴影面进行投影得到图乙。①已知晶胞中A点的原子坐标为 ,则B点的原子坐标为_______。
②该晶体的化学式为_______,密度为_______ (结果保留两位有效数字)。
【答案】(1)3d104s1 (2)O>N>C (3)sp2、sp3 (4)②④
(5)盐酸或硫酸 (6) Al Cu(或CuAl ) 4.0
2 2
【解析】(1)铜元素的原子序数为29,基态铜原子价电子排布式为3d104s1,故答案为:3d104s1;(2)同周
期元素,从左到右元素的非金属性依次增强,电负性依次增大,则C、N、O三种元素的电负性由大到小
的顺序为O>N>C;(3)由结构简式可知,螯合物CuA 中氮原子形成双键、氧原子形成单键,则氮原子的杂
2
化方式为sp2杂化、氧原子的杂化方式为sp3杂化;(4)①由结构简式可知,CuA 中氮原子与铜离子形成配位
2
键,则氮原子的配位能力比氧原子强,故①错误;②类比铜离子与氨分子形成的配合物的结构可知,与铜
离子配位的2个氧原子和2个氮原子有可能位于同一平面上,即有可能呈平面构型,故②正确;③由铜离
子与有机物HA可形成一种螯合物CuA,从而萃取水中的铜离子可知,CuA 不溶于水易溶于有机溶剂,
2 2
故③错误;④由结构简式可知,每个CuA 中含有如图所示的2个氢键、2个π键:
2
,故④正确;故选②④;(5)由萃取反应的离子方程式可
知,反萃取时增大溶液中的氢离子浓度,可使平衡向逆反应方向移动,使螯合物释放出铜离子进入水相,
则反萃取时常加入的试剂是盐酸或硫酸,故答案为:盐酸或硫酸;(6)①由晶胞中位于正面面上A点的原子坐标为 可知,位于左侧面面上B点的原子坐标为 ;②由晶胞结构可知,晶胞中位于顶点、
面心、棱上和体内的铝原子个数为8× +2× +4× +1=4,位于面上的铜原子个数为4× =2,则该晶体的
化学式为Al Cu(或CuAl ),设晶体的密度为d ,由晶胞的质量公式可得:(0.412×0.58×10—21)d=
2 2
,解得d≈4.0。