文档内容
专项训练 水的电离程度大小比较
一、单选题
1.常温下,用浓度为 的 标准溶液滴定浓度均为 的
和 的混合溶液,滴定过程中溶液的 随 ( )的变化
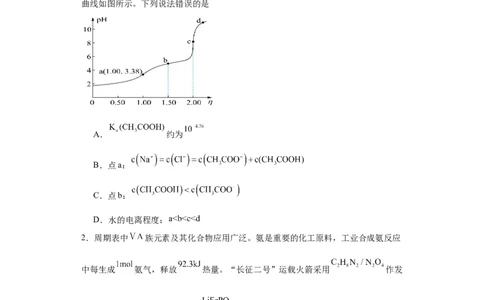
曲线如图所示。下列说法错误的是
A. 约为
B.点a:
C.点b:
D.水的电离程度:
2.周期表中 族元素及其化合物应用广泛。氨是重要的化工原料,工业合成氨反应
中每生成 氨气,释放 热量。“长征二号”运载火箭采用 作发
动机推进剂,燃烧产物无污染。 常作锂电池的正极材料,电池充电时,
脱出部分 ,形成 。砷化镓 是制备第三代半导体材料
的重要原料。常温下,下列有关氨水的说法正确的是
A.相同浓度的氨水和 溶液的导电能力相同
B.相同浓度的氨水和 溶液中,水的电离程度相同
资料收集整理【淘宝店铺:向阳百分百】C. 均为10的氨水和 溶液中, 的物质的量浓度相同
D.将 均为10的氨水和 溶液稀释相同倍数后, 溶液的 大于氨
水
3.已知电解质溶液的电导率越大,导电能力越强。现用 的NaOH溶液分
别滴定 浓度均为 的盐酸和 溶液,利用传感器测得滴定
过程中溶液的电导率随加入NaOH溶液体积的变化情况如图所示。下列说法正确的是
A.曲线①代表NaOH溶液滴定盐酸的曲线
B.A点溶液中:
C.D点溶液中:
D.相同温度下A、B、C三点溶液中,水的电离程度:Ac(Na+)>c(CH COO-)
3 3
资料收集整理【淘宝店铺:向阳百分百】D.NH ·H O—NHCl溶液具有与试剂②相似的缓冲作用
3 2 4
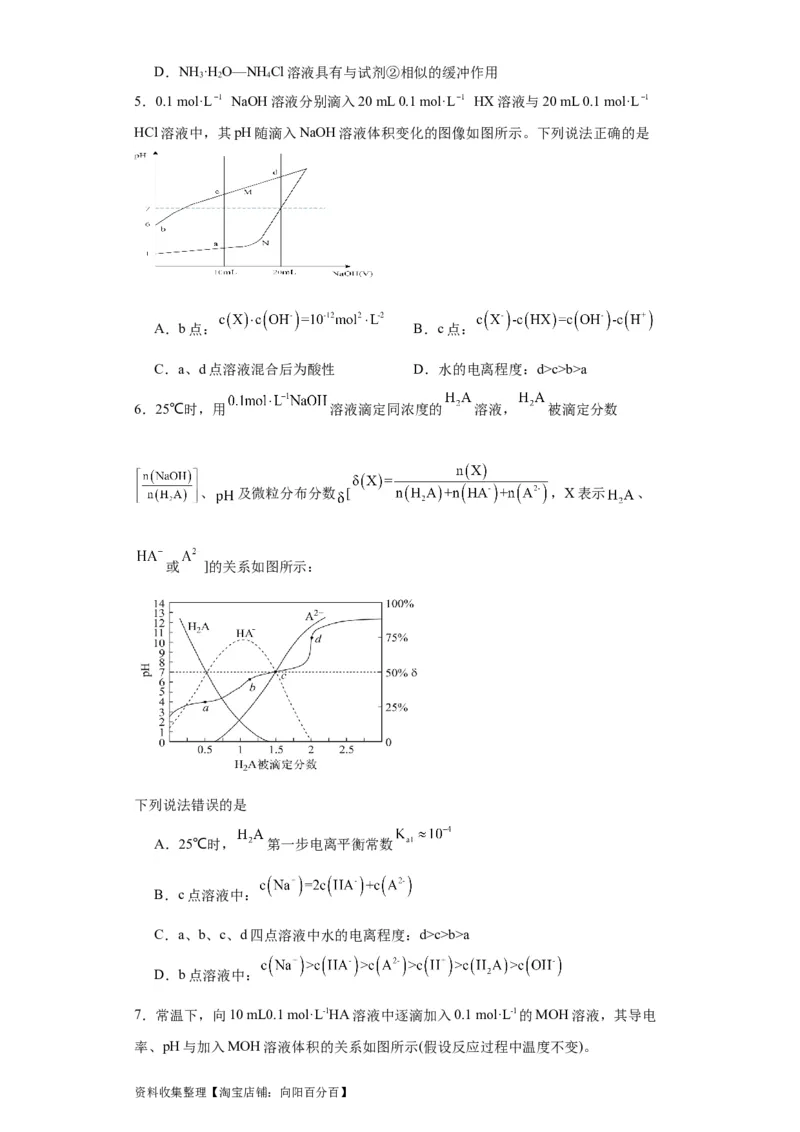
5.0.1 mol·L NaOH溶液分别滴入20 mL 0.1 mol·L HX溶液与20 mL 0.1 mol·L
HCl溶液中,其pH随滴入NaOH溶液体积变化的图像如图所示。下列说法正确的是
A.b点: B.c点:
C.a、d点溶液混合后为酸性 D.水的电离程度:d>c>b>a
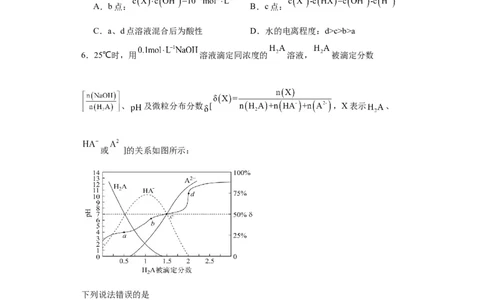
6.25℃时,用 溶液滴定同浓度的 溶液, 被滴定分数
、 及微粒分布分数 [ ,X表示 、
或 ]的关系如图所示:
下列说法错误的是
A.25℃时, 第一步电离平衡常数
B.c点溶液中:
C.a、b、c、d四点溶液中水的电离程度:d>c>b>a
D.b点溶液中:
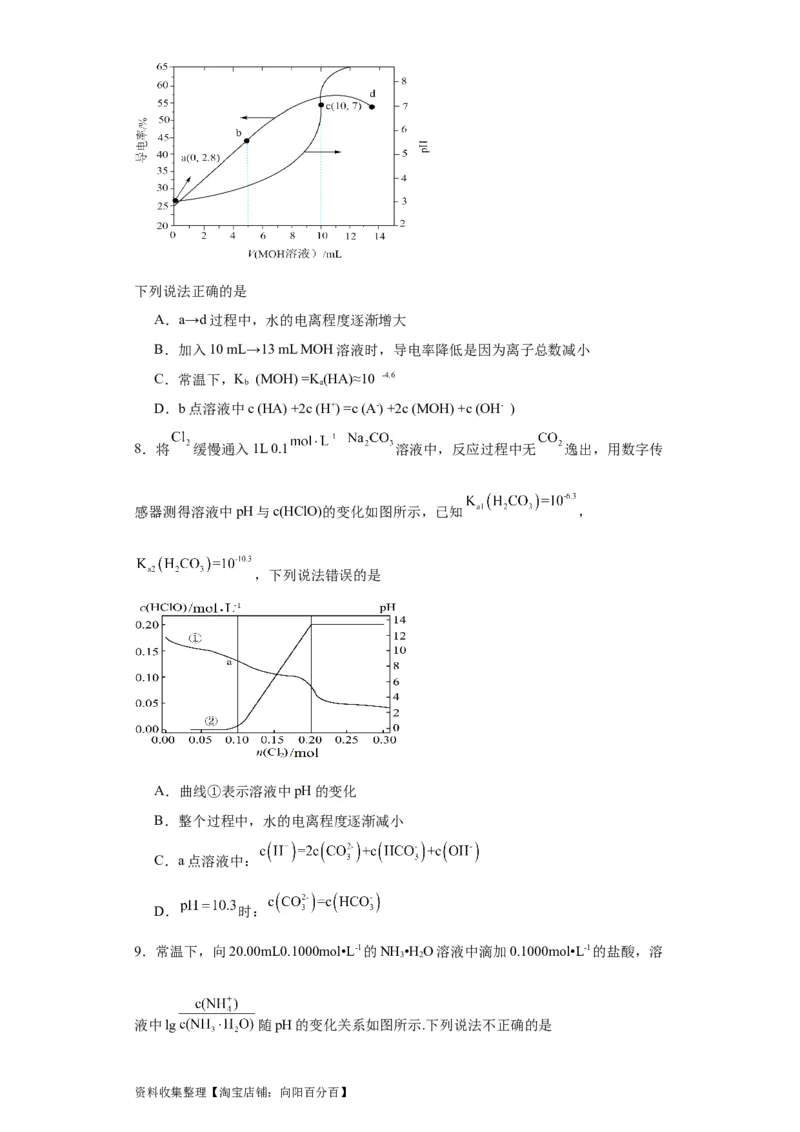
7.常温下,向10 mL0.1 mol·L-1HA溶液中逐滴加入0.1 mol·L-1的MOH溶液,其导电
率、pH与加入MOH溶液体积的关系如图所示(假设反应过程中温度不变)。
资料收集整理【淘宝店铺:向阳百分百】下列说法正确的是
A.a→d过程中,水的电离程度逐渐增大
B.加入10 mL→13 mL MOH溶液时,导电率降低是因为离子总数减小
C.常温下,K (MOH) =K(HA)≈10 -4.6
b a
D.b点溶液中c (HA) +2c (H+) =c (A-) +2c (MOH) +c (OH- )
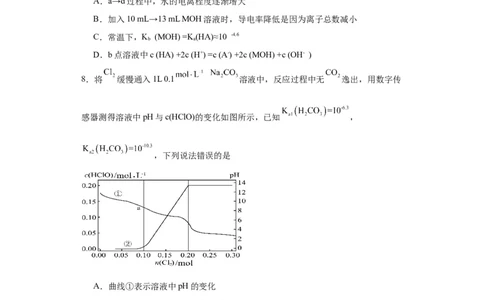
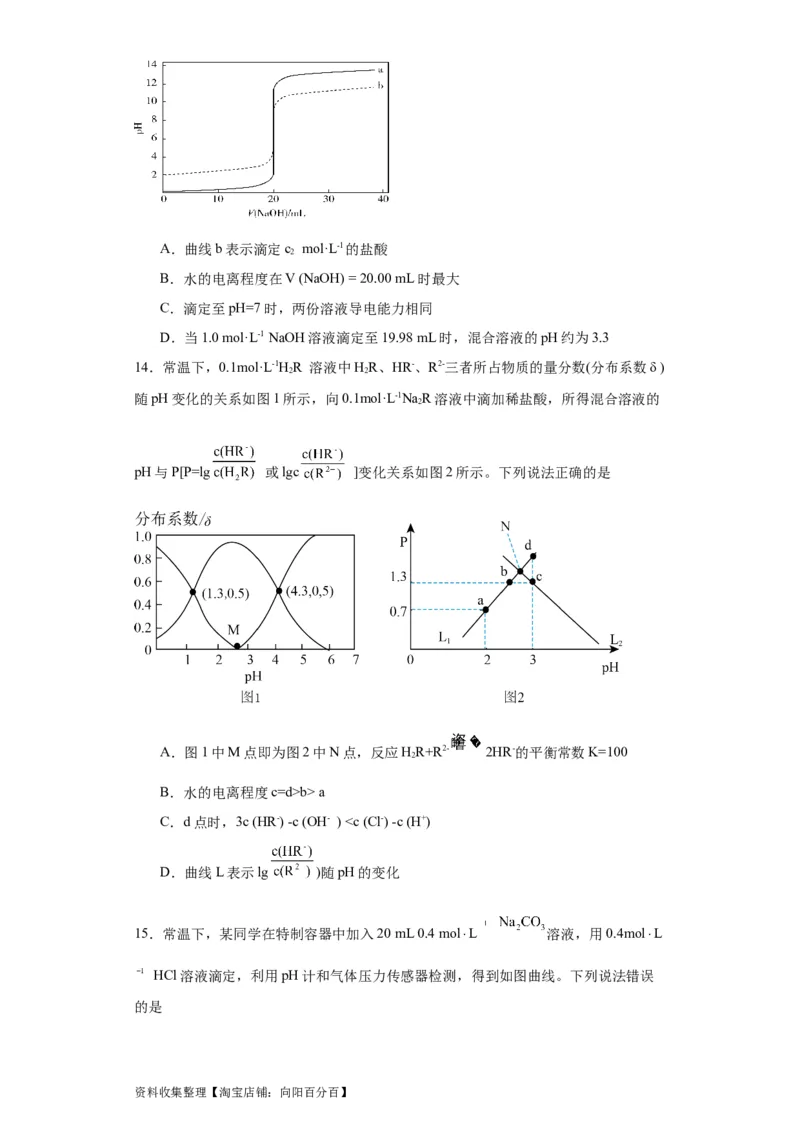
8.将 缓慢通入1L 0.1 溶液中,反应过程中无 逸出,用数字传
感器测得溶液中pH与c(HClO)的变化如图所示,已知 ,
,下列说法错误的是
A.曲线①表示溶液中pH的变化
B.整个过程中,水的电离程度逐渐减小
C.a点溶液中:
D. 时:
9.常温下,向20.00mL0.1000mol•L-1的NH •H O溶液中滴加0.1000mol•L-1的盐酸,溶
3 2
液中lg 随pH的变化关系如图所示.下列说法不正确的是
资料收集整理【淘宝店铺:向阳百分百】A.常温下,NH •H O电离常数为10-4.75
3 2
B.当溶液的pH=7时,消耗盐酸的体积小于20mL
C.溶液中水的电离程度:c>b>a
D. 点溶液中:c(NH )>c(Cl-)
10.已知: 。室温下,向0.10mol/LHX溶液中滴加0.10mol/
LNaOH溶液,溶液pH随 变化关系如图所示。下列说法错误的是
A.溶液中水的电离程度:a<b<c
B.b点溶液中:
C.c点溶液中:
D.室温下NaX的水解平衡常数为
11.某种天然碱的化学式为 ,取一定质量该天然碱溶于水,
逐滴加入稀盐酸,溶液中的 的物质的量与加入HCl的物质的量变化如图所示,
资料收集整理【淘宝店铺:向阳百分百】以下说法正确的是
A.
B.水的电离程度:
C.N点溶液中存在:
D.P点溶液中:
12.已知:MOH的碱性比NOH强。常温下,用HCl分别调节浓度均为 的
MOH溶液和NOH溶液的pH(溶液体积变化忽略不计),溶液中 、 的物质的量浓
度的负对数与溶液的pH关系如图所示,下列说法正确的是
A.曲线Ⅰ表示 与pH的关系
B.溶液中水的电离程度:YZ
D.常温时,反应 的平衡常数
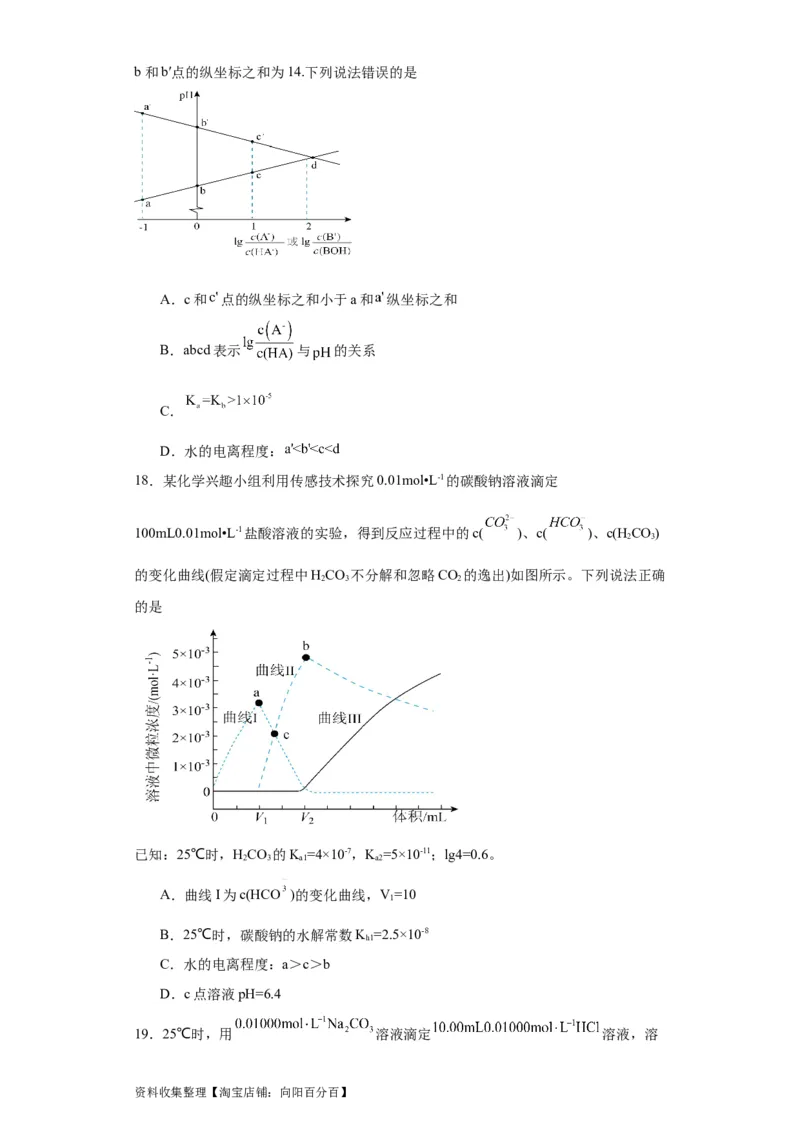
13.25°C时,用1.0 mol·L-1 NaOH溶液滴定20.00 mL c mol·L-1的盐酸,用0.010
1
mol·L-1 NaOH溶液滴定20.00 mL c mol·L-1的盐酸,滴定曲线如图所示。下列说法不正
2
确的是(已知lg5=0.7)
资料收集整理【淘宝店铺:向阳百分百】A.曲线b表示滴定c mol·L-1的盐酸
2
B.水的电离程度在V (NaOH) = 20.00 mL时最大
C.滴定至pH=7时,两份溶液导电能力相同
D.当1.0 mol·L-1 NaOH溶液滴定至19.98 mL时,混合溶液的pH约为3.3
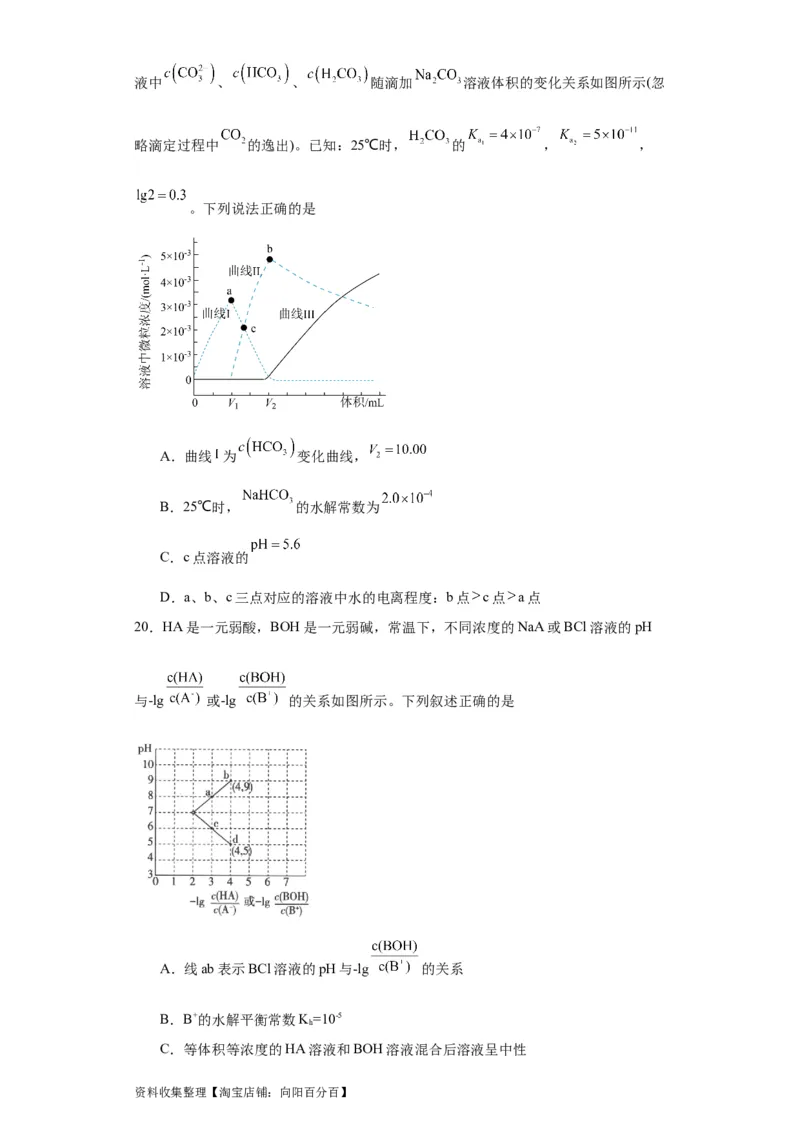
14.常温下,0.1mol·L-1HR 溶液中HR、HR-、R2-三者所占物质的量分数(分布系数δ )
2 2
随pH变化的关系如图1所示,向0.1mol·L-1NaR溶液中滴加稀盐酸,所得混合溶液的
2
pH与P[P=lg 或lgc ]变化关系如图2所示。下列说法正确的是
A.图1中M点即为图2中N点,反应HR+R2- 2HR-的平衡常数K=100
2
B.水的电离程度c=d>b> a
C.d点时,3c (HR-) -c (OH- )