文档内容
专项训练 水的电离程度大小比较(解析版)
一、单选题
1.常温下,用浓度为 的 标准溶液滴定浓度均为 的
和 的混合溶液,滴定过程中溶液的 随 ( )的变化
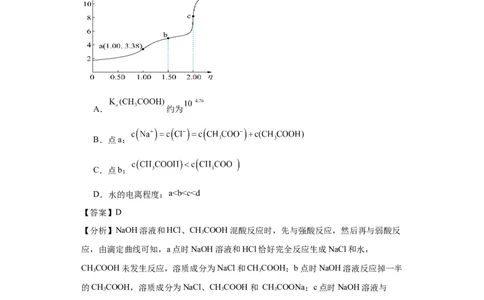
曲线如图所示。下列说法错误的是
A. 约为
B.点a:
C.点b:
D.水的电离程度:
【答案】D
【分析】NaOH溶液和HCl、CHCOOH混酸反应时,先与强酸反应,然后再与弱酸反
3
应,由滴定曲线可知,a点时NaOH溶液和HCl恰好完全反应生成NaCl和水,
CHCOOH未发生反应,溶质成分为NaCl和CHCOOH;b点时NaOH溶液反应掉一半
3 3
的CHCOOH,溶质成分为NaCl、CHCOOH和 CHCOONa;c点时NaOH溶液与
3 3 3
CHCOOH恰好完全反应,溶质成分为NaCl、CHCOONa;d点时NaOH过量,溶质成
3 3
分为NaCl、CHCOONa和NaOH,据此解答。
3
【详解】A.由分析可知,a点时溶质成分为NaCl和CHCOOH,
3
c(CHCOOH)=0.0100mol/L,c(H+)=10-3.38mol/L, =
3
资料收集整理【淘宝店铺:向阳百分百】=10-4.76,故A正确;
B.a点溶液为等浓度的NaCl和CHCOOH混合溶液,存在物料守恒关系
3
c(Na+)=c(Cl-)=c(CH COOH)+c(CH COO-),故B正确;
3 3
C.点b溶液中含有NaCl及等浓度的CHCOOH和 CHCOONa,由于pH<7,溶液显
3 3
酸性,说明CHCOOH的电离程度大于CHCOO-的水解程度,则
3 3
c(CHCOOH)d,故D错误;
答案选D。
2.周期表中 族元素及其化合物应用广泛。氨是重要的化工原料,工业合成氨反应
中每生成 氨气,释放 热量。“长征二号”运载火箭采用 作发
动机推进剂,燃烧产物无污染。 常作锂电池的正极材料,电池充电时,
脱出部分 ,形成 。砷化镓 是制备第三代半导体材料
的重要原料。常温下,下列有关氨水的说法正确的是
A.相同浓度的氨水和 溶液的导电能力相同
B.相同浓度的氨水和 溶液中,水的电离程度相同
C. 均为10的氨水和 溶液中, 的物质的量浓度相同
D.将 均为10的氨水和 溶液稀释相同倍数后, 溶液的 大于氨
水
【答案】C
【详解】A.氨水部分电离出离子,NaOH是强碱能完全电离,则相同浓度的氨水和
溶液后者的浓度大,离子浓度越大导电性越强,所以NaOH溶液导电能力强,
故A错误;
B.氨水属于碱,电离出氢氧根离子抑制水的电离, 为强酸弱碱盐,铵根能与
资料收集整理【淘宝店铺:向阳百分百】水发生水解反应,促进水的电离,则 溶液中水的电离程度更大,故B错误;
C.相同温度下, 均为10的氨水和 溶液中氢离子浓度相等,根据
K =c(H+)∙c(OH-),则 的物质的量浓度相同,故C正确;
w
D.根据越稀越电离原理,氨水稀释后促进其电离,生成c(OH-)比NaOH的大,则氨水
的 较大,故D错误;
故选:C。
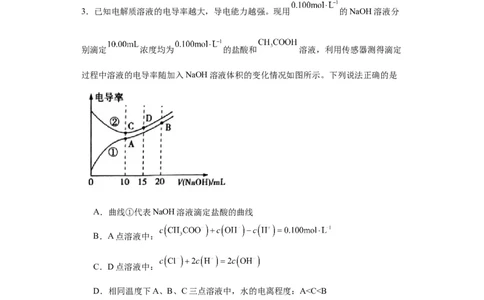
3.已知电解质溶液的电导率越大,导电能力越强。现用 的NaOH溶液分
别滴定 浓度均为 的盐酸和 溶液,利用传感器测得滴定
过程中溶液的电导率随加入NaOH溶液体积的变化情况如图所示。下列说法正确的是
A.曲线①代表NaOH溶液滴定盐酸的曲线
B.A点溶液中:
C.D点溶液中:
D.相同温度下A、B、C三点溶液中,水的电离程度:Ac(Na+)>c(CH COO-)
3 3
D.NH ·H O—NHCl溶液具有与试剂②相似的缓冲作用
3 2 4
【答案】C
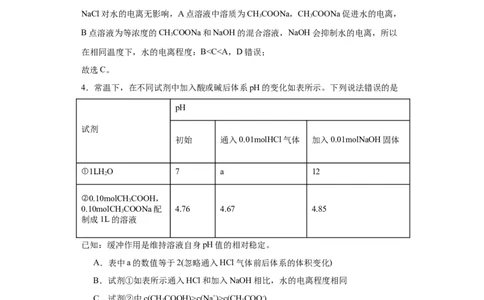
【分析】0.10molCHCOOH,0.10molCHCOONa配制成1L的溶液是缓冲溶液,开始
3 3
时pH=4.76,通入0.01molHCl后,pH变成4.67,变化不大,加入0.01molNaOH后pH
变为4.85,也变化不大,有缓冲酸碱的作用。
【详解】A.0.01molHCl气体通入1L水中,忽略体积变化,浓度是0.01mol/L,由于
盐酸是强酸完全电离,H+浓度为0.01mol/L,a=2,故A正确;
B.0.01molHCl气体通入1L水中与0.01molNaOH加入水中,二者的浓度相同,都是一
资料收集整理【淘宝店铺:向阳百分百】元强酸碱,都抑制水的电离,抑制的程度一样,因此水电离程度一样,故B正确;
C.试剂②是0.10molCHCOOH,0.10molCHCOONa配制成1L的溶液,溶液呈酸性,
3 3
说明CHCOOH的电离大于CHCOO-的水解,因此CHCOO-的浓度大于CHCOOH的
3 3 3 3
浓度,故C错误;
D.NH ·H O—NHCl溶液同样具有与试剂②相似的缓冲作用,故D正确;
3 2 4
答案选C。
5.0.1 mol·L NaOH溶液分别滴入20 mL 0.1 mol·L HX溶液与20 mL 0.1 mol·L
HCl溶液中,其pH随滴入NaOH溶液体积变化的图像如图所示。下列说法正确的是
A.b点: B.c点:
C.a、d点溶液混合后为酸性 D.水的电离程度:d>c>b>a
【答案】D
【分析】NaOH是一元强碱,HCl是一元强酸,当滴加20mLNaOH溶液时溶液为中性,
则N曲线为HCl溶液的滴定曲线,M曲线为HX溶液的滴定曲线且可以判断该酸为弱
酸。
【详解】A.b点的pH=6则 ,则
,故A错误;
B.c点是NaX与HX1:1的混合溶液,根据质子守恒可得:
,故B错误;
C.a、d点溶液混合即30mLNaOH溶液与20 mL 0.1 mol·L HX溶液与20 mL 0.1
mol·L HCl溶液混合,溶质为NaCl 和1:1的NaX与HX,酸碱性等价于c点,由图
可知呈碱性,故C错误;
D.d点溶质只有NaX对水的电离起促进作用,c点NaX与HX1:1的混合溶液,溶液
显碱性说明水解程度大于电离程度,HCl是一元强酸而HX为弱酸,强酸对水的电离
的抑制程度更大,所以水的电离程度:d>c>b>a,故D正确;
资料收集整理【淘宝店铺:向阳百分百】故选D。
6.25℃时,用 溶液滴定同浓度的 溶液, 被滴定分数
、 及微粒分布分数 [ ,X表示 、
或 ]的关系如图所示:
下列说法错误的是
A.25℃时, 第一步电离平衡常数
B.c点溶液中:
C.a、b、c、d四点溶液中水的电离程度:d>c>b>a
D.b点溶液中:
【答案】D
【分析】由图可知,a、b、c、d所在实线为0.1 mol·L-1NaOH溶液滴定二元弱酸HA
2
的滴定曲线,当 <1时,HA部分反应,溶液中溶质为NaHA和HA;当
2 2
=1时,反应生成NaHA,NaHA溶液显酸性;当1< <2时,溶液
中溶质为NaHA和NaA;当 =2时,反应生成NaA,NaA溶液显碱性。
2 2 2
【详解】A.由图可知,25℃时,c(HA-)=c(H A)时,pH约为4,则HA第一步电离平
2 2
资料收集整理【淘宝店铺:向阳百分百】衡常数K = ≈10-4,A正确;
a1
B.c点溶液中,溶液中溶质为NaHA和NaA,且c(HA-)=c(A2-),由电荷守恒可知
2
c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-),pH=7,c(H+)=c(OH-),故c(Na+)=c(HA-)
+2c(A2-)=3c(HA-)=3c(A2-)=2c(HA-)+c(A2-),B正确;
C.未加氢氧化钠溶液时,HA电离出氢离子,抑制水的电离,加入氢氧化钠溶液,酸
2
逐渐被中和为盐,对水的抑制程度减弱,生成的NaHA、NaA能水解,促进水的电离,
2
当酸碱恰好中和为NaA,即d点附近(pH突变),对水的电离促进程度最大,故a、b、
2
c、d四点溶液中水的电离程度:d>c>b>a,C正确;
D.b点溶液中溶质为NaHA和NaA,结合图像可知c(Na+)>c(HA-)>c(A2-)>c(H A),b
2 2
点pH<7,c(H+)>c(OH-),HA被滴定分数 >1,c(OH-)>c(H A),D错误;
2 2
故选D。
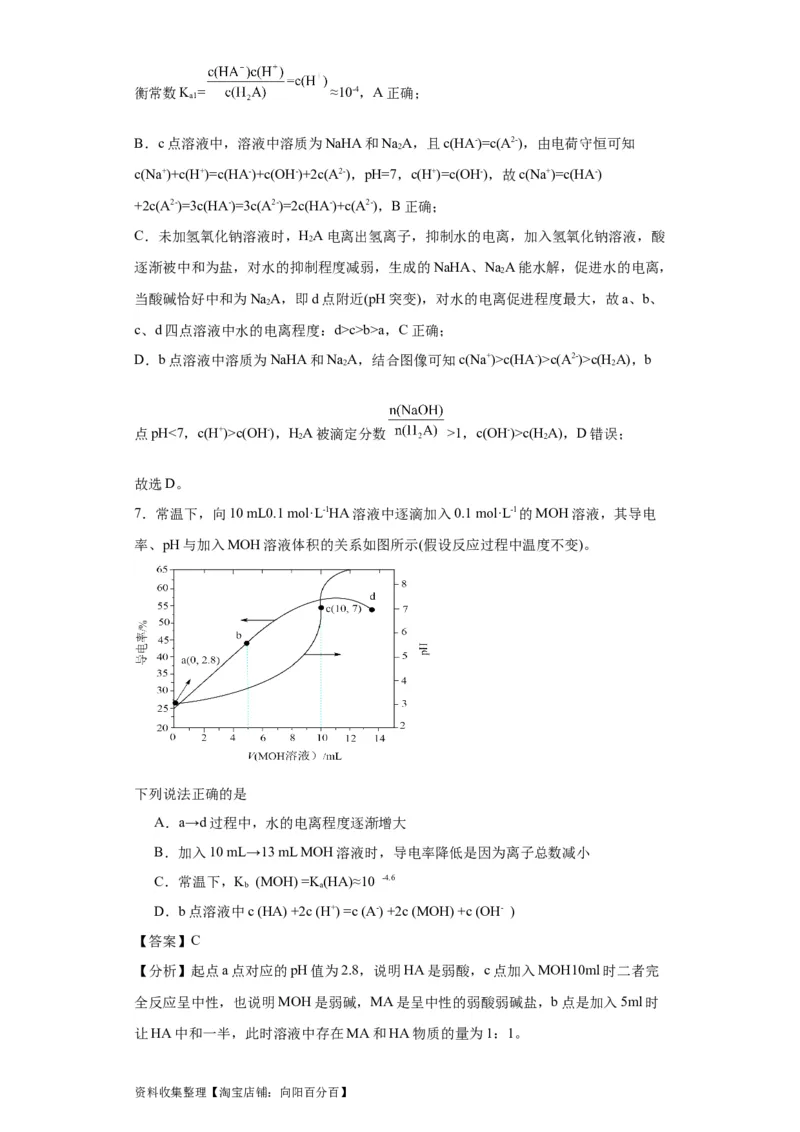
7.常温下,向10 mL0.1 mol·L-1HA溶液中逐滴加入0.1 mol·L-1的MOH溶液,其导电
率、pH与加入MOH溶液体积的关系如图所示(假设反应过程中温度不变)。
下列说法正确的是
A.a→d过程中,水的电离程度逐渐增大
B.加入10 mL→13 mL MOH溶液时,导电率降低是因为离子总数减小
C.常温下,K (MOH) =K(HA)≈10 -4.6
b a
D.b点溶液中c (HA) +2c (H+) =c (A-) +2c (MOH) +c (OH- )
【答案】C
【分析】起点a点对应的pH值为2.8,说明HA是弱酸,c点加入MOH10ml时二者完
全反应呈中性,也说明MOH是弱碱,MA是呈中性的弱酸弱碱盐,b点是加入5ml时
让HA中和一半,此时溶液中存在MA和HA物质的量为1:1。
资料收集整理【淘宝店铺:向阳百分百】【详解】A.a→c过程是由酸到正盐的过程,水的电离程度逐渐增大,c→d是碱过量
又抑制水的电离,故A错误;
B.10 mL→13 mL是碱过量,离子数目继续增加,溶液体积继续增大,但是离子浓度
在减小,所以导电率减小,故B错误;
C.因为生成的弱酸弱碱盐呈中性,说明K (MOH) =K(HA),在a点pH=2.8,
b a
c(H+)=c(A-)= ,c(HA)=0.1mol/L,
,故C正确;
D.b点是加入5ml时让HA中和一半,此时溶液中存在MA和HA物质的量为1:1,
根据物料守恒和电荷守恒得出如下式子c(HA)+c(A-)=2c(M+)+2c(MOH)(1)和c(H+)
+c(M+)=c(A-)+c(OH-)(2),(1)+ 得到如下式子:c (HA) +2c (H+) =c (A-) +2c
(MOH) +2c (OH- ),故D错误;
答案选C。
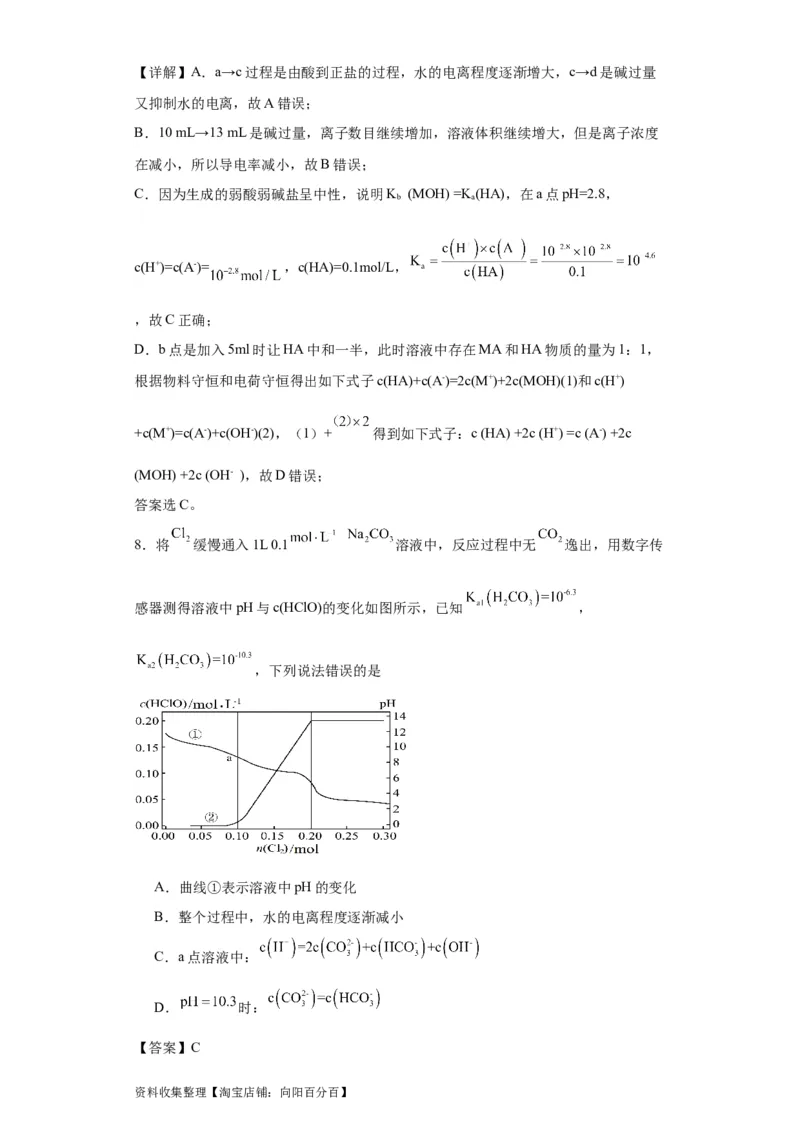
8.将 缓慢通入1L 0.1 溶液中,反应过程中无 逸出,用数字传
感器测得溶液中pH与c(HClO)的变化如图所示,已知 ,
,下列说法错误的是
A.曲线①表示溶液中pH的变化
B.整个过程中,水的电离程度逐渐减小
C.a点溶液中:
D. 时:
【答案】C
资料收集整理【淘宝店铺:向阳百分百】【分析】碳酸钠是强碱弱酸盐,在溶液中水解使溶液呈碱性,促进水的电离,氯气与
水反应生成盐酸和次氯酸,次氯酸的酸性弱于碳酸,但强于碳酸氢根离子,向碳酸钠
溶液中通入氯气时,盐酸和次氯酸均能与碳酸钠溶液反应,完全反应得到氯化钠、碳
酸氢钠和次氯酸钠的混合溶液,溶液pH减小、水的电离程度减小,再通入氯气,盐酸
与碳酸氢钠溶液反应,次氯酸与碳酸氢钠溶液不反应,完全反应得到氯化钠、碳酸和
次氯酸的混合溶液,溶液中次氯酸的浓度增大、溶液pH减小、水的电离程度减小,再
通入氯气至饱和,氯气与水反应生成盐酸和次氯酸,反应得到氯化钠、盐酸、碳酸和
次氯酸的混合溶液,溶液pH减小、水的电离程度减小,则由图可知,曲线①表示溶液
中pH的变化,曲线②表示溶液中次氯酸浓度的变化。
【详解】A.由分析可知,曲线①表示溶液中pH的变化,故A正确;
B.由分析可知,随着氯气的通入,水的电离程度逐渐减小,故B正确;
C.由图可知,a点氯气的物质的量为0.1mol,氯气与水反应得到的盐酸和次氯酸与碳
酸钠溶液恰好反应得到等浓度的氯化钠、碳酸氢钠和次氯酸钠的混合溶液,溶液中存
在电荷守恒关系c(Na+)+c(H+)=2c(CO )+c(HCO )+c(ClO—)+c(Cl—)+c(OH—)和存在物料
守恒关系c(Na+)= c(CO )+c(HCO )+c(H CO)+c(ClO—)+c(Cl—)+ c(HClO),整合两式可
2 3
得c(H CO)+ c(HClO) +c(H+)= c(CO )+ c(OH—),故C错误;
2 3
D.由电离常数公式可知,碳酸的电离常数K (H CO)= =10-10.3,若溶
a2 2 3
液pH为10-10.3,则溶液中c(CO )=c(HCO ),故D正确;
故选C。
9.常温下,向20.00mL0.1000mol•L-1的NH •H O溶液中滴加0.1000mol•L-1的盐酸,溶
3 2
液中lg 随pH的变化关系如图所示.下列说法不正确的是
资料收集整理【淘宝店铺:向阳百分百】A.常温下,NH •H O电离常数为10-4.75
3 2
B.当溶液的pH=7时,消耗盐酸的体积小于20mL
C.溶液中水的电离程度:c>b>a
D. 点溶液中:c(NH )>c(Cl-)
【答案】C
【详解】A.常温下,NH •H O的电离常数为K= ,c点pH=9.25时,
3 2 a
lg =0,c( )=c(NH•H O),NH •H O的电离常数= =10-4.75,故A
3 2 3 2
正确;
B.向20.00mL .1000mol/L的氨水中滴加0.1000mol/L的盐酸20mL,此时正好反应生
0
成氯化铵,氯化铵为强酸弱碱盐,水解显酸性,此时溶液的pH<7,因此维持溶液
pH=7,所加盐酸的体积小于20mL,故B正确;
C.溶液酸性或者碱性越强,水的电离程度越小,a点溶液中的溶质为NH Cl、
4
HCl,HCl的量较多,对水的电离抑制程度较大,而b点溶液为中性,水正常电离。c点
溶液中溶质为NH Cl和少量NH •H O,水的电离程度:c<a<b,故C错误;
4 3 2
D.c代表氨水和氯化铵的混合溶液,溶液为碱性,c(OH-)>c(H+),根据电荷守恒,c(
)+c(H+)=c(Cl-)+c(OH-),推出c( )>c(Cl-),故D正确;
故选:C。
10.已知: 。室温下,向0.10mol/LHX溶液中滴加0.10mol/
资料收集整理【淘宝店铺:向阳百分百】LNaOH溶液,溶液pH随 变化关系如图所示。下列说法错误的是
A.溶液中水的电离程度:a<b<c
B.b点溶液中:
C.c点溶液中:
D.室温下NaX的水解平衡常数为
【答案】C
【分析】电离平衡常数只受温度的影响,因此用a或c点进行判断,用a点进行分析,
,c(H+)=10-3.75mol·L-1,HX的电离平衡常数的表达式
,代入数值,Ka=10-4.75,由于a、b、c均为酸性溶液,因此溶质均
为HX和NaX,不可能是NaX或NaX和NaOH,pH<7说明HX的电离程度大于X-的
水解程度,即只考虑HX电离产生H+对水的抑制作用,然后进行分析;
【详解】A.根据图示可知,a、b、c均为酸性溶液,则溶质为HX和NaX,pH<7的
溶液中,HX的电离程度大于X-的水解程度,可只考虑H+对水的电离的抑制,溶液pH
越大氢离子浓度越小,水的电离程度越大,则溶液中水的电离程度:a c(OH-),则c(Na+)<10c(HX),C错误;
D.HX在溶液中存在电离平衡:HX H++X-,Ka= ,则pH=pKa+p[
⇌
],带入c点坐标(1,5.75)可知,pKa=4.75,则Ka=10-4.75,则室温下室温下NaX
的水解平衡常数K = =10-9.25,D正确;
h
故合理选项是C。
11.某种天然碱的化学式为 ,取一定质量该天然碱溶于水,
逐滴加入稀盐酸,溶液中的 的物质的量与加入HCl的物质的量变化如图所示,
以下说法正确的是
A.
B.水的电离程度:
C.N点溶液中存在:
D.P点溶液中:
【答案】C
【分析】天然碱溶于水,加入稀盐酸,先发生①NaCO+HCl=NaHCO +NaCl,当
2 3 3
NaCO 消耗完后,继续加入稀盐酸,发生②NaHCO +HCl=NaCl+CO↑+HO,根据
2 3 3 2 2
图象可知,0~1发生反应①,1~4发生②,据此分析;
【详解】A.MN段发生NaCO+HCl=NaHCO +NaCl,消耗盐酸的物质的量为
2 3 3
资料收集整理【淘宝店铺:向阳百分百】1mol,生成n(NaHCO )=1mol,原溶液中n(Na CO)=1mol,1~4发生NaHCO +
3 2 3 3
HCl=NaCl+CO↑+HO,该段消耗盐酸的物质的量为3mol,消耗碳酸氢钠的物质的量
2 2
为3mol,则原溶液中NaHCO 的物质的量为2mol,天然碱中碳酸钠与碳酸氢钠的物质
3
的量之比为1∶2,即a:b=1∶2,故A错误;
B.NaCO、NaHCO 均属于强碱弱酸盐, 均发生水解,促进水的电离,
2 3 3
但 的水解程度大于 水解程度,随着反应进行水的电离程度:M>N>P,故
B错误;
C.N点的溶质为NaHCO 和NaCl,根据质子守恒,因此有
3
,故C正确;
D.根据分析可知,P点溶质为NaHCO3和NaCl,电荷守恒,
,故D错误;
答案为C。
12.已知:MOH的碱性比NOH强。常温下,用HCl分别调节浓度均为 的
MOH溶液和NOH溶液的pH(溶液体积变化忽略不计),溶液中 、 的物质的量浓
度的负对数与溶液的pH关系如图所示,下列说法正确的是
A.曲线Ⅰ表示 与pH的关系
B.溶液中水的电离程度:YZ
D.常温时,反应 的平衡常数
【答案】D
资料收集整理【淘宝店铺:向阳百分百】【详解】A. ,图像中X和Y点对应的溶液中,
,pH大的碱性强,所以曲线Ⅰ代表 与pH的关系,故A错误;
B.溶液中 来自水的电离,Y点对应的溶液中水的电离程度大于X点,故B错误;
C.由电荷守恒 和 可
知,两点对应的溶液pH相同, 相同,由图中 ,则有
,故C错误;
D. ,X、Y点对应的溶液中 ,
,故 ,故D正确;
答案选D。
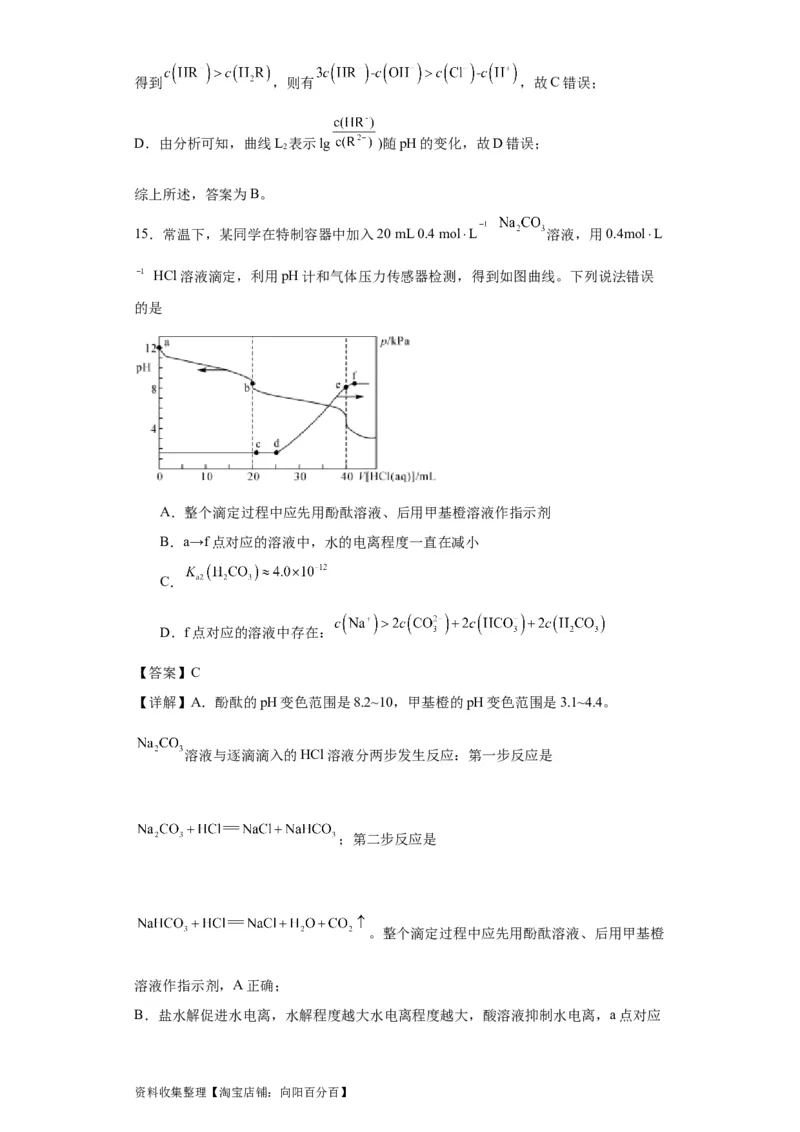
13.25°C时,用1.0 mol·L-1 NaOH溶液滴定20.00 mL c mol·L-1的盐酸,用0.010
1
mol·L-1 NaOH溶液滴定20.00 mL c mol·L-1的盐酸,滴定曲线如图所示。下列说法不正
2
确的是(已知lg5=0.7)
A.曲线b表示滴定c mol·L-1的盐酸
2
B.水的电离程度在V (NaOH) = 20.00 mL时最大
C.滴定至pH=7时,两份溶液导电能力相同
D.当1.0 mol·L-1 NaOH溶液滴定至19.98 mL时,混合溶液的pH约为3.3
【答案】C
【详解】A.根据图像,两种浓度的盐酸与两种浓度的NaOH溶液混合后完全反应时
消耗V(NaOH)=20.00mL,pH达到中性,所以c=1.0mol/L,c=0.01mol/L,故曲线a表
1 2
资料收集整理【淘宝店铺:向阳百分百】示c 浓度的盐酸,曲线b表示滴定c mol·L-1的盐酸,故A正确;
1 2
B.已知强酸或强碱会抑制水的电离,所以酸碱恰好反应时水的电离程度最大,而V
(NaOH) = 20.00 mL时酸碱恰好反应,则此时水的电离程度最大,故B正确;
C.已知离子浓度越高的溶液导电性越强,pH=7时,曲线a表示的溶液离子浓度更大,
导电能力更强,故C错误;
D.曲线a表示c 浓度的盐酸,当1.0 mol·L-1 NaOH溶液滴定至19.98 mL时,剩余
1
0.02mL1.0 mol·L-1HCl溶液,混合溶液的 ,
pH=-lgc(H+)=4-lg5=3.3,故D正确;
故选:C。
14.常温下,0.1mol·L-1HR 溶液中HR、HR-、R2-三者所占物质的量分数(分布系数δ )
2 2
随pH变化的关系如图1所示,向0.1mol·L-1NaR溶液中滴加稀盐酸,所得混合溶液的
2
pH与P[P=lg 或lgc ]变化关系如图2所示。下列说法正确的是
A.图1中M点即为图2中N点,反应HR+R2- 2HR-的平衡常数K=100
2
B.水的电离程度c=d>b> a
C.d点时,3c (HR-) -c (OH- ) 2, 则有Kb= ,即 ,C正确;
D.b和b'点的纵坐标之和为14,b点溶液中c(H+)等于b'点溶液中c ( OH- ), 两点
对水的电离影响程度相等,d点两曲线pH相同,由A项推出BOH和HA电离平衡常
数相同,则该点的pH=7,因此对于碱的溶液,pH逐渐减小,溶液中水电离程度逐渐
增大,故a'~ d水的电离程度逐渐增大,D正确;
故选A。
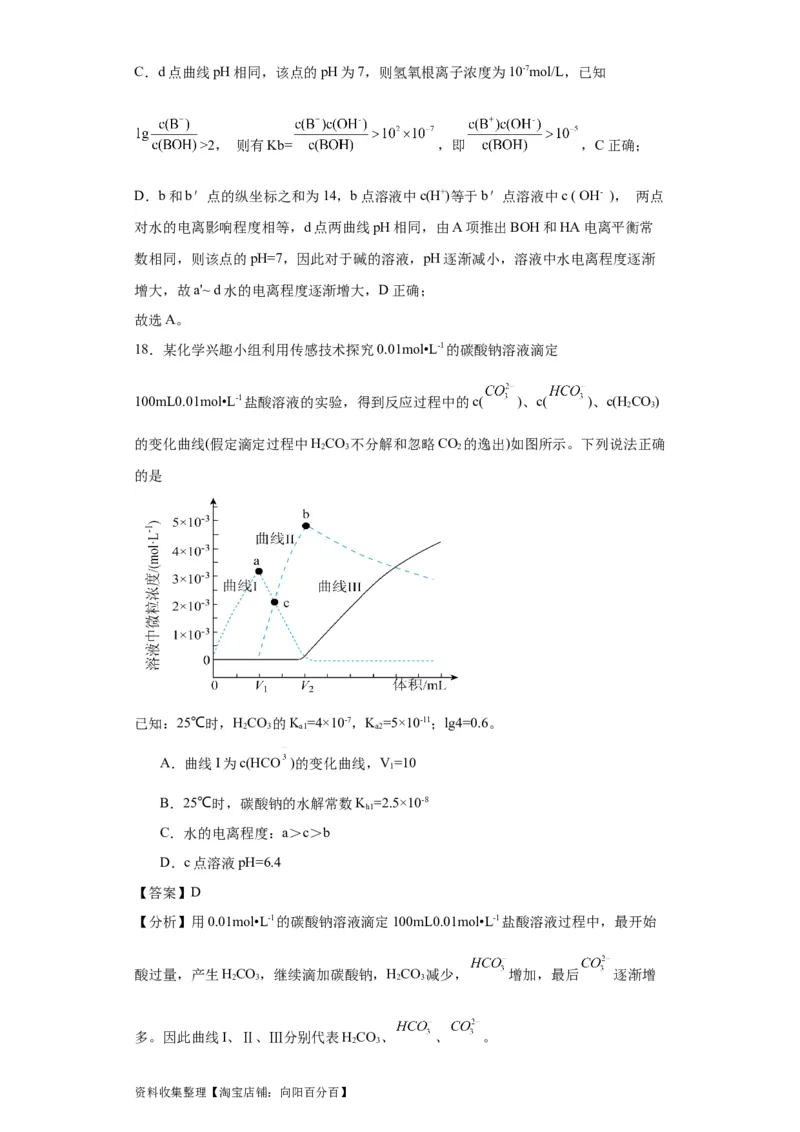
18.某化学兴趣小组利用传感技术探究0.01mol•L-1的碳酸钠溶液滴定
100mL0.01mol•L-1盐酸溶液的实验,得到反应过程中的c( )、c( )、c(HCO)
2 3
的变化曲线(假定滴定过程中HCO 不分解和忽略CO 的逸出)如图所示。下列说法正确
2 3 2
的是
已知:25℃时,HCO 的K =4×10-7,K =5×10-11;lg4=0.6。
2 3 a1 a2
A.曲线I为c(HCO )的变化曲线,V=10
1
B.25℃时,碳酸钠的水解常数K =2.5×10-8
h1
C.水的电离程度:a>c>b
D.c点溶液pH=6.4
【答案】D
【分析】用0.01mol•L-1的碳酸钠溶液滴定100mL0.01mol•L-1盐酸溶液过程中,最开始
酸过量,产生HCO,继续滴加碳酸钠,HCO 减少, 增加,最后 逐渐增
2 3 2 3
多。因此曲线I、Ⅱ、Ⅲ分别代表HCO、 、 。
2 3
资料收集整理【淘宝店铺:向阳百分百】【详解】A.由分析可知,曲线I代表HCO,根据
2 3
可知100mL 0.01mol•L-1HCl应恰好消耗50mL 0.01mol•L-1的碳酸钠溶液,故V=50,A
1
错误;
B.25℃时,碳酸钠的水解常数 ,B错误;
C. 、 均促进水电离, 含量越高,水电离程度越大,根据图像可知,
水的电离程度:ac点>a点,
D正确。
故选D。
20.HA是一元弱酸,BOH是一元弱碱,常温下,不同浓度的NaA或BCl溶液的pH
与-lg 或-lg 的关系如图所示。下列叙述正确的是
资料收集整理【淘宝店铺:向阳百分百】A.线ab表示BCl溶液的pH与-lg 的关系
B.B+的水解平衡常数K=10-5
h
C.等体积等浓度的HA溶液和BOH溶液混合后溶液呈中性
D.水的电离程度:b=d<c=a
【答案】C
【分析】 , ,即-lg =-
lg =pH-lg ,故-lg 与pH与正比关系,即线ab表示NaA
溶液的pH与-lg 的关系,则线cd表示BCl溶液的pH与-lg 的关系,据此
解答。
【详解】A.由分析可知,线ab表示NaA溶液的pH与-lg 的关系,故A错误;
B.d点时,pH=5=-lg c(H+)时,-lg =4,则c(H+)=10-5mol·L-1, =10-4,
K(B+)= ·c(H+)=10-5×10-4=10-9,故B错误;
h
C. ,由b点可知pH=9=-lgc(H+)时,-lg =4,即
资料收集整理【淘宝店铺:向阳百分百】=10-4, ,等体积等浓度的HA溶液与BOH溶液
混合得BA溶液,由于K(HA)=K (BOH),BA溶液呈中性,故C正确;
a b
D.a点溶液pH=8,溶液质为NaA,c点溶液pH=6,溶质为BCl,这两点溶液中由水
电离的c(H+)=c(OH-)=10-6 mol·L-1;b点溶液pH=9,溶质为NaA,d点溶液pH=5,溶
质为BCl,这两点溶液中由电离的c(HL)=c(OH-)=10-5 mol·L-1,水的电离程度b=d>
c=a,故D错误;
故选C。
资料收集整理【淘宝店铺:向阳百分百】