文档内容
专题 02 物质的分离与提纯、物质的检验与鉴别
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 物质的分离与提纯
考点二 物质的检验与鉴别
考点一 物质的分离与提纯
一、选择题
1.(2023·广东·模拟预测)下列除去杂质的方法中,所用试剂不能达到目的的是
物质(杂质) 除杂试剂
A FeCl 溶液(FeCl ) Fe粉
2 3
B Cl(HCl) 饱和的食盐水
2
C NaCl溶液(CaCl ) NaCO 溶液、HCl溶液
2 2 3
D CH=CH (SO ) 酸性高锰酸钾溶液
2 2 2
2.(2023·上海嘉定·统考二模)制备下列物质过程中,净化除杂的有关操作(括号内是杂质)其中正确的是
A.C H(SO )——气体通过盛有溴水的洗气瓶
2 4 2
B.CHCOOC H(CHCOOH)——用饱和NaCO 溶液洗涤
3 2 5 3 2 3
C.Cl(HCl)——通过水洗,再干燥
2
D.NH (H O)——浓HSO 洗气
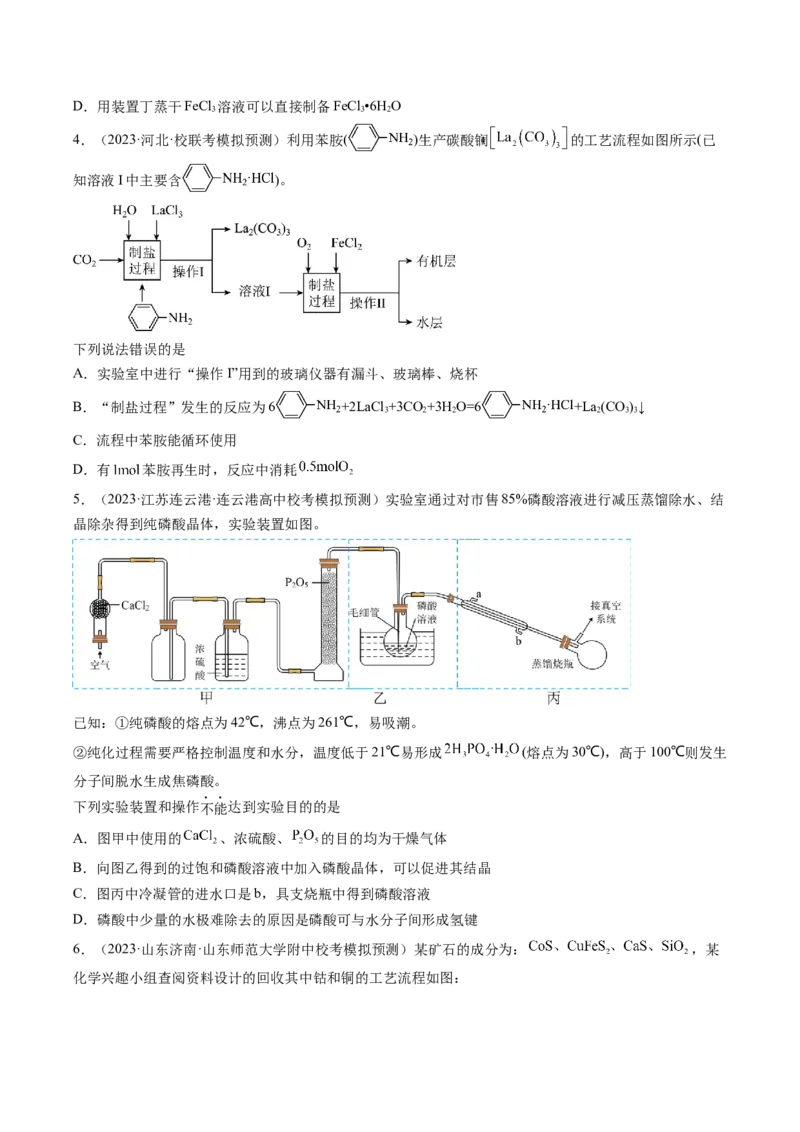
3 2 2 4
3.(2023·江苏南京·统考模拟预测)利用废蚀刻液(含FeCl 、CuCl 及FeCl )制备碱性蚀刻液[Cu(NH )Cl
2 2 3 3 4 2
溶液]和FeCl •6H O步骤:用HO 氧化废蚀刻液、制备氨气、制备碱性蚀刻液[CuCl +4NH=Cu(NH)Cl]、
3 2 2 2 2 3 3 4 2
固液分离、用盐酸溶解沉淀并制备FeCl •6H O。下列有关实验的说法不正确的是
3 2
A.用装置甲制备氨气
B.用装置乙可以制备Cu(NH )Cl 溶液并沉铁
3 4 2
C.用装置丙可以分离Cu(NH )Cl 溶液和Fe(OH)
3 4 2 3
1
原创精品资源学科网独家享有版权,侵权必究!D.用装置丁蒸干FeCl 溶液可以直接制备FeCl •6H O
3 3 2
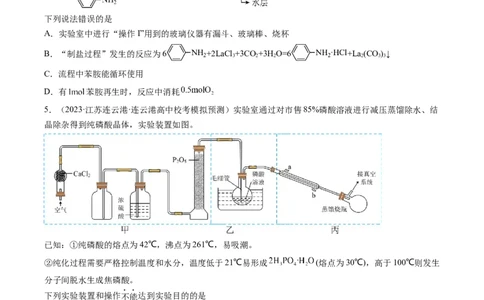
4.(2023·河北·校联考模拟预测)利用苯胺( )生产碳酸镧 的工艺流程如图所示(已
知溶液I中主要含 )。
下列说法错误的是
A.实验室中进行“操作I”用到的玻璃仪器有漏斗、玻璃棒、烧杯
B.“制盐过程”发生的反应为6 +2LaCl +3CO +3H O=6 +La(CO)↓
3 2 2 2 3 3
C.流程中苯胺能循环使用
D.有 苯胺再生时,反应中消耗
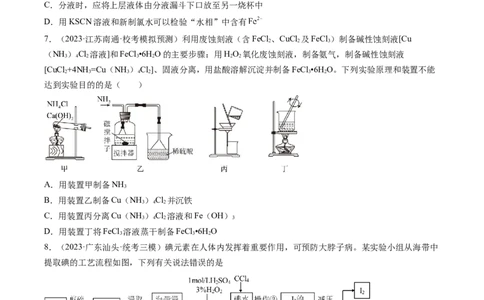
5.(2023·江苏连云港·连云港高中校考模拟预测)实验室通过对市售85%磷酸溶液进行减压蒸馏除水、结
晶除杂得到纯磷酸晶体,实验装置如图。
已知:①纯磷酸的熔点为42℃,沸点为261℃,易吸潮。
②纯化过程需要严格控制温度和水分,温度低于21℃易形成 (熔点为30℃),高于100℃则发生
分子间脱水生成焦磷酸。
下列实验装置和操作不能达到实验目的的是
A.图甲中使用的 、浓硫酸、 的目的均为干燥气体
B.向图乙得到的过饱和磷酸溶液中加入磷酸晶体,可以促进其结晶
C.图丙中冷凝管的进水口是b,具支烧瓶中得到磷酸溶液
D.磷酸中少量的水极难除去的原因是磷酸可与水分子间形成氢键
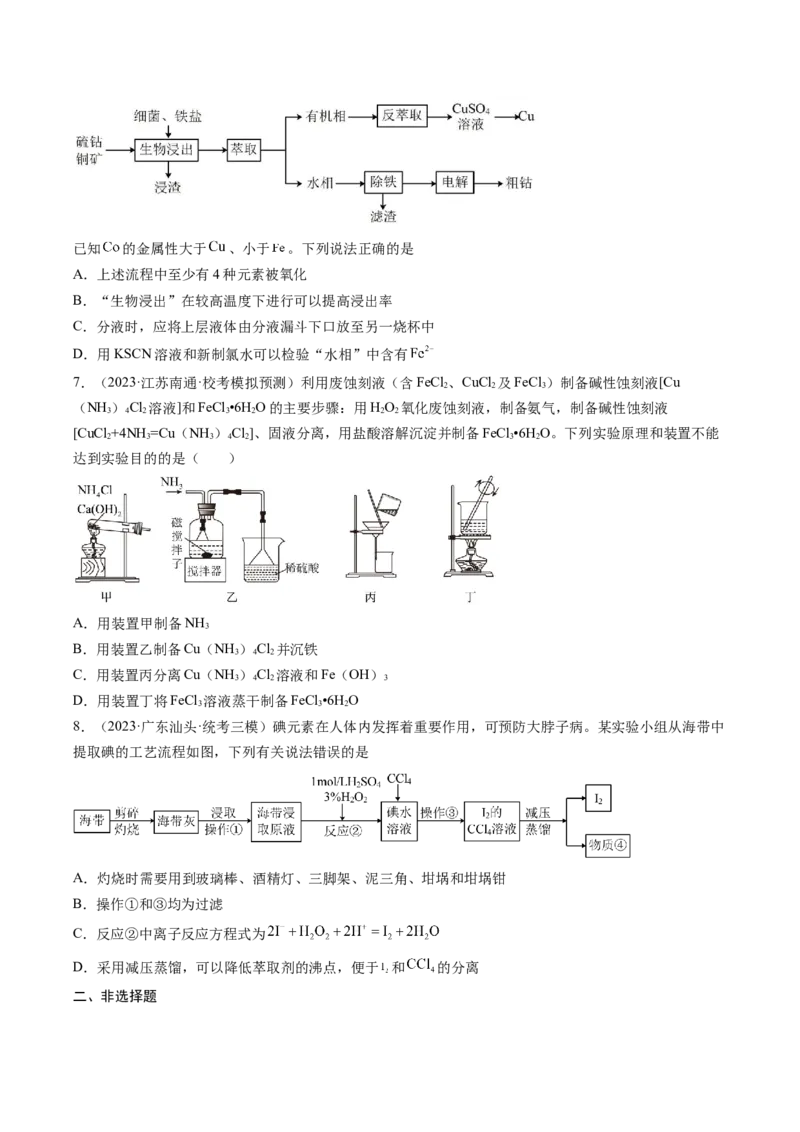
6.(2023·山东济南·山东师范大学附中校考模拟预测)某矿石的成分为: ,某
化学兴趣小组查阅资料设计的回收其中钴和铜的工艺流程如图:已知 的金属性大于 、小于 。下列说法正确的是
A.上述流程中至少有4种元素被氧化
B.“生物浸出”在较高温度下进行可以提高浸出率
C.分液时,应将上层液体由分液漏斗下口放至另一烧杯中
D.用KSCN溶液和新制氯水可以检验“水相”中含有
7.(2023·江苏南通·校考模拟预测)利用废蚀刻液(含FeCl 、CuCl 及FeCl )制备碱性蚀刻液[Cu
2 2 3
(NH )Cl 溶液]和FeCl •6H O的主要步骤:用HO 氧化废蚀刻液,制备氨气,制备碱性蚀刻液
3 4 2 3 2 2 2
[CuCl +4NH=Cu(NH )Cl]、固液分离,用盐酸溶解沉淀并制备FeCl •6H O。下列实验原理和装置不能
2 3 3 4 2 3 2
达到实验目的的是( )
A.用装置甲制备NH
3
B.用装置乙制备Cu(NH )Cl 并沉铁
3 4 2
C.用装置丙分离Cu(NH )Cl 溶液和Fe(OH)
3 4 2 3
D.用装置丁将FeCl 溶液蒸干制备FeCl •6H O
3 3 2
8.(2023·广东汕头·统考三模)碘元素在人体内发挥着重要作用,可预防大脖子病。某实验小组从海带中
提取碘的工艺流程如图,下列有关说法错误的是
A.灼烧时需要用到玻璃棒、酒精灯、三脚架、泥三角、坩埚和坩埚钳
B.操作①和③均为过滤
C.反应②中离子反应方程式为
D.采用减压蒸馏,可以降低萃取剂的沸点,便于 和 的分离
二、非选择题9.(2023·河北·统考一模)高纯超细氧化铝粉是一种新型无机功能材料,以 和 为原
料制备复盐硫酸铝铵晶体[ ],将硫酸铝铵晶体热分解可制得高纯超细氧化铝粉,其流
程如下:
回答下列问题:
(1)操作①需加入适量稀硫酸,其目的是 ,采用的纯化方法为 。
(2)取 加热分解,加热过程中固体质量随温度的变化如图所示。硫酸铝铵晶体在
633℃、975℃分解生成的固体分别为 、 。(填化学式)
(3)实验室以 和 为原料,在一定条件下反应生成制备纳米 的前驱体
沉淀,同时生成 、 和 。 高温分解即得超细氧
化铝粉。反应生成 沉淀的化学方程式为 。
(4)为了测定高纯超细氧化铝粉中 的质量分数,可用EDTA标准溶液滴定。取0.2035g高纯超细氧化
铝粉溶于盐酸,加入过量的30.00mL0.1600 EDTA标准溶液并加热煮沸,充分反应后,再用
标准溶液滴定过量的EDTA至终点,消耗 标准溶液。已知 、 与
EDTA反应的化学计量数之比均为1:1。
①加入过量的EDTA标准溶液并加热煮沸,其原因是 。
②高纯超细氧化铝粉中, 的质量分数为 %(保留1位小数)。
考点二 物质的检验与鉴别
一、选择题
1.(2023·广东肇庆·高要一中校考二模)在允许加热的前提下,只用一种试剂不能鉴别对应溶液的是
A.用Ba(OH) 溶液鉴别NH Cl、(NH )SO 、NaCl、NaSO
2 4 4 2 4 2 4
B.用FeCl 溶液鉴别NaI、Ba(OH) 、NaS、NaHCO
3 2 2 3
C.用NaOH溶液鉴别MgCl 、FeCl 、Al (SO )、(NH )SO
2 2 2 4 3 4 2 4D.用红色石蕊试纸鉴别NaSO 、浓HNO、NaHCO 、氯水
2 3 3 3
2.(2023春·湖南·高三湖南师大附中校联考开学考试)地壳表面分布很多阳离子,下列关于指定阳离子的
检验方法正确的是
A. :向样品溶液中逐滴滴加氨水,先产生蓝色沉淀,然后沉淀消失,则有
B. :向样品溶液中滴加氯水,再加入 溶液,溶液血红色,则有
C. :向样品溶液中滴加 溶液,产生白色沉淀,再滴加稀盐酸,产生使澄清石灰水变浑浊的
气体,则有
D. :向样品溶液中滴加 溶液,产生使湿润的红色石蕊试纸变蓝的气体,则有
3.(2023·广东惠州·统考一模)为检验下列久置于空气中的物质是否变质,所选检验试剂(括号内)能达到
目的的是
A.新制氯水(AgNO 溶液) B.FeCl 溶液(KSCN溶液)
3 2
C.漂白粉(Na CO 溶液) D.NaSO 溶液(BaCl 溶液)
2 3 2 3 2
4.(2023·西藏拉萨·统考一模)鉴别下列各组气体时,所选用的试剂无法实现实验目的的是
选项 气体 试剂
A CO、SO 品红溶液
2 2
B NO 、溴蒸气 淀粉碘化钾溶液
2
C CH、C H 溴的四氯化碳溶液
4 2 4
D HCl、HS 硫酸铜溶液
2
5.(2023·上海徐汇·统考一模)只用水不能鉴别的是
A.苯和乙醇 B.KMnO 晶体和I 晶体
4 2
C.NaO 和硫粉 D.乙酸乙酯和乙酸丁酯
2 2
6.(2023·广东梅州·统考三模)下列各组物质中,只用蒸馏水(可用组内物质)无法检验的是
A.无水硫酸铜、氢氧化钡、硫酸镁、碳酸钡
B.乙醇、硝基苯、甲苯
C.硫酸铝、氢氧化钠、碳酸氢钠、硝酸镁
D.碳酸钠、碳酸钾、硫酸钾、氯化钡
7.(2023秋·全国·高三开学考试)某溶液仅由 、Cl-、 、 、 、Fe3+、Al3+和K+中的若
干种离子组成,且各离子浓度相等,取适量溶液进行如下实验:
①取该溶液加入过量NaOH溶液,加热,产生无色气体;②将①过滤、洗涤、灼烧,得到固体a;③向上
述滤液中加足量BaCl 溶液,产生白色沉淀:
2根据以上实验,下列推断错误的是
A.根据操作①,推断一定存在
B.②中固体a为氧化铁
C.原溶液中一定不存在 、Al3+,可能含有K+
D.说明原溶液中一定存在 、Cl-、 、 、Fe3+、
8.(2023·福建三明·统考模拟预测) 的KOH溶液称为奈斯勒(Nessler)试剂,其制备流程及特色
反应如图所示。
下列说法错误的是
A.反应①的离子方程式为:
B.由反应②可知用KI溶液可除去 中的
C.反应③中消耗的 和 的物质的量之比为1:4
D.可用奈斯勒试剂检验 中微量的
二、非选择题
9.(2023·安徽安庆·安庆一中校考三模)胆矾(CuSO ·5H O)又名蓝矾,是化学工业、医药领域中的常见物
4 2
质。某实验小组利用有色金属加工企业的废材制得粗胆矾晶体。
(1)制得的粗晶体中可能含有Fe (SO )、FeCl 杂质,选用下列试剂,确定所含杂质。可选试剂有:蒸馏水、
2 4 3 3
稀硫酸、氨水、Ba(NO ) 溶液、BaCl 溶液、AgNO 溶液。请补充以下实验步骤:
3 2 2 3
①取一定量样品,加入蒸馏水、稀硫酸,固体溶解,得到蓝色透明溶液;②取少量①所得溶液,滴加
至过量,先析出沉淀,后沉淀部分溶解,过滤得深蓝色溶液,滤渣为红褐色;③另取少量①所得溶液,加
入足量的 溶液,出现白色沉淀;④取③中所得上层清液,加入 溶液,无明显现象。
实验结论:粗胆矾晶体中含有Fe (SO ),不含FeCl 。
2 4 3 3
(2)CuSO ·5H O的含量测定:
4 2
①称取1.250g产品配成100 mL溶液,取25.00 mL溶液于锥形瓶中,加入足量NaF溶液后,再滴加KI溶
液至不再产生CuI沉淀;②以淀粉溶液作为指示剂,用0.1000 mol·L-1 Na SO 标准溶液进行滴定,平行滴
2 2 3
定3次。已知:Fe3++6F-= ;I+2Na SO=2NaI+Na SO
2 2 2 3 2 4 6
请回答:步骤①中,加入足量NaF溶液的可能原因是 ,若不加NaF溶液,可导致最终的测量值
(填 “偏大”“偏小”或“无影响”)。滴加KI溶液生成沉淀的离子方程式为 ; 若NaSO 标准溶
2 2 3
液的平均用量为10.00 mL,则产品中胆矾的质量分数为 。