文档内容
专题 02 物质的量及化学计算
1.下列对于“摩尔”的理解正确的是( )
A.摩尔是一个物理量,它表示含有一定数目粒子的集合体
B.摩尔是物质的量的单位,简称摩,符号为mol
C.国际上规定,0.012 kg碳原子所含有的碳原子数目为 1摩尔
D.1摩尔任何物质均含有6.02×1023个原子
【答案】B
【解析】物质的量是一个物理量,摩尔是其单位,A错误;摩尔是物质的量的单位,简称摩,符号为
mol,B正确;国际上规定,0.012 kg 12C所含的碳原子数目为阿伏加德罗常数,即0.012 kg 12C所含的碳
原子数目为1 mol,C错误;构成物质的微粒不同,1摩尔任何物质不一定含有6.02×1023个原子,D错误。
2.(2022·浙江省浙北G2联盟高一期中联考)下列关于物质的量的叙述中,正确的是( )
A.1mol任何物质都含有6.02×1023个分子
B.0.012kg12C中含有约6.02×1023个碳分子
C.1molNH 中含有1 mol 氮和3 mol氢
3
D.1mol Na+中含有6.02×1024个电子
【答案】D
【解析】A项,由原子、离子构成的物质不含分子,A错误;B项,0.012kg12C中含有约6.02×1023个碳原
子,B错误;C项,1molNH 中含有1 mol 氮原子和3 mol氢原子,C错误;D项,1mol Na+中含10mol电
3
子,有6.02×1024个电子,D正确;故选D。
3.(2022·浙江省绿谷高中联盟高一期中联考)下列溶液Cl-物质的量浓度与200mL1mol·L-1AlCl 溶液中Cl-物
3
质的量浓度相等的是( )
A.150mL3mol·L-1NaClO溶液 B.75mL3mol·L-1CaCl 溶液
2
C.150mL3mol·L-1KCl溶液 D.150mL2mol·L-1MgCl 溶液
2
【答案】C
【解析】200mL1mol·L-1AlCl 溶液中Cl-物质的量浓度3mol·L-1。A项,150mL3mol·L-1NaClO溶液中NaClO
3
电离出Na+和ClO-,不存在Cl-,A不符合题意;B项,75mL3mol·L-1CaCl 溶液中Cl-物质的量浓度
2
6mol·L-1,B不符合题意;C项,150mL3mol·L-1KCl溶液中Cl-物质的量浓度3mol·L-1,C符合题意;D项,
150mL2mol·L-1MgCl 溶液中Cl-物质的量浓度4mol·L-1,D不符合题意;故选C。
2
4.下列关于物质的量浓度表述正确的是
A.0.3 mol·L-1的NaSO 溶液中含有Na+和SO 2-的总物质的量为0.9 mol
2 4 4
B.在KSO 和NaCl的中性混合水溶液中,如果Na+和SO 2-的物质的量相等,则K+和Cl-的物质的量浓度
2 4 4
一定相同
C.当1 L水吸收22.4 L氨气时所得氨水的浓度不是1 mol·L-1,只有当22.4 L(标准状况)氨气溶于水制得1 L
氨水时,其浓度才是1 mol·L-1D.10 ℃时,100 mL 0.35 mol·L-1的KCl饱和溶液蒸发掉5 g水,冷却到10 ℃时,其体积小于100 mL,它
的物质的量浓度大于0.35 mol·L-1
【答案】C
【解析】A项,0.3 mol•L-1的NaSO 溶液中Na+、SO 2-的物质的量浓度为:0.6mol•L-1、0.3 mol•L-1,由于缺
2 4 4
少溶液的体积,所以无法计算出离子的物质的量,故A错误;B项,在KSO 和NaCl的中性混合水溶液中
2 4
存在:c(Na+)+c(K+)=c(Cl-)+2c(SO2-),Na+和SO 2-的物质的量相等,即物质的量浓度相等,所以 K+和Cl-的
4 4
物质的量浓度一定不相同,故B错误;C项,溶液的体积不等于溶剂的体积,所以 1 L水吸收22.4 L氨气
时所得氨水的浓度不是1 mol•L-1;标况下22.4 L氨气的物质的量为1mol,溶于水制得1 L氨水时,其浓度
一定等于1 mol•L-1,故C正确;D项,10℃时,0.35 mol•L-1的KCl饱和溶液100 mL蒸发掉5 g水,冷却到
10℃时,其体积小于100 mL,溶液仍然是饱和溶液,溶质的物质的量浓度不变,它的物质的量浓度仍为
0.35 mol•L-1,故D错误;故选C。
5.(2022·浙江省浙北G2联盟高一期中联考)下列关于物质的量的叙述中,正确的是( )
A.1mol任何物质都含有6.02×1023个分子
B.0.012kg12C中含有约6.02×1023个碳分子
C.1molNH 中含有1 mol 氮和3 mol氢
3
D.1mol Na+中含有6.02×1024个电子
【答案】D
【解析】A项,由原子、离子构成的物质不含分子,A错误;B项,0.012kg12C中含有约6.02×1023个碳原
子,B错误;C项,1molNH 中含有1 mol 氮原子和3 mol氢原子,C错误;D项,1mol Na+中含10mol电
3
子,有6.02×1024个电子,D正确;故选D。
6.(2022·浙江省杭州二中模拟)2021年4月29日11时23分,搭载空间站天和核心舱的长征五号B遥二运
载火箭,在我国文昌航天发射场升空,任务圆满成功。偏二甲肼(C HN)是一种高能燃料,燃烧产生的巨
2 8 2
大能量可作为航天运载火箭的推动力。下列叙述正确的是( )
A.偏二甲肼的摩尔质量为60g
B.6.02×1023个偏二甲肼分子的质量约为60g
C.1mol偏二甲肼的质量为60g·mol-1
D.6g偏二甲肼含有N 个偏二甲肼分子
A
【答案】B
【解析】A项,摩尔质量不能以g作单位,偏二甲肼的摩尔质量应为60g·mol-1,A错误;B项,6.02×1023
个偏二甲肼约为1mol,其质量约为60g,B正确;C项,质量不能以g·mol-1作单位,C错误;D项,6g偏
二甲肼的物质的量为6g÷60g·mol-1=0.1mol,含有的分子数为0.1N ,D错误;故选B。
A1.(2022·湖南师范大学附属中学模拟)N 是阿伏加德罗常数的值,下列说法正确的是
A
A.16.25 g FeCl 水解形成的Fe(OH) 胶体粒子数为0.1 N
3 3 A
B.22.4 L(标准状况)氩气含有的质子数为18 N
A
C.92.0 g甘油(丙三醇)中含有羟基数为1.0 N
A
D.1.0 mol CH 与Cl 在光照下反应生成的CHCl分子数为1.0 N
4 2 3 A
【答案】B
【解析】16.25g氯化铁的物质的量是16.25g÷162.5g/mol=0.1mol,由于氢氧化铁胶体是分子的集合体,因
此水解生成的Fe(OH) 胶体粒子数小于0.1 N ,A错误;标准状况下22.4L氩气的物质的量是1mol,氩气
3 A
是一个Ar原子组成的单质,其中含有的质子数是18 N ,B正确;1分子丙三醇含有3个羟基,92.0g丙三
A
醇的物质的量是1mol,其中含有羟基数是3 N ,C错误;甲烷与氯气在光照条件下发生取代反应生成的卤
A
代烃不止一种,因此生成的CHCl分子数小于1.0 N ,D错误。答案选B。
3 A
2.(2022·浙江省嘉兴市模拟)某实验小组用如下方法测定废水中苯酚的含量(其他杂质不参加反应)。
Ⅰ.用已准确称量的KBrO 固体配制250 mL 0.1000 mol·L−1 KBrO 标准溶液;
3 3
Ⅱ.取25 mL上述溶液,加入过量KBr,加HSO 酸化,溶液颜色呈棕黄色;
2 4
Ⅲ.向Ⅱ所得溶液中加入100 mL废水,加入过量KI;
Ⅳ.用0.2000 mol·L−1 NaSO 标准溶液滴定Ⅲ中溶液,滴加2滴淀粉溶液,至滴定终点,消耗NaSO 溶液
2 2 3 2 2 3
15.00 mL。
已知:BrO + 5Br- + 6H+ = 3Br + 3H O
2 2
I + 2Na SO = 2NaI + Na SO
2 2 2 3 2 4 6
请计算:
(1)Ⅰ中KBrO 固体的质量是____g。
3
(2)该废水中苯酚的含量为____g·L−1(列式计算)。
【答案】
【解析】(1)Ⅰ中用KBrO 固体配制250 mL 0.1000 mol·L−1 KBrO 标准溶液,则所需KBrO 固体的物质的量
3 3 3
为 ,质量为
;
(2) 结合化学方程式:2KI+ Br =I + 2KBr;I + 2Na SO = 2NaI + Na SO 可知消耗的NaSO 的量就是与
2 2 2 2 2 3 2 4 6 ; 2 2 3
Br 反应的KI的量, ,消耗的Br 为
2 2
,由化学方程式BrO + 5Br- + 6H+ = 3Br + 3H O可知,Ⅱ中反应得到的Br 一共有
2 2 2
0.0075mol,所以和苯酚反应的Br 的量为0.0075mol-0.0015mol=0.006mol,消耗的苯酚的物质的量为
2
,其质量为 ,由于废水的体积为100mL,所以废水中苯酚的含量为 。
3.(2022·浙江省普通高校招仿真模拟)重铬酸铵[(NH )Cr O]用作分析试剂、催化剂及媒染剂等。实验
4 2 2 7
室常利用甲醛法测定重铬酸铵样品中氮的质量分数,其反应原理为2Ba2++Cr O2−+H O = 2BaCrO ↓+2H+、
2 7 2 4
4NH ++6HCHO = 3H++6H O+(CH)NH+ [滴定时,1 mol (CH )NH+与1 mol H+相当],然后用NaOH标准
4 2 2 6 4 2 6 4
溶液滴定反应生成的酸。
实验步骤:称取样品2.800 g,配成250 mL溶液,移取25.00 mL样品溶液于锥形瓶中,加入硝酸钡溶液使
Cr O2−完全沉淀后,加入10 mL 20%的中性甲醛溶液,摇匀,静置5 min后,加入1~2滴酚酞溶液,用
2 7
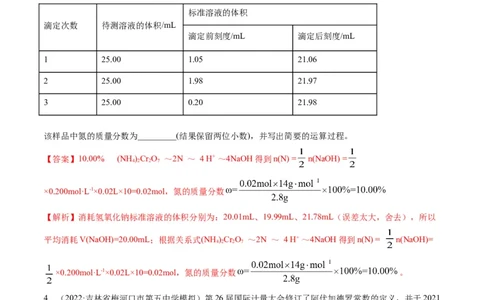
0.200 mol·L-1 NaOH标准溶液滴定至终点,重复上述操作3次。滴定结果如下表所示:
标准溶液的体积
滴定次数 待测溶液的体积/mL
滴定前刻度/mL 滴定后刻度/mL
1 25.00 1.05 21.06
2 25.00 1.98 21.97
3 25.00 0.20 21.98
该样品中氮的质量分数为_________(结果保留两位小数),并写出简要的运算过程。
【答案】10.00% (NH )Cr O ~2N ~ 4 H+ ~4NaOH得到n(N) = n(NaOH) =
4 2 2 7
×0.200mol·L-1×0.02L×10=0.02mol,氮的质量分数
【解析】消耗氢氧化钠标准溶液的体积分别为:20.01mL、19.99mL、21.78mL(误差太大,舍去),所以
平均消耗V(NaOH)=20.00mL;根据关系式(NH )Cr O ~2N ~ 4 H+ ~4NaOH得到n(N) = n(NaOH)=
4 2 2 7
×0.200mol·L-1×0.02L×10=0.02mol,氮的质量分数 。
4.(2022·吉林省梅河口市第五中学模拟)第26届国际计量大会修订了阿伏加德罗常数的定义,并于2021
年5月20日正式生效。下列说法正确的是( )
A.8.8 g乙酸乙酯中所含共用电子对数为1. 3N
A
B.常温常压下,28 g Fe与足量浓硝酸混合,转移的电子数为1.5 N
A
C.标准状况下,2.24 LCl 与CH 反应完全,形成C-Cl键的数目为0.1 N
2 4 A
D.常温下pH=12的NaOH溶液中,由水电离出的氢离子的数目为10 N
A
【答案】C
【解析】8.8 g乙酸乙酯的物质的量是0.1mol,乙酸乙酯的结构简式是 ,1个分子含有14个共用电子对,所含共用电子对数为1. 4N ,故A错误;常温常压下,Fe在浓硝酸中钝化,故B错误;标准状
A
况下,2.24 LCl 的物质的量是0.1mol,氯气与CH 发生取代反应,形成C-Cl键的数目为0.1 N ,故C正
2 4 A
确;常温下pH=12的NaOH溶液,没有溶液体积,不能计算水电离出的氢离子的数目,故D错误;故选
C。
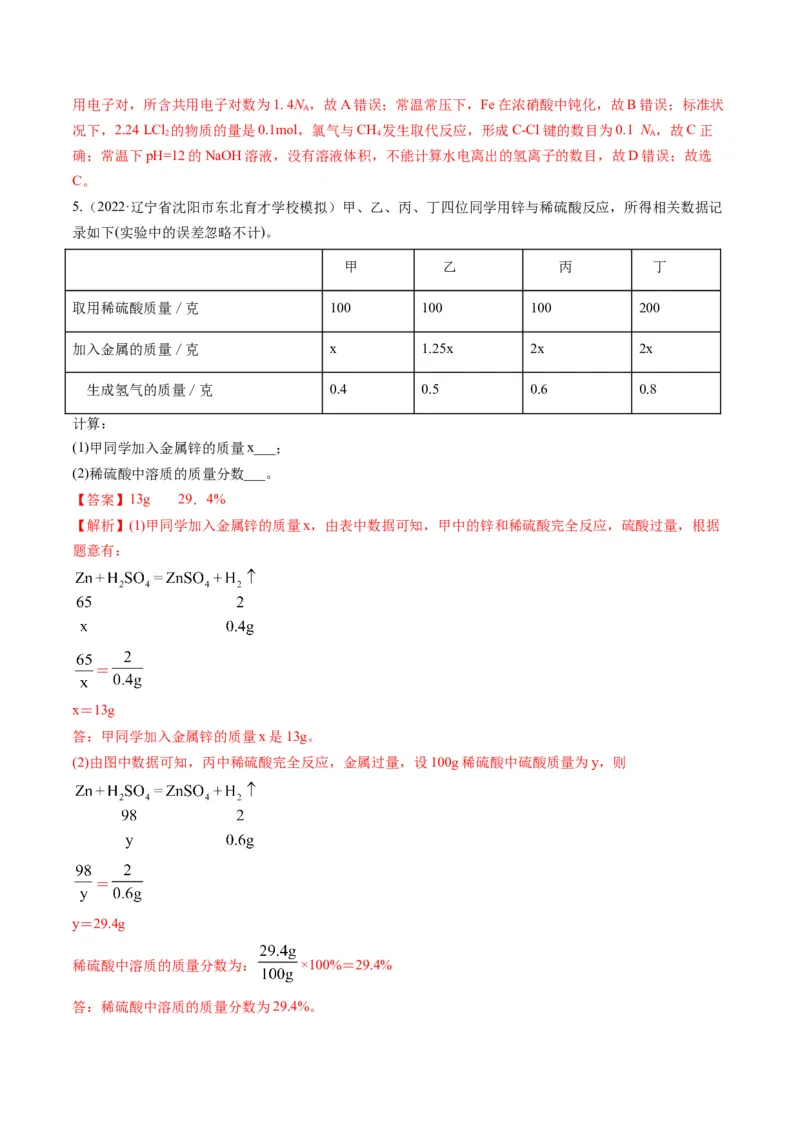
5.(2022·辽宁省沈阳市东北育才学校模拟)甲、乙、丙、丁四位同学用锌与稀硫酸反应,所得相关数据记
录如下(实验中的误差忽略不计)。
甲 乙 丙 丁
取用稀硫酸质量/克 100 100 100 200
加入金属的质量/克 x 1.25x 2x 2x
生成氢气的质量/克 0.4 0.5 0.6 0.8
计算:
(1)甲同学加入金属锌的质量x___;
(2)稀硫酸中溶质的质量分数___。
【答案】13g 29.4%
【解析】(1)甲同学加入金属锌的质量x,由表中数据可知,甲中的锌和稀硫酸完全反应,硫酸过量,根据
题意有:
=
x=13g
答:甲同学加入金属锌的质量x是13g。
(2)由图中数据可知,丙中稀硫酸完全反应,金属过量,设100g稀硫酸中硫酸质量为y,则
=
y=29.4g
稀硫酸中溶质的质量分数为: ×100%=29.4%
答:稀硫酸中溶质的质量分数为29.4%。6.(2022·浙江省名校协作体联考)已知氧钒(+4) 碱式碳酸铵晶体[分子式:(NH )(VO) (CO)(OH) ·10H O)
4 5 6 3 4 9 2
],是制备纳米VN粉体的前驱体,工业上通常以钒炉渣制备氧钒(+4) 碱式碳酸铵晶体。为测定粗产品的纯
度,进行如下实验:分别称量三份a g产品于三只锥形瓶中,每份.分别用20 mL蒸馏水与30mL稀硫酸溶
解后,加入0.0200 mol/LKMnO 溶液至稍过量,充分反应后继续滴加1%的NaNO 溶液至稍过量,再用尿
4 2
素除去过量NaNO ,最后用0.100 mol/L (NH )Fe(SO ) 标准溶液分别滴定至终点,消耗标准溶液的体积如
2 4 2 4 2
下表所示。(已知滴定反应为 +Fe2++2H+=VO2++Fe3++H O)
2
序号 滴定前读数/mL 滴定终点读数/mL
第一份 0.00 19.98
第二份 1.20 22. 40
第三份 1.56 21.58
(1)粗产品中钒的质量分数为_________(假设 V的相对原子质量为M)。
(2)写出简要计算过程:______________。
【答案】
【解析】由表格数据可知,用0.100 mol/L (NH )Fe(SO ) 标准溶液分别滴定至终点,消耗标准溶液的体积
4 2 4 2
为20.00mL,根据题干信息,氧钒(+4) 碱式碳酸铵晶体被氧化为 , 再用
0.100 mol/L (NH )Fe(SO ) 标准溶液滴定,发生发应 +Fe2++2H+=VO2++Fe3++H O,则根据原子守恒有:
4 2 4 2 2
n(V)=n(Fe2+)=20.00mL×10-3×
0.1mol/L=0.002mol,则m(V)=0.002M g,粗产品中钒的质量分数为 。
7.(2022·浙江省杭州市教学质量检测)已知粗盐水中含 ,含
。向粗盐水中加入 除Mg2+:MgCl +Ca(OH) →Mg(OH) ↓+CaCl 。然后加入 除 。
2 2 2 2
(1)处理上述粗盐水 ,至少需要加 ________ 。(保留三位有效数字)
(2)如果用碳酸化尾气(含 体积分数为0.100、 体积分数0.0400)代替碳酸钠,发生如下反Ca2+
+2NH+CO +H O→CaCO↓+2 。处理上述 粗盐水至少需要通入标准状况下________ 碳酸化
3 2 2 3
尾气。(需列式计算,保留三位有效数字)
【答案】10.4
【解析】(1)设至少需要加 的物质的量是xmol;x =98mol,需要碳酸钠的质量是98mol×106g/mol=10388g=10.4 ;
(2) 需要通入二氧化碳的物质的量是ymol;
y=98mol,通入碳酸化尾气的体积是 。
8.(2022·辽宁省沈阳市郊联体模拟)I.水中溶解氧气的测定方法如下:向一定量水样中加入适量MnSO
4
和碱性KI溶液,生成MnO(OH) 沉淀,密封静置;加入适量稀HSO ,待MnO(OH) 与I-完全反应生成
2 2 4 2
Mn2+和I 后,以淀粉作指示剂,用NaSO 标准溶液滴定至终点,反应方程式为2SO +I=SO +2I
2 2 2 3 2 2 4
-,测定过程中物质的转化关系如下:O 2MnO(OH) I SO 。
2 2 2 4
(1)写出O 将Mn2+氧化成MnO(OH) 的离子方程式:____________________。
2 2
(2)取池塘水样100.00 mL,按上述方法测定水中溶解的氧气浓度,消耗0.01000 mol·L-1 NaSO 标准溶液
2 2 3
13.50 mL。计算该水样中溶解的氧气浓度为_________mg·L-1。
II.益源生(药品名叫复方硫酸亚铁叶酸片)是一种治疗缺铁性贫血的药物其主要成分有硫酸亚铁、叶酸、干
酵母、当归、黄芪、白术等,下面是测定益源生中硫酸亚铁质量分数的实验。取10片复方硫酸亚铁片(每
片a毫克)研成粉末,加水溶解,过滤,再将滤液配成100 mL溶液,取出25 mL与双氧水反应(假设叶酸、
干酵母、当归、黄芪、白术均不与双氧水反应)。
(1)配制一定浓度的双氧水溶液用质量分数30%、密度1.l g/cm3)的双氧水配制1.0 mol/L的双氧水100 mL,
则30%双氧水物质的量浓度为________mol/L(保留一位小数),需用量简量取30%的双氧水_________mL。
(2)该实验在酸性条件下进行,则实验设计的反应原理是_____________(用离子方程式表示)。
(3)若上述实验消耗1.0 mol/L的双氧水b mL,则每片复方硫酸亚铁叶酸片中硫酸亚铁的质量分数为
_________(用含a、b的式子表示)。
【答案】O+2Mn2++4OH-=2MnO(OH)↓ 10.80 9.7 10.3 2Fe2++H O+2H+=2Fe3++2H O
2 2 2 2 2
×100%
【解析】I.(1)由题意可知,碱性条件下,溶液中O 与Mn2+发生氧化还原反应生成MnO(OH) 沉淀,反应的
2 2
离子方程式为O+2Mn2++4OH-=2MnO(OH)↓;
2 2
(2)由题意可知,酸性条件下,MnO(OH) 与I-发生氧化还原反应生成Mn2+和I,反应的化学方程式为
2 2
MnO(OH) +2I-+4H+= Mn2++I +3H O,由三个方程式可得如下关系式:O—2MnO(OH) —2I—4SO ,则
2 2 2 2 2 2 2水样中n(O )=4n(S O )= ×0.01000 mol•L-1×13.50×10—3L=3.375×10—5mol,100.00 mL水样中溶解的氧气
2 2
浓度为 =10.80mg/L;
II.(1)由物质的量浓度c= 可知,质量分数30%、密度1.l g/cm3)的双氧水的物质的量浓度为
mol/L=9.7 mol/L,设需要的浓双氧水的体积为VmL,由稀释定律可知,V=
×103mL/L=10.3mL;
(2)由题意可知,在酸性条件下溶液中亚铁离子与双氧水发生氧化还原反应生成铁离子和水,反应的离子方
程式为2Fe2++H O+2H+=2Fe3++2H O;
2 2 2
(3)b mL1.0 mol/L的双氧水的物质的量为10—3bmol,由反应的化学方程式可知,100 mL溶液溶液中亚铁离
子的物质的量为10—3bmol×2× =8×10—3bmol,则每片复方硫酸亚铁叶酸片中硫酸亚铁的质量分数为
×100%= ×100%。