文档内容
专题 04 氧化还原反应及其应用
一、单选题
1.人们曾认为的N
2
+3H 2⇌2NH
3
化学反应速率小,原料利用率低,不可能用于工业化生产,化学家们不断
地研究和改进该反应的条件,如催化剂、温度、压强等,并更新设备,成功地开发了合成氨的生产工艺。
从此,人类能为植物的生长提供足够的氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛
盾。该反应是氧化还原反应,下时说法正确的是
A.N 是还原剂 B.H 是氧化剂 C.N 失去电子 D.H 发生氧化反应
2 2 2 2
2.SO 是一种酸性氧化物,它溶于水时生成亚硫酸(H SO ),HSO 中S元素的化合价为
2 2 3 2 3
A.-2 B.0 C.+4 D.+6
3.下列变化过程中,需加入氧化剂才能实现的是
A.Cl→Cl- B.CO →CO C.Al→Al3+ D.CuO→Cu
2 2
4.下列化学反应中电子转移的表示方法正确的是
A. B.
C. D.
5.下列反应属于氧化还原反应的是
A.
B.
C.
D.
6.下列反应不属于氧化还原反应的是
A.2NaHCO NaCO+CO↑+HO
3 2 3 2 2B.2Al+3CuSO =Al(SO )+3Cu
4 2 4 3
C.Cl+2NaOH=NaCl+NaClO+HO
2 2
D.4HNO 4NO +O↑+2HO
3 2 2 2
7.下列变化中,气体被还原的是
A.将SO 气体通入品红溶液,溶液红色褪去
2
B.将氯气通入KBr溶液,溶液变黄
C.氢气通入氧化铜中加热,黑色固体变为红色
D.氨气通入AlCl 溶液产生白色沉淀
3
8.下列叙述中,正确的是
A.有氧元素参加的反应一定是氧化还原反应
B.反应前后元素化合价没有变化的反应一定不是氧化还原反应
C.氧化还原反应中可能没有电子转移
D.氧化还原反应中,一种物质被氧化,另一种物质一定被还原
9.火法炼锌: ,下列说法正确的是
A.被还原的元素只有Zn
B. 在反应中失去电子
C.还原剂与氧化剂的物质的量之比为1∶2
D.氧化产物与还原产物的物质的量之比为1∶1
10.海水综合利用部分流程如图所示,下列有关说法错误的是
A.实验室进行①的操作需用到坩埚、玻璃棒、酒精灯
B.②③④⑤涉及的反应均为氧化还原反应
C.X试剂可选用NaSO 饱和溶液
2 3
D.⑤中离子方程式可为2Br-+Cl=Br +2Cl-
2 2
11.根据物质的组成、结构等信息可以预测其性质或用途。下列预测中,明显不合理的是
2A.根据化合价预测,高铜酸钠( )与 可生成硫酸盐
B.根据组成预测,铝酸三钙( )溶于足量盐酸,生成白色沉淀
C.根据在周期表中位置预测,单质砷(第ⅤA族)是重要的半导体材料
D.根据结构预测,葡萄糖[ ]溶液中加入新制氢氧化铜,溶液呈绛蓝色
12.已知某合金(仅含铜、铁)中铜和铁的物质的量之和为1mol,其中Cu的物质的量分数为a,将其全部投
入100mlbmol/L的硝酸溶液中,加热使其充分反应(假设NO是唯一还原产物)。下列说法正确的是
A.若金属有剩余,余下的金属可能有铁无铜
B.若金属全部溶解,反应中转移的电子数目可能为2N
A
C.若硝酸充分反应产生2.24L气体(标准状况),则b>1
D.当溶液中金属离子只有Fe3+,Cu2+时,则a与b的关系为:b=40(1- )
13.处理工业废液中的NH 的反应为:NH +2O =NO +HO+2H+(反应I),5NH +3NO =4N +9HO
2 2 2 2
+2H+(反应II)。下列说法错误的是
A.两个反应中,NH 被氧化
B.反应I中每转移1mol电子可产生0.125molNO
C.要使废液中的NH 能完全转化为N,应使反应I与反应II投入废液的体积之比为5∶3
2
D.反应II中被氧化与被还原的氮原子之比为5∶3
14.化学中很多“规律”都可以类推,下列有关“规律”推理正确的
A.铁与氯气反应生成FeCl ,则铁与碘蒸气反应生成FeI
3 3
B.CO 通入Ba(NO ) 溶液中不产生沉淀,则SO 通入Ba(NO ) 溶液中也不产生沉淀
2 3 2 2 3 2
C.CH 为正四面体分子,则CCl 也为正四面体分子
4 4
D.卤族元素单质随核电荷数增加熔点升高,则碱金属单质熔点也随核电荷数增加而升高
15.铊(Tl)是某超导材料的组成元素之一,与铝同族,位于第六周期。Ti3+与Ag在酸性介质中发生反应:
。下列推断正确的是
A.Tl+的最外层有1个电子B.Tl(OH) 能够溶于氢氧化钠溶液
3
C.Tl+的还原性比Ag弱
D.通过化学反应可使203Tl转化为204Tl
16.科学家利用原子序数依次递增的W、X、Y、Z四种短周期元素,“组合”成一种具有高效催化性能的
超分子,其分子结构示意图如图所示(短线代表共价键)。其中W、X、Z分别位于不同周期,Z是同周期中
金属性最强的元素。下列说法正确的是
A.原子半径:Y>Z>W
B.Y与W、X、Z均能形成至少两种化合物
C.氢化物的沸点:Y>X
D.1molZW与水发生反应生成1molW ,转移电子2mol
2
17.向Cu、Cu O和CuO组成的混合物中,加入 的稀HNO 溶液恰好使混合物完全溶解,同
2 3
时收集到2.24LNO气体(标准状况)。[已知: 。]下列说法错误的是
A.发生氧化还原反应的HNO 物质的量为0.1mol
3
B.得到的溶液中n(Cu2+)=0.25mol
C.Cu与稀硝酸反应的离子方程式为
D.若混合物中含0.1molCu,则该混合物与足量稀硫酸充分反应,最后剩余固体12.8g
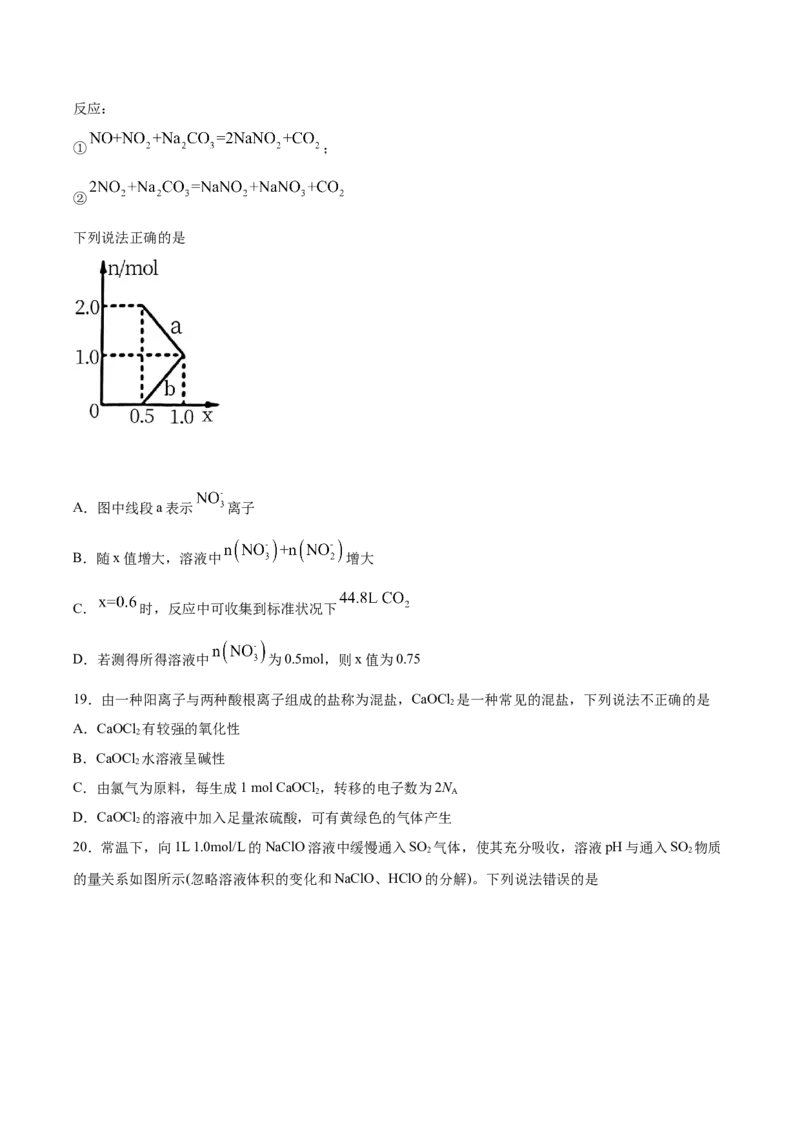
18.硝酸工业生产中常用纯碱溶液吸收排出的氮氧化物废气,废气中只含有NO、 两种气体。将一定
量废气通入到足量的 溶液中被完全吸收,溶液中生成的 、 两种离子的物质的量与废气
中 的物质的量分数 变化关系可用右下图所示。已知溶液中可发生以下两个
4反应:
① ;
②
下列说法正确的是
A.图中线段a表示 离子
B.随x值增大,溶液中 增大
C. 时,反应中可收集到标准状况下
D.若测得所得溶液中 为0.5mol,则x值为0.75
19.由一种阳离子与两种酸根离子组成的盐称为混盐,CaOCl 是一种常见的混盐,下列说法不正确的是
2
A.CaOCl 有较强的氧化性
2
B.CaOCl 水溶液呈碱性
2
C.由氯气为原料,每生成1 mol CaOCl ,转移的电子数为2N
2 A
D.CaOCl 的溶液中加入足量浓硫酸,可有黄绿色的气体产生
2
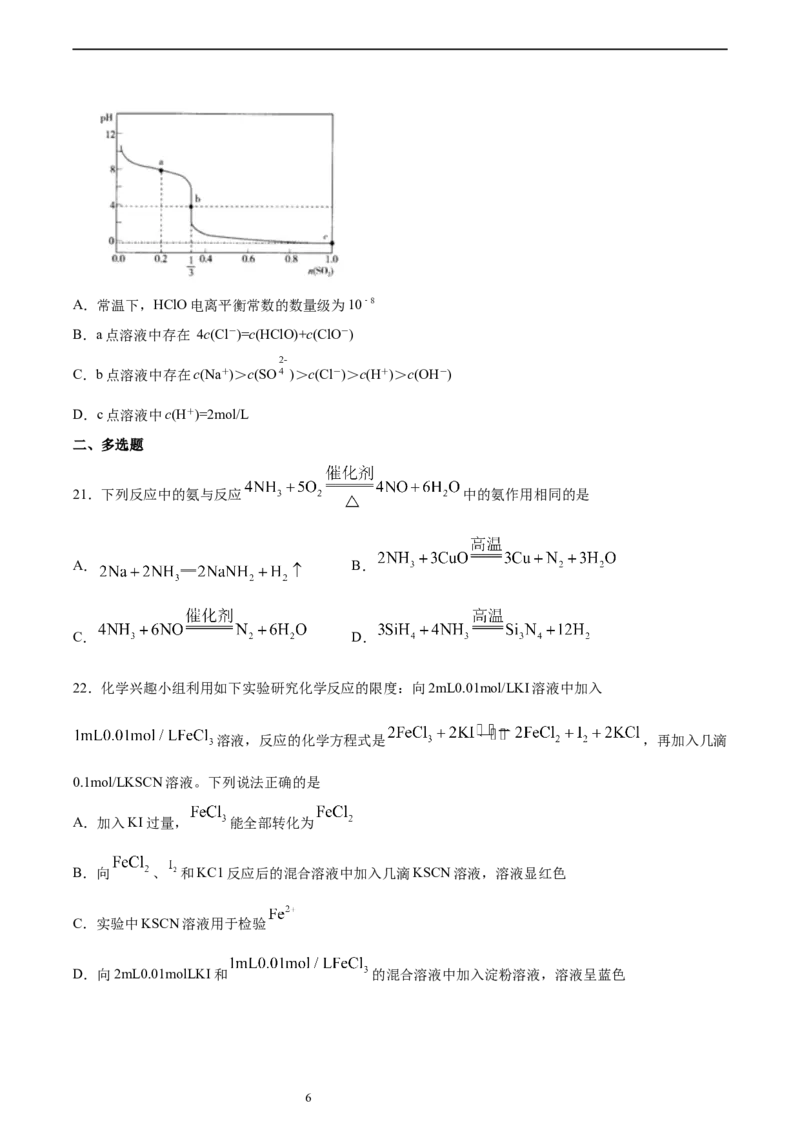
20.常温下,向1L 1.0mol/L的NaClO溶液中缓慢通入SO 气体,使其充分吸收,溶液pH与通入SO 物质
2 2
的量关系如图所示(忽略溶液体积的变化和NaClO、HClO的分解)。下列说法错误的是A.常温下,HClO电离平衡常数的数量级为10﹣8
B.a点溶液中存在 4c(Cl-)=c(HClO)+c(ClO-)
C.b点溶液中存在c(Na+)>c(SO )>c(Cl-)>c(H+)>c(OH-)
D.c点溶液中c(H+)=2mol/L
二、多选题
21.下列反应中的氨与反应 中的氨作用相同的是
A. B.
C. D.
22.化学兴趣小组利用如下实验研究化学反应的限度:向2mL0.01mol/LKI溶液中加入
溶液,反应的化学方程式是 ,再加入几滴
0.1mol/LKSCN溶液。下列说法正确的是
A.加入KI过量, 能全部转化为
B.向 、 和KC1反应后的混合溶液中加入几滴KSCN溶液,溶液显红色
C.实验中KSCN溶液用于检验
D.向2mL0.01molLKI和 的混合溶液中加入淀粉溶液,溶液呈蓝色
623.双氧水溶液中的HO 的含量可以用KMnO 溶液来进行测定,反应中HO 被氧化为O,MnO 被还原
2 2 4 2 2 2
为X(X可能是MnO 、MnO 、MnO 或Mn2+中的一种)。若HO 与KMnO 反应的物质的量之比为5∶2,
2 2 4 2 2 4
下列说法正确的是
A.HO 中O的化合价为-2
2 2
B.KMnO 是还原剂
4
C.氧化性:KMnO >O
4 2
D.X为Mn2+
24.食品抗氧化剂焦亚硫酸钠(Na SO)为具有强还原性的白色细小结晶状固体。工业制备原理为
2 2 5
NaSO +SO=Na SO,某种制备NaSO 的基本流程如下图所示。
2 3 2 2 2 5 2 2 5
下列说法错误的是
A.可用pH计测定溶液的pH=4.1
B.溶液1溶质的成分为NaSO
2 3
C.操作a应在还原氛围下进行
D.抗氧化时,1 mol Na SO 可以消除2 mol O
2 2 5 2
25.铋(Bi)位于元素周期表中第VA族,其价态为+3时较稳定,铋酸钠(NaBiO)溶液呈无色。现取一定量的
3
硫酸锰MnSO 溶液,向其中依次滴加下列溶液,对应现象如表所示:
4
加入溶液 ①适量铋酸钠溶液 ②过量双氧水 ③适量KI-淀粉溶液
实验现象 溶液呈紫红色 溶液紫红色消失,产生气泡 溶液缓慢变成蓝色
在上述实验条件下,下列结论正确的是
A.氧化性强弱顺序为:BiO ->MnO->H O>I
3 4 2 2 2
B.HO 被高锰酸根离子还原成O
2 2 2
C.HO 具有氧化性,把KI氧化成I
2 2 2
D.KI-淀粉溶液中滴加铋酸钠溶液,溶液不一定变蓝色
三、填空题
26.(一)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO+C+S=KS+2NO ↑+CO ↑。其中被还原的元素是_____,被氧
3 2 2 2
化的元素是_____,氧化剂是_____,还原剂是______
(二)已知铜在常温下能被稀HNO 溶解,反应为3Cu+8HNO (稀)=3Cu(NO)+2NO↑+4HO。
3 3 3 2 2
(1)请将上述反应改写成离子方程式:______。
(2)氧化剂是______,还原剂是_______。
(3)用双线桥法标出该反应的电子转移情况:_______。
(4)在参加反应的硝酸中,起氧化作用的HNO 与起酸性作用的HNO 的质量比为______。
3 3
四、实验题
27.水中的溶解氧是水生生物生存不可缺少的条件。某课外小组采用碘量法测定学校周边河水中的溶解
氧。实验步骤及测定原理如下:
I.取样、氧的固定
用溶解氧瓶采集水样。记录大气压及水体温度,将水样与 碱性悬浊液(含有 )混合,反应生成
,实现氧的固定。
Ⅱ.酸化、滴定
将固氧后的水样酸化, 被 还原为 ,在暗处静置 ,然后用标准 溶液滴
定,生成的 反应为: 。
回答下列问题:
(1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是_______。
(2)“氧的固定”中发生反应的化学方程式为_______。
(3) 被 还原为 的离子反应方程式_______。
(4)取 水样经固氧、酸化后,用 溶液滴定,以淀粉溶液作指示剂,终点现象为
_______.若消耗 溶液的体积为 ,则水样中溶解氧的含量为_______ 。
(5)上述滴定完成时,若滴定管尖嘴处留有气泡会导致测定结果偏_______(填“高”或“低”)。
五、计算题
28.(1)现有以下物质:①NaCl溶液②干冰③NaO固体④铜⑤BaSO 固体⑥蔗糖⑦液态HCl⑧熔融状态的
2 4
8KNO,其中属于电解质的是_______(填序号,下同),该状态下能导电的是_______。
3
(2)三氟化氮(NF )是一种无色、无味的气体,它是微电子工业技术创新必不可少的关键原料之一,可由氨气
3
和氟气反应得到:4NH +3F =NF+3NHF。则:上述反应中,氧化剂为_______,还原剂为_______,氧化
3 2 3 4
剂与还原剂的物质的量之比为_______;若反应中有0.5molNH 被氧化,转移电子的数目为_______。
3
(3)某硫酸铝溶液的密度为1.20g·cm-3,其中铝离子的质量分数为5.4%,则300mL该溶液中SO 的物质的
量为_______
(4)标准状况下,将VL的氨气溶于1L的水中(密度为1g·cm-3),得到的溶液密度为ρg·cm-3,试求得到的氨
水中溶质NH 的物质的量浓度为_______
3
六、元素或物质推断题
29.铁、铝的混合物进行如下实验:
(1)操作X的名称是____;
(2)气体A是_____(填化学式);
(3)A与Cl 混合光照可能发生爆炸,生成___(填化学式),A在该反应中作为____(填“氧化剂”或“还原
2
剂”);
(4)溶液B中阴离子除OH-外还有____(填离子符号),溶液D中存在的金属离子为___(填离子符号);
(5)加入足量NaOH溶液时发生反应的离子方程式为:____;
七、工业流程题
30.海洋中蕴含丰富的资源,下图涉及多个以海水为原料的生产流程。
完成下列填空:(1)步骤①中电解饱和食盐水的化学方程式是_______。
(2)工业上用 与 (热溶液)制备 ,反应如下: 。配平上述
反应方程式,并标出电子转移方向和数目_______。
(3)关于卤素的下列说法错误的是_______。
a.单质的熔点:
b.元素的非金属性:
c.单质的氧化性:
d.从海洋中获得 、 的过程均涉及氧化还原反应
(4)对图中所示生产过程的说法正确的是_______
a.溶解度:
b.第④⑤⑥步骤中,溴元素均被还原
c.第⑤⑥步骤的目的是进行溴的富集,提高 的浓度
d.联碱法与氨碱法相比, 利用率较高,且能耗低
(5)步骤②是在饱和食盐水中先通入 再通入 ,原因是_______。
(6)某同学将 通入 溶液中,当溶液呈中性时,溶液中浓度最大的微粒是_______。
a. b. c. d.
10参考答案
1.D
【详解】
A.反应中N元素化合价降低,被还原,N 做氧化剂,故A不符合题意;
2
B.H元素化合价升高,被氧化,H 为还原剂,故B不符合题意;
2
C.该反应中N元素化合价降低,N 得到电子,故C不符合题意;
2
D.H元素化合价升高,被氧化,H 发生氧化反应,故D符合题意;
2
故选D。
2.C
【详解】
设化合物HSO 中S元素的化合价为n价,根据化合物中各元素化合价代数之和为零的原则,有
2 3
,解得n=+4。
答案选C。
3.C
【详解】
A.Cl→Cl-氯元素的化合价降低,需要还原剂,且氯气自身歧化也可以得到Cl-,A不符合题意;
2
B.CO →CO,碳、氧元素的化合价均未变化,既不需要氧化剂也不需要还原剂,B不符合题意;
2
C.Al→Al3+,铝元素化合价升高,且Al不能自身歧化,所以一定需要氧化剂,C符合题意;
D.CuO→Cu,Cu元素化合价降低,需要还原剂,D不符合题意;
综上所述答案为C。
4.C
【分析】
根据化合价升降判断得失电子,化合价升高数值等于失去电子数,降低数值等于得到电子数,双线桥箭头
由反应物中的变价元素指向生成物中同种变价元素。
【详解】
A.硅元素化合价降低,得到电子,碳元素化合价升高失去电子,故A不正确;
B.钠元素化合价升高失去电子,氢元素的化合价降低得到电子,故B不正确;
C.符合双线桥的规则,故C正确;
D.双线桥的箭头方向错误,故D不正确;故选答案C。
【点睛】
根据化合价的变化判断得失电子数,注意变价元素原子的个数根据前后变化的原子进行判断。
5.B
【详解】
A.亚硫酸钠与浓硫酸的反应没有元素发生化合价变化,属于非氧化还原反应,故A不合题意;
B.次氯酸遇光分解的反应有元素发生化合价变化,属于氧化还原反应,故B合题意;
C.碳酸氢钠受热分解的反应没有元素发生化合价变化,属于非氧化还原反应,故C不合题意;
D.氨气和二氧化碳在饱和食盐水中的反应没有元素发生化合价变化,属于非氧化还原反应,故D不合题
意;
故选B。
6.A
【分析】
反应前后有元素化合价变化的反应是氧化还原反应,据此解答。
【详解】
A.2NaHCO NaCO+CO↑+HO中元素化合价均不变化,不是氧化还原反应,A符合;
3 2 3 2 2
B.2Al+3CuSO =Al(SO )+3Cu中Al和Cu元素化合价变化,是氧化还原反应,B不符合;
4 2 4 3
C.Cl+2NaOH=NaCl+NaClO+HO中氯元素的化合价发生变化,是氧化还原反应,C不符合;
2 2
D.4HNO 4NO +O↑+2HO中氮元素和氧元素的化合价发生变化,属于氧化还原反应,D不符合;
3 2 2 2
答案选A。
7.B
【详解】
A.将二氧化硫气体通入品红溶液,溶液红色褪去说明二氧化硫表现漂白性,故A不符合题意;
B.将氯气通入溴化钾溶液,溶液变黄说明有单质溴生成,反应中氯气被还原,故B符合题意;
C.氢气通入氧化铜中加热,黑色固体变为红色说明有铜生成,反应中氢气被氧化,故C不符合题意;
D.氨气通入氯化铝溶液产生白色沉淀说明氨气表现碱性,故D不符合题意;
故选B。
8.B
【详解】
2A.有氧元素参加的反应不一定是氧化还原反应,如氧气变为臭氧,A错误;
B.化合价变化是氧化还原反应的特征,反应前后元素化合价没有变化的反应一定不是氧化还原反应,B
正确;
C.电子转移是氧化还原反应的本质,在氧化还原反应中一定有电子转移,C错误;
D.氧化还原反应中,可能是同一种物质既被氧化又被还原,如氯气与氢氧化钠反应生成氯化钠和次氯酸
钠,D错误;
答案为B。
9.D
【详解】
A.由反应方程式可知,Zn的化合价由+2价变成0价,C的化合价由+4变成+2,0变成+2,所以被还原的
元素有Zn和C,A错误;
B.Zn的化合价由+2价变成0价,反应过程中得到电子,B错误;
C.由反应方程式可知还原剂为C,氧化剂为ZnCO ,还原剂与氧化剂的物质的量之比为2∶1,C错误;
3
D.由反应方程式可知氧化产物为CO,系数为2,还原产物为Zn和CO,系数分别为1,故氧化产物与还
原产物的物质的量之比为1∶1,D正确;
故选D。
10.A
【详解】
A.实验室进行①的操作是蒸发,需用到蒸发皿、玻璃棒、酒精灯,故A错误;
B.②③④⑤均有单质参加或生成,均有元素化合价发生变化,都是氧化还原反应,故B正确;
C.单质溴与NaSO 溶液反应:NaSO +Br +HO=2HBr+NaSO ,所以吸收Br 可选用NaSO 溶液,故
2 3 2 3 2 2 2 4 2 2 3
C正确;
D.⑤是把溴离子氧化为溴单质,可用氯气,离子方程式为2Br-+Cl=Br +2Cl-,故D正确;
2 2
故答案为A。
11.B
【详解】
A.高铜酸钠( )中铜元素的化合价为+3价,具有氧化性,二氧化硫具有还原性,所以二者反应可
生成硫酸盐,故A合理;
B.铝酸三钙( )溶于足量盐酸,反应生成氯化钙、氯化铝,不能生成白色沉淀,B不合理;
C.根据在周期表中位置预测,砷在金属和非金属的分界线附近,所以单质砷(第ⅤA族)是重要的半导体材料,C合理;
D.根据结构预测,葡萄糖[ ]为多羟基醛,多羟基的物质溶液中加入新制氢氧化
铜,溶液呈绛蓝色,D合理;
故选B。
12.B
【详解】
A.铁的还原性大于铜,若金属有剩余,余下的金属不可能有铁无铜,故A错误;
B.若铁、铜都变为+2价阳离子,反应中转移的电子数目为2N ;若铁变为+3价阳离子,反应中转移的电
A
子数目大于2N ,故B正确;
A
C.若硝酸充分反应产生2.24L气体(标准状况),NO的物质的量是0.1mol,则转移电子0.3mol,根据电荷
守恒,表现酸性的硝酸0.3mol,根据氮元素守恒,参加反应的硝酸为0.4mol,则b=4,故C错误;
D.当溶液中金属离子只有Fe3+,Cu2+时,根据电荷守恒,表现酸性的硝酸[3(1-a)+2a]mol,根据电子守
恒,被氧化的硝酸 ,则a与b的关系为:b 40(1- ),故D错误;
选B。
13.C
【详解】
A.两个反应中,NH 中氮元素化合价均升高,被氧化,故A正确;
B.由反应I的方程式可知,每生成1mol NO 转移8mol电子,则每转移1mol电子可产生0.125molNO ,
故B正确;
C.根据反应II知NH 与NO 的反应物质的量之比为5:3,所以要使废液中的NH 能完全转化为N,应
2
使反应I与反应II投入废液的体积之比为3:5,故C错误;
D.根据方程式5NH +3NO =4N +9HO+2H+,NH 中氮元素化合价升高,被氧化,NO 中氮元素化
2 2
合价降低,被还原,则被氧化与被还原的氮原子之比为5:3,故D正确;
答案选C。
14.C
4【分析】
氧化还原反应中,根据强强制弱弱判断,氧化性强的能制氧化性弱的;具有氧化性的离子和还原性的物质
能发生氧化还原反应,溶液中反应的实质是离子间的反应,根据离子反应的条件判断产物;分子的空间构
型可以根据价层电子对互斥理论判断,也可利用元素原子特点进行类比;对于物质的熔点比较根据物质熔
化时破坏的作用力的强弱进行判断;
【详解】
A.碘单质氧化性弱于三价铁,不能将铁氧化为三价铁,故A不正确;
B.二氧化硫具有还原性,硝酸根在二氧化硫溶于水后提供的酸性条件下具有强氧化性,两者发生氧化还
原反应,生成硫酸钡沉淀,故B不正确;
C.CH 为正四面体分子, CCl 可以看成是氯原子取代了氢原子,故空间结构不变,故C正确;
4 4
D.碱金属单质属于金属晶体,核电荷数增加,金属半径也在增大,导致金属键减弱,熔沸点降低,故D
不正确;
故选答案C。
【点睛】
对于卤族元素单质都属于分子晶体,熔化时克服的是分子间的作用力,根据范德华力的强弱判断方法进行
判断熔点的高低。
15.C
【详解】
A.Tl是81号元素,位于元素周期表第六周期第IIIA族,原子核外最外层有3个电子,Tl+是Tl原子失去
最外层的1个电子形成的,因此其最外层有2个电子,A错误;
B.同一主族元素从上到下元素的金属性逐渐增强,Al(OH) 呈两性,但Tl(OH) 呈碱性,因此Tl(OH) 不能
3 3 3
与氢氧化钠溶液反应,B错误;
C.若Tl+还原性比Ag强,则反应 反应产生的Tl+还会进一步与Ag发生反应,但反
应只能产生Tl+,说明Tl+还原性比Ag弱,C正确;
D.化学反应过程就是原子重新组合的过程,在反应过程中原子种类不变。203Tl与204Tl是不同的原子,因
此不能通过化学反应产生,D错误;
故合理选项是C。
16.B
【分析】
W、X、Y、Z为短周期元素,原子序数依次递增,Z是同周期中金属性最强的元素,且W、X、Z分别位于不同周期,可知,Z为Na,W为H;X、Y位于第二周期,由超分子的结构示意图知,X连四条键、Y
连两条键,则X为C,Y为O。
【详解】
A.W、Y、Z分别为H、O、Na,同周期,原子序数越大,半径越小,则原子半径:Na>O>H,A说法
错误;
B.O与H可形成HO、HO,O与C可形成CO、CO,O与Na可形成NaO、NaO,B说法正确;
2 2 2 2 2 2
C.C的氢化物为烃,含C原子数少的烃为气态或液态,含C原子数多的烃为固态,O的氢化物为HO、
2
HO,呈液态,则C的氢化物的沸点不一定比O的氢化物的沸点低,C说法错误;
2 2
D.1molNaH和HO发生反应生成1molH ,NaH+H O= H ↑+NaOH,1molNaH反应转移1mol电子,D说
2 2 2 2
法错误;
答案为B。
17.D
【分析】
HNO 的物质的量为0.6mol/L×1L=0.6mol,NO的物质的量为 =0.1mol。
3
【详解】
A.HNO 作为氧化剂,还原产物为NO,根据分析,生成NO为0.1mol,故发生还原反应的HNO 为
3 3
0.1mol,A正确;
B.反应后溶液中的溶质为Cu(NO ),根据分析,起到酸性作用的HNO 为0.6mol-0.1mol=0.5mol,故
3 2 3
n(Cu2+)= n(HNO)=0.25mol,B正确;
3
C.Cu与稀硝酸反应生成Cu(NO )、NO和HO,离子方程式为
3 2 2
,C正确;
D.混合物与硝酸反应时,Cu和Cu O被氧化,失去的总电子为HNO 所得电子,物质的量为
2 3
0.1mol×3=0.3mol,故Cu O转移电子的物质的量为0.3mol -0.1mol×2=0.1mol,n(Cu O)=
2 2
×0.1mol=0.05mol,根据溶液中n(Cu2+)=0.25mol,可知Cu元素共0.25mol,原混合物中n(CuO)=
0.25mol-0.05mol×2-0.1mol=0.05mol。混合物与稀硫酸反应时, Cu不与稀HSO 反应,根据
2 4
6可知,生成的Cu的物质的量n’(Cu)= n(Cu O)=0.05mol,故反应后所得的Cu
2
的物质的量为n(Cu)+n’(Cu)=0.15mol,质量为0.15mol×64g/mol=9.6g,D错误;
故选D。
18.D
【分析】
由方程式和图象可知,NO单独不能被吸收:
①当NO和NO 混合气体被NaOH溶液恰好完全吸收,满足n(NO ):n(NO)=1,即x=0.5,此时只生
2 2
成 ,n( )=0,n( )=2mol,所以a曲线表示 离子、b曲线表示 离子;
②当气体只有NO 时,即x=1,发生反应2NO +Na CO=NaNO +NaNO +CO ,此时生成n( )=n(
2 2 2 3 2 3 2
)=1mol;
③由x=0.5和x=1可知,一定量废气中n(NO )≥n(NO),并且n(NO )+n(NO)=2mo1,生成n( )+n(
2 2
)=2mol;
④反应NO+NO +Na CO=2NaNO +CO 和2NO +Na CO=NaNO +NaNO +CO 均有n(N)=2n(C),即
2 2 3 2 2 2 2 3 2 3 2
n(NO )+n(NO)=2n(CO )=2mol,所以n(CO)=1mol;
2 2 2
综上可知:2mol废气通入到足量的NaCO 溶液中被完全吸收,即n(NO )≥n(NO),生成n( )+n(
2 3 2
)=2mol;n(CO)=lmol;a曲线表示 离子、b曲线表示 离子。
2
【详解】
A.当x=0.5时,只发生反应NO+NO +Na CO=2NaNO +CO ,n( )=0,n( )=2mol,所以a曲线表
2 2 3 2 2
示 离子、b曲线表示 离子,故A错误;
B.当x=0.5时,只生成 ,n( )=2mol;当x=1只发生反应
2NO +Na CO=NaNO +NaNO +CO ,此时生成n( )=n( )=1mol;根据N原子守恒可知混合气体的
2 2 3 2 3 2总的物质的量为2mol,即溶液中n( )+n( )不变,始终等于2mol,故B错误;
C.由于废气中n(NO )≥n(NO),并且n(NO )+n(NO)=2n(CO )=2mol,根据反应①②可知n
2 2 2
(NO )+n(NO)=2n(CO )=2mol,即n(CO)=1mol,标准状况下体积为22.4L,故C错误;
2 2 2
D.设n(NO )=a,n(NO)=b,则a+b=2mol,发生反应①余下NO 的物质的量为(a-b)mol,发生反应②生
2 2
成n( )=0.5(a-b)=0.5mol,即a-b=1mol,联立方程组解得a=1.5mol,b=0.5mol,废气中NO 的物质的
2
量分数x= ×100%=75%,故D正确;
答案选D。
19.C
【详解】
A.混盐CaOCl 中相当于含有CaCl 和Ca(ClO) ,其中Ca(ClO) ,具有强的氧化性,所以混盐CaOCl 有较
2 2 2 2 2
强的氧化性,故A正确;
B.Ca(ClO) 显碱性,因为次氯酸根离子水解,CaCl 显中性,所以CaOCl 水溶液呈碱性,故B正确;
2 2 2
C.混盐CaOCl 中相当于含有CaCl 和Ca(ClO) ,Cl的化合价分别是+1价、-1价,由氯气为原料,每生成
2 2 2
1 mol CaOCl ,转移的电子数为N ,故C错误;
2 A
D.混盐CaOCl 中的CaCl 和Ca(ClO) 在酸性条件下反应生成氯气,氯气会黄绿色气体,故D正确;
2 2 2
故答案为C。
20.C
【分析】
向1L 1.0mol•L-1的NaClO溶液中级慢通入SO 气体,开始时发生反应①SO +H O+3ClO-=SO +Cl-
2 2 2
+2HClO,由于HClO为弱酸,所以溶液的pH缓慢减小,当该反应完全进行后继续通SO 反应为
2
SO +H O+HClO= SO +Cl-+3H+,所以b点pH突然减小,说明此时反应①恰好完全进行,开始进行反应
2 2
②,到c点反应②完全进行。
【详解】
A.根据分析可知b点溶液显酸性是因为HClO的电离,b点溶液pH约为3.8,即c(H+)≈10-3.8mol/L,
8n(HClO)=2n(SO )= mol×2= mol,溶液的体积为1L,所以溶液中的c(HClO)≈ mol/L,c(ClO-)≈c(H+)=10-
2
3.8mol/L,则K(HClO)≈ =1.5×10-7.6,即HClO电离平衡常数的数量级为10-8,故A正确;
a
B.a点通入0.2molSO ,n(Cl-)=n(SO )=n(SO )=0.2mol,n(HClO)=2n(SO )=0.4mol,反应消耗的
2 2 2
n(NaClO)=3n(SO )=0.6mol,反应后含有的n(NaClO)=1mol/L×1L-0.6mol=0.4mol,则n(HClO)
2
+n(NaClO)=0.8mol、n(Cl-)=0.2mol,结合物料守恒可知:4c(Cl-)=c(HClO)+c(ClO-),故B正确;
C.b点SO +H O+3ClO-=SO +Cl-+2HClO恰好完全进行,n(Cl-)=n(SO )=n(SO )= mol,
2 2 2
n(HClO)=2n(SO )= mol,n(Na+)始终不变为1mol,所以正确的浓度关系为:c(Na+)>c(SO )=c(Cl-)>
2
c(H+)>c(OH-),故C错误;
D.NaClO溶液中通入SO 至过量的总反应为NaClO+ SO + H O=NaCl+ HSO ,c点完全反应,所以
2 2 2 2 4
n(H SO )=n(SO )=1.0mol,c(H+)=2.0mol•L-1,故D正确;
2 4 2
故选:C。
21.BC
【分析】
题干所给反应中,NH 中N元素的化合价升高,H元素的化合价不变,故NH 作还原剂。
3 3
【详解】
A.NH 中N元素的化合价不变,H元素的化合价降低,故NH 作氧化剂,故A不符合题意;
3 3
B.NH 中N元素的化合价升高,H元素的化合价不变,故NH 作还原剂,故B符合题意;
3 3
C.NH 中N元素的化合价升高,H元素的化合价不变,故NH 作还原剂,故C符合题意;
3 3
D.NH 中N元素的化合价不变,H元素的化合价降低,故NH 作氧化剂,故D不符合题意;
3 3
综上所述答案为BC。
22.BD
【分析】
,为可逆反应,不能完全进行,反应物与生成物共存,Fe3+、Fe2+、I、I-,同时存在,据此分析解题。
2
【详解】
A.由于反应可逆,加入KI过量, 不能全部转化为 ,故A错误;
B.向 、 和KC1反应后的混合溶液中加入几滴KSCN溶液,由于存在Fe3+,溶液显红色,故B正
确;
C.实验中KSCN溶液用于检验Fe3+,故C错误;
D.向2mL0.01molLKI和 的混合溶液中加入淀粉溶液,由于生成碘单质,溶液呈蓝
色,故D正确;
故选BD。
23.CD
【分析】
在氧化还原反应中元素化合价升降总数相等。由于HO 与KMnO 反应的物质的量之比为5∶2,则反应后
2 2 4
Mn元素化合价为+2价,故反应方程式为5HO+2KMnO +3H SO =K SO +2MnSO +5O ↑+8H O,然后根据
2 2 4 2 4 2 4 4 2 2
氧化还原反应规律分析、解答。
【详解】
A.在HO 中,H元素化合价为+1价,根据化合物中元素化合价代数和为0,可知O的化合价为-1价,A
2 2
错误;
B.在该反应中,Mn元素化合价由反应前KMnO 中的+7价变为反应后MnSO 中的+2价,化合价降低,
4 4
得到电子被还原,作氧化剂,B错误;
C.在该反应中KMnO 是氧化剂,O 是氧化产物,由于氧化剂的氧化性比氧化产物强,所以物质的氧化
4 2
性:KMnO >O,C正确;
4 2
D.在氧化还原反应中电子转移数目相等,等于元素化合价升降总数,可知反应后Mn转化为Mn2+,D正
确;
故合理选项是CD。
24.BD
【分析】
根据pH计的精确度进行判断;根据流程中所加物质判断反应产物;根据溶液的酸碱性判断溶质的可能情
况;根据已知反应NaSO +SO=Na SO,可以判断反应属于氧化还原反应,根据化合价的变化可以判断二
2 3 2 2 2 5
氧化硫是还原剂,以此来判断反应的氛围。
10【详解】
A.测定溶液pH的精确度为0.1,可用pH计(或酸度计,或pH传感器)等,A项正确;
B.向NaCO 饱和溶液通入SO 至pH=4.1得到溶液1,由于NaSO 水解使溶液显碱性,pH>7,B项错
2 3 2 2 3
误;
C.由流程图可知溶液3的主要溶质为NaSO,NaSO 具有强还原性,所以从NaSO 溶液中析出
2 2 5 2 2 5 2 2 5
NaSO 晶体,应在还原氛围下进行,C项正确;
2 2 5
D.NaSO 中硫元素化合价为+4,当氧化至最高价+6时,1 mol Na SO 最多可以提供4 mol电子,可以消
2 2 5 2 2 5
除1 mol O ,D项错误。
2
故选答案BD。
【点睛】
根据反应物及溶液的环境判断产物,溶质的存在与所处环境不能发生反应。
25.AD
【分析】
由①中现象可知:NaBiO 把Mn2+氧化生成MnO -,则NaBiO(氧化剂)的氧化性强于MnO -(氧化产
3 4 3 4
物)的氧化性;
由②中现象可知:MnO -氧化HO 产生O,自身被还原为Mn2+,则MnO -(氧化剂)的氧化性强于HO
4 2 2 2 4 2 2
的氧化性;
由③中现象可知:I-被HO 氧化成I,则HO(氧化剂)的氧化性强于I(氧化产物)的氧化性;
2 2 2 2 2 2
综上所述,NaBiO、MnO -、I、HO 的氧化性由强到弱的顺序是:NaBiO>MnO ->HO>I。
3 4 2 2 2 3 4 2 2 2
【详解】
A.由分析可知,氧化性强弱顺序为:BiO ->MnO ->HO>I,A正确;
3 4 2 2 2
B.HO 被MnO -氧化成O,B错误;
2 2 4 2
C.HO 具有氧化性,将I-氧化成I,但是也可能是溶于溶液中的氧气氧化了I-,C错误;
2 2 2
D.根据分析可知,BiO -的氧化性强于I。则KI-淀粉溶液中滴加铋酸钠溶液,会生成I,溶液变蓝色,
3 2 2
也可能将I-氧化成更高的价态,不变蓝,D正确。
答案选AD。
【点睛】
C选需要考虑O 氧化I-的情况,而D选需要考虑将I-氧化到更高的价态,而不是I,考虑一定要全面。
2 2
26.N、S C KNO、S C 3Cu+8H++2 =3Cu2++2NO↑+4HO HNO Cu
3 2 31:3
【分析】
根据化合价的变化判断氧化还原反应中的对应项,化合价升高的元素是被氧化,所含元素的物质是还原
剂;降低的元素是被还原,所含元素的反应物是氧化剂;化合价的变化值即是得电子数、失电子数、转移
电子数。
【详解】
(一)根据元素的化合价变化判断:N元素由+5价降到+4价,S元素由0价降到-2价,故N、S元素被还
原,C元素的化合价由0价升为+4价,被氧化。含N、S元素的反应物做氧化剂,即是KNO、S,含化合
3
价升高的反应物做还原剂,是C;
(二)(1)根据单质、氧化物不能改写为离子,得出离子方程式为:3Cu+8H++2 =3Cu2+
+2NO↑+4HO;
2
(2)元素N由+5价变为+2价,故含氮的硝酸做氧化剂,Cu元素化合价由0升为+2价,Cu做为还原剂;
(3) 根据双线桥法的规则:
(4)根据变价元素N由+5价变为+2价有2个N,没有发生变化N有6个,故起氧化作用的HNO 与起酸性作
3
用的HNO 的质量比为1:3;
3
【点睛】
转移电子数等于化合价的升高总数等于化合价的降低总数,根据化合价的变化判断对应项。
27.使测定值与水体中的实际值保持一致,避免产生误差
当滴入最后一滴标准液时,溶液由蓝色变为无色,且
半分钟内无变化 低
12【详解】
(1)取水样时应尽量避免扰动水体表面,防止水样中溶解氧的量发生变化,使测定值与水体中的实际值保持
一致,避免产生误差;
(2)“氧的固定”中 被氧气氧化为 ,发生反应的化学方程式为
;
(3) 被 还原为 、 被氧化为碘单质,反应的离子方程式为
;
(4)滴定终点时,碘完全被消耗,以淀粉溶液作指示剂,终点现象为:当滴入最后一滴标准液时,溶液由蓝
色变为无色,且半分钟内无变化;
根据 、 、
,得关系式 ,若消耗 溶液的
体积为 ,消耗 的物质的量是 mol,则氧气的物质的量是 mol,水样中溶解
氧的含量为 = 。
(5)滴定完成时,若滴定管尖嘴处留有气泡,消耗标准液体积偏小,会导致测定结果偏低。
28. ③⑤⑦⑧ ①④⑧ F NH 3:1 3N 1.08mol
2 3 A
【详解】
(1)电解质:在水溶液里或熔融状态下能够导电的化合物;故根据定义可知,属于电解质的是:③⑤⑦⑧;
存在自由移动的离子或电子的物质能导电,则以上几种物质中只有①④⑧能导电,故答案为:③⑤⑦⑧;
①④⑧(2)该反应中NH 转化成NF 氮元素的化合价由-3价变为+3价,一个氮气分子失去6个电子,所以氨作还原
3 3
剂被氧化;F 转化为F-,氟元素得电子化合价降低,一个氟气分子得2个电子,氟气作氧化剂被还原,得
2
失电子最小公倍数是6,所以氧化剂与还原剂的物质的量之比为3:1;1mol氨被氧化转移电子数为6N ,
A
故0.5mol氨被氧化转移电子数为3N ;故答案为:F;NH ;3:1;3N ;
A 2 3 A
(3)300mL密度为1.20g·cm-3的硫酸铝溶液的质量为:300mL×1.20 g·cm-3=360g,溶液中铝离子的质量分数为
5.4%,则m(Al3+)=360g×5.4%=19.44g,n(Al3+)= =0.72mol,根据电荷守恒可知3n(Al3+)=2n(
),故n( )= n(Al3+)=1.08mol,故答案为1.08mol;
(4)ω= = ,故答案为: 。
29.过滤 H HCl 还原剂 Fe2+ 2Al+2OH-+2H O=2 +3H ↑
2 2 2
【分析】
Fe和Al的混合物中加足量NaOH溶液,Al和NaOH溶液反应生成偏铝酸钠和氢气,Fe和NaOH溶液不反
应,A为氢气,B为偏铝酸钠和NaOH混合溶液,C为Fe,操作X为过滤;固体C即Fe和盐酸反应生成
氯化亚铁和氢气,D为氯化亚铁。
【详解】
(1)操作X后获得溶液B和固体C可知X名称是过滤;
(2)气体A是H;
2
(3)A(H )与Cl 混合光照可能发生爆炸,生成HCl;A(H )中H化合价升高,被氧化,在该反应中作为还原
2 2 2
剂;
(4)由分析可知,B为偏铝酸钠和NaOH混合溶液,则溶液B中阴离子除OH-外还有 ;溶液D为FeCl
2
溶液,存在的金属离子为Fe2+;
(5)加入足量NaOH溶液时Al和NaOH溶液反应生成偏铝酸钠和氢气,发生反应的离子方程式为2Al+2OH-
+2H O=2 +3H ↑。
2 2
1430.2NaCl+2H O 2NaOH+H ↑+Cl↑ 3,6,5,1,3, ac cd
2 2 2
NH 极易溶于水,使溶液呈碱性可以吸收大量的二氧化碳,才能产生较多的HCO ,以析出更多的固体
3
a
【分析】
海水的综合利用,涉及到制碱,提取镁,和提取溴,该过程中涉及到物质鉴别,氧化还原反应及金属冶炼
等问题,以此解答;
【详解】
(1) 步骤①中电解饱和食盐水的化学方程式是2NaCl+2H O 2NaOH+H ↑+Cl↑,故答案为:
2 2 2
2NaCl+2H O 2NaOH+H ↑+Cl↑;
2 2 2
(2) Cl→KCl,化合价降低1价,Cl→KClO,化合价升高5价,最小公倍数为5,即KClO 的化学计量数
2 2 3 3
为1,KCl 的化学计量数为5,配平其他物质,化学方程式为3Cl+6KOH =5KCl +KClO +3H O,
2 3 2
,故答案为:3,6,5,1,3, ;
(3) a.卤素单质结构相似且都是分子晶体,其单质的熔沸点与其相对分子质量成正比,所以卤素单质的熔
沸点随着原子序数的增大而增大,故a错误;
b.卤素元素,从上到下元素非金属性逐渐减弱,故b正确;
c.元素的非金属性越强其单质的氧化性越强,卤素元素的非金属性随着原子序数的增大而减弱,所以卤
族单质的氧化性随着原子序数的增大而减弱,故c错误;
d.Cl,Br2在海水中均以化合态形式存在,故从海洋中获得 、 的过程均涉及氧化还原反应,故d
2
正确;故答案为:ac;
(4) a.可溶性碳酸盐的溶解度大于相应的碳酸氢盐,故a错误;
b.第④⑥步骤中,溴元素均被氧化,仅⑤溴元素被还原,故b错误;
c. 稀溶液中 少,所以第⑤⑥步骤的目的是进行溴的富集,提高 的浓度,故c正确;
d.联碱法与氨碱法相比, 利用率较高,且能耗低,故d正确;
故答案为:cd;
(5)步骤②是在饱和食盐水中先通入 再通入 ,原因是NH3极易溶于水,使溶液呈碱性可以吸收大
量的二氧化碳,才能产生较多的HCO ,以析出更多的固体,故答案为:NH3极易溶于水,使溶液呈碱性
可以吸收大量的二氧化碳,才能产生较多的HCO ,以析出更多的固体;
(6)溶液呈电中性,即c(H+)=c(OH-),根据电荷守恒可知,c(Na+)+ c(H+) = 2c(CO ) + c(HCO )+ c(OH-),
c(Na+)=2c(CO ) + c(HCO ),所以c(Na+)最大,故答案为:a。
16