文档内容
专题 11 化学实验基础
1.(2022·浙江卷)名称为“吸滤瓶”的仪器是
A. B. C. D.
【答案】D
【解析】A.图示实验仪器为蒸馏烧瓶,A不合题意;
B.图示实验仪器为分液漏斗,B不合题意;
C.图示实验仪器为容量瓶,C不合题意;
D.图示实验仪器为吸滤瓶,其特征是一个厚壁的带分支的锥形瓶,D符合题意;
故答案为:D。
2.(2022·浙江卷)下列说法不正确的是
A.用标准液润洗滴定管后,应将润洗液从滴定管上口倒出
B.铝热反应非常剧烈,操作时要戴上石棉手套和护目镜
C.利用红外光谱法可以初步判断有机物中具有哪些基团
D.蒸发浓缩硫酸铵和硫酸亚铁(等物质的量)的混合溶液至出现晶膜,静置冷却,析出硫酸亚铁铵晶体
【答案】A
【解析】A.用标准液润洗滴定管,要将整个滴定管内壁进行润洗,因此,应将润洗液的一部分从滴定管
上口倒出,另一部分从滴定管下口放出,A说法不正确;
B.铝热反应非常剧烈,反应过程中放出大量的热,有大量火星飞溅出来,因此,在操作时要戴上石棉手
套和护目镜以保护手和眼睛,B说法正确;
C.有机物中的基团在红外光谱中会呈现出其特征谱线,因此,可以利用红外光谱法初步判断有机物中具
有哪些基团,C说法正确;
D.硫酸亚铁铵的溶解度随着温度降低而减小,蒸发浓缩硫酸铵和硫酸亚铁(等物质的量)的混合溶液至出现
晶膜,溶液达到饱和状态,静置冷却后,由于在该温度下的混合体系中硫酸亚铁铵的溶解度最小,因此,
析出的晶体是硫酸亚铁铵晶体,D说法正确。
综上所述,本题选A。
1
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司3.(2022·湖南卷)化学实验操作是进行科学实验的基础。下列操作符合规范的是
A.碱式滴定管排气泡 B.溶液加热 C.试剂存放 D.溶液滴加
【答案】A
【解析】A.碱式滴定管排气泡时,把橡皮管向上弯曲,出口上斜,轻轻挤压玻璃珠附近的橡皮管可以使
溶液从尖嘴涌出,气泡即可随之排出,A符合规范;
1
B.用试管加热溶液时,试管夹应夹在距离管口的 处,B不符合规范;
3
C.实验室中,盐酸和NaOH要分开存放,有机物和无机物要分开存放,C不符合规范;
D.用滴管滴加溶液时,滴管不能伸入试管内部,应悬空滴加,D不符合规范;
故选A。
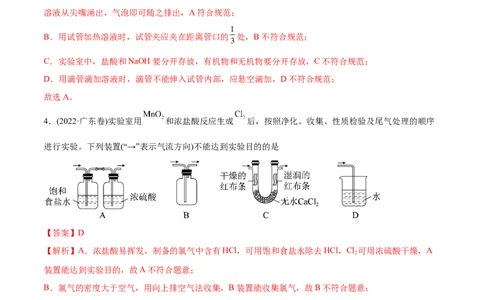
4.(2022·广东卷)实验室用 和浓盐酸反应生成 后,按照净化、收集、性质检验及尾气处理的顺序
进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是
【答案】D
【解析】A.浓盐酸易挥发,制备的氯气中含有HCl,可用饱和食盐水除去HCl,Cl 可用浓硫酸干燥,A
2
装置能达到实验目的,故A不符合题意;
B.氯气的密度大于空气,用向上排空气法收集,B装置能收集氯气,故B不符合题意;
C.湿润的红布条褪色,干燥的红色布条不褪色,可验证干燥的氯气不具有漂白性,故C不符合题意;
D.氯气在水中的溶解度较小,应用NaOH溶液吸收尾气,D装置不能达到实验目的,故D符合题意;
答案选D。
5.(2022·全国乙卷)由实验操作和现象,可得出相应正确结论的是
实验操作 现象 结论
A 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液 先变橙色,后变蓝色 氧化性:
Cl Br I
2 2 2
2
原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的
B 无砖红色沉淀 蔗糖未发生水解
Cu(OH)
2悬浊液
气体中含有不饱和
C 石蜡油加强热,将产生的气体通入 Br 2的 CCl 4溶液 溶液红棕色变无色
烃
试管口润湿的蓝色石蕊 氯乙烯加聚是可逆
D 加热试管中的聚氯乙烯薄膜碎片
试纸变红 反应
【答案】C
【解析】A.向NaBr溶液中滴加过量氯水,溴离子被氧化为溴单质,但氯水过量,再加入淀粉KI溶液,
过量的氯水可以将碘离子氧化为碘单质,无法证明溴单质的氧化性强于碘单质,A错误;
B.向蔗糖溶液中滴加稀硫酸,水浴加热后,应加入氢氧化钠溶液使体系呈碱性,若不加氢氧化钠,未反
应的稀硫酸会和新制氢氧化铜反应,则不会产生砖红色沉淀,不能说明蔗糖没有发生水解,B错误;
C.石蜡油加强热,产生的气体能使溴的四氯化碳溶液褪色,说明气体中含有不饱和烃,与溴发生加成反
应使溴的四氯化碳溶液褪色,C正确;
D.聚氯乙烯加强热产生能使湿润蓝色湿润试纸变红的气体,说明产生了氯化氢,不能说明氯乙烯加聚是
可逆反应,可逆反应是指在同一条件下,既能向正反应方向进行,同时又能向逆反应的方向进行的反应,
而氯乙烯加聚和聚氯乙烯加强热分解条件不同,D错误;
答案选C。
6.(2022·全国甲卷)根据实验目的,下列实验及现象、结论都正确的是
选
实验目的 实验及现象 结论
项
CH COO
分别测浓度均为0.1molL1
的
A
比较 3 和
CH COONH NaHCO pH K
CH
COO-
Fe
酸性:苯酚>
C 向苯酚浊液中滴加饱和NaCO 溶液 浊液变澄清
2 3 碳酸
分别在20℃、30℃下,取0.1mol·L-1KI溶液,向其中先加入 30℃下出现
探究反应速率
D 0.1mol·L-1的硫酸,再加入淀粉溶液,发生反应4H++O +4I- 蓝色的时间
2 与温度的关系
=2I +2H O 短
2 2
【答案】A
【解析】A.加热NaI固体和浓磷酸的混合物,由于HI氢易挥发,浓磷酸不易挥发,会有HI气体生成,
故A正确;
B.取等物质的量的Al和Fe,分别与足量的稀盐酸反应, Al产生的氢气多, 说明Al失去的电子数多,
但金属性与失去电子数多少无关,不能比较Al、Fe的金属性,故B错误;
C.向苯酚浊液中滴加饱和NaCO 溶液,反应生成苯酚钠、碳酸氢钠,浊液变澄清,说明酸性:苯酚>碳
2 3
酸氢根,故C错误;
D.若先加硫酸,先发生反应4H++O +4I-=2I +2H O,在20℃、30℃都会反应生成碘,加入淀粉都会变蓝,
2 2 2
应先加入淀粉,再加硫酸进行反应,故D错误;
答案选A。
16.(2022·陕西咸阳·一模)下列实验操作所得现象及结论均正确的是
选项 实验操作 实验现象 结论
A 向固体 MnO 2上滴加浓盐酸 产生黄绿色气体 氧化性: Cl 2 MnO 2
镁、铝为电极,氢氧化钠为电解质
B 铝表面有气泡 金属活动性:Mg>Al
的原电池装置
海带中提取碘单质时,用苯做萃取 碘在有机溶剂中溶解
C 液体分层,下层溶液为紫红色
剂 度较大
D 将10mL2mol/L的KI溶液与 充分反应后,滴加数滴KSCN溶 该反应为可逆反应
1mol/LFeCl
3
1
原创精品资源学科网独家享有版权,侵权必究! 6
学科网(北京)股份有限公司1mol/LFeCl 3溶液混合 液,溶液颜色变红
【答案】D
MnO
【解析】A.该反应需要加热,氧化剂的氧化性大于氧化产物的氧化性,则氧化性: 2>Cl,故A错误;
2
B.形成原电池反应,由于铝与氢氧化钠溶液反应,铝为负极,但活泼性Mg>Al,故B错误;
C.碘易溶于苯,苯的密度比水小,可观察到液体分层,上层为紫红色,故C错误;
D.KI过量,由现象可知还反应后存在铁离子,则KI与FeCl 的反应具有可逆性,故D正确;
3
故选:D。
SbCl SbCl 220.3℃
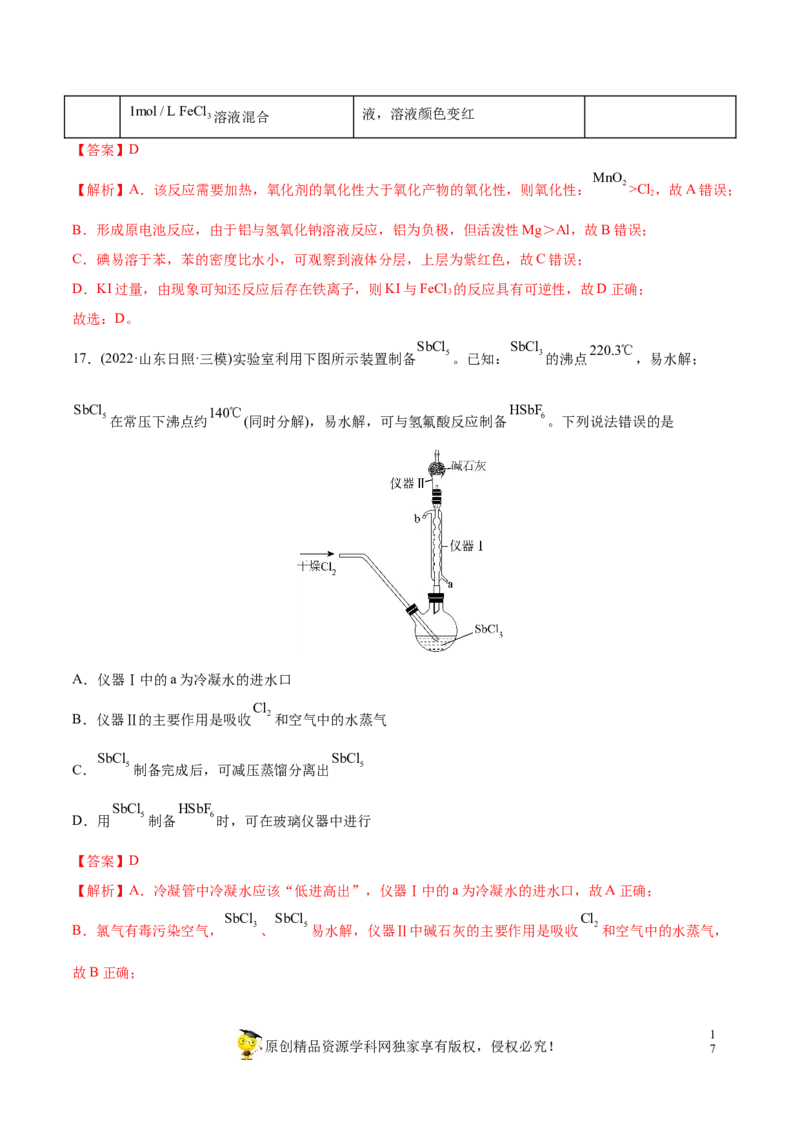
17.(2022·山东日照·三模)实验室利用下图所示装置制备 5。已知: 3的沸点 ,易水解;
SbCl 140℃ HSbF
5在常压下沸点约 (同时分解),易水解,可与氢氟酸反应制备 6。下列说法错误的是
A.仪器Ⅰ中的a为冷凝水的进水口
Cl
B.仪器Ⅱ的主要作用是吸收 2和空气中的水蒸气
SbCl SbCl
C. 5制备完成后,可减压蒸馏分离出 5
SbCl HSbF
D.用 5制备 6时,可在玻璃仪器中进行
【答案】D
【解析】A.冷凝管中冷凝水应该“低进高出”,仪器Ⅰ中的a为冷凝水的进水口,故A正确;
SbCl SbCl Cl
B.氯气有毒污染空气, 3、 5易水解,仪器Ⅱ中碱石灰的主要作用是吸收 2和空气中的水蒸气,
故B正确;
1
原创精品资源学科网独家享有版权,侵权必究! 7
学科网(北京)股份有限公司SbCl SbCl SbCl 140℃ SbCl
C. 5的沸点比 3低, 5在常压下沸点约 (同时分解),为防止 5分解,制备完成后减压
SbCl
蒸馏分离出 5,故C正确;
SbCl HSbF HSbF
D. 5与氢氟酸反应制备 6,玻璃中的二氧化硅和氢氟酸反应,所以不能在玻璃仪器中制备 6,
故D错误;
选D。
NH COONH CCl
18.(2022·山东淄博·三模)氨基甲酸铵 2 4 易分解,易水解,难溶于 4。某小组设计如图所
示装置制备氨基甲酸铵。已知: 2NH 3 gCO 2 g NH 2 COONH 4 s ΔH<0
下列分析错误的是
A.A装置的优点是能够随时控制反应的发生和停止
PO
B.装置B、C、E中试剂可分别为饱和碳酸氢钠溶液、浓硫酸、 2 5固体
C.装置D使用冰水浴
NH Cl
D.装置F中所用试剂可为 4 与熟石灰
【答案】B
CO
【解析】A装置为碳酸钙与盐酸反应制备 2,氨基甲酸铵易水解,进入制备氨基甲酸铵装置D的气体必
NH Cl
须干燥纯净气体,左侧装置B、C试剂可分别为饱和碳酸氢钠溶液、浓硫酸,装置F可用 4 与碱石灰
制备氨气,E中试剂需干燥氨气,可以选用碱石灰;
CO
A.A装置为碳酸钙与盐酸反应制备 2简易制备装置,装置的优点是能够随时控制反应的发生和停止,A
正确;
1
原创精品资源学科网独家享有版权,侵权必究! 8
学科网(北京)股份有限公司B.氨基甲酸铵易水解,进入制备氨基甲酸铵装置D的气体必须干燥纯净气体,左侧装置B、C试剂可分
CO NH Cl
别为饱和碳酸氢钠溶液、浓硫酸,制的纯净干燥的 2,装置F可用 4 与碱石灰制备氨气,E中试剂
PO
需干燥氨气,可以选用碱石灰,但不能选用 2 5固体,B错误,
C.制备氨基甲酸铵的反应为放热反应,制得的物质易分解,所以装置D需降温,使用冰水浴,C正确;
NH Cl
D.装置F可用 4 与碱石灰反应制备氨气,D正确;
故选:B。
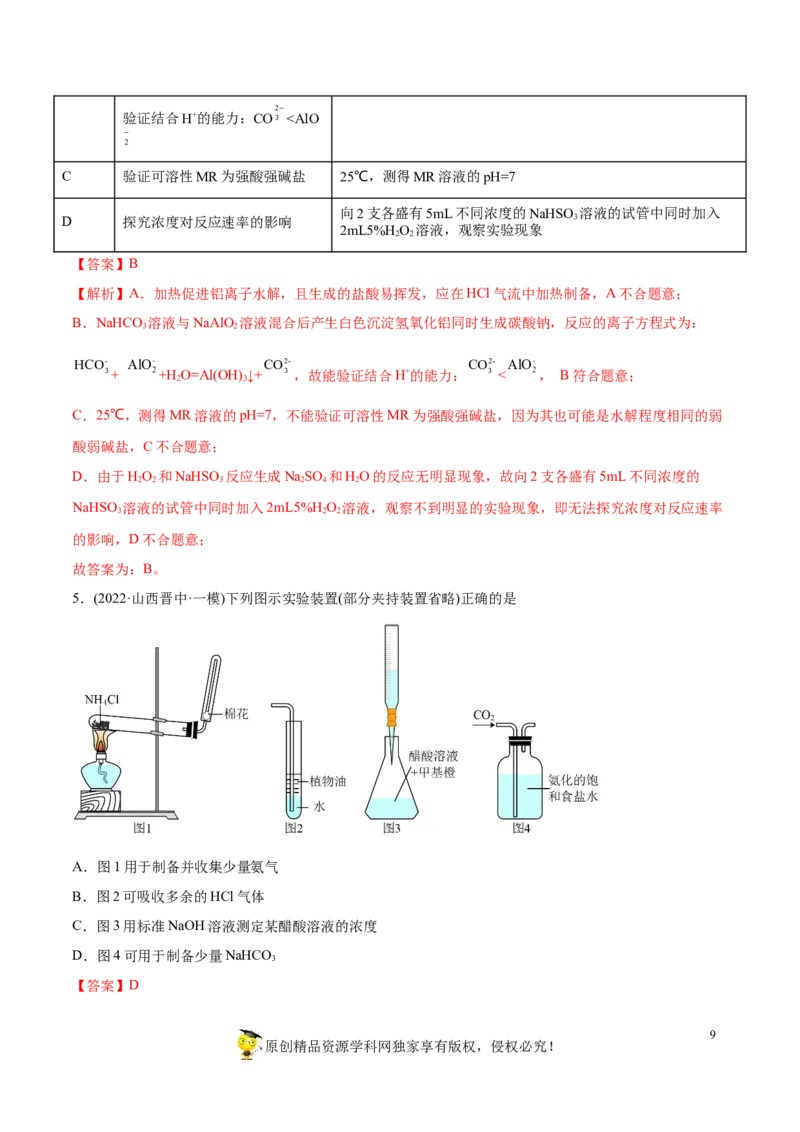
19.(2022·山东聊城·三模)为完成下列各组实验,所选玻璃仪器和试剂均准确、完整的是(不考虑存放试剂
的容器和连接装置)
选项 实验目的 玻璃仪器 试剂
MgCl 溶液、AlCl 溶液、浓
A 比较Mg、Al金属性的强弱 试管、胶头滴管 2 3
NaOH溶液
观察[Cu(NH )]SO •H O晶体的形
B 3 4 4 2 试管、胶头滴管、玻璃棒 CuSO 溶液、氨水
成和析出 4
通过气味消失的快慢比较乙酸乙酯 试管、烧杯、量筒、胶头 乙酸乙酯、蒸馏水、HSO 溶
C 2 4
的水解速率 滴管、酒精灯 液、NaOH溶液
实验室由粗盐(含Mg2+、Ca2+、SO
漏斗、烧杯、玻璃棒、酒 粗食盐水、NaOH溶液、NaCO
D 2 3
2
4
)制备精盐
精灯 溶液、BaCl
2
溶液
【答案】AC
【解析】A.实验原理:通过氯化铝,氯化镁与浓氢氧化钠反应生成的氢氧化铝,氢氧化镁的碱性大小来
比较铝镁的金属性,取等量氯化铝和氯化镁分别置与两支试管中,同时用胶头滴管加入浓氢氧化钠溶液,
直至出现白色沉淀,继续滴加氢氧化钠(过量),装有氯化铝的烧杯沉淀消失,装有氯化镁的烧杯沉淀不消
失,因为碱与碱不发生反应,故氢氧化铝不是碱,可以得出镁的金属性比铝强,故A项正确;
B.通过将过量氨水加入硫酸铜溶液中反应得[Cu(NH )]SO HO,但[Cu(NH )]SO HO溶于水不溶于乙
3 4 4 2 3 4 4 2
醇,因此在[Cu(NH )]SO HO溶液中需要缓慢加入乙醇降低溶解度,即可析出深蓝色的晶体,试剂缺乙
3 4 4 2
醇溶液,故B项错误;
C.实验原理:CHCOOCH CH + HO CHCOOH +CH CHOH,乙酸乙酯在蒸馏水中滴加热水解较为缓
3 2 3 2 3 3 2
慢,若滴加HSO 溶液,稀硫酸起催化作用,则促进乙酸乙酯水解。若滴加NaOH溶液,不仅起催化作用,
2 4
还能和水解产物中的乙酸反应而使该反应的平衡向水解向移动,因此水解速率大小为碱性条件大于酸性条
1
原创精品资源学科网独家享有版权,侵权必究! 9
学科网(北京)股份有限公司件大于蒸馏水。由于乙酸乙酯具有芳香味,故可以通过气味消失的快慢比较乙酸乙酯的水解速率,涉及玻
璃仪器试管、烧杯、量筒、胶头滴管、酒精灯,故C项正确;
D.粗盐提纯第一步溶解得粗食盐水,所需玻璃仪器为玻璃棒、烧杯、过滤后向溶液中先滴加过量的BaCl
2
2
溶液,过滤,除去SO4 ,随后向所得滤液中加入NaOH溶液,过滤,除去氯化镁,在所得滤液加入
NaCO 溶液,过滤,除去氯化钙及氯化镁。最后需要加入盐酸中和过量的氢氧化钠、碳酸钠溶液。在蒸发
2 3
皿上加热蒸发即可获得精盐。缺乏试剂盐酸溶液,蒸发皿仪器,故D项错误;
故答案选AC。
2
原创精品资源学科网独家享有版权,侵权必究! 0
学科网(北京)股份有限公司2
原创精品资源学科网独家享有版权,侵权必究! 1
学科网(北京)股份有限公司