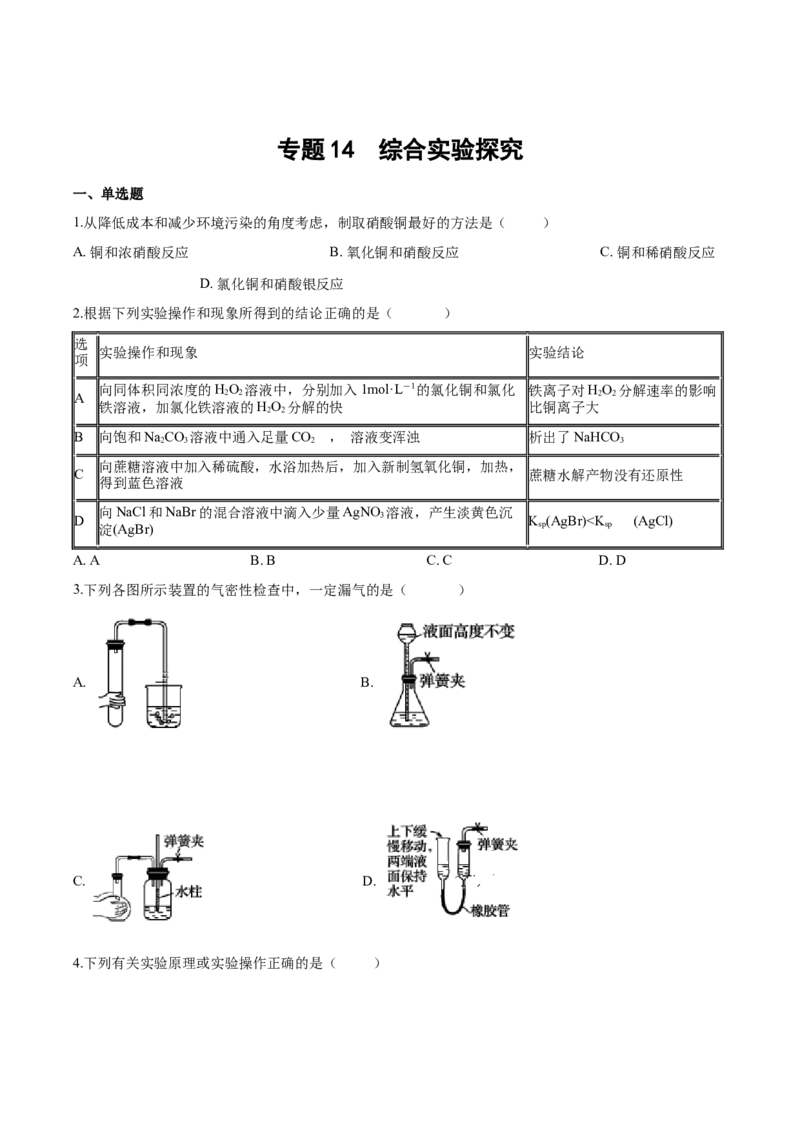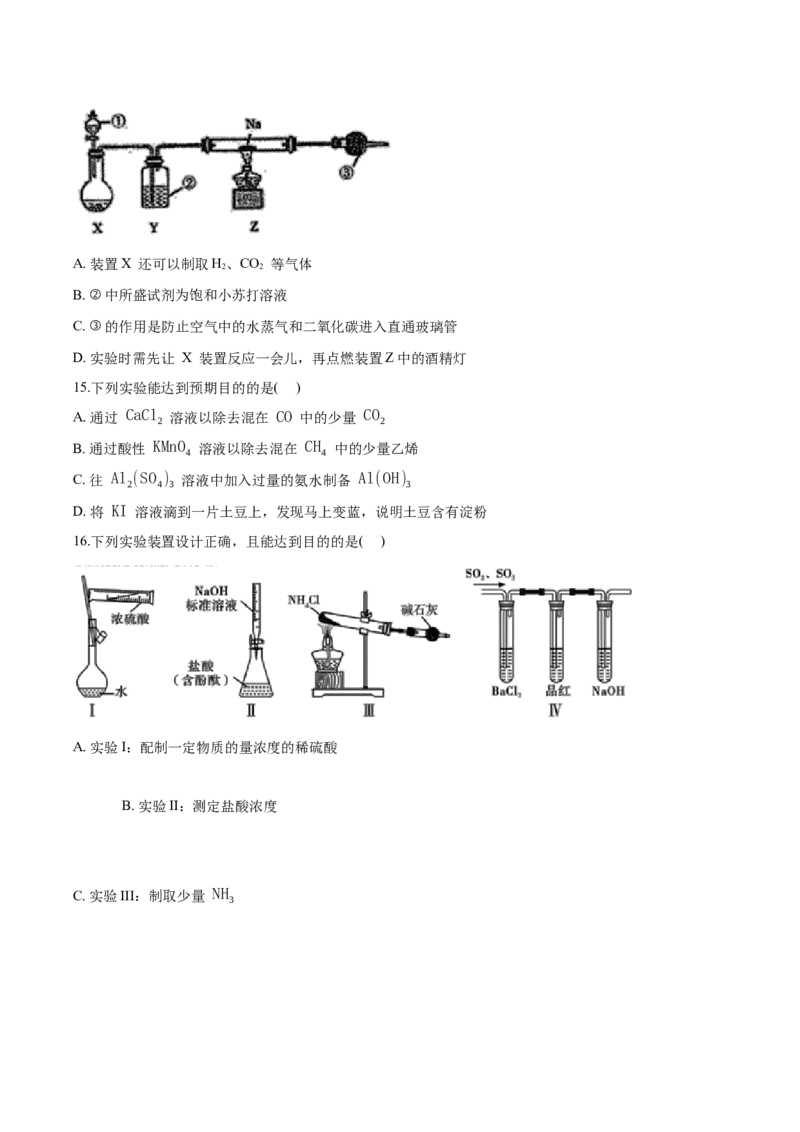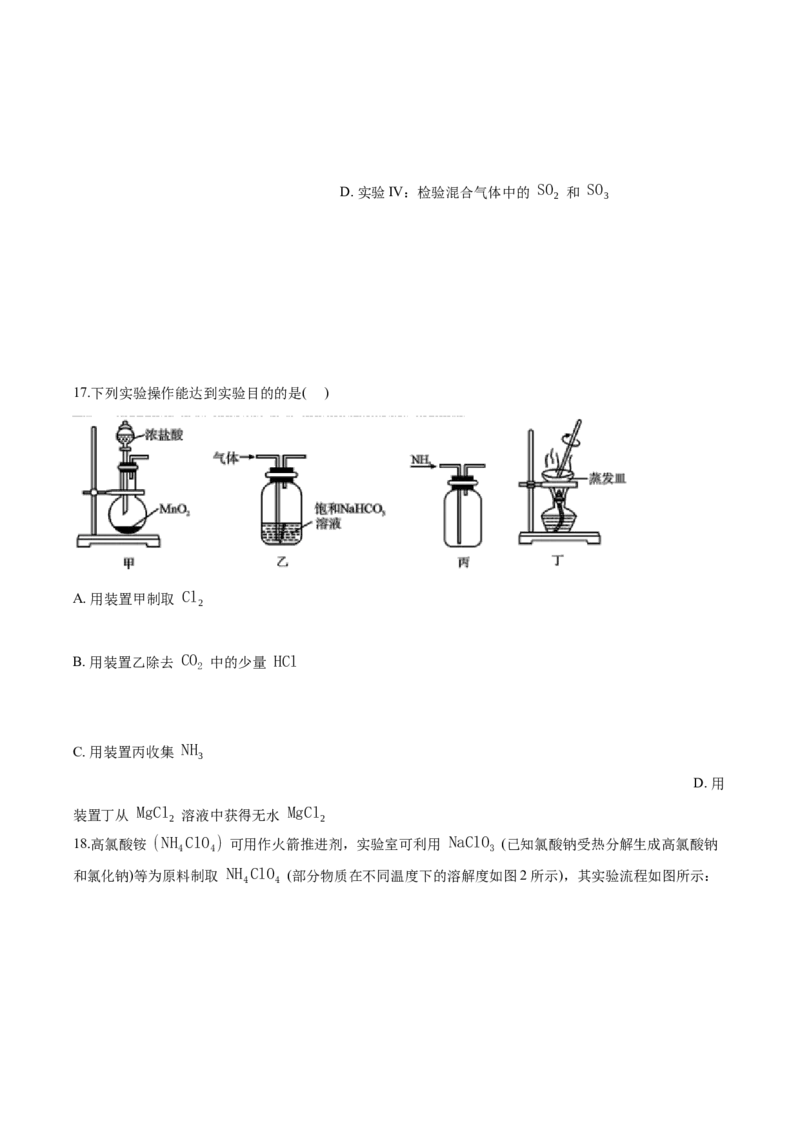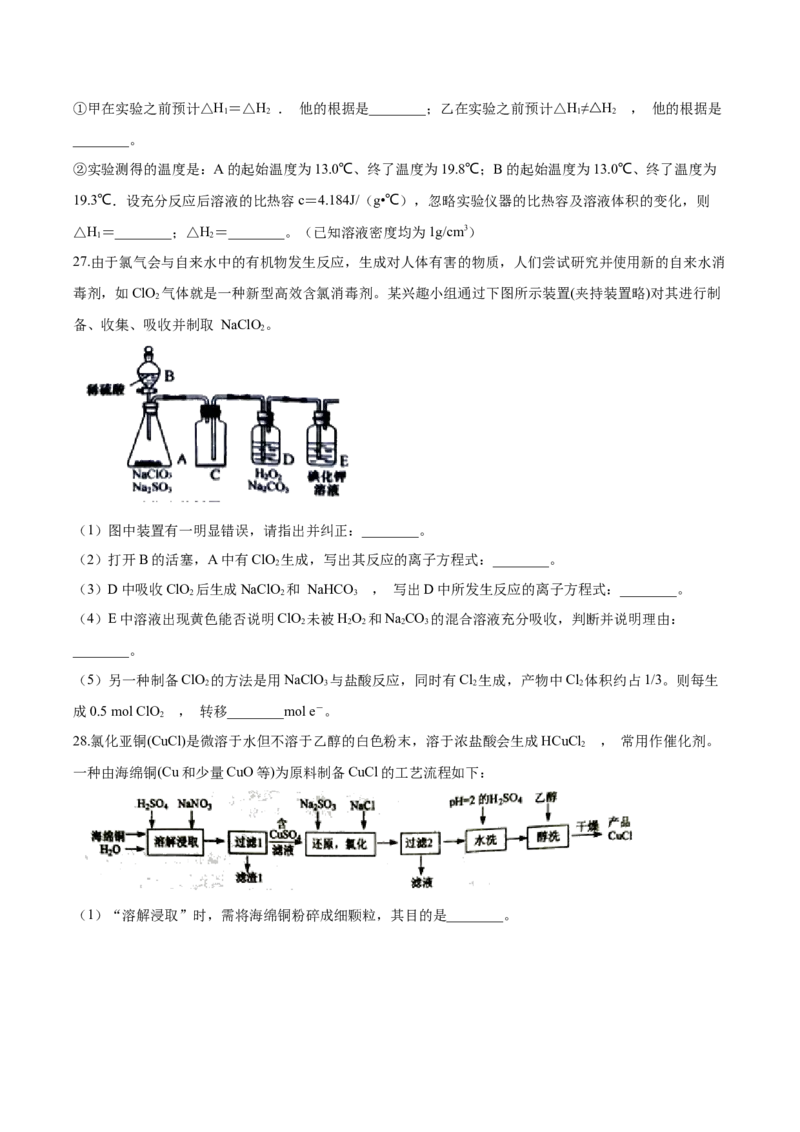文档内容
专题 14 综合实验探究
一、单选题
1.从降低成本和减少环境污染的角度考虑,制取硝酸铜最好的方法是( )
A. 铜和浓硝酸反应 B. 氧化铜和硝酸反应 C. 铜和稀硝酸反应
D. 氯化铜和硝酸银反应
2.根据下列实验操作和现象所得到的结论正确的是( )
选
实验操作和现象 实验结论
项
向同体积同浓度的HO 溶液中,分别加入1mol·L-1的氯化铜和氯化 铁离子对HO 分解速率的影响
A 2 2 2 2
铁溶液,加氯化铁溶液的HO 分解的快 比铜离子大
2 2
B 向饱和NaCO 溶液中通入足量CO , 溶液变浑浊 析出了NaHCO
2 3 2 3
向蔗糖溶液中加入稀硫酸,水浴加热后,加入新制氢氧化铜,加热,
C 蔗糖水解产物没有还原性
得到蓝色溶液
向NaCl和NaBr的混合溶液中滴入少量AgNO 溶液,产生淡黄色沉
D 3 K (AgBr)K (AgBr)
溶液 浑浊 sp sp
N aAlO 和Na HCO 发生相互促进的水解
D NaAlO 溶液中滴加 NaHCO 溶液 产生白色沉淀 2 3
2 3 反应
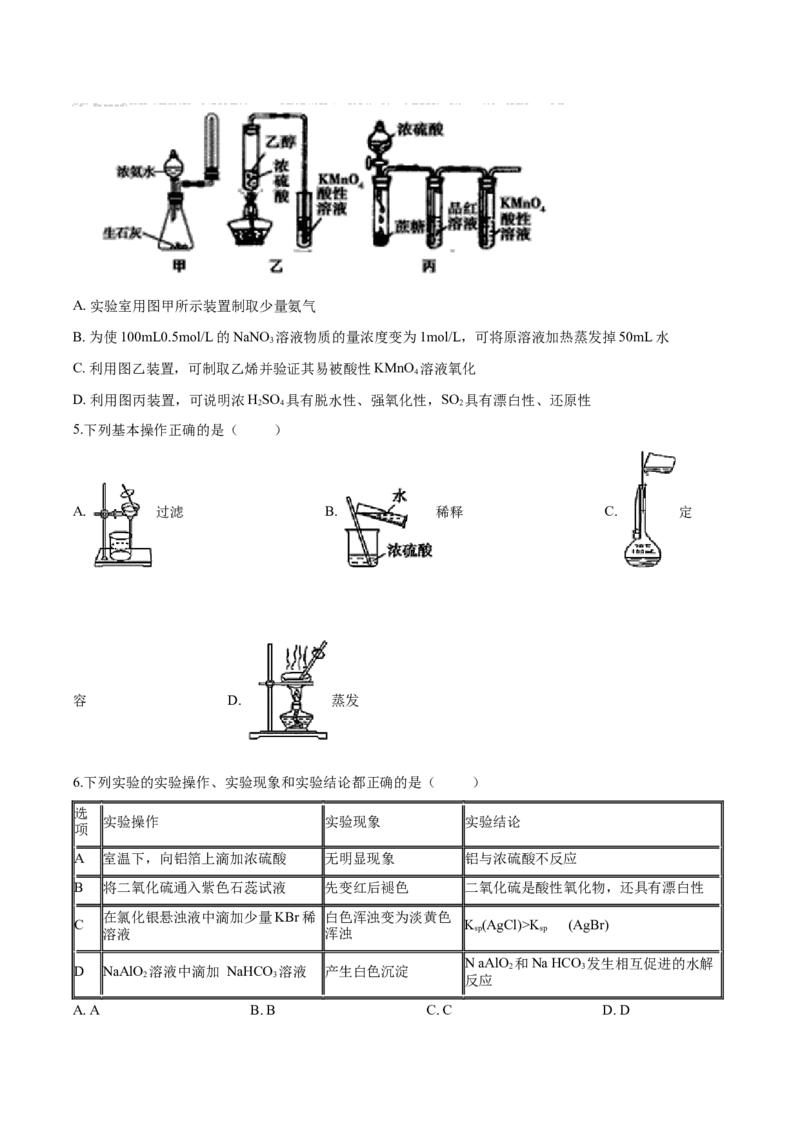
A. A B. B C. C D. D7.下列实验操作中错误的是( )
A. 蒸发操作时,当溶液中出现较多固体应停止加热
B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C. 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D. 如果没有试管夹,可以临时手持试管给固体或液体加热
8.为了鉴别某白色纺织品的成分是蚕丝(蛋白质)还是人造丝(合成纤维),可选用的方法是( )
A. 滴加酒精 B. 灼烧
C. 滴加食盐水溶液
D. 滴加食醋
9.在测定中和热的实验中,下列说法错误的是( )
A. 在测定中和热实验中需要使用的仪器有天平、量筒﹑烧杯、滴定管、温度计
B. 为了准确测定反应混合溶液的温度,实验中温度计水银球不能与小烧杯底部接触
C. 用50 mL 0.55 mol ·L-1的NaOH 溶液与60 mL 0.50 mol ·L-1的盐酸反应,测得的中和热数值不变
D. 使用环形玻璃搅拌棒是为了加大反应速率,减小实验误差
10.下列化学实验操作与对应现象均正确,且能得出对应结论的是( )
实验操作 现象 结论
A
取样品于试管中,加足量 NaOH 溶液,加热,将湿润的红色石
试纸不变色 样品中无
NH+
蕊试纸置于试管口 4
向
2mL0.1mol⋅L−1FeCl
溶液中加适量铜粉,振荡,滴加 还原性:
B 3 产生蓝色沉淀
K [Fe(CN) ] 溶液 Cu Fe
铁片不溶解
向鸡蛋清溶液中加入少量CuSO 溶液,出现浑浊,分离沉淀后加足量水,沉
C 4 蛋白质发生了变性
淀不溶解
该乙醇中含有一定量的
D 向某乙醇中加入一小块金属钠,有气泡生成
水
A. A B. B C. C D. D
22.下列实验设计方案错误的是( )
A. 分离碘和CCl 的混合物:用分液漏斗分液 B. 区分NaCl和KCl溶液:焰色反应
4
C. 除去乙醇中混有的少量水:加入生石灰蒸馏 D. 检验某未知溶液中的SO 2—:加入稀硝
4
酸酸化的BaCl 溶液
2
23.下列设计的实验方案能达到实验目的的是( )
A. 制取无水AlCl :将AlCl 溶液加热蒸干并灼烧
3 3
B. 提纯含有少量苯酚的苯:向含有少量苯酚的苯中加入浓溴水,然后过滤
C. 配制Hg(NO) 溶液:将Hg(NO) 溶解在较浓硝酸中,然后加水稀释
3 2 3 2
D. 除去MgCl 溶液中混有的少量FeCl :向混有FeCl 的MgCl 溶液中加入足量MgCO , 微热并充分搅
2 3 3 2 3
拌,然后过滤
24.下列生产或实验事实得出的相应结论错误的是( )
选
事实 结论
项
A 其他条件相同,NaSO 溶液和HSO 溶液反应,升高溶液的温度,析出硫沉淀 当其他条件不变时,
2 2 3 2 4 升高反应温度,化学所需时间缩短 反应速率加快
A、B两支试管,各加入4mL0.01mol/L的KMnO 酸性溶液,在A试管中加入 当其他条件不变时,
4
B 2mL0.01mol/LH C O 溶液和在B试管中加入4mL 0.02mol/L的HC O 溶液, 增大反应物浓度,化
2 2 4 2 2 4
记录溶液褪色所需时间,B试管褪色时间短 学反应速率加快
❑
在容积可变的密闭容器中发生反应:2NH (g) NH(l)+H(g),把容器的体积正反应速率加快,逆
C 3 ⇌ 2 4 2
反应速率减慢
缩小一半
当其他条件不变时,
A、B两支试管中分别加入等体积5%的HO 溶液,在B试管中加入2~3滴
D 2 2 催化剂可以改变化学
FeCl 溶液,B试管中产生气泡快
3 反应速率
A. A B. B C. C D. D
25.有关下列实验各装置图的叙述,不正确的是( )
A. 装置①可用于吸收实验中多余的Cl B. 装置②可用于收集H、NH 、Cl、HCl、NO 等
2 2 3 2 2
C. 装置③中X为苯,可用于吸收氨气或氯化氢 D. 装置④中可用于收集氨气,并吸收多余的
氨气
三、填空题
26.
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、________、________。
(2)量取反应物时,取50mL 0.50mol•L﹣1的盐酸,还需加入的试剂是 (填序号)。
A.50mL 0.50mol•L﹣1 NaOH溶液
B.50mL 0.55mol•L﹣1 NaOH溶液
C.1.0g NaOH固体
(3)由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法进行两组测定中和
热的实验,实验试剂及其用量如下表所示。
反应物 起始温度t/℃终了温度t/℃中和热/kJ•mol﹣
1 2
1
A.1.0mol/L HCl溶液50mL、1.1mol/L NaOH溶液50mL 13.0 △H
1
B.1.0mol/L HCl溶液50mL、1.1mol/L NH •H O溶液50mL 13.0 △H
3 2 2①甲在实验之前预计△H=△H . 他的根据是________;乙在实验之前预计△H≠△H , 他的根据是
1 2 1 2
________。
②实验测得的温度是:A的起始温度为13.0℃、终了温度为19.8℃;B的起始温度为13.0℃、终了温度为
19.3℃.设充分反应后溶液的比热容c=4.184J/(g•℃),忽略实验仪器的比热容及溶液体积的变化,则
△H=________;△H=________。(已知溶液密度均为1g/cm3)
1 2
27.由于氯气会与自来水中的有机物发生反应,生成对人体有害的物质,人们尝试研究并使用新的自来水消
毒剂,如ClO 气体就是一种新型高效含氯消毒剂。某兴趣小组通过下图所示装置(夹持装置略)对其进行制
2
备、收集、吸收并制取 NaClO。
2
(1)图中装置有一明显错误,请指出并纠正:________。
(2)打开B的活塞,A中有ClO 生成,写出其反应的离子方程式:________。
2
(3)D中吸收ClO 后生成NaClO 和 NaHCO , 写出D中所发生反应的离子方程式:________。
2 2 3
(4)E中溶液出现黄色能否说明ClO 未被HO 和NaCO 的混合溶液充分吸收,判断并说明理由:
2 2 2 2 3
________。
(5)另一种制备ClO 的方法是用NaClO 与盐酸反应,同时有Cl 生成,产物中Cl 体积约占1/3。则每生
2 3 2 2
成0.5 mol ClO , 转移________mol e-。
2
28.氯化亚铜(CuCl)是微溶于水但不溶于乙醇的白色粉末,溶于浓盐酸会生成HCuCl , 常用作催化剂。
2
一种由海绵铜(Cu和少量CuO等)为原料制备CuCl的工艺流程如下:
(1)“溶解浸取”时,需将海绵铜粉碎成细颗粒,其目的是________。(2)“还原,氯化”时,NaSO 和NaC1的用量对CuCl产率的影响如图所示:
2 3
①CuSO 与NaSO 、NaCl在溶液中反应生成CuCl的离子方程式为________。
4 2 3
②当n(Na SO )/n(CuSO)>1.33时,比值越大CuCl产率越小,其原因是________。
2 3 4
③当1.0Fe2+ ,故B不符合题意;
C.在 2mL0.1mol⋅L−1AgNO 溶液中滴入几滴 NaCl 溶液,再滴入 Na S 溶液,先生成白色沉淀,后
3 2
变成黄色,是因为 AgNO 溶液过量,加入 Na S 溶液,过量的 AgNO 与 Na S 反应生成黄色沉淀,不
3 2 3 2
能说明溶度积常数的关系,故C不符合题意;
D.将活性炭放入盛有 NO 的锥形瓶中,气体颜色变浅,是利用了活性炭的吸附性,故D不符合题意;
2
故答案为:A。
11.【答案】 A
【解析】A.SOCl 易水解,应该在里面放浓硫酸,吸收水蒸气,A项符合题意;
2
B.球形冷凝管的作用是冷凝、回流,B项不符合题意;C.可以通过氯气和二氧化硫产生气泡的速度来控制反应物比例,C项不符合题意;
D.三颈瓶可以适当降温,D项不符合题意;
故答案为:A。
12.【答案】 A
【解析】A.AlCl 溶液与氨水反应生成氢氧化铝白色沉淀,而硝酸银与氨水生成氢氧化银沉淀,但是氢氧
3
化银在常温下不稳定,易分解生成氧化银,氧化银灰黑色,所以可以鉴别,A项符合题意;
B.浓硝酸见光易分解所以用棕色瓶:其具有氧化性所以不能用橡胶塞,B项不符合题意;
C, 测出的pH值偏大,C项不符合题意;
D.应该用稀盐酸清洗做焰色反应的铂丝,D项不符合题意;
故答案为:A。
13.【答案】 C
【解析】A.由于反应后的溶液中有剩余的浓硫酸,故稀释时应该把反应后的混合物沿玻璃棒缓慢加入蒸
馏水中,并不断搅拌,A不符合题意;
B.KMnO 具有强氧化性,可将HO 氧化为O , 体现HO 的还原性,B不符合题意;
4 2 2 2 2 2
C.KCr O 溶液中, c(Cr O2-) > c(CrO2-) ,但加入AgNO 后生成Ag CrO 沉淀,而没有生成
2 2 7 2 7 4 3 2 4
Ag Cr O 沉淀,说明Ag CrO 比Ag Cr O 更难溶,即K (Ag CrO)<K (Ag Cr O),C符合题意;
2 2 7 2 4 2 2 7 sp 2 4 sp 2 2 7
D.加入碘水检验淀粉是否有剩余,不需要加入NaOH碱化,如果加NaOH,则I 与NaOH反应,导致无
2
法检测淀粉,也就无法确定淀粉是否完全水解,D不符合题意;
故答案为:C。
14.【答案】 B
【解析】A.装置X可以利用液体和固体或液体反应制取气体,氢气可以用稀硫酸和锌粒制取,二氧化碳
可以利用稀盐酸和石灰石制取,所以装置X 还可以制取H、CO 等气体,A不符合题意;
2 2
B.②中液体应是用来干燥氧气的,所以为浓硫酸,B符合题意;
C.装置③中应盛放碱石灰,防止空气中的水和二氧化碳进入装置Z,导致过氧化钠变质,C不符合题意;
D.实验时需先让 X 装置反应一会儿,排尽装置内的空气,再点燃装置Z中的酒精灯,D不符合题意;
故答案为:B。
15.【答案】 C
【解析】A. CaCl 和 CO 不反应,应用氢氧化钠溶液除去CO中的 CO ,故A不符合题意;
2 2 2
B.酸性高锰酸钾能将乙烯氧化成二氧化碳气体,引入新杂质,故B不符合题意;
C. Al (SO ) 与一水合氨反应产生氢氧化铝,且氢氧化铝不溶于氨水,故C符合题意;
2 4 3D.KI溶液遇到淀粉不变蓝,应用碘水检验淀粉,故D不符合题意;
故答案为:C。
16.【答案】 D
【解析】A.容量瓶中不能进行稀释,应在烧杯中稀释浓硫酸冷却后转移至容量瓶中,故A不符合题意;
B.氢氧化钠应用碱式滴定管盛装,故B不符合题意;
C.直接加热氯化铵生成氨气和HCl遇冷又重新化合形成氯化铵,得不到氨气,故C不符合题意;
D. SO 和 SO 通入氯化钡中,二氧化硫与氯化钡不反应,若生成白色沉淀说明存在 SO ,通入品红溶
2 3 3
液若褪色说明存在,多余的气体用氢氧化钠溶液吸收,故D符合题意;
故答案为:D。
17.【答案】 B
【解析】A.实验室用 MnO 和浓盐酸在加热条件下取 Cl ,甲装置缺少加热装置,A项不符合题意;
2 2
B. CO 在饱和 NaHCO 溶液中溶解度很小,且不与 NaHCO 反应, HCl 与 NaHCO 溶液反应生成
2 3 3 3
CO ,用装置乙除去CO 中的少量HCl,B项符合题意;
2 2
C. NH 密度比空气小,用向下排空气法收集,C项不符合题意;
3
D.从 MgCl 溶液中获得无水 MgCl 先采用蒸发浓缩、冷却结晶的方法获得 MgCl ·6H O ,再在 HCl
2 2 2 2
的氛围中加热获得无水 MgCl ,D项不符合题意;
2
故答案为:B。
18.【答案】 C
【解析】A.可由图知,NaClO 的溶解度受温度影响很大,NaCl溶解度受温度影响不大,80℃时浸取液冷
4
却至0℃过滤,高氯酸钠的溶解度迅速降低,析出晶体,但是氯化钠的溶解度受温度的影响不大,不会析
出晶体,则滤渣的主要成分为NaClO , 故A不符合题意;
4
B.反应器高氯酸钠中加入氯化铵饱和溶液,反应向着更难溶的物质转化,根据物质的溶解情况,可知析
出高氯酸铵,即发生反应的离子方程式为
NH+
+
ClO-
═NH ClO ↓,故B不符合题意;
4 4 4 4
C.洗涤NH ClO 固体时应避免NH ClO 溶解,不能用超过80℃的热水,故C符合题意;
4 4 4 4
Δ
D.NH ClO 发生分解反应时,发生2NH ClO N↑+2O ↑+Cl↑+4H O,会产生大量气体,故D不符合题
4 4 4 4 2 2 2 2
¿
意;
故答案为C。
19.【答案】 D+ +
【解析】A.VO2+中V元素为+4价,VO ❑ 中V元素为+5价,3molVO2+被氧化成VO ❑ ,失去3mol
2 2
电子,而1mol KClO 变为KCl失去6mol电子,故需要0.5mol KClO , 故A不符合题意;
3 3
B.由上述分析可知,滤液1中主要的阴离子有[Al(OH) ]-、VO ❑ − 、Cl-、OH- , 故B不符合题意;
4 3
C.“煅烧”时需要的仪器主要有坩埚、玻璃棒、三脚架、酒精灯、泥三角等,故C不符合题意;
高温
D.NH VO 煅烧生成VO , 化学方程式为:2NH VO VO+2NH↑+H O,故D符合题意。
4 3 2 5 4 3 2 5 3 2
¿
故答案为:D。
20.【答案】 C
【解析】A.氢氧化钠溶液不能吸收水,故A不符合题意
B.碳酸钙上还会吸附少量的氢氧化钙,故B不符合题意
C.若酒精中含有碳元素,则烧杯内壁澄清石灰水变浑浊,故C符合题意
D.俯视读数,液体的体积减小,溶质的质量分数增加, 故D不符合题意
故答案为:C
二、多选题
21.【答案】 A,C
【解析】A.气体能使湿润的红色石蕊试纸变蓝,说明该气体溶于水,溶液成碱性,为氨气,故A符合题
意;
B.常温下,分别将铁片和铜片置于浓硝酸中,铁片不溶解,而铜片溶解,其中铁发生的是钝化,不能说明金属
性铁强于铜,故B不符合题意;
C.向鸡蛋清溶液中加入重金属盐硫酸铜溶液,蛋白质发生变性,则有沉淀出现,再加入蒸馏水,沉淀不溶
解,故C符合题意;
D.乙醇能与金属钠反应生成乙醇钠和氢气,故D不符合题意。
故答案为:AC。
22.【答案】 A,D
【解析】A、碘不易溶于水,易溶于四氯化碳,则用分液的方法不能分离,应该采用蒸馏的方法分离,A
符合题意;
B、钠和钾的焰色反应不同,可用焰色反应鉴别,B不符合题意;
C、加入生石灰,生石灰与水反应生成不挥发的氢氧化钙,再蒸馏可制取无水乙醇,C不符合题意;
D、加入硝酸,不能排除SO 2-以及银离子等的影响,应先加入盐酸,再加入氯化钡鉴别,D符合题意;
3
故答案为:AD23.【答案】 C,D
❑
【解析】A、AlCl 水解存在平衡AlCl +3H O Al(OH)(胶体)+3HCl,加热HCl挥发,水解彻底进
3 3 2 ⇌ 3
行,生成Al(OH) 沉淀,灼烧Al(OH) 得Al O , 而无法得到无水AlCl , 选项A不符合题意;
3 3 2 3 3
B.溴水与苯酚反应、且溴易溶于苯,不能除杂,应选NaOH溶液、分液,选项B不符合题意;
C、配制Hg(NO) 溶液:为抑制Hg(NO) 的水解,将Hg(NO) 溶解在较浓硝酸中,然后加水稀释,选项C
3 2 3 2 3 2
符合题意;
D.向含有少量FeCl 的MgCl 溶液中加入足量Mg(OH) 粉末,溶液pH增大,利于Fe3+的水解,可转化为
3 2 2
Fe(OH) 沉淀而除去,选项D符合题意;
3
故答案为:CD。
24.【答案】 B,C
【解析】A、其他条件相同,NaSO 溶液和HSO 溶液反应,升高溶液的温度,析出硫沉淀所需时间缩
2 2 3 2 4
短,反应速率加快,故当其他条件不变时,升高反应温度,化学反应速率加快,A不符合题意;
B、A、B两支试管中反应混合物的体积不同,不能根据B试管褪色时间短得出当其他条件不变时,增大反
应物浓度,化学反应速率加快的结论,B符合题意;
C、把容器的体积缩小一半,压强增大,正、逆反应速率均加快,不能得出题给结论,C符合题意;
D、A、B两支试管中分别加入等体积5%的HO 溶液,在B试管中加入2~3滴FeCl 溶液,B试管中产生
2 2 3
气泡快,可以 得出当其他条件不变时,催化剂可以改变化学反应速率的结论,D不符合题意;
故答案为:BC
25.【答案】AC
【解析】解:A.导管在液面下,可发生倒吸,则图中装置可收集尾气,但易发生倒吸,故A错误;
B.a进气可收集密度比空气密度大的气体,b进入可收集密度比空气密度小的气体,则装置②可用于收集
H、NH 、Cl、HCl、NO 等,故B正确;
2 3 2 2
C.X为苯,密度比水的小,则X在上层,不能隔绝气体和水,X应为四氯化碳,故C错误;
D.碱石灰可干燥氨气,氨气的密度比空气密度小,易溶于水,则图④中可用于收集氨气,并吸收多余的
氨气,故D正确;
故选AC.
三、填空题
26.【答案】 (1)环形玻璃搅拌棒;量筒
(2)B(3)中和热的大小和反应物的用量多少无关,是一个定值;NaOH是强碱,NH3•H2O是弱碱电离吸热;
﹣56.8 kJ/mol;﹣52.7 kJ/mol
【解析】(1)中和热测定中,用到的玻璃仪器由烧杯、温度计、环形玻璃棒、量筒玻璃仪器
(2)选择的氢氧化钠的浓度要稍微高一些一些,保证实验进行完全, 50mL 0.55mol•L﹣1 NaOH溶液
(3)①中和热的大小与用量无关,是一个定值,氢氧化钠是强碱,氨水是弱碱,电离时吸热
②根据公式计算 △H= cm △t/n=100x4.184x(19.8-13)/0.05KJ/mol=56.8KJ/mol
1
△H= cm △t/n=100x4.184x(19.3-13)/0.05KJ/mol= ﹣52.7 kJ/mol
2
27.【答案】 (1)C装置中导气管应该长进短出
(2)SO 2-+ 2H++2ClO -=2ClO ↑+ H O+SO 2-
3 3 2 2 4
(3)2CO2-+ 2H O+2ClO =2ClO -+ O +2HCO-
3 2 2 2 2 2 3
(4)不能。因为D装置中有O 产生,O 也可能将I-氧化为I
2 2 2
(5)0.5
【解析】(1)ClO 气体的密度比空气大,应该选用向上排空气法收集,装置C中进气导管口应接近集气瓶底
2
部,出气导管口应与瓶塞平齐,所以图中装置C中导气管应该“长进短出”。
(2)依题意,稀硫酸、NaClO 和NaSO 混合能产生ClO , 氯元素化合价由+5价降低到+4价,表明
3 2 3 2
ClO -表现氧化性,而SO 2-具有较强的还原性,所以其离子方程式为SO 2-+ 2H++2ClO -=2ClO ↑+
3 3 3 3 2
HO+SO 2-。
2 4
(3)由题意知ClO 与HO、NaCO 接触生成NaClO 和 NaHCO , 氯元素化合价由ClO 的+4价变化到
2 2 2 2 3 2 3 2
NaClO 的+3价,ClO 作氧化剂,碳元素化合价没变,只能是HO 中的-1价氧被氧化为O , HO 作还
2 2 2 2 2 2 2
原剂,所以D中发生反应的离子方程式为2CO2-+ 2H O+2ClO =2ClO -+ O ↑+2HCO-。
3 2 2 2 2 2 3
(4)KI溶液变黄说明有I 生成,即I-被氧化成I , 除ClO 能氧化I-外,混合气体中的O 也能氧化I- ,
2 2 2 2
所以E中溶液出现黄色不能说明ClO 未被HO 和NaCO 的混合溶液充分吸收,因为D装置中有O 产
2 2 2 2 3 2
生,O 也可能将I-氧化为I。
2 2
(5) NaClO 与盐酸反应有ClO 和Cl 生成,根据“互不交叉原理”,NaClO 转化为ClO , HCl转化为
3 2 2 3 2
Cl , 且ClO 与Cl 化学计量数之比为2:1,其反应方程式及转移的电子数为
2 2 2
2NaClO+4HCl=2ClO ↑+Cl↑+2NaCl+2HO~转移电子2e-。根据方程式计量关系可知每0.5molClO 生成时转
3 2 2 2 2
移0.5mole-。
28.【答案】 (1)增大固体与空气的接触面积,增大反应速率,提高原料利用率
(2)2Cu2++SO2-+2Cl-+H O =2CuCl↓+SO 2-+2H+;随着n(Na SO )/n(CuSO) 不断增大,溶液的碱性不断增
3 2 4 2 3 4强,Cu2+及CuCl的水解程度增大;适当增大c(Cl-),有利于平衡Cu+(aq)+Cl-(aq) CuCl(s)向生成
CuCl方向移动
(3)CuCl的产率降低
(4)4CuCl + O + 4H O = 2Cu (OH) Cl + 2HCl
2 2 2 3
(5)93.28%
【解析】(1)将海绵铜粉碎成细颗粒是为了增大固体与空气的接触面积,增大反应速率,提高原料利用率。
(2) ①CuSO 转化为CuCl,表明+2价铜元素得电子,Cu2+是氧化剂,而SO 2-具有较强还原性,故而SO 2-
4 3 3
失去电子生成SO 2- , 其离子方程式为2Cu2++SO2-+2Cl-+H O =2CuCl↓+SO 2-+2H+。
4 3 2 4
②Na 2 SO 3 水解呈碱性:SO 3 2-+H 2 O ⇌ HSO 3 -+OH- , Cu2+水解呈酸性:Cu2++2H 2 O ⇌ Cu(OH) 2 +2H+ ,
溶液中NaSO 浓度越大时,溶液碱性越强,对CuSO 水解的促进作用就越大。所以n(Na SO )/n(CuSO)比
2 3 4 2 3 4
值越大CuCl产率越小的原因是:随着n(Na SO )/n(CuSO ) 不断增大,溶液的碱性不断增强,Cu2+及CuCl
2 3 4
的水解程度增大。
③CuCl微溶于水,在水溶液中存在溶解平衡Cu+(aq)+Cl-(aq) ⇌ CuCl(s),所以n(NaCl)/n(CuSO 4 )比值越大
CuCl产率越大的原因是:适当增大c(Cl-),有利于平衡Cu+(aq)+Cl-(aq) ⇌ CuCl(s)向生成CuCl方向移
动。
(3)稀硝酸能够氧化CuCl:3CuCl+4H++NO-=3Cu2++NO↑+3Cl-+2H O,所以若不慎用稀硝酸进行稀释,则
3 2
CuCl的产率降低。
(4)2个CuCl被氧化为1个Cu (OH) C1失去2个电子,1个O 得到4个电子转化为O2- , 反应物中应该
2 3 2
有HO提供氢元素,所以其化学方程式为4CuCl + O + 4H O = 2Cu (OH) Cl + 2HCl。
2 2 2 2 3
(5)氯化亚铜产品中加入足量的FeCl 溶液:CuCl+Fe3+=Cu2++Fe2++Cl- , 再用KMnO 酸性溶液滴定:
3 4
5Fe2++MnO-+8H+=5Fe3++Mn2++4H O,得关系式5CuCl~5Fe2+~MnO-。样品中CuCl的物质的量
4 2 4
n(CuCl)=5·n(KMnO )=5×0.2mol/L×0.015L=0.015mol,则产品中氯化亚铜的质量分数=
4
0.015mol×99.5g/mol
=93.28%。
1.600g
四、实验探究题
Δ _
_
29.【答案】 (1)2N H 4 Cl+Ca(OH) 2¿CaCl +2N H ↑+2H O
2 3 2
¿
(2)球形干燥管;不能
(3)浓硫酸(或浓HSO );干燥N , 吸收未反应的NH
2 4 2 3(4)②③
(5)高温时LiN可与玻璃中的SiO 反应而腐蚀玻璃
3 2
(6)87.5
【解析】 (1)装置A的固体在加热条件下可制备氨气,其发生反应的化学方程式为
Δ _
_
2N H 4 Cl+Ca(OH) 2¿CaCl +2N H ↑+2H O ;
2 3 2
¿
(2)根据仪器构造可知,仪器B、F的名称为球形干燥管;两者所盛装的试剂作用分别是干燥氨气、防止外
界空气中的水蒸气进入装置E,使制备的Lin水解,两者不能交换,因为氨气可以与氯化钙发生反应,不
3
能达到干燥氨气的目的,故答案为:不能;
(3) 装置D中所装试剂a的作用是干燥净化氮气,所以应该为浓硫酸,不能可以干燥氮气,还可以吸收多
余的氨气,故答案为:干燥N , 吸收未反应的NH ;
2 3
(4)根据(3)问分析可知,装置D吸收未反应的氨气,因为氨气极易溶于水,密度比空气小,可采用设计
防倒吸装置进行吸收,则①进气装置不符合题意,不能达到目的,故不符合题意;②③符合要求,可防倒
吸;④中有机物苯的密度比水小,在水的上面,导气管导入试剂a中不能达到防倒吸的目的,故不符合题
意,故答案为:②③;
(5)根据给定资料可知,“LiN高温时能腐蚀镍、铜、石英等”可知,高温时LiN可与玻璃中的SiO 反应
3 3 2
而腐蚀玻璃,所以装在氧化锆小舟中的Li粒不能直接放在反应管中,故答案为:高温时LiN可与玻璃中
3
的SiO 反应而腐蚀玻璃;
2
(6) 根据元素守恒可知,24.0 g金属锂全部转化为LiN的话,得到LiN的质量为
3 3
24.0g 1
× ×35g/mol=40.0g ,置于质量为30.2 g的氧化锆小舟中,待反应一段时间后, 使产品在
7g/mol 3
氮气氛围中充分冷却后再对氧化锆小舟进行称重,总质量为68.2 g,则质量增加68.2g-(24.0g+30.2g)=14g,
14g
即实际消耗的氮气的质量为14g,所以生成的LiN的质量为 ×2×35g/mol =35g,所以产率约为
3 28/mol
35g
×100%=87.5% ,故答案为:87.5。
40g
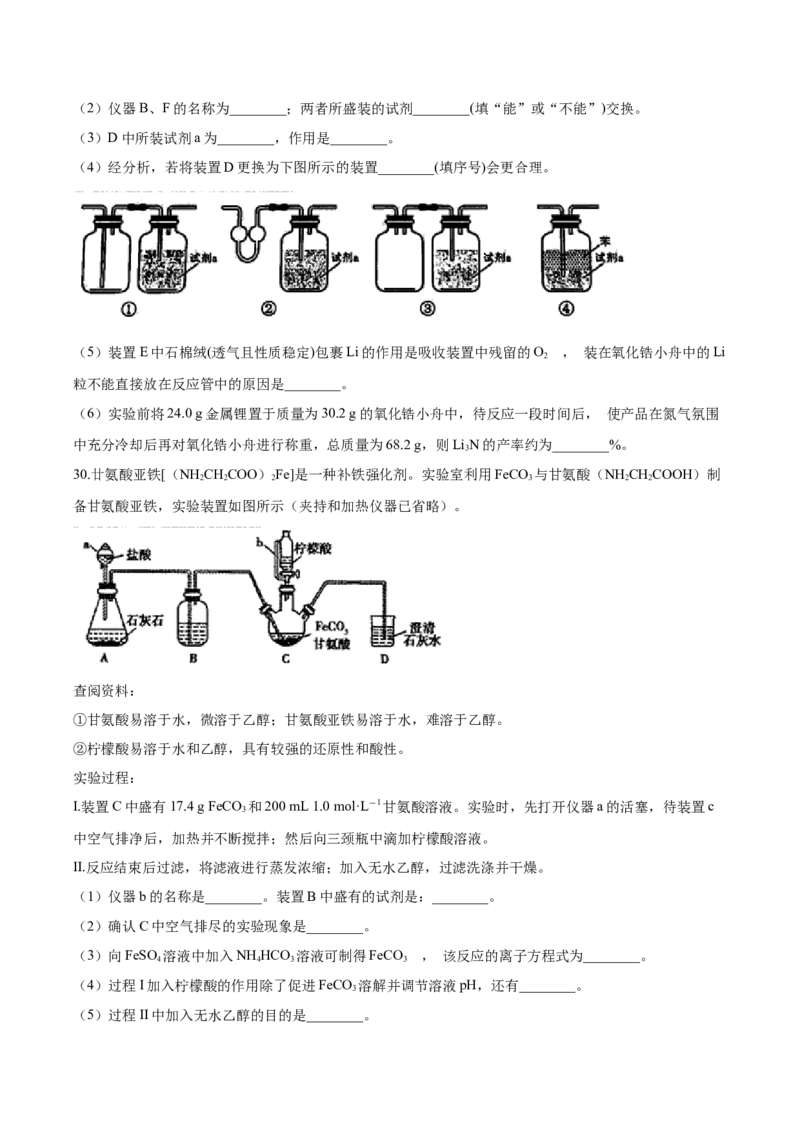
30.【答案】 (1)恒压滴液漏斗;饱和NaHCO 溶液
3
(2)D中的澄清石灰水变浑浊-
(3)Fe2+ +2HCO ❑ = FeCO↓+CO ↑+H O
3 3 2 2
(4)防止甘氨酸亚铁被氧化
(5)降低甘氨酸亚铁的溶解度,使其结晶析出
(6)75
【解析】(1)仪器b的名称为恒压滴液漏斗,置B的作用是除去CO 中混有的HCl,则装置B中盛有的试剂
2
饱和NaHCO 溶液,故答案为:恒压滴液漏斗,饱和NaHCO 溶液;(2) 用二氧化碳气体将实验装置中的
3 3
空气排干净,当D中的澄清石灰水变浑浊,则说明C中空气排干净,故答案为:D中的澄清石灰水变浑
浊;(3) 向FeSO 溶液中加入NH HCO 溶液可制得FeCO , 同时应有CO 气体生成,发生反应的离子方
4 4 3 3 2
- -
程式为Fe2+ +2HCO ❑ = FeCO↓+CO ↑+H O,故答案为:Fe2+ +2HCO ❑ = FeCO↓+CO ↑+H O;(4) 根
3 3 2 2 3 3 2 2
据题给信息可知,过程I加入柠檬酸的作用除了促进FeCO 溶解并调节溶液pH,还有防止甘氨酸亚铁被氧
3
化,故答案为:防止甘氨酸亚铁被氧化;(5) 甘氨酸亚铁易溶于水,难溶于乙醇,则过程I中加入无水乙醇
可降低甘氨酸亚铁的溶解度,使其结晶析出,故答案为:降低甘氨酸亚铁的溶解度,使其结晶析出;(6)
17.4g
17.4 g FeCO 的物质的量为 =0.15mol ,200 mL甘氨酸溶液中甘氨酸的物质的量为0.2L×1.0
3 116g/mol
mol·L-1=0.2 mol,理论上生成0.1mol的甘氨酸亚铁,理论上可产生甘氨酸亚铁:204g·mol-
15.3g
1×0.1mol=20.4g,产率为 ×100%=75% ,故答案为:75%。
20.4g