文档内容
专题七 能力提升检测卷
1.下列说法正确的是
A.自发反应是指不需要条件就能发生的反应
B.非自发过程在任何条件下都不可能变为自发过程
C.在其他外界条件不变的情况下,使用催化剂可以改变化学反应进行的方向
D.常温下,反应C(s)+CO(g) 2CO(g)不能自发进行,则该反应的 H>0
2
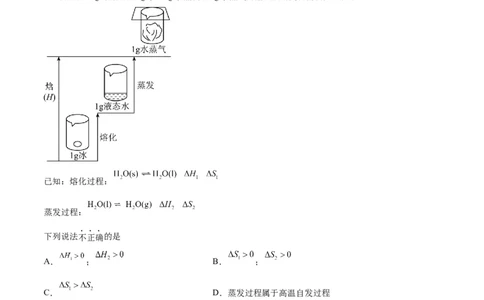
2.常压下,1g冰熔化成1g水、1g水蒸发成1g水蒸气的焓和熵的变化△情况如图所示。
已知:熔化过程:
蒸发过程:
下列说法不正确的是
A. ; B. ;
C. D.蒸发过程属于高温自发过程
3.在恒容密闭容器中进行反应:C(s)+CO(g) 2CO(g) ∆H>0。下列说法不正确的是
2
A.∆S>0
B.反应在高温下能自发进行
C.当混合气体的密度不再变化时,反应一定达到平衡状态
D.容器内气体浓度c(CO)∶c(CO)=1∶2时,反应一定达到平衡状态
2
4.通过2NO(g)+2CO(g) 2CO(g)+N(g) ΔH=-746.5kJ·mol-1催化还原的方法,可将汽车尾气中有害气体转
2 2
⇌化为无害气体。下列说法正确的是
A.该反应在任何条件下都能自发进行
B.反应的平衡常数可表示为K=
C.其它条件不变,增大 的值,NO的转化率下降
D.使用高效的催化剂可以降低反应的焓变
5.反应A+3B=4C+2D,在不同条件下反应,其平均反应速率v(X)(表示反应物的消耗速率或生成物的生成
速率)如下,其中反应速率最快的
A.v(A)=2.4mol/(L·min) B.v(B)=0.08mol/(L·s)
C.v(C)=7.2mol/(L·min) D.v(D)=0.7mol/(L·s)
6.化学反应速率的研究对工农业生产和日常生活有着十分重要的意义,下列操作不能加快化学反应速率
的是
A.合成氨反应中增大容器的容积
B.燃煤发电时用煤粉代替煤块
C.用 制备 时,使用 作催化剂
D.用70%的硫酸溶液代替98%的浓硫酸与 粉末反应制备
7.可使反应C(s)+HO(g) CO(g)+H(g)的反应速率增大的措施是
2 2
①增大压强 ②恒容通入HO(g) ③增加碳的用量 ④适当提高温度 ⑤恒容下充入N
2 2
A.④⑤ B.①③⑤ C.①③④ D.①②④
8.下列说法不正确的是
A.恒温恒容下,对于反应 ,压强不再变化,说明反应已达到平衡状态
B.绝热体系中,对于反应 ,正反应为放热反应,若反应体系的温
度不变,说明反应已达到平衡状态
C.在恒容容器中,发生反应 ,若混合气体的颜色不再变化,说明反应达到平衡状
态
D.恒温恒容下,对于反应: ,当 ,反应达到平衡状态9.反应 的速率方程为 (k为速率常数,其中
,A、R为常数, 为活化能,T为开氏温度),其半衰期(反应物消耗一半所需的时
间)为 。改变反应物浓度时,反应的瞬时速率如表所示。下列说法正确的是
0.25 0.5 l 0.5 l
0.05 0.05 0.1 0.1 0.2
1.6 3.2 3.2
A.
B.
C.在过量的B存在时,A剩余25%所需的时间是
D.升温、加入催化剂,缩小容积(加压),均能使k增大,导致反应的瞬时速率加快
10.在T℃、 时,将1mol CO和3mol 充入体积可变的密闭容器中,发生反应:
。能说明该反应达到平衡状态的是
A.
B.容器内压强不再发生变化
C.CO(g)和 (g)的物质的量之比不再发生变化
D.混合气体的密度不再发生变化
11.在恒温恒容的密闭容器中,在某催化剂表面上发生分解反应: ,测得不同起始
浓度和不同催化剂表面积时Z的浓度随时间的变化如表所示。下列说法错误的是
编
0 20 40 60 80
号
① a 2.40 2.00 1.60 1.20 0.80② a 1.20 0.80 0.40 x
③ 2a 2.40 1.60 0.80 0.40 0.40
A.实验①,100 min时反应达到平衡状态
B.实验②,60 min时反应处于平衡状态
C.相同条件下,增大催化剂的表面积,Z的平衡转化率不变
D.相同条件下,增加Z的浓度,反应速率增大
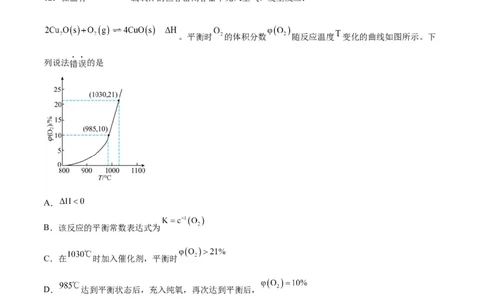
12.在盛有 载氧体的恒容密闭容器中充入空气,发生反应:
。平衡时 的体积分数 随反应温度 变化的曲线如图所示。下
列说法错误的是
A.
B.该反应的平衡常数表达式为
C.在 时加入催化剂,平衡时
D. 达到平衡状态后,充入纯氧,再次达到平衡后,
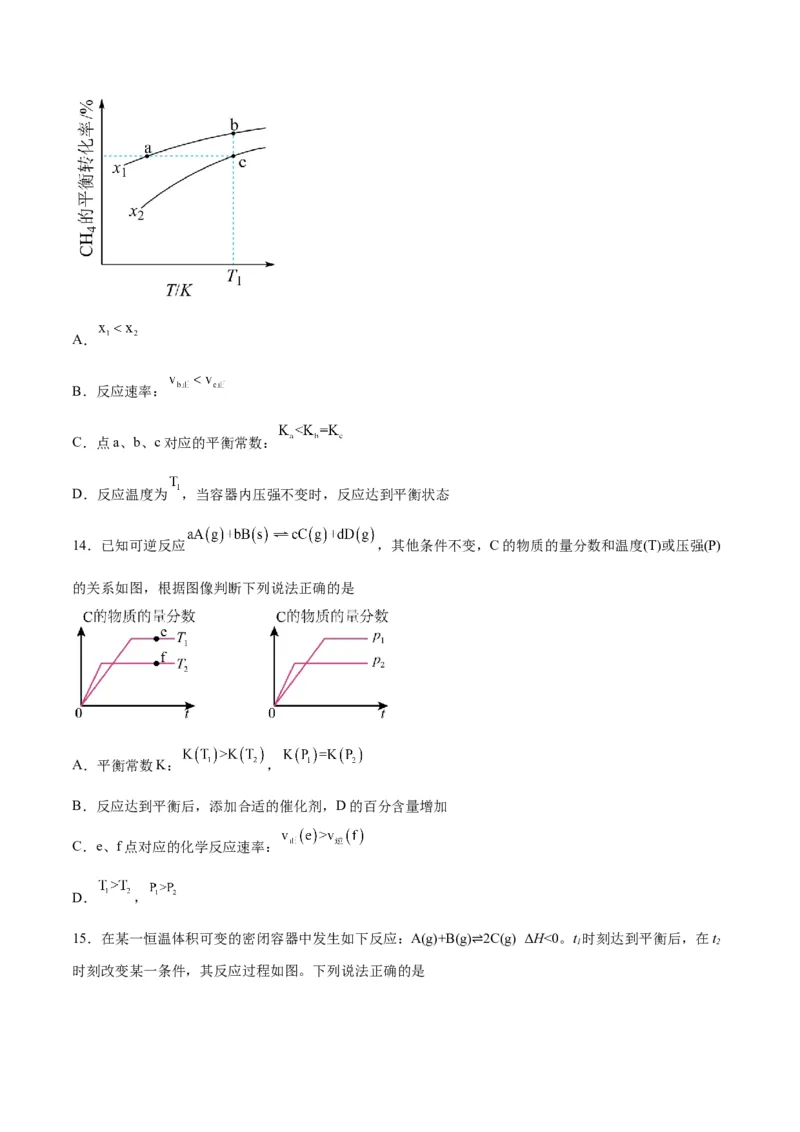
13.向一恒容密闭容器中加入 和一定量的 ,发生反应:
。 的平衡转化率按不同投料比 随温度的变化曲线如图所示。下列说法错误的是A.
B.反应速率:
C.点a、b、c对应的平衡常数:
D.反应温度为 ,当容器内压强不变时,反应达到平衡状态
14.已知可逆反应 ,其他条件不变,C的物质的量分数和温度(T)或压强(P)
的关系如图,根据图像判断下列说法正确的是
A.平衡常数K: ,
B.反应达到平衡后,添加合适的催化剂,D的百分含量增加
C.e、f点对应的化学反应速率:
D. ,
15.在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g) 2C(g) ΔH<0。t 时刻达到平衡后,在t
1 2
时刻改变某一条件,其反应过程如图。下列说法正确的是 ⇌A.0~t 时,v >v
2 正 逆
B.t 时刻改变的条件可以是向密闭容器中加C
2
C.Ⅰ、Ⅱ两过程达到平衡时,A的体积分数Ⅰ>Ⅱ
D.Ⅰ、Ⅱ两过程达到平衡时,平衡常数I<Ⅱ
16.科学家研究出一种新的催化剂能有效处理汽车尾气,其反应的化学方程式为
,若反应在恒容密闭容器中进行,由该反应相关图像作出的判断正确的是
A.图甲中改变的反应条件为加入等量的NO和CO
B.图乙中纵坐标可代表NO的百分含量
C.图丙中纵坐标可代表CO的百分含量
D.图丁中a、b、c三点均已达到化学平衡状态
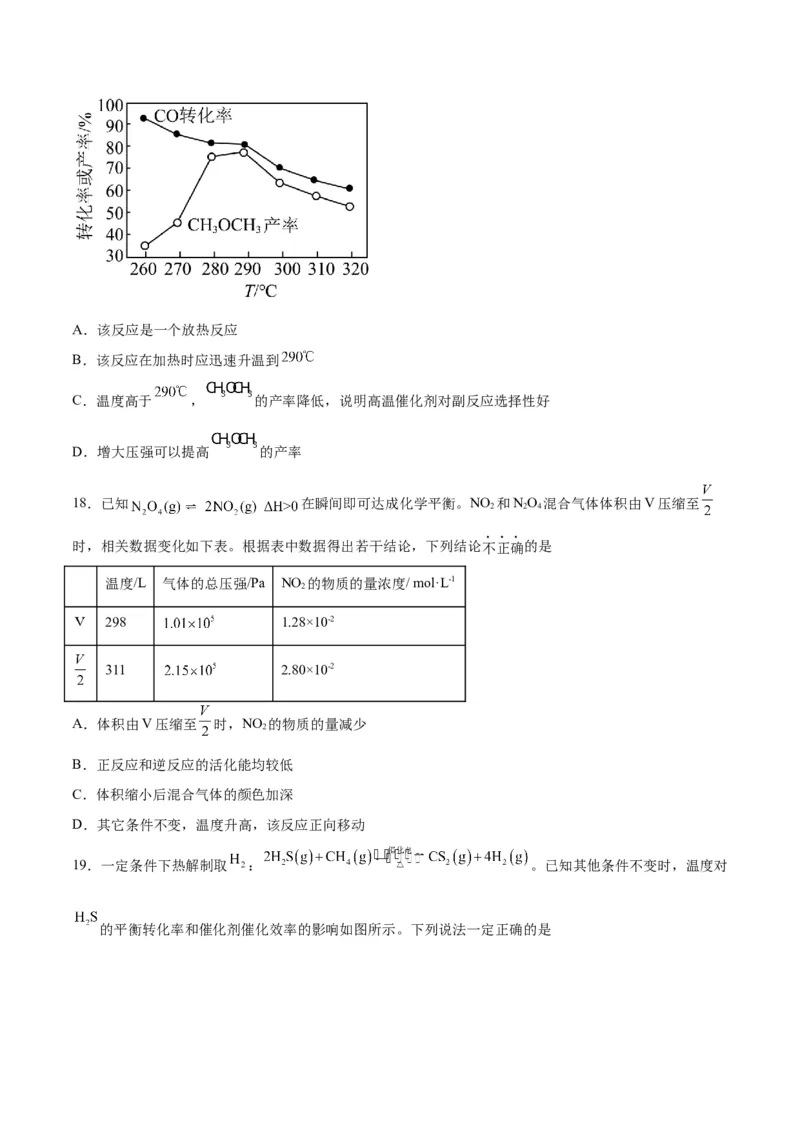
17.在新型的催化剂(主要成分是 的合金)、压强为 的条件下,利用 和 制备二甲醚(
),反应为 ,实验测得CO的平衡转化率和二甲醚的产
率随温度的变化曲线如图所示,下列有关说法错误的是A.该反应是一个放热反应
B.该反应在加热时应迅速升温到
C.温度高于 , 的产率降低,说明高温催化剂对副反应选择性好
D.增大压强可以提高 的产率
18.已知 在瞬间即可达成化学平衡。NO 和NO 混合气体体积由V压缩至
2 2 4
时,相关数据变化如下表。根据表中数据得出若干结论,下列结论不正确的是
温度/L 气体的总压强/Pa NO 的物质的量浓度/ mol·L-1
2
298 1.28×10-2
311 2.80×10-2
A.体积由V压缩至 时,NO 的物质的量减少
2
B.正反应和逆反应的活化能均较低
C.体积缩小后混合气体的颜色加深
D.其它条件不变,温度升高,该反应正向移动
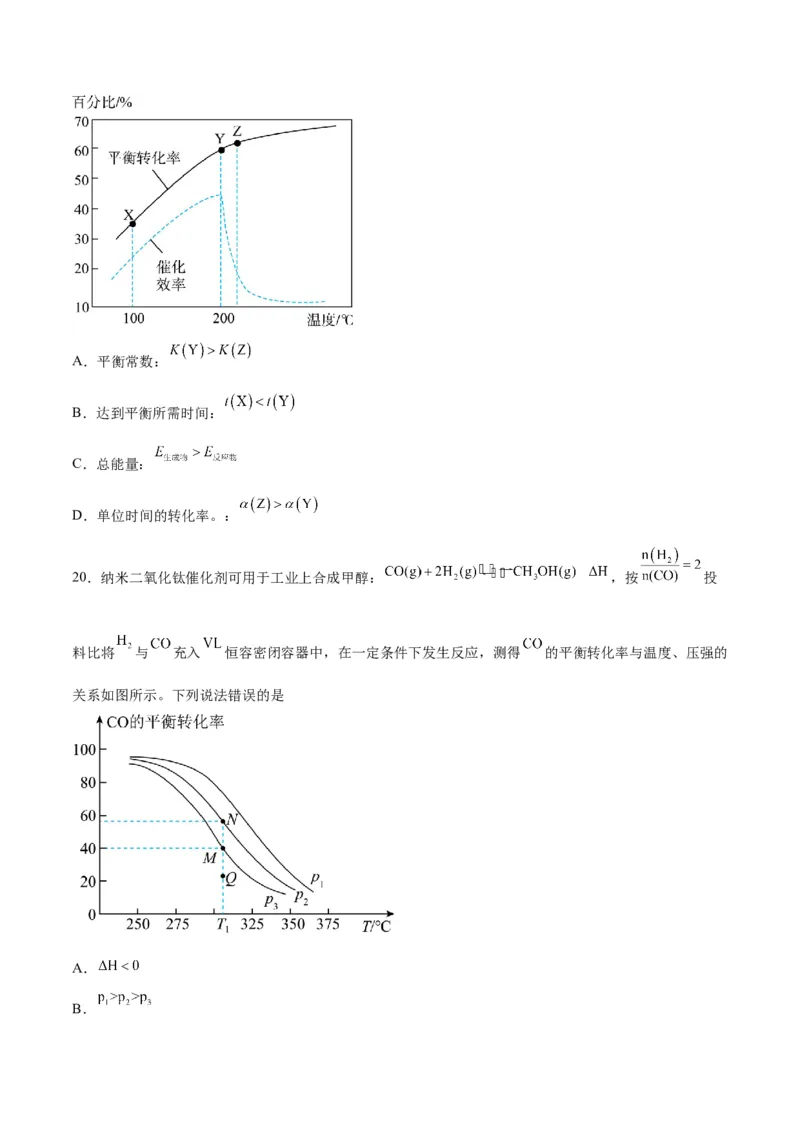
19.一定条件下热解制取 : 。已知其他条件不变时,温度对
的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定正确的是A.平衡常数:
B.达到平衡所需时间:
C.总能量:
D.单位时间的转化率。:
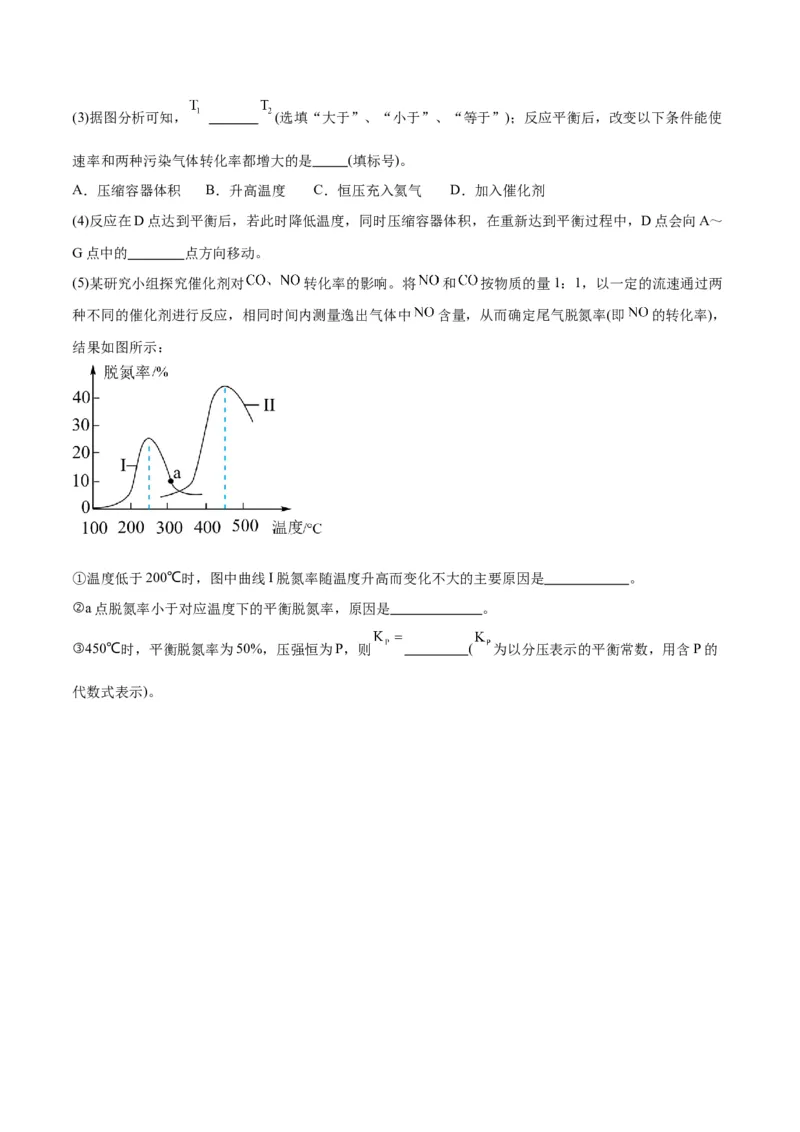
20.纳米二氧化钛催化剂可用于工业上合成甲醇: ,按 投
料比将 与 充入 恒容密闭容器中,在一定条件下发生反应,测得 的平衡转化率与温度、压强的
关系如图所示。下列说法错误的是
A.
B.C.N点 转化率、平衡常数均大于M点
D. 、 压强下,Q点对应的
21.某实验小组探究外界条件对化学反应速率的影响,进行了以下实验。
Ⅰ.探究温度、浓度对硫代硫酸钠与稀硫酸反应速率的影响
(1)写出 与 反应的离子方程式 。
(2)该小组同学设计了如下表所示系列实验:
溶液 稀 溶液
实验序
反应温度/℃
号
V/mL c/(mol/L) V/mL c/(mol/L) V/mL
① 20 10.0 0.10 10.0 0.50 0
② 0.10 0.50
③ 0.10 0.50
实验①和②探究温度对该反应速率的影响,则实验②中, (填“20℃”或“60℃”)、
mL。
实验①和③探究 浓度对该反应速率的影响,则实验③中,若 ,则 mL、
mL。
Ⅱ.探究催化剂对 分解速率的影响
(3)按下图进行定量实验研究。挤压注射器使 溶液全部加入试管中,记录数据;用 溶液代替
溶液进行平行实验,比较催化剂对反应速率的影响。该实验需测定的实验数据是 。(4)用上图中的装置,探究 催化 分解的最佳条件。此时注射器中应加入的试剂是 。挤压
注射器使液体全部加入试管中开始至不再有气体产生,记录反应时间。反应物用量和反应时间如下表:
0.1g 0.3g 0.8g
10mL1.5% 223s 67s 56s
10mL3.0% 308s 109s 98s
10mL4.5% 395s 149s 116s
分析表中数据,从实验效果和“绿色化学”的角度考虑, 的浓度一定时,加入 g的 为
较佳选择。
22.将CO 转化为更有价值的化工原料,正成为科学家们研究的一个重要领域。回答下列问题:
2
(1)已知:①2H(g)+O(g) 2HO(g) ΔH= − 484 kJ∙mol−1
2 2 2
②2CH OH(g)+ 3O(g) 2CO(g)+4HO(g) ΔH =−1353 kJ∙mol−1
3 2 2 2
则CO(g)+ 3H(g) CHOH(g)+HO(g) ΔH = kJ∙mol−1.
2 2 3 2
(2)CO 催化加氢制甲醇过程中,存在竞争的副反应主要是: CO(g)+H(g) CO(g)+HO(g) ΔH =+
2 2 2 2
41 kJ∙mol−1.在恒温密闭容器中,CO 的平衡转化率[α(CO )%]和甲醇选择性[(CH OH)%=
2 2 3×100%]随着温度变化关系如下图所示。
①分析温度高于236°C时图中曲线下降的原因 。
②按1 mol CO (g)、3 mol H (g)投料反应,计算 244°C时反应生成CHOH的物质的量为 mol。
2 2 3
(保留两位有效数字)
③在压强为p的反应条件下,1 mol CO (g)和3 mol H (g)反应并达到平衡状态,CO 平衡转化率为20%,甲
2 2 2
醇选择性为50%,该温度下主反应的平衡常数K= 。 (列出计算式即可)
p
23.CS 为无色液体,是一种常见的溶剂,在化工生产中有重要作用,如制造人造丝、杀虫剂、促进剂等。
2
(1)天然气法合成CS 相关反应如下:
2
反应I.CH(g)+2S (g)=CS (g)+2HS(g) ΔH
4 2 2 2 1
反应Ⅱ.S(g)=4S (g) ΔH=+411.15kJ·mol-1
8 2 2
反应Ⅲ.2CH(g)+S (g)=2CS (g)+4HS(g) ΔH=+201.73kJ·mol-1。
4 8 2 2 3
则ΔH= ;反应I的活化能E(正) E(逆)(填“>”“<”或“=”)。
1 a a
(2)一定条件下,向一体积为1L的密闭容器中充入S(g)、CH 发生反应I、Ⅱ,CH 与S 反应中CH 的平衡
8 4 4 2 4
转化率、S 分解产生S 的体积分数随温度的变化曲线如图所示。
8 2
①工业上通常采用在600~650℃的条件下进行此反应,而不采用低于600℃的原因是 。
②某温度下若S 完全分解成S,在密闭容器中,以n(S ):n(CH)=2:1开始反应,当CS 体积分数为10%
8 2 2 4 2
时,CH 转化率为 。
4
(3)利用工业废气H
2
S生产CS
2
的反应为CH
4
(g)+2H
2
S(g)⇌CS
2
(g)+4H
2
(g)。向某密闭容器充入1molCH
4
、
2molH S,维持体系压强为pkPa,反应达到平衡时,四种组分的物质的量分数随温度T的变化如图。
2 0①图中表示CH 的曲线是 (填“a”“b”“c”或“d”)。
4
②780℃时,该反应的K= (列出表达式即可,用平衡分压代替平衡浓度,分压=总压×物质的量
p
分数)。
③维持m点温度不变,向容器中再通入CH、HS、CS、H 各1mol,此时速率关系为v(正)
4 2 2 2
v(逆)(填“>”“<”或“=”)。
24.汽车尾气的污染不容忽视,对汽车尾气中污染气体NO和CO的转化是研究热点。
I.汽车尾气中的 对人体健康有严重危害,一种新技术用 还原 的反应原理为:
。该反应的能量变化过程如图:
(1)△H= (用图中字母a、b、c、d表示) 。
Ⅱ.已知反应: 可以有效转化汽车尾气。在密
闭容器中充入2molCO和2molNO,平衡时NO的体积分数与温度、压强的关系如图所示:
(2)充分反应达到平衡后,放出的热量Q (选填“大于”、“小于”、“等于”)(3)据图分析可知, (选填“大于”、“小于”、“等于”);反应平衡后,改变以下条件能使
速率和两种污染气体转化率都增大的是 (填标号)。
A.压缩容器体积 B.升高温度 C.恒压充入氦气 D.加入催化剂
(4)反应在D点达到平衡后,若此时降低温度,同时压缩容器体积,在重新达到平衡过程中,D点会向A~
G点中的 点方向移动。
(5)某研究小组探究催化剂对 转化率的影响。将 和 按物质的量1:1,以一定的流速通过两
种不同的催化剂进行反应,相同时间内测量逸出气体中 含量,从而确定尾气脱氮率(即 的转化率),
结果如图所示:
①温度低于200℃时,图中曲线I脱氮率随温度升高而变化不大的主要原因是 。
②a点脱氮率小于对应温度下的平衡脱氮率,原因是 。
③450℃时,平衡脱氮率为50%,压强恒为P,则 ( 为以分压表示的平衡常数,用含P的
代数式表示)。