文档内容
晶体结构的分析应用
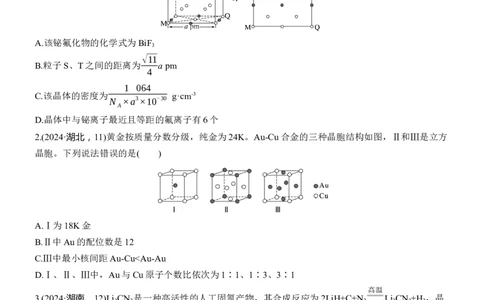
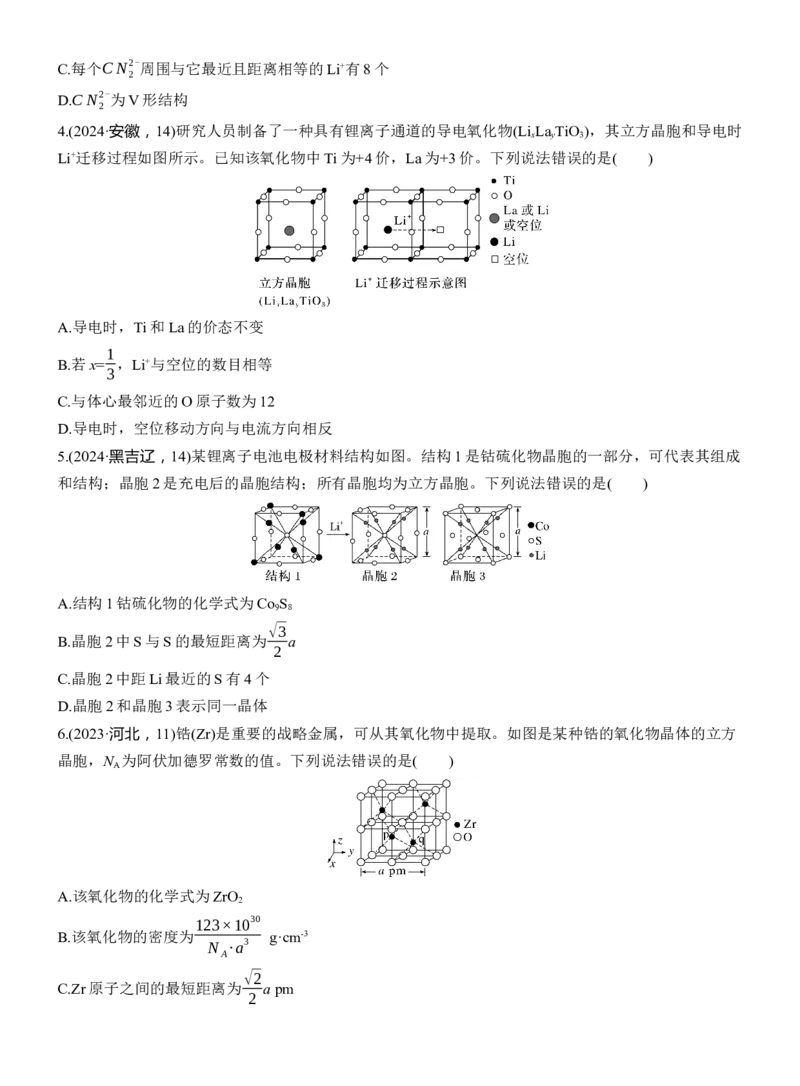
1.(2024·河北,12)金属铋及其化合物广泛应用于电子设备、医药等领域。如图是铋的一种氟化物的立方
晶胞及晶胞中M、N、P、Q点的截面图,晶胞的边长为a pm,N 为阿伏加德罗常数的值。下列说法错
A
误的是( )
A.该铋氟化物的化学式为BiF
3
√11
B.粒子S、T之间的距离为 a pm
4
1 064
C.该晶体的密度为 g·cm-3
N ×a3×10-30
A
D.晶体中与铋离子最近且等距的氟离子有6个
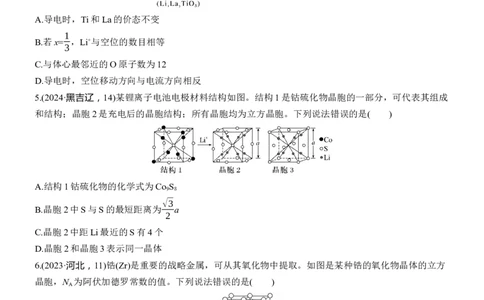
2.(2024·湖北,11)黄金按质量分数分级,纯金为24K。Au-Cu合金的三种晶胞结构如图,Ⅱ和Ⅲ是立方
晶胞。下列说法错误的是( )
A.Ⅰ为18K金
B.Ⅱ中Au的配位数是12
C.Ⅲ中最小核间距Au-CuLaH
2 x
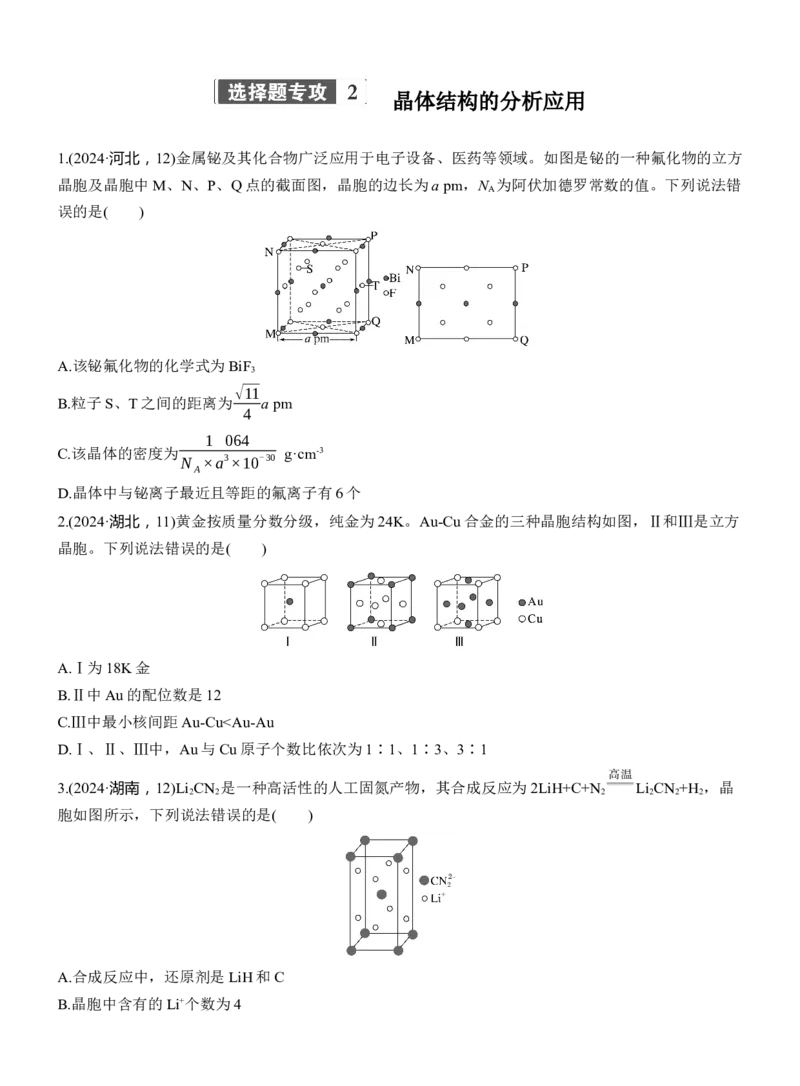
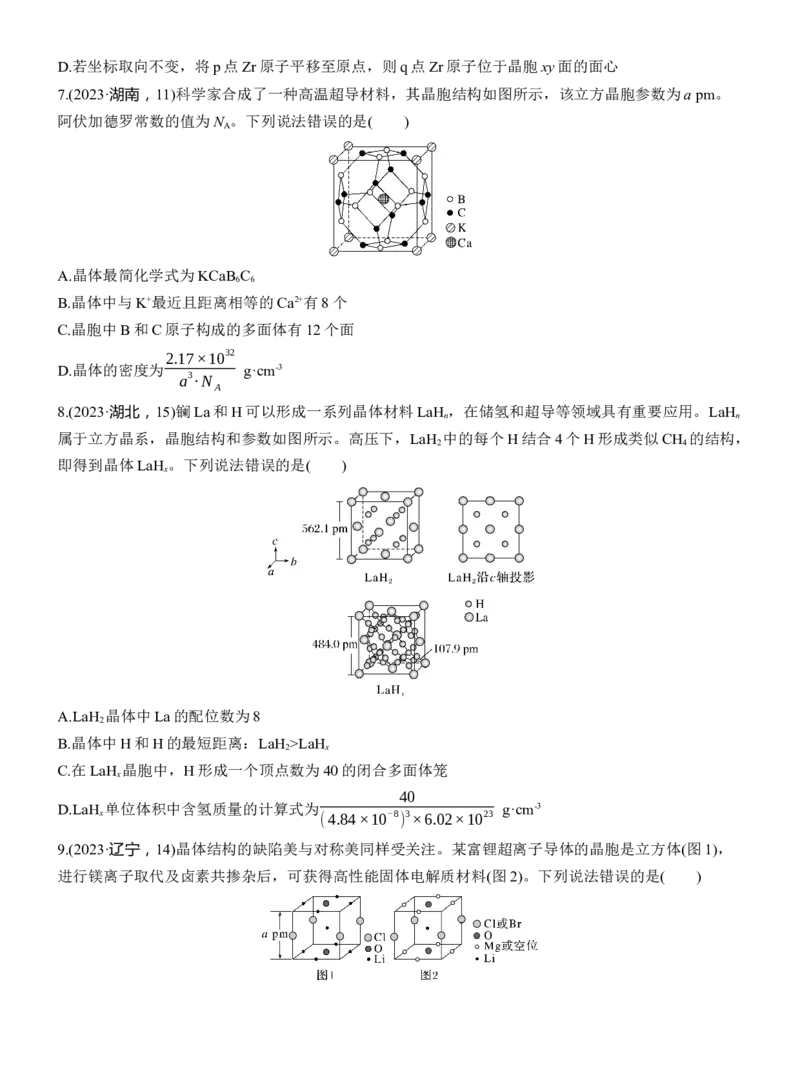
C.在LaH 晶胞中,H形成一个顶点数为40的闭合多面体笼
x
40
D.LaH 单位体积中含氢质量的计算式为 g·cm-3
x (4.84×10-8
)
3×6.02×1023
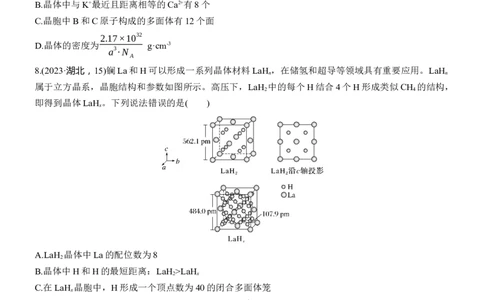
9.(2023·辽宁,14)晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方体(图1),
进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是( )72.5
A.图1晶体密度为 g∙cm-3
N ×a3×10-30
A
B.图1中O原子的配位数为6
C.图2表示的化学式为LiMg OClBr
2 x 1-x
D.Mg2+取代产生的空位有利于Li+传导答案精析
1.D [根据题给立方晶胞及晶胞中M、N、P、Q点的截面图可知,若将晶胞均分为8个小立方体,晶胞体
1
内的8个F-位于8个小立方体的体心,由均摊法可知,每个晶胞中含有铋离子个数为1+12× =4个,含有
4
1 1
氟离子个数为8+8× +6× =12个,故该铋氟化物的化学式为BiF ,A正确;以M点为原点建立坐标系,
8 2 3
令N点的原子分数坐标为(0,0,1),Q点的原子分数坐标为(1,1,0),则T点的原子分数坐标为
( 1 1) (1 1 3)
1, , ,S点的原子分数坐标为 , , ,所以粒子S、T之间的距离为
2 2 4 4 4
√ ( 1- 1) 2 + (1 - 1) 2 + (1 - 3) 2 ×a pm= √11 a pm,B正确;由A项分析可知,每个晶胞中有4个Bi3+ 、12个
4 2 4 2 4 4
m 4×(209+19×3)
F-,晶胞体积为a3×10-30 cm3,则晶体密度为ρ= = g·cm-3,C正确;以晶胞体心处Bi3+为
V N ×a3×10-30
A
分析对象,距离Bi3+最近且等距的F-位于8个小立方体的体心,即有8个F-,D错误。]
18
2.C [24K金的质量分数为100%,则18K金的质量分数为 ×100%=75%,Ⅰ中Au和Cu原子个数比值为
24
197
1∶1,则Au的质量分数为 ×100%≈75%,A正确;Ⅱ中Au处于立方体的八个顶角,则Au的配位
197+64
√2 √2
数为12,B正确;设Ⅲ的晶胞参数为a,Au-Cu的核间距为 a,Au-Au的最小核间距也为 a,最小核
2 2
间距Au-Cu=Au-Au,C错误;Ⅰ中,Au处于内部,Cu处于晶胞的八个顶角,其原子个数比为1∶1,Ⅱ中,
( 1) ( 1)
Au处于立方体的八个顶角,Cu处于面心,其原子个数比为 8× ∶ 6× =1∶3,Ⅲ中,Au处于立方
8 2
( 1) ( 1)
体的面心,Cu处于顶角,其原子个数比为 6× ∶ 8× =3∶1,D正确。]
2 8
3.D [反应2LiH+C+N Li CN +H 中,LiH中H元素由-1价升高到0价,C元素由0价升高到+4价,N
2 2 2 2
1
元素由0价降低到-3价,还原剂是LiH和C,A正确;Li+位于晶胞中的面上,晶胞中含有的Li+个数为8×
2
=4,B正确;以位于体心的CN2- 为标准,与它最近且距离相等的Li+有8个,C正确;CN2-
的中心原子C
2 2
1
原子的价层电子对数为2+
×(4+2-3×2)=2,C原子为sp杂化,或CN2-
与CO
互为等电子体,可知CN2-
为
2 2 2 2
直线形分子,D错误。]
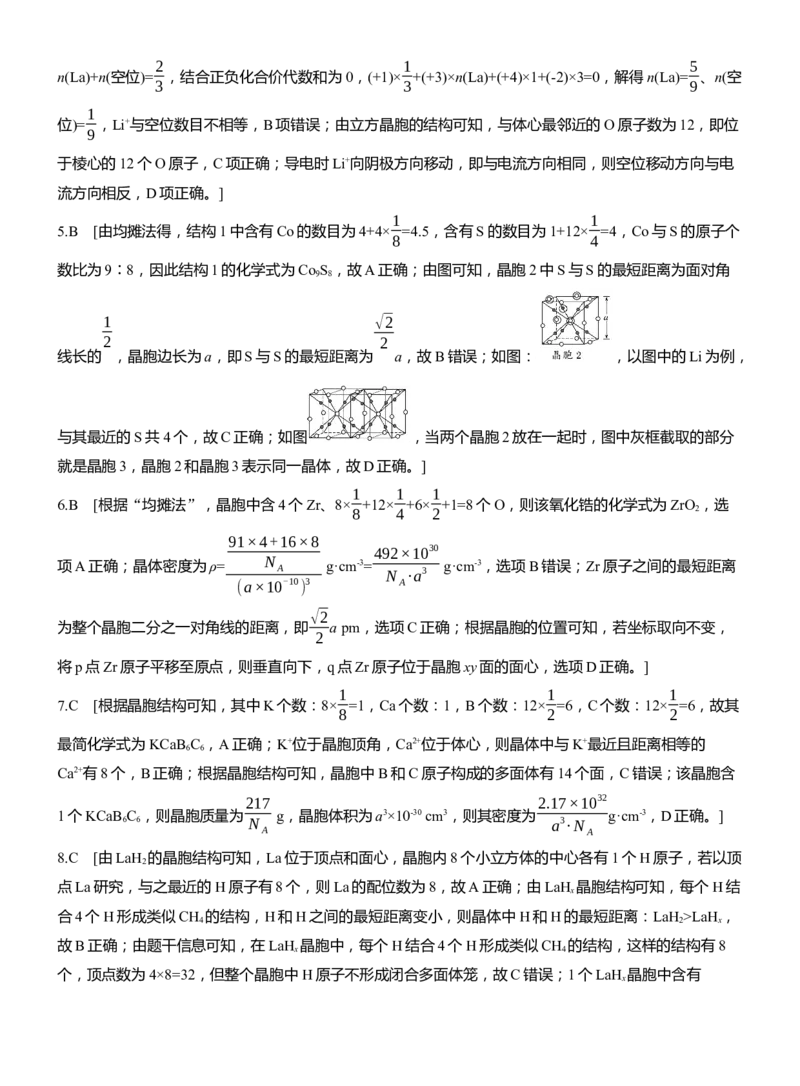
4.B [根据题意,导电时Li+发生迁移,化合价不变,则Ti和La的价态不变,A项正确;根据“均摊法”,
1 1 1 2
1个晶胞中含Ti:8× =1个,含O:12× =3个,含La或Li或空位共1个,若x= ,则La和空位共 ,
8 4 3 32 1 5
n(La)+n(空位)= ,结合正负化合价代数和为0,(+1)× +(+3)×n(La)+(+4)×1+(-2)×3=0,解得n(La)= 、n(空
3 3 9
1
位)= ,Li+与空位数目不相等,B项错误;由立方晶胞的结构可知,与体心最邻近的O原子数为12,即位
9
于棱心的12个O原子,C项正确;导电时Li+向阴极方向移动,即与电流方向相同,则空位移动方向与电
流方向相反,D项正确。]
1 1
5.B [由均摊法得,结构1中含有Co的数目为4+4× =4.5,含有S的数目为1+12× =4,Co与S的原子个
8 4
数比为9∶8,因此结构1的化学式为Co S ,故A正确;由图可知,晶胞2中S与S的最短距离为面对角
9 8
1 √2
2 2
线长的 ,晶胞边长为a,即S与S的最短距离为 a,故B错误;如图: ,以图中的Li为例,
与其最近的S共4个,故C正确;如图 ,当两个晶胞2放在一起时,图中灰框截取的部分
就是晶胞3,晶胞2和晶胞3表示同一晶体,故D正确。]
1 1 1
6.B [根据“均摊法”,晶胞中含4个Zr、8× +12× +6× +1=8个O,则该氧化锆的化学式为ZrO ,选
8 4 2 2
91×4+16×8
492×1030
项A正确;晶体密度为ρ= N
A
g·cm-3=
N ·a3
g·cm-3,选项B错误;Zr原子之间的最短距离
(a×10-10 ) 3 A
√2
为整个晶胞二分之一对角线的距离,即 a pm,选项C正确;根据晶胞的位置可知,若坐标取向不变,
2
将p点Zr原子平移至原点,则垂直向下,q点Zr原子位于晶胞xy面的面心,选项D正确。]
1 1 1
7.C [根据晶胞结构可知,其中K个数:8× =1,Ca个数:1,B个数:12× =6,C个数:12× =6,故其
8 2 2
最简化学式为KCaB C ,A正确;K+位于晶胞顶角,Ca2+位于体心,则晶体中与K+最近且距离相等的
6 6
Ca2+有8个,B正确;根据晶胞结构可知,晶胞中B和C原子构成的多面体有14个面,C错误;该晶胞含
217 2.17×1032
1个KCaB C ,则晶胞质量为 g,晶胞体积为a3×10-30 cm3,则其密度为 g·cm-3,D正确。]
6 6 N a3·N
A A
8.C [由LaH 的晶胞结构可知,La位于顶点和面心,晶胞内8个小立方体的中心各有1个H原子,若以顶
2
点La研究,与之最近的H原子有8个,则La的配位数为8,故A正确;由LaH 晶胞结构可知,每个H结
x
合4个H形成类似CH 的结构,H和H之间的最短距离变小,则晶体中H和H的最短距离:LaH >LaH,
4 2 x
故B正确;由题干信息可知,在LaH 晶胞中,每个H结合4个H形成类似CH 的结构,这样的结构有8
x 4
个,顶点数为4×8=32,但整个晶胞中H原子不形成闭合多面体笼,故C错误;1个LaH 晶胞中含有
x40
5×8=40个H原子,含H质量为 g,晶胞的体积为(484.0×10-10cm)3=(4.84×10-8)3 cm3,则LaH 单位体积中
N x
A
40
含氢质量的计算式为 g·cm-3,故D正确。]
(4.84×10-8
)
3×6.02×1023
1 1 1
9.C [根据均摊法,图1的晶胞中含Li:8× +1=3,O:2× =1,Cl:4× =1,1个晶胞的质量为
4 2 4
3×7+16+35.5 72.5 72.5
g= g,晶胞的体积为(a×10-10cm)3=a3×10-30 cm3,则晶体的密度为
N N N ×a3×10-30
A A A
g·cm-3,A项正确;图1晶胞中,O位于面心,与O等距离最近的Li有6个,O原子的配位数为6,B项正
1 1 1
确;根据均摊法,图2中Li:1,Mg或空位为8× =2,O:2× =1,Cl或Br:4× =1,Mg的个数小于
4 2 4
2,根据正、负化合价的代数和为0,图2的化学式为LiMgOClBr ,C项错误;进行镁离子取代及卤素共
x 1-x
掺杂后,可获得高性能固体电解质材料,说明Mg2+取代产生的空位有利于Li+的传导,D项正确。]