文档内容
晶体结构的分析应用
(选择题1~10题,每小题5分,共50分)
1.(2024·广西模拟)CaTiO 是某些太阳能薄膜电池的材料。如图所示为CaTiO 的晶胞结构,已知晶胞参数为
3 3
(1 1)
a pm,2号氧原子的分数坐标为 ,0, ,下列说法不正确的是( )
2 2
(1 1 )
A.1号氧原子的分数坐标为 , ,0
2 2
B.晶胞中与Ca等距离且最近的O有4个
C.元素 Ti在元素周期表中处于d区
22
√3
D.Ti和Ca原子间的最短距离为 a pm
2
2.(2024·贵州模拟)新型钙钛矿材料可用于太阳能电池。一种钙钛矿晶体由Sn2+、I-和有机阳离子(CH N H+ )
3 3
构成,其立方晶胞结构如图所示。下列说法错误的是( )
A.晶体的化学式为CH NH SnI
3 3 3
B.基态碘原子的价层电子排布式为5s25p5
C.晶体中Sn2+的配位数是8
D.晶胞中Sn2+和I-构成的是正八面体
3.(2024·武汉汉阳一模)硫代硫酸盐是一类具有应用前景的浸金试剂,浸金时S
O2-
与Au+配位形成[Au
2 3
(S O ) ]3-。硫代硫酸根(S O2- )可看作是SO2-中的1个O原子被S原子取代的产物。MgS O ·6H O的晶胞
2 3 2 2 3 4 2 3 2
形状为长方体,结构如图所示。设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1个[Mg(H O) ]2+中σ键的数目为12
2 6
B.S
O2-的空间结构是四面体形
2 34×244×1036
C.MgS O ·6H O晶体的密度为 g·cm-3
2 3 2 abcN
A
D.与Au+配位时,S O2-的中心S原子可作配位原子
2 3
4.(2024·重庆十八中两江实验学校一模)硒化锌是一种重要的半导体材料,图甲为其晶胞结构,图乙为晶胞
(1 1)
的俯视图。已知a点的坐标(0,0,0),b点的坐标 ,1, 。下列说法正确的是( )
2 2
A.Se2-的配位数为8
B.基态Se核外有34种不同空间运动状态的电子
(3 1 3)
C.晶胞中d点原子分数坐标为 , ,
4 4 4
D.若Se2-换为S2-,则晶胞棱长保持不变
5.(2024·湖北宜荆一模)如图是氮化镓的一种晶体结构,N 表示阿伏加德罗常数的值。下列说法正确的是(
A
)
A.每个N原子周围距离最近且相等的N原子数目为4
B.氮化镓分子式为GaN
(1 1 1) (1 3 3)
C.a、b原子坐标参数依次为(0,0,0)、 , , ,则c原子坐标参数为 , ,
4 4 4 4 4 4
√3 √ 84
D.已知该晶体密度为d g·cm-3,则镓原子和氮原子间最短距离为 × 3 ×1010 pm
4 dN
A
6.(2024·河北邢台一模)FeTiO 常用于制备磁芯、磁盘和传感器等,它的晶胞(如图)为等轴晶系。下列叙述
3
错误的是( )
已知:晶胞参数为a nm,N 为阿伏加德罗常数的值。
A
(1 1 1)
A.Fe2+的分数坐标为 , ,
2 2 2
B.氧离子构成正八面体形√2
C.Fe2+和Ti4+之间的距离为 a pm
2
1.52×1023
D.FeTiO 晶体密度为 g·cm-3
3 N ×a3
A
7.(2024·河南许昌部分学校模拟)实验室制取HF的原理为CaF +H SO (浓) CaSO +2HF↑,氢氟酸可用来
2 2 4 4
刻蚀玻璃,发生反应:SiO +4HF===SiF ↑+2H O。CaF 的立方晶胞如图所示,其晶胞参数为a pm。下列说
2 4 2 2
法错误的是( )
A.氢化物的稳定性:HF>H O
2
B.SiF 、H O、SO2-三者的中心原子价层电子对数相等
4 2 4
312
C.CaF 的晶体密度为 g·cm-3(N 为阿伏加德罗常数的值)
2 a3×10-30N A
A
√6
D.CaF 晶体中F-与Ca2+之间的最近距离为 a pm
2 4
8.(2024·江西吉安一中一模)具有双钙钛矿型氧化物通过掺杂改性可用作固体电解质材料,其晶体的一种完
整结构单元如图所示,但真实的晶体中存在5%的O空位缺陷,下列说法错误的是( )
A.Ni原子与Mn原子的配位数相等
B.不考虑晶体缺陷,该晶体的化学式为La MnNiO
2 3
C.O空位的形成有利于O2-的传导
D.考虑晶体缺陷,该晶体的+3价与+4价La原子个数比为4∶1
9.(2024·湖北襄阳四中一模)镧镍合金是一种储氢材料,其晶胞可认为由两种结构不同的层交替堆积而成,
如图所示。已知该合金的密度为ρ g·cm-3,该合金的晶胞中最多可容纳9个氢原子。设N 为阿伏加德罗常
A
数的值,下列叙述错误的是( )
A.基态Ni原子的价层电子排布式为3d84s2
B.该合金的化学式为LaNi
59ρ
C.假定吸氢后体积不变,则合金中氢的最大密度为 g·cm-3
434
(2 1 ) (2 2 )
D.设A处La的原子坐标为(0,0,0),则晶胞底面上Ni的原子坐标为 , ,0 或 , ,0
3 3 3 3
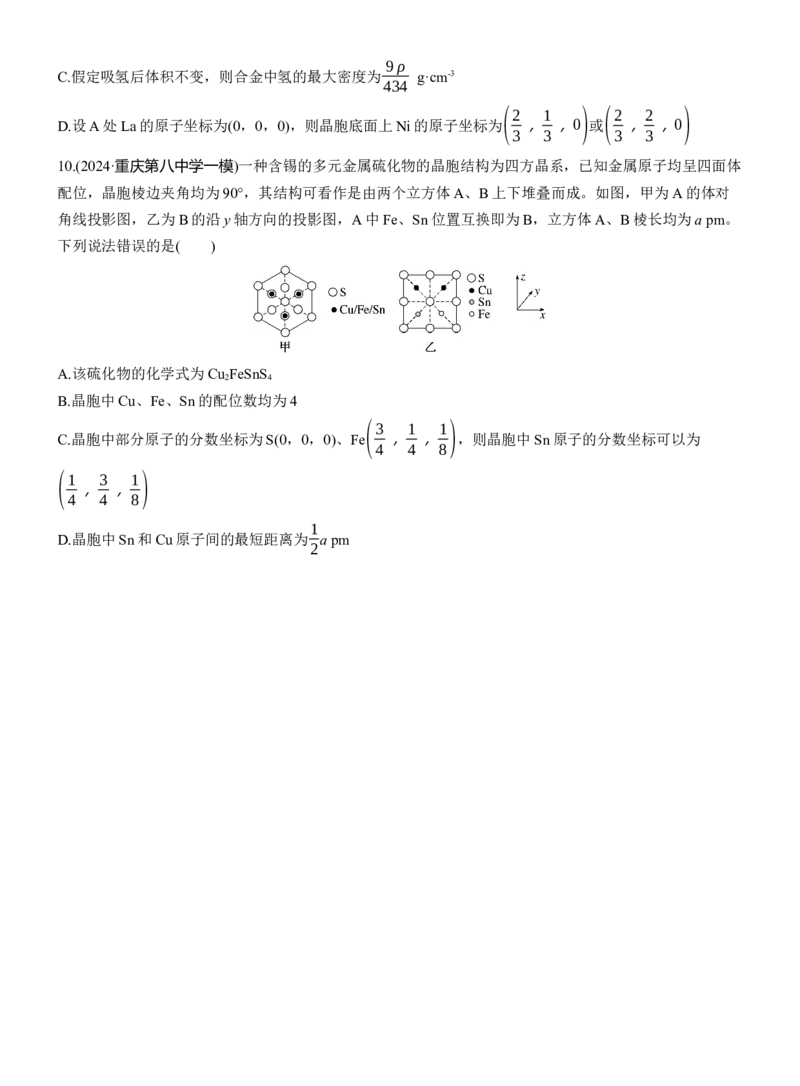
10.(2024·重庆第八中学一模)一种含锡的多元金属硫化物的晶胞结构为四方晶系,已知金属原子均呈四面体
配位,晶胞棱边夹角均为90°,其结构可看作是由两个立方体A、B上下堆叠而成。如图,甲为A的体对
角线投影图,乙为B的沿y轴方向的投影图,A中Fe、Sn位置互换即为B,立方体A、B棱长均为a pm。
下列说法错误的是( )
A.该硫化物的化学式为Cu FeSnS
2 4
B.晶胞中Cu、Fe、Sn的配位数均为4
(3 1 1)
C.晶胞中部分原子的分数坐标为S(0,0,0)、Fe , , ,则晶胞中Sn原子的分数坐标可以为
4 4 8
(1 3 1)
, ,
4 4 8
1
D.晶胞中Sn和Cu原子间的最短距离为 a pm
2答案精析
8×3
1.B [以顶角的钙原子分析,该晶胞中与Ca等距离且最近的O有 =12个,故B错误;根据晶胞结构
2
√3
可知,钙原子和钛原子之间的最短距离为体对角线长的一半,即 a pm,故D正确。]
2
1 1
2.C [由晶胞示意图可知,一个晶胞中含有CH N H+ 的个数为8× =1,I-的个数为6× =3,Sn2+的个数为
3 3 8 2
1,故该晶体的化学式为CH NH SnI ,A正确;已知I是第五周期第ⅦA族元素,故基态碘原子的价层电
3 3 3
子排布式为5s25p5,B正确;晶体中Sn2+的配位数即离Sn2+最近且距离相等的I-的数目,配位数是6,C错
误;晶胞中Sn2+和周围最近的6个I-构成的是正八面体,D正确。]
2+
3.B [1个H O中含2个σ键,每个H O与Mg2+形成1个配位键,所以1个[Mg(H O) ] 中形成σ键的数
2 2 2 6
目为6+2×6=18,故A错误;S
O2- 可看作是SO2-
中的1个O原子被S原子取代的产物,二者结构相似,
2 3 4
6+2-4×2
SO2-
的中心原子S的价层电子对数为4+
=4,即SO2-
的空间结构为正四面体形,所以S
O2-
的
4 2 4 2 3
1 1 1
2+
空间结构为四面体形,故B正确;1个MgS O ·6H O晶胞中,[Mg(H O) ] 的个数为8× +4× +2×
2 3 2 2 6 8 4 2
4×244×1030
+1=4,S
O2-
的个数为4,晶胞体积为abc×10-30 cm3,则晶胞密度为 g·cm-3,故C错误;S
O2-
2 3 abcN 2 3
A
的中心S原子的价层电子对数为4,不含孤电子对,即不能作配位原子,故D错误。]
4.C [由晶胞结构可知,Se2-周围距离最近且相等的Zn2+有4个,配位数为4,故A错误;Se的电子排布式:
1s22s22p63s23p63d104s24p4,核外含有电子的轨道有1+1+3+1+3+5+1+3=18个,则基态Se核外有18种不同空
间运动状态的电子,故B错误;Se2-和S2-半径不同,若Se2-换为S2-,则晶胞棱长将改变,D错误。]
5.C [每个N原子周围距离最近且相等的N原子数目为12,A项错误;氮化镓为共价晶体,没有分子,每
1 1
个晶胞中Ga的个数为8× +6× =4,N的个数为4,则其化学式为GaN,B项错误;根据a、b原子坐标参
8 2
(1 1 1) (1 3 3)
数依次为(0,0,0)、 , , ,判断c原子坐标参数为 , , ,C项正确;由B项分析知,
4 4 4 4 4 4
√4×84
每个晶胞中含有4个GaN,则晶胞的边长为 3 ×1010pm,则镓原子和氮原子间最短距离为体对角线长
dN
A
1 √3 √4×84
的 ,为 × 3 ×1010 pm,D项错误。]
4 4 dN
A
6.C [根据图中已知的两个Ti原子的坐标(0,0,0)和(1,1,1),Fe2+在体心位置,分数坐标为
(1 1 1) 1 √3
, , ,故A正确;Fe2+和Ti4+之间的距离为体对角线长的 ,即为 a nm,故C错误;晶胞中含
2 2 2 2 2152 g 1.52×1023
一个FeTiO ,晶胞的体积为(a×10-7 ) 3 cm3,则FeTiO 晶体的密度为 =
3 3 N (a×10-7 ) 3cm3 N ×a3
A A
g·cm-3,故D正确。]
7.D [非金属性:F>O,则氢化物的稳定性:HF>H O,故A正确;SiF 、H
O和SO2-
的中心原子的价层电
2 4 2 4
子对数均为4,故B正确;由氟化钙晶胞可知每个晶胞中含有4个Ca2+、8个F-,由晶胞结构可知其密度为
312 1 √3
a3×10-30N g·cm-3故C正确;F-与Ca2+之间的最近距离为立方晶胞体对角线长的 4 ,即为 4 a pm,故D
A
错误。]
8.B [Ni与Mn原子均位于顶角,且个数相同,因此配位数也相同,A正确;La个数为1,Ni与Mn的个
1 1
数均为4× =0.5,O的个数为6× =3,晶体的化学式为La NiMnO ,B错误;O空位的形成有利于O2-的传
8 2 2 6
导,因为空位处动能大,离子移动快,C正确;晶体化学式为La NiMnO ,考虑缺陷则是La NiMnO ,设
2 6 2 5.7
+3价La为x个,+4价La为y个,则x+y=2,3x+4y+5=5.7×2=11.4,解得x=1.6,y=0.4,+3价与+4价La原
子个数比为4∶1,D正确。]
9.D [Ni元素的原子序数为28,基态原子的价层电子排布式为3d84s2,A正确;该晶胞中La原子的个数为
1 1 1
4× +4× =1,Ni原子的个数为8× +1=5,则La、Ni原子的个数之比为1∶5,化学式为LaNi ,B正确;
6 12 2 5
434
设晶胞体积为V cm3,该晶胞的密度为ρ= ,假定吸氢后体积不变,当晶胞中最多容纳9个氢原子时合
V N
A
9 9ρ
金中氢的密度最大,氢的密度为 g·cm-3= g·cm-3,C正确;晶胞底面为两个正三角形组成的菱形,
V·N 434
A
(1 2 ) (2 1 )
Ni原子处于两个正三角形的中心,则晶胞底面上Ni的原子坐标为 , ,0 或 , ,0 ,D错
3 3 3 3
误。]
10.D [根据题意分析该晶胞是一个面心立方晶胞,S原子位于晶胞(立方体A、B)的顶角和面心,Cu、
Fe、Sn分别位于体对角线上,因此用均摊法算出各原子个数:S:8,Cu:4,Fe:2,Sn:2,因此该硫化
物的化学式为Cu FeSnS ,A正确;晶胞中距离Sn和Cu最近且相等的S都是4个,晶胞中Cu、Fe、Sn的
2 4
√2
配位数均为4,B正确;晶胞中Sn和Cu原子间的最短距离为立方体面对角线长的一半,为 a pm,D错
2
误。]