文档内容
平谷区 2019-2020 学年度第二学期质量监控试卷
高一化学 2020.6
1.本试卷共8页,包括两部分,34道小题,满分100分。考试时间90分钟。
注 2.在答题卡上准确填写学校名称、班级、姓名和考号。
意
3.试题答案一律填涂或书写在答题卡上,在试卷上作答无效。
事
项 4.在答题卡上,选择题用2B铅笔作答,其他试题用黑色字迹签字笔作答。
5.考试结束,请将答题卡交回。
可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 S:32
第一部分选择题(共50分)
在下列各题的四个选项中,只有一个选项符合题意(每小题2分,共50分)。
1.盛装浓硫酸的试剂瓶上,最适合贴的图标是( )
A. B. C. D.
【答案】D
【解析】
【分析】
浓硫酸具有强腐蚀性,属于腐蚀品。
【详解】A.为剧毒品标志,A不符合题意;
B.为易燃液体标志,B不符合题意;
C.为爆炸品标志,C不符合题意;
D.为腐蚀品标志,浓硫酸属于腐蚀品,D符合题意;
答案选D。
2.下列物质中,属于电解质的是( )
A. 金属铜 B. 氯化钾 C. 稀硫酸 D. 乙醇
【答案】B
【解析】
【详解】电解质是在水溶液中或者熔融状态下能够导电的化合物,单质和混合物不属于电解质。A.金属铜是单质不属于电解质,故A不符合;
B.氯化钾溶于水能够电离成钾离子和氯离子,溶液导电,属于电解质,故B符合题意;
C.稀硫酸是混合物不属于电解质,故C不符合;
D.乙醇溶于水不能电离,溶液不导电,乙醇是非电解质,故D不符合;
故选:B。
3.当光束通过下列分散系时,能观察到丁达尔效应的是( )
A. HSO 溶液 B. Fe(OH) 胶体
2 4 3
C. 蔗糖溶液 D. 浓氨水
【答案】B
【解析】
【分析】
当光束通过下列分散系时,能观察到丁达尔效应的是胶体的性质,溶液不能观察到。
【详解】A.HSO 溶液、C.蔗糖溶液、D.浓氨水,这三者都是溶液,不能观察到丁达尔效应,B.
2 4
Fe(OH) 胶体能观察到丁达尔效应,故B正确。
3
答案为B。
4.在周期表中,下列各组元素位于同一主族的是( )
A. H、C B. Mg、Al C. N、P D. Si、S
【答案】C
【解析】
【分析】
根据元素周期表的结构,结合元素在周期表中的位置判断。
【详解】A.H是第ⅠA族而C是第ⅣA族元素,不位于同一主族,A错误;
B.Mg是第ⅡA族而Al是第ⅢA族元素,不位于同一主族,B错误;
C. N、P都是第ⅤA族元素,位于同一主族,C正确;
D. Si是第ⅣA族而S是第ⅥA族元素,不位于同一主族,D错误。
答案选C。
5.下列金属中,通常采用热还原法冶炼的是
A. Na B. Al C. Fe D. Ag
【答案】C
【解析】
【详解】A.Na用电解方法冶炼,A错误;
B.Al用电解方法冶炼,B错误;
C.Fe采用热还原法冶炼,C正确;D.Ag用热分解的方法冶炼,D错误。
答案选C。
6.不能由两种单质直接化合而成的是( )
A. FeCl B. NaS C. CuS D. SO
3 2 2
【答案】C
【解析】
【详解】A.氯气的氧化性强,能将变价金属氧化为最高价,即 Fe与Cl 化合生成FeCl ,故FeCl 能由两种
2 3 3
单质直接化合而成,故A不符合题意;
B.单质钠和硫加热化合生成硫化钠,NaS能由两种单质直接化合而成,故B不符合题意;
2
C. 硫的氧化性弱,将变价金属氧化为较低价,即Cu与S化合生成Cu S,故CuS不能由两种单质直接化合
2
而成,故C符合题意;
D.硫在氧气中燃烧生成的是二氧化硫,S+O SO ,故SO 能由两种单质直接化合而成,故D不符合题
2 2 2
意;
。
答案选C
7.下列物质的电子式书写正确的是( )
A. H:O:H B. C. H+ D.
【答案】B
【解析】
【详解】A.H:O:H还差两对孤对电子,应该为 ,故A错误;
B. ,碳和每个氧共用两对电子,氧还有两对孤对电子,故B正确;
C.HCl是共价化合物,应该共用电子对即 ,故C错误;
D. 还应有一对孤对电子,应该为 ,故D错误。
综上所述,答案为B。
8.2019年是“国际化学元素周期表年”(IYPT2019)。我国华东师范大学80后科学家姜雪峰教授被遴选为
硫元素的代言人。其课题组运用“从无机硫向有机硫”转化的理念,构建起了“3S绿色硫化学”。下列有关S
的说法正确的是( )
A. 位于元素周期表中第三周期第VA族B. 硫元素原子结构示意图:
C. S原子的中子数是32
D. 有机化合物中可能含有硫元素
【答案】D
【解析】
【详解】A. 硫为16号元素,位于元素周期表中第三周期第VIA族,A错误;
B. 硫原子核外16个电子,原子结构示意图为: ,B错误;
C. S原子的质子数是16,质量数是32,中子数是32-16=16,C错误;
D. 有机化合物中如蛋白质中就可能含有硫元素,D正确;
答案选D。
9.下列关于氨气性质的描述中,不正确的是( )
A. 无色、有刺激性气味气体
B. 极易溶于水
C. 相同条件下,密度比空气的大
D. 能与水反应生成碱性物质
【答案】C
【解析】
【详解】A.氨气是无色、有刺激性气味的气体,A正确;
B.在室温下,1体积水能够溶解700体积的氨气,因此氨气极易溶于水,B正确;
C.NH 的相对分子质量是17,比空气平均相对分子质量29小,因此相同条件下,氨气的密度比空气的小,
3
C错误;
D.氨气能与水反应产生NH ·H O,NH ·H O电离产生OH-,使溶液显碱性,因此氨气与水反应生成的
3 2 3 2
NH ·H O是碱性物质,D正确;
3 2
故合理选项是C。
10.SO 可用作红酒的防腐剂。下列关于SO 的叙述不正确的是( )
2 2
A. 能使品红溶液褪色B. 能与氢氧化钠溶液反应
C. 一定条件下,能与氧气反应
D. 可在红酒中大量添加SO
2
【答案】D
【解析】
【详解】A. SO 具有漂白性,能使品红溶液褪色,A正确;
2
B. SO 属于酸性氧化物,能与氢氧化钠溶液反应生成亚硫酸钠和水,B正确;
2
C. SO 具有还原性,一定条件下,能与氧气反应生成SO ,C正确;
2 3
D. 红酒中添加SO ,SO 具有还原性,可以防止红酒被氧化变质;SO 有毒,服用含有大量SO 的红酒能致
2 2 2 2
癌,对身体健康带来危害,D错误;
答案选D。
11.下列物质中的氮元素只能表现还原性的是( )
A. N B. NH C. NO D. HNO
2 3 3
【答案】B
【解析】
【分析】
元素化合价处于最低价态,化合价只能升高,只有还原性;处于最高价态,化合价只能降低,只有氧化性;
处于中间价态,化合价既能升高又能降低,既有氧化性又有还原性。
【详解】A. N 中氮元素的化合价是0价,既能升高又能降低,既有氧化性又有还原性,A不符合题意;
2
B. NH 中氮元素的化合价是-3价,只能升高,只有还原性,B符合题意;
3
C. NO中氮元素的化合价是+2价,既能升高又能降低,既有氧化性又有还原性,C不符合题意;
D. HNO 中氮元素的化合价是+5价,只能降低,只有氧化性,D不符合题意。
3
答案选B。
12.乙烯是一种重要的化工原料。下列物质中,不能通过乙烯的加成反应一步制得的是( )
A. CHCOOH B. CHCHOH C. CHCHCl D. CHBrCHBr
3 3 2 3 2 2 2
【答案】A
【解析】
【详解】A.CHCOOH不能通过乙烯的加成反应得到,A符合题意;
3
B.乙烯与水发生加成反应生成CHCHOH,B不符合题意;
3 2
C.乙烯与氯化氢发生加成反应生成CHCHCl,C不符合题意;
3 2
D.乙烯与溴发生加成反应生成CHBrCHBr,D不符合题意。
2 2
答案选A。
13.下列反应中,属于加成反应的是( )A. 乙醇与钠反应生成乙醇钠
B. 乙烯燃烧生成二氧化碳和水
C. 乙烯与氯化氢反应生成氯乙烷
D. 乙醇与乙酸反应生成乙酸乙酯
【答案】C
【解析】
【分析】
有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应。
【详解】A. 乙醇与钠反应生成乙醇钠,为置换反应,故A不符合题意;
B. 乙烯燃烧生成二氧化碳和水,为氧化反应,故B不符合题意;
C. 乙烯与氯化氢反应生成氯乙烷,为加成反应,故C符合题意;
D. 乙醇与乙酸反应发生酯化反应生成乙酸乙酯,为取代反应,故D不符合题意;
答案选C。
14.下列实验方法不.能.用来鉴别乙醇和乙酸的是
A. 加入蒸馏水 B. 加入碳酸氢钠溶液
C. 滴加紫色石蕊溶液 D. 滴加酸性高锰酸钾溶液
【答案】A
【解析】
【详解】A、乙醇和乙酸与水均是互溶的,水不能鉴别二者,选项A选;
B、碳酸氢钠和乙酸反应放出气体,乙醇和碳酸氢钠不反应,可以鉴别二者,选项B不选;C、乙酸呈酸性,
使紫色石蕊试液显红色,乙醇不能,可以鉴别二者,选项C不选;
D、乙醇能使酸性高锰酸钾溶液褪色,乙酸不能,可以鉴别二者,选项D不选;
答案选A。
15.下列有关糖类、油脂、蛋白质的说法中,不正确的是
A. 灼烧蚕丝织物有烧焦羽毛的气味
B. 蔗糖可以水解生成葡萄糖与果糖
C. 将碘化钾溶液滴在土豆片上,可观察到蓝色
D. 利用油脂在碱性条件下的水解,可以制肥皂
【答案】C
【解析】
【详解】A项、蚕丝的主要成分是蛋白质,灼烧蛋白质有烧焦羽毛气味,故A正确;
B项、蔗糖为二糖,可以发生水解反应生成葡萄糖与果糖,故B正确;
C项、土豆中含有淀粉,碘单质遇淀粉溶液变蓝色,与碘化钾溶液无现象,故C错误;D项、油脂为高级脂肪酸甘油酯,可在碱性条件下水解生成高级脂肪酸钠和甘油,常用于制造肥皂,故D
正确;
故选C。
16.用如右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是( )
A. 上下移动①中铜丝可控制SO 的量
2
B. ②中选用品红溶液验证SO 的生成
2
C. ③中选用NaOH溶液吸收多余的SO
2
D. 为确认CuSO 生成,向①中加水,观察颜色
4
【答案】D
【解析】
【详解】A、当铜丝与浓硫酸接触时才能反应,当往上抽动铜丝时,铜丝与硫酸不接触,反应停止,故可
通过上下移动①中铜丝可控制SO 的量,故A正确;
2
B、SO 具有漂白性,可用品红溶液验证SO 的生成,故B正确;
2 2
C、SO 为酸性气体,具有污染性,可与碱发生反应,用NaOH溶液吸收多余的SO ,故C正确;
2 2
D、铜与浓硫酸反应后①中溶液显蓝色即可证明有CuSO 生成,无需向其中加水,并且将水加入浓硫酸中
4
会使试管中液滴飞溅,发生危险,故D错误。
答案选D。
17.合成氨工业为人类解决粮食问题做出了巨大贡献。一定条件下,在密闭容器中进行合成氨反应:N
2
(g)+3H(g) NH (g),当正、逆反应速率相等且不等于零时,下列说法不正确的是( )
2 3
A. N、H 完全转化为NH B. N、H、NH 在容器中共存
2 2 3 2 2 3
C. 反应已达到化学平衡状态 D. N、H、NH 的浓度不再改变
2 2 3
【答案】A
【解析】
【详解】反应N(g) + 3H(g) 2NH (g),当正、逆反应速率相等且不等于零时,反应处于化学
2 2 3
平衡状态。则
A.可逆反应中,反应物不能完全转化为氨气,A错误;
B.N、H、NH 在容器中共存,B正确;
2 2 3C.正、逆反应速率相等且不等于零时的状态是化学平衡状态,C正确;
D.化学平衡状态时,各组分的浓度不随时间的变化而变化,D正确。
答案选A。
【点晴】掌握化学平衡状态的含义是解答的关键,在一定条件下,当可逆反应的正反应速率和逆反应速率
相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,平衡
状态具有逆、等、动、定、变等特征。
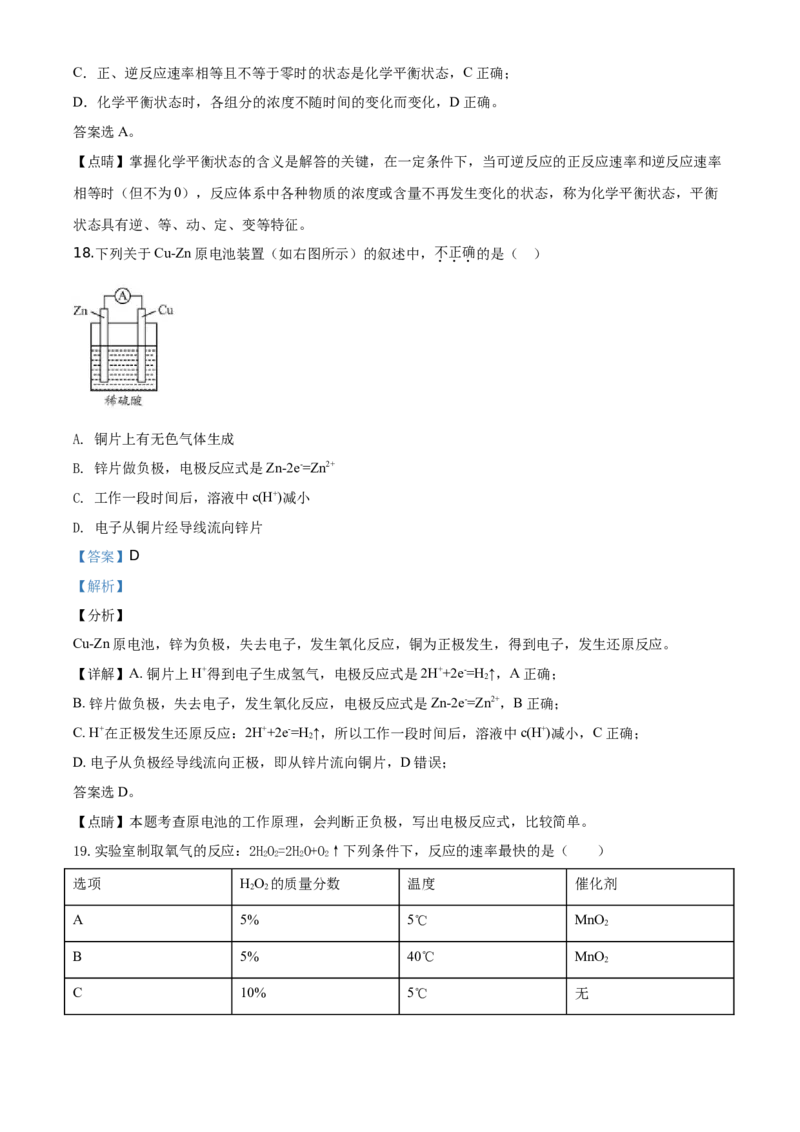
18.下列关于Cu-Zn原电池装置(如右图所示)的叙述中,不正确的是( )
A. 铜片上有无色气体生成
B. 锌片做负极,电极反应式是Zn-2e-=Zn2+
C. 工作一段时间后,溶液中c(H+)减小
D. 电子从铜片经导线流向锌片
【答案】D
【解析】
【分析】
Cu-Zn原电池,锌为负极,失去电子,发生氧化反应,铜为正极发生,得到电子,发生还原反应。
【详解】A. 铜片上H+得到电子生成氢气,电极反应式是2H++2e-=H ↑,A正确;
2
B. 锌片做负极,失去电子,发生氧化反应,电极反应式是Zn-2e-=Zn2+,B正确;
C. H+在正极发生还原反应:2H++2e-=H ↑,所以工作一段时间后,溶液中c(H+)减小,C正确;
2
D. 电子从负极经导线流向正极,即从锌片流向铜片,D错误;
答案选D。
【点睛】本题考查原电池的工作原理,会判断正负极,写出电极反应式,比较简单。
19.实验室制取氧气的反应:2HO=2HO+O↑下列条件下,反应的速率最快的是( )
2 2 2 2
选项 HO 的质量分数 温度 催化剂
2 2
A 5% 5℃ MnO
2
B 5% 40℃ MnO
2
C 10% 5℃ 无D 10% 40℃ MnO
2
A. A B. B C. C D. D
【答案】D
【解析】
【分析】
题中涉及影响反应速率的因素有温度、浓度和催化剂,一般来说,温度越高、浓度越大且加入催化剂,可
增大反应速率,以此解答该题。
【详解】A、C与B、D相比较,B、D反应温度高、加入催化剂,反应速率较大,B、D相比较,D浓度
较大,则D反应速率最大。
答案选D。
【点睛】本题考查化学反应素的影响因素,为高频考点,侧重于学生的分析能力和基本概念、理论知识的
综合理解和运用的考查,注意相关基础知识的积累。
20.在实验室或生产生活中,安全措施是避免伤害和事故的保障。下列安全问题的处理方法中,不符合要
求的是( )
A. 少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
B. 金属钠着火时应立即用沙土盖灭
C. 点燃CH 前,必须检验气体的纯度
4
D. 大量氯气泄漏时,迅速离开现场并尽量往高处去
【答案】A
【解析】
【详解】A.少量浓硫酸沾在皮肤上,应该立即用大量水冲洗,冲洗后再涂上碳酸氢钠溶液,不符合处理
方法,故A符合题意;
B.金属钠着火时应立即用沙土盖灭,不能用泡沫灭火器或水灭火,符合处理方法,故B不符合题意;
C.点燃CH 可燃性气体前,必须检验气体的纯度,符合处理方法,故C不符合题意;
4
D.氯气有毒且密度比空气大,大量氯气泄漏时,迅速离开现场并尽量往高处去,符合处理方法,故D不
符合题意。
综上所述,答案为A。
21.下列物质性质与用途的对应关系不正确的是( )
选项 性质 用途A. 氧化铁呈红棕色 红色涂料
B. 次氯酸钠具有漂白性 漂白剂
C. 浓硫酸具有脱水性 干燥剂
D. 液氨汽化时要吸收大量的热 制冷剂
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.氧化铁为红棕色固体,所以常用作红色涂料,故A正确;
B.次氯酸根具有强氧化性,所以次氯酸钠具有漂白性,可用作漂白剂,故B正确;
C.浓硫酸具有吸水性,所以可以作为干燥剂,与其脱水性无关,故C错误;
D.液氨汽化时要吸收大量的热,使周围环境温度降低,常用作制冷剂,故D正确;
故答案为C。
22.下列实验结论与实验操作及现象不相符的一组是( )
选项 实验操作及现象 实验结论
向某酸雨样品中加入Ba(OH) 溶液,有白色沉
A 2 酸雨试样中一定含SO 2-
淀生成 4
B 向KI-淀粉溶液中滴入氯水,溶液变成蓝色 I-的还原性强于Cl-
将Ba(OH) ·8H O和NH Cl晶体在小烧杯中混 Ba(OH) ·8H O与NH Cl
C 2 2 4 2 2 4
合搅拌,用手触摸烧杯外壁感觉变凉 的反应是吸热反应
向某盐溶液中加入NaOH溶液,加热,用湿润
D 该盐溶液中含有NH +
的红色石蕊试纸放在试管口,试纸变蓝 4
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A.酸雨中可能含有亚硫酸,亚硫酸与氢氧化钡反应会生成亚硫酸钡白色沉淀,A错误;
B.淀粉遇碘单质变蓝色,加入氯水变蓝,说明氯水将 氧化为 ,故 的还原性强于 ,B正确;C.用手触摸烧杯外壁感觉变凉,温度降低,说明该反应是吸热反应,C正确;
D.湿润的红色石蕊试纸变蓝,说明生成了氨气,则原溶液中含有 ,D正确;
故答案选A。
23.下列解释事实的离子方程式中,不正确的是( )
A. 防止FeCl 溶液变质而加入Fe粉:2Fe3++Fe=3Fe2+
2
B. 向铜粉中滴加稀硝酸,产生气体:Cu+4H++2NO =Cu2++2NO↑+2H O
2 2
C. 向CuSO 溶液中滴加NaOH溶液,产生蓝色沉淀:Cu2++2OH-=Cu(OH) ↓
4 2
D. NaO 是重要的供氧剂:2NaO+2H O=4Na++4OH-+O ↑
2 2 2 2 2 2
【答案】B
【解析】
【详解】A.铁粉能把Fe3+还原为Fe2+,防止FeCl 溶液变质而加入Fe粉:2Fe3++Fe=3Fe2+,故A正确;
2
B.向铜粉中滴加稀硝酸生成硝酸铜、一氧化氮、水,反应的离子方程式是3Cu+8H++2NO =3Cu2+
+2NO↑+4HO,故B错误;
2
C.向CuSO 溶液中滴加NaOH溶液生成硫酸钠和氢氧化铜沉淀,反应的离子方程式是Cu2++2OH-
4
=Cu(OH) ↓,故C正确;
2
D.NaO 是重要的供氧剂,能与水反应生成氢氧化钠和氧气,反应的离子方程式是2NaO+2H O=4Na+
2 2 2 2 2
+4OH-+O ↑,故D正确;
2
选B。
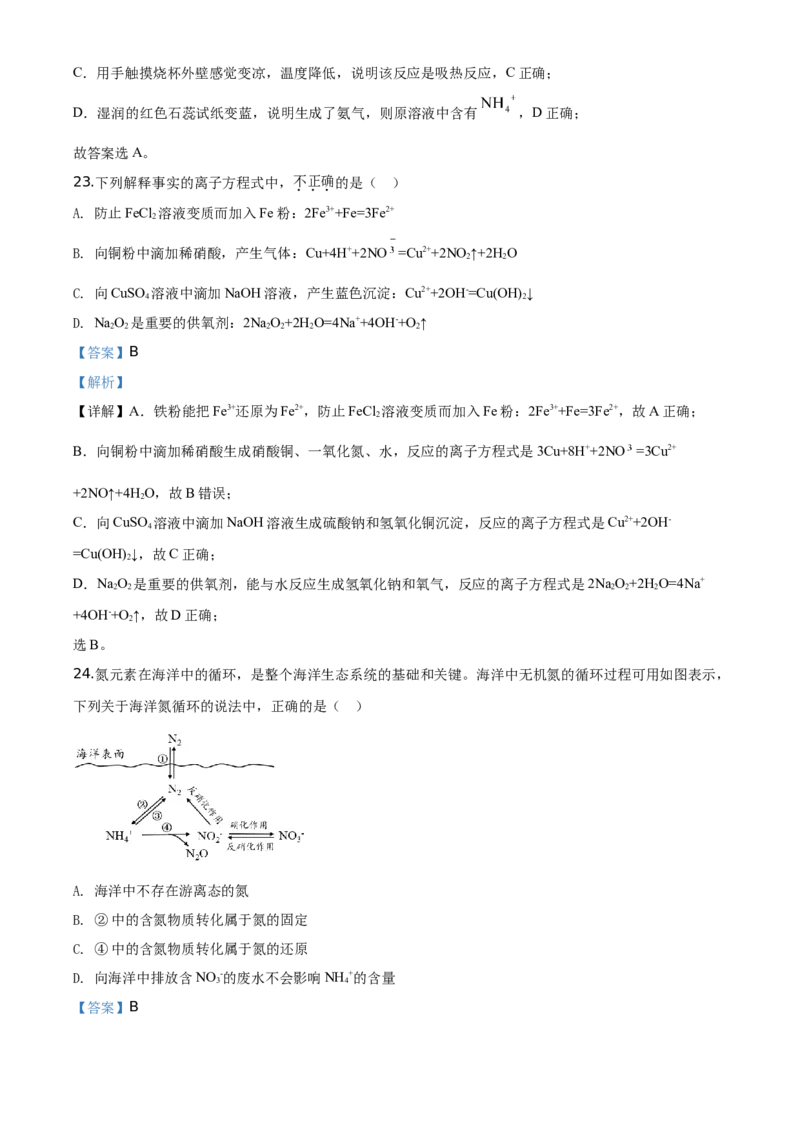
24.氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用如图表示,
下列关于海洋氮循环的说法中,正确的是( )
A. 海洋中不存在游离态的氮
B. ②中的含氮物质转化属于氮的固定
C. ④中的含氮物质转化属于氮的还原
D. 向海洋中排放含NO -的废水不会影响NH +的含量
3 4
【答案】B【解析】
【详解】A.根据图像,海水中存在氮气,A错误;
B. ②中氮气转化为 含氮化合物,属于氮的固定,B正确;
C. ④中 转化为 或 ,化合价升高,属于氮的氧化反应,C错误;
D.根据图像, 能转化为 , 转为氮气,氮气转化为 ,故向海水中排放 会造成
浓度增大,D错误;
故答案选B。
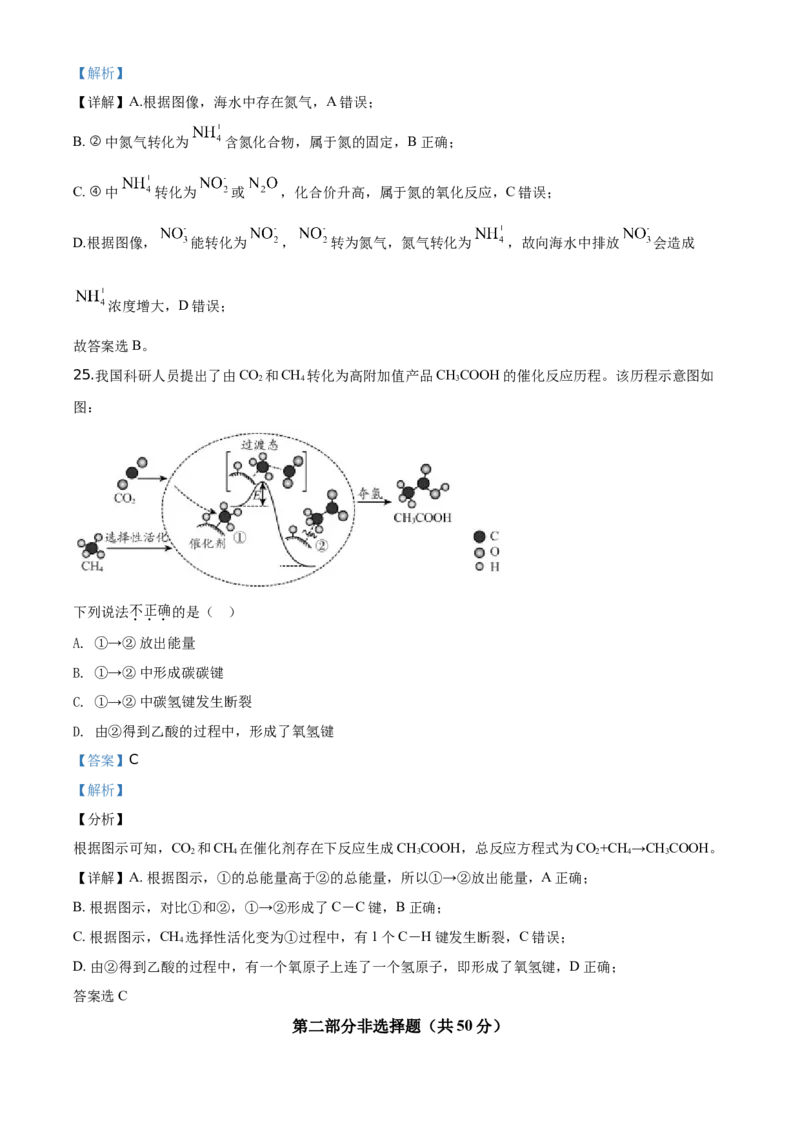
25.我国科研人员提出了由CO 和CH 转化为高附加值产品CHCOOH的催化反应历程。该历程示意图如
2 4 3
图:
下列说法不正确的是( )
A. ①→②放出能量
B. ①→②中形成碳碳键
C. ①→②中碳氢键发生断裂
D. 由②得到乙酸的过程中,形成了氧氢键
【答案】C
【解析】
【分析】
根据图示可知,CO 和CH 在催化剂存在下反应生成CHCOOH,总反应方程式为CO+CH →CHCOOH。
2 4 3 2 4 3
【详解】A. 根据图示,①的总能量高于②的总能量,所以①→②放出能量,A正确;
B. 根据图示,对比①和②,①→②形成了C-C键,B正确;
C. 根据图示,CH 选择性活化变为①过程中,有1个C-H键发生断裂,C错误;
4
D. 由②得到乙酸的过程中,有一个氧原子上连了一个氢原子,即形成了氧氢键,D正确;
。
答案选C
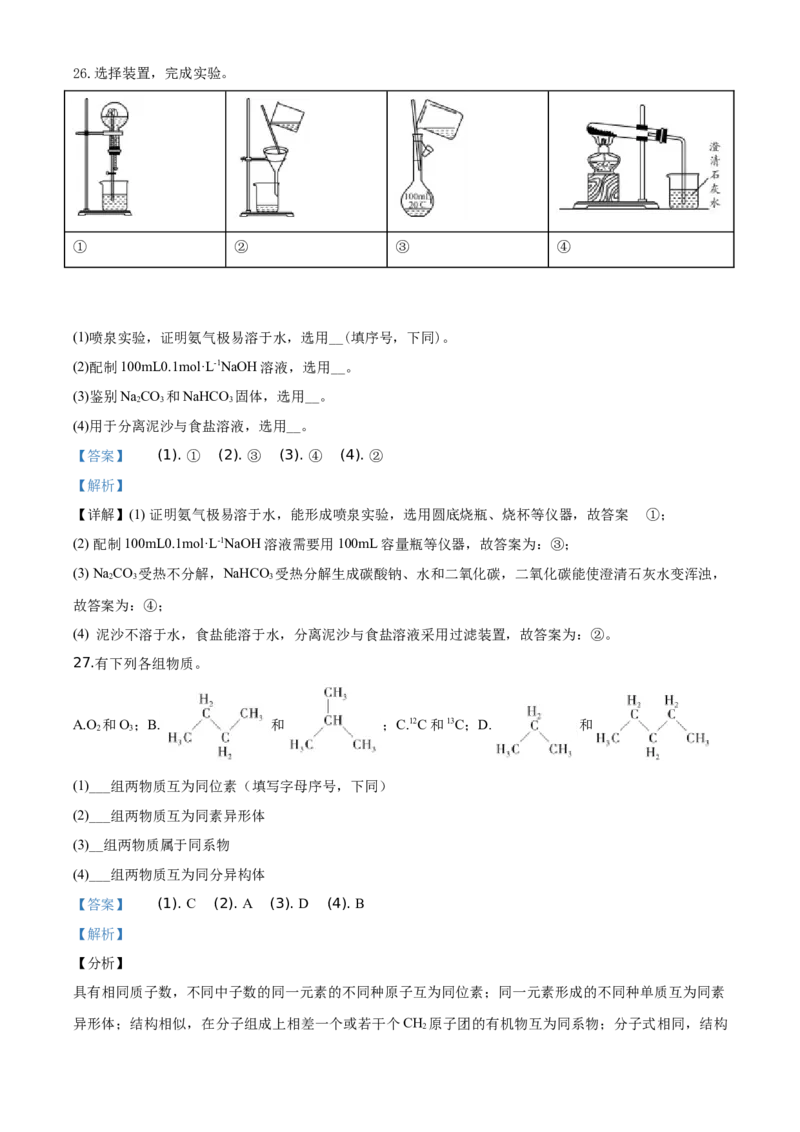
第二部分非选择题(共50分)26.选择装置,完成实验。
① ② ③ ④
(1)喷泉实验,证明氨气极易溶于水,选用__(填序号,下同)。
(2)配制100mL0.1mol·L-1NaOH溶液,选用__。
(3)鉴别NaCO 和NaHCO 固体,选用__。
2 3 3
(4)用于分离泥沙与食盐溶液,选用__。
【答案】 (1). ① (2). ③ (3). ④ (4). ②
【解析】
【详解】(1) 证明氨气极易溶于水,能形成喷泉实验,选用圆底烧瓶、烧杯等仪器,故答案 为①;
(2) 配制100mL0.1mol·L-1NaOH溶液需要用100mL容量瓶等仪器,故答案为:③;
(3) Na CO 受热不分解,NaHCO 受热分解生成碳酸钠、水和二氧化碳,二氧化碳能使澄清石灰水变浑浊,
2 3 3
故答案为:④;
(4) 泥沙不溶于水,食盐能溶于水,分离泥沙与食盐溶液采用过滤装置,故答案为:②。
27.有下列各组物质。
A.O 和O;B. 和 ;C.12C和13C;D. 和
2 3
(1)___组两物质互为同位素(填写字母序号,下同)
(2)___组两物质互为同素异形体
(3)__组两物质属于同系物
(4)___组两物质互为同分异构体
【答案】 (1). C (2). A (3). D (4). B
【解析】
【分析】
具有相同质子数,不同中子数的同一元素的不同种原子互为同位素;同一元素形成的不同种单质互为同素
异形体;结构相似,在分子组成上相差一个或若干个CH 原子团的有机物互为同系物;分子式相同,结构
2不同的有机物互为同分异构体。
【详解】(1) 具有相同质子数,不同中子数的同一元素的不同核素互为同位素,选择C;
(2) 同一元素形成的不同种单质互为同素异形体,选择A;
(3) 结构相似,在分子组成上相差一个或若干个CH 原子团的有机物互为同系物,选择D;
2
(4) 分子式相同,结构不同的有机物互为同分异构体,选择B。
28.铝热法是铝与某些金属氧化物反应获得高熔点金属单质的方法。工业上可用于制造无碳或低碳铁合金。
铝粉和赤铁矿发生铝热反应的化学方程式为:Fe O+2Al 2Fe+Al O
2 3 2 3
(1)上述反应中,作为还原剂的物质是__(化学式),化合价降低的元素是__(名称)。
(2)若反应中消耗了0.2mol Al,生成Fe的物质的量为__mol,转移电子的物质的量为__mol。
【答案】 (1). Al (2). 铁 (3). 0.2 (4). 0.6
【解析】
【分析】
Fe O+2Al 2Fe+Al O,该反应中铁的化合价降低,铝的化合价升高,反应转移6个电子。
2 3 2 3
【详解】(1) Fe O+2Al 2Fe+Al O ,该反应中铝从0价升高到+3价,故Al做还原剂,铁从+3价降低
2 3 2 3
到0价,降低的元素为铁;
(2) Fe O+2Al 2Fe+Al O,反应中铝和铁系数比为1:1,故消耗了0.2mol Al的同时会生成0.2mol铁,
2 3 2 3
一个铝失去3个电子,故转移电子的物质的量为0.6mol。
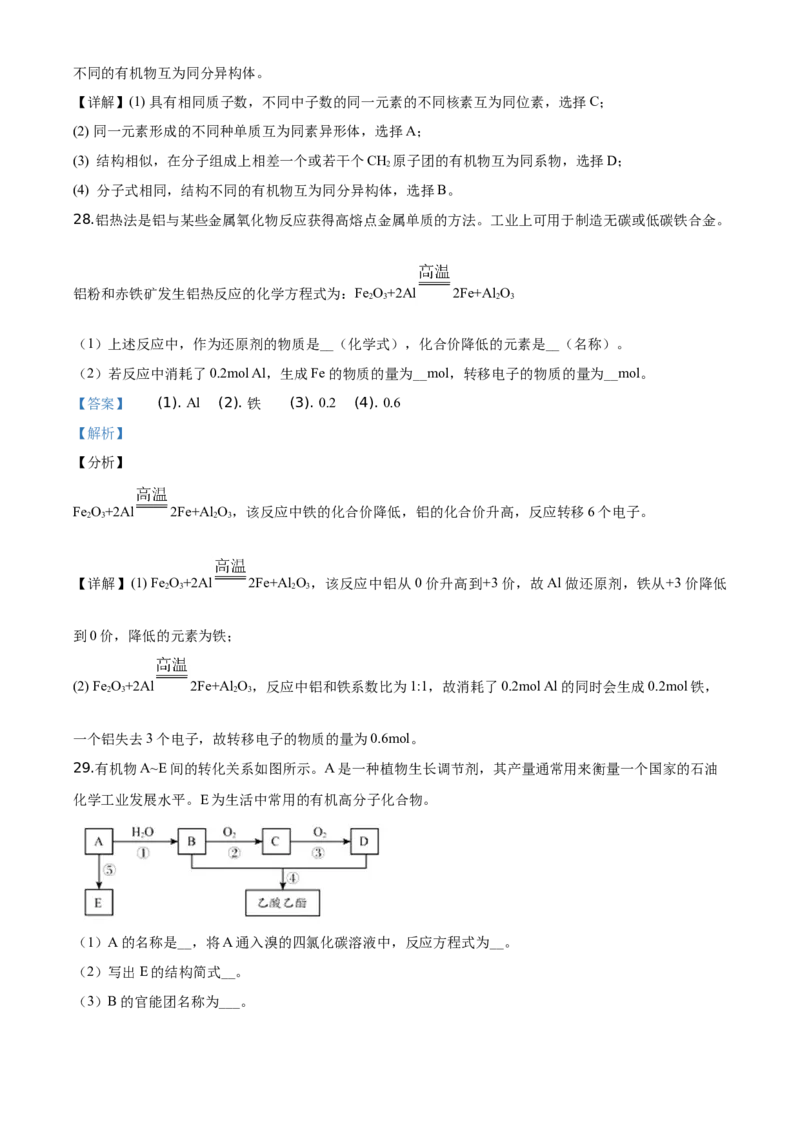
29.有机物A~E间的转化关系如图所示。A是一种植物生长调节剂,其产量通常用来衡量一个国家的石油
化学工业发展水平。E为生活中常用的有机高分子化合物。
(1)A的名称是__,将A通入溴的四氯化碳溶液中,反应方程式为__。
(2)写出E的结构简式__。
(3)B的官能团名称为___。(4)④的反应方程式为__。
【答案】 (1). 乙烯 (2). CH=CH +Br →CHBrCHBr (3). (4). 羟基 (5).
2 2 2 2 2
CHCOOH+HOC H CHCOOC H+H O
3 2 5 3 2 5 2
【解析】
【分析】
推断出各物质分别是什么是解题的关键:A是石油裂解气的主要成分,它的产量通常用来衡量一个国家石
油化工水平,则A是乙烯;乙烯和水发生加成反应生成B,则B为乙醇,乙醇和氧气反应生成C,则C是
乙醛;C和氧气反应生成D,D为乙酸,乙醇和乙酸反应生成乙酸乙酯,据此进行解答。
【详解】A是石油裂解气的主要成分,它的产量通常用来衡量一个国家石油化工水平,故 A是乙烯,乙烯
和水发生加成反应生成B,则B是乙醇,乙醇和氧气反应生成C,则C是乙醛,C和氧气反应生成D,D
是乙酸,乙醇和乙酸反应生成乙酸乙酯。
(1)根据分析可知,A为乙烯,将乙烯通入溴的四氯化碳溶液中,乙烯与溴发生加成反应生成1,2-二溴
乙烷,反应的化学方程式为CH=CH +Br →CHBrCHBr;
2 2 2 2 2
(2)E为生活中常用的有机高分子化合物。乙烯发生加聚反应生成有机高分子化合物E,E为聚乙烯,其
结构简式为: ;
(3)B 为乙醇,官能团名称为羟基;
(4)反应④为乙酸与乙醇的酯化反应,也属于取代反应;反应的化学方程式为:CHCOOH + HOC H
3 2 5
CHCOOC H + H O。
3 2 5 2
30.阅读有关硫代硫酸钠(NaSO)的相关资料:
2 2 3
硫代硫酸钠是一种白色的晶体,可用作冲洗照相底片的定影剂、棉织物漂白后的脱氯剂及定量分析中的还
原剂。它在碱性环境中能稳定存在,在酸性条件下发生反应生成SO 和S。制备NaSO 的方法很多,常用
2 2 2 3
的方法有:Ⅰ.将纯碱溶解后,与二氧化硫作用生成亚硫酸钠,再加入硫磺沸腾反应,经过滤、浓缩、结晶,
制得五水硫代硫酸钠(NaSO·5H O)。Ⅱ.硫化碱法:利用碳酸钠、硫化钠和废气中的二氧化硫反应,经
2 2 3 2
吸硫、蒸发、结晶,制得硫代硫酸钠。Ⅲ.氧化、亚硫酸钠和重结晶法:由含硫化钠、亚硫酸钠和烧碱的液
体经加硫氧化……。
回答下列问题:
(1)NaSO 和HCl反应的离子方程式___。
2 2 3(2)方法Ⅰ中所包含的反应___(写方程式)。
(3)方法Ⅱ中做氧化剂的物质是___(化学式),做还原剂的是__(化学式)。
【答案】 (1). +2H+=S↓+SO ↑+H O (2). NaCO+SO=Na SO +CO 、NaSO +S=Na SO (3).
2 2 2 3 2 2 3 2 2 3 2 2 3
SO (4). NaS
2 2
【解析】
【分析】
纯碱与二氧化硫作用生成亚硫酸钠,亚硫酸钠与加入硫磺沸腾反应得到硫代硫酸钠;碳酸钠、硫化钠和废
气中的二氧化硫反应生成硫代硫酸钠。
【详解】(1)Na SO 和 HCl 反应生成氯化钠、硫单质、二氧化硫和水,其离子方程式
2 2 3
+2H+=S↓+SO ↑+H O;故答案为: +2H+=S↓+SO ↑+H O。
2 2 2 2
(2)方法Ⅰ中溶解的纯碱,与二氧化硫作用生成亚硫酸钠所包含的反应NaCO+SO = Na SO +CO ,加入硫磺
2 3 2 2 3 2
沸腾反应NaSO +S=Na SO;故答案为:NaCO+SO=Na SO +CO 、NaSO +S=Na SO。
2 3 2 2 3 2 3 2 2 3 2 2 3 2 2 3
(3)方法Ⅱ中是碳酸钠、硫化钠和废气中的二氧化硫反应,经吸硫、蒸发、结晶,制得硫代硫酸钠,硫化钠
中硫化合价升高,二氧化硫化合价降低,因此做氧化剂的物质是SO ,做还原剂的是NaS;故答案为:
2 2
SO ;NaS。
2 2
【点睛】根据信息书写化学方程式和分析氧化还原反应是常考题型,主要考查学生知识 的应用和学会学习
的能力考查。
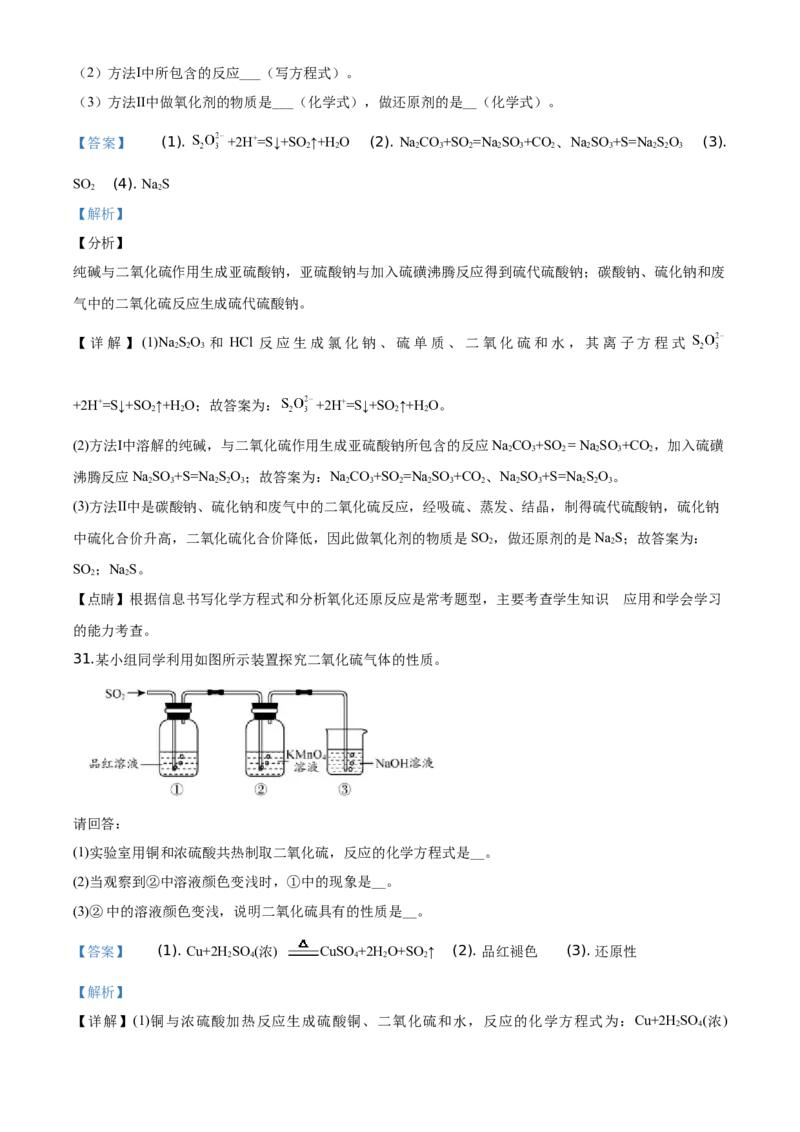
31.某小组同学利用如图所示装置探究二氧化硫气体的性质。
请回答:
(1)实验室用铜和浓硫酸共热制取二氧化硫,反应的化学方程式是__。
(2)当观察到②中溶液颜色变浅时,①中的现象是__。
(3)②中的溶液颜色变浅,说明二氧化硫具有的性质是__。
【答案】 (1). Cu+2H SO (浓) CuSO +2H O+SO ↑ (2). 品红褪色 (3). 还原性
2 4 4 2 2
【解析】
【详解】(1)铜与浓硫酸加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式为:Cu+2H SO (浓)
2 4CuSO +2H O+SO ↑;
4 2 2
(2)②中溶液颜色变浅时,说明②中有二氧化硫与高锰酸钾反应,则①中二氧化硫过量,由于二氧化硫具有
漂白性,将二氧化硫通入品红溶液后,会观察到①中品红溶液褪色;
(3)装置②中酸性高锰酸钾具有强氧化性,二氧化硫能够使酸性高锰酸钾溶液变浅,证明了二氧化硫具有还
原性。
【点睛】本题考查了二氧化硫的化学性质,题目难度中等,明确二氧化硫的性质为解答关键,试题培养了
学生根据实验现象分析物质性质的能力。
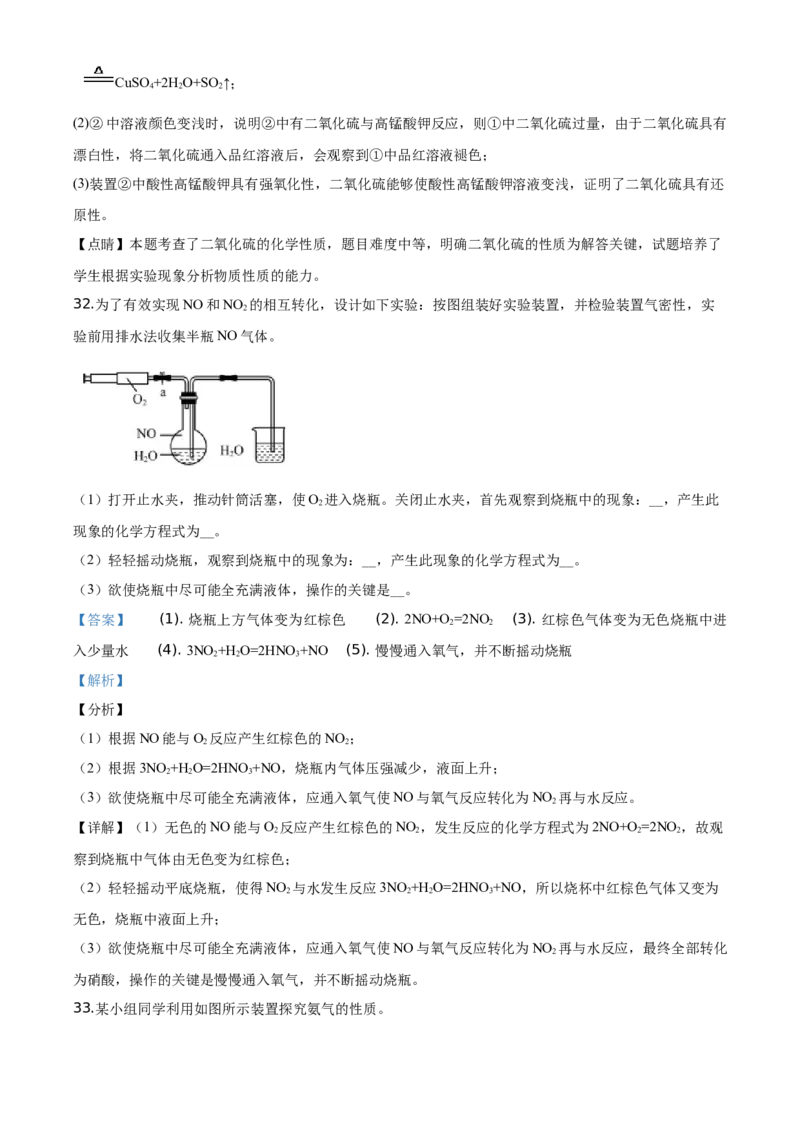
32.为了有效实现NO和NO 的相互转化,设计如下实验:按图组装好实验装置,并检验装置气密性,实
2
验前用排水法收集半瓶NO气体。
(1)打开止水夹,推动针筒活塞,使O 进入烧瓶。关闭止水夹,首先观察到烧瓶中的现象:__,产生此
2
现象的化学方程式为__。
(2)轻轻摇动烧瓶,观察到烧瓶中的现象为:__,产生此现象的化学方程式为__。
(3)欲使烧瓶中尽可能全充满液体,操作的关键是__。
【答案】 (1). 烧瓶上方气体变为红棕色 (2). 2NO+O =2NO (3). 红棕色气体变为无色烧瓶中进
2 2
入少量水 (4). 3NO +H O=2HNO +NO (5). 慢慢通入氧气,并不断摇动烧瓶
2 2 3
【解析】
【分析】
(1)根据NO能与O 反应产生红棕色的NO ;
2 2
(2)根据3NO +H O=2HNO +NO,烧瓶内气体压强减少,液面上升;
2 2 3
(3)欲使烧瓶中尽可能全充满液体,应通入氧气使NO与氧气反应转化为NO 再与水反应。
2
【详解】(1)无色的NO能与O 反应产生红棕色的NO ,发生反应的化学方程式为2NO+O =2NO,故观
2 2 2 2
察到烧瓶中气体由无色变为红棕色;
(2)轻轻摇动平底烧瓶,使得NO 与水发生反应3NO +H O=2HNO +NO,所以烧杯中红棕色气体又变为
2 2 2 3
无色,烧瓶中液面上升;
(3)欲使烧瓶中尽可能全充满液体,应通入氧气使NO与氧气反应转化为NO 再与水反应,最终全部转化
2
为硝酸,操作的关键是慢慢通入氧气,并不断摇动烧瓶。
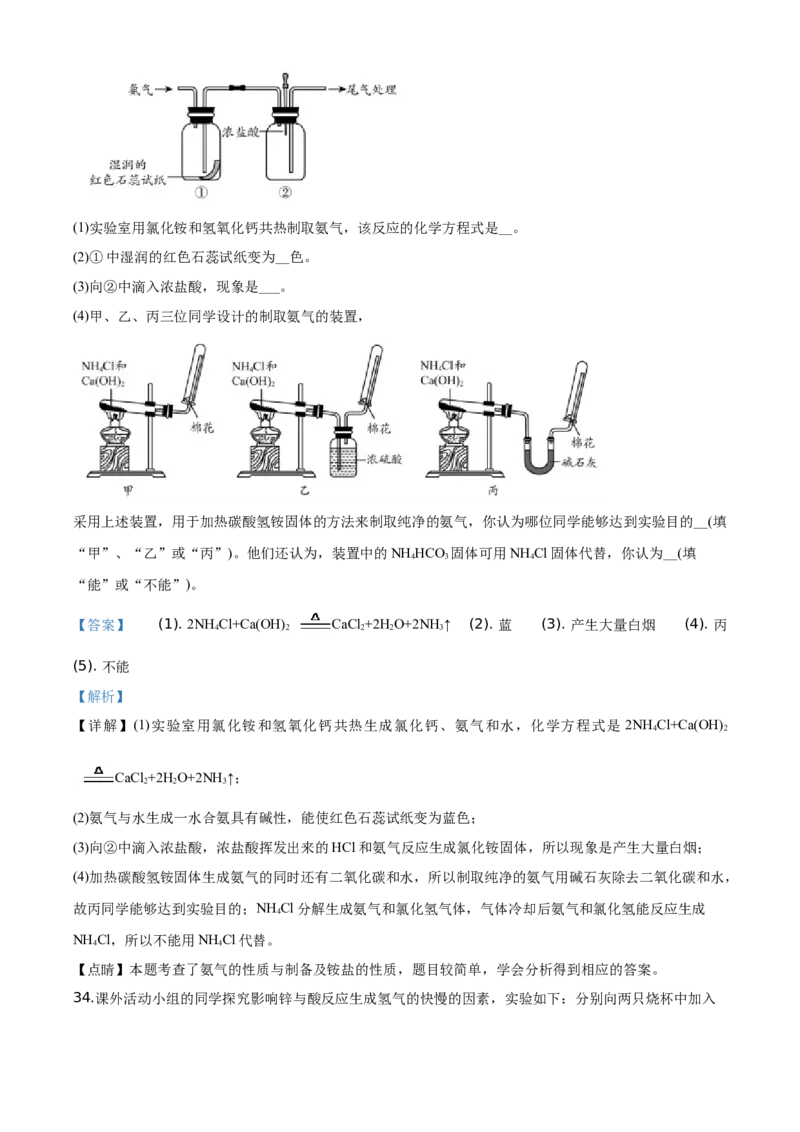
33.某小组同学利用如图所示装置探究氨气的性质。(1)实验室用氯化铵和氢氧化钙共热制取氨气,该反应的化学方程式是__。
(2)①中湿润的红色石蕊试纸变为__色。
(3)向②中滴入浓盐酸,现象是___。
(4)甲、乙、丙三位同学设计的制取氨气的装置,
采用上述装置,用于加热碳酸氢铵固体的方法来制取纯净的氨气,你认为哪位同学能够达到实验目的__(填
“甲”、“乙”或“丙”)。他们还认为,装置中的NH HCO 固体可用NH Cl固体代替,你认为__(填
4 3 4
“能”或“不能”)。
【答案】 (1). 2NH Cl+Ca(OH) CaCl +2H O+2NH ↑ (2). 蓝 (3). 产生大量白烟 (4). 丙
4 2 2 2 3
(5). 不能
【解析】
【详解】(1)实验室用氯化铵和氢氧化钙共热生成氯化钙、氨气和水,化学方程式是 2NH Cl+Ca(OH)
4 2
CaCl +2H O+2NH ↑;
2 2 3
(2)氨气与水生成一水合氨具有碱性,能使红色石蕊试纸变为蓝色;
(3)向②中滴入浓盐酸,浓盐酸挥发出来的HCl和氨气反应生成氯化铵固体,所以现象是产生大量白烟;
(4)加热碳酸氢铵固体生成氨气的同时还有二氧化碳和水,所以制取纯净的氨气用碱石灰除去二氧化碳和水,
故丙同学能够达到实验目的;NH Cl分解生成氨气和氯化氢气体,气体冷却后氨气和氯化氢能反应生成
4
NH Cl,所以不能用NH Cl代替。
4 4
【点睛】本题考查了氨气的性质与制备及铵盐的性质,题目较简单,学会分析得到相应的答案。
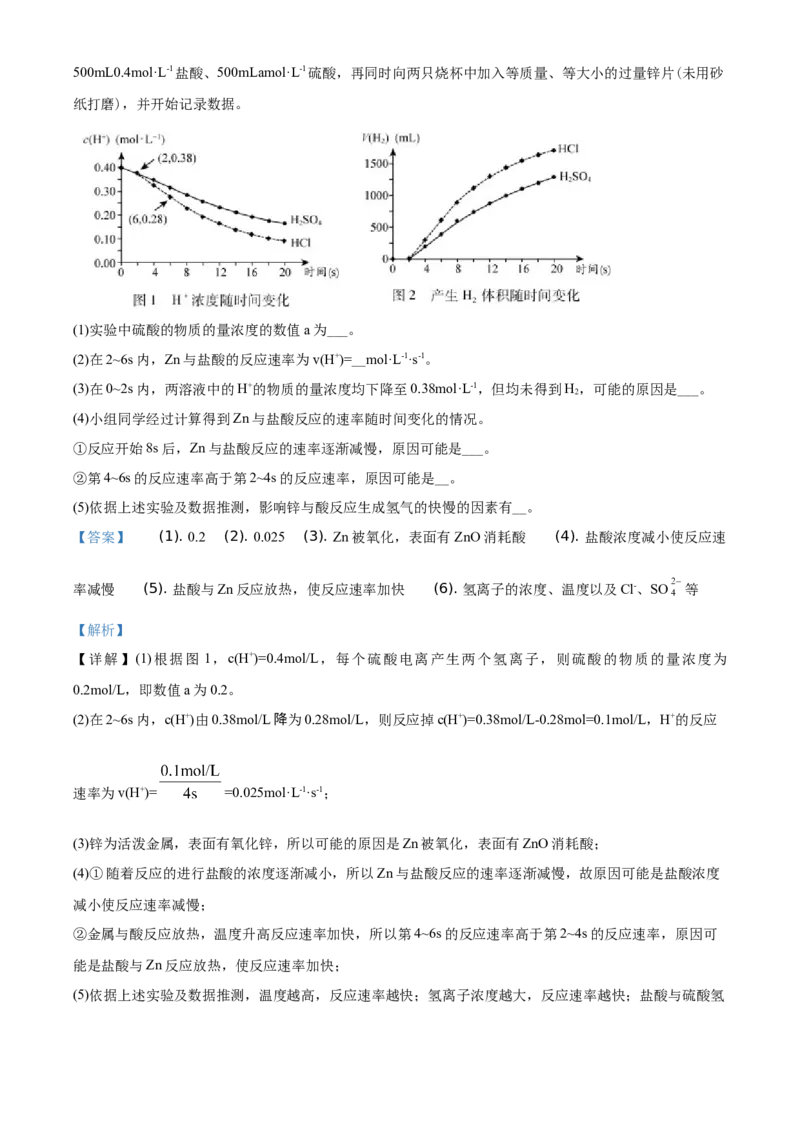
34.课外活动小组的同学探究影响锌与酸反应生成氢气的快慢的因素,实验如下:分别向两只烧杯中加入500mL0.4mol·L-1盐酸、500mLamol·L-1硫酸,再同时向两只烧杯中加入等质量、等大小的过量锌片(未用砂
纸打磨),并开始记录数据。
(1)实验中硫酸的物质的量浓度的数值a为___。
(2)在2~6s内,Zn与盐酸的反应速率为v(H+)=__mol·L-1·s-1。
(3)在0~2s内,两溶液中的H+的物质的量浓度均下降至0.38mol·L-1,但均未得到H,可能的原因是___。
2
(4)小组同学经过计算得到Zn与盐酸反应的速率随时间变化的情况。
①反应开始8s后,Zn与盐酸反应的速率逐渐减慢,原因可能是___。
②第4~6s的反应速率高于第2~4s的反应速率,原因可能是__。
(5)依据上述实验及数据推测,影响锌与酸反应生成氢气的快慢的因素有__。
【答案】 (1). 0.2 (2). 0.025 (3). Zn被氧化,表面有ZnO消耗酸 (4). 盐酸浓度减小使反应速
率减慢 (5). 盐酸与Zn反应放热,使反应速率加快 (6). 氢离子的浓度、温度以及Cl-、SO 等
【解析】
【详解】(1)根据图 1,c(H+)=0.4mol/L,每个硫酸电离产生两个氢离子,则硫酸的物质的量浓度为
0.2mol/L,即数值a为0.2。
(2)在2~6s内,c(H+)由0.38mol/L降为0.28mol/L,则反应掉c(H+)=0.38mol/L-0.28mol=0.1mol/L,H+的反应
速率为v(H+)= =0.025mol·L-1·s-1;
(3)锌为活泼金属,表面有氧化锌,所以可能的原因是Zn被氧化,表面有ZnO消耗酸;
(4)①随着反应的进行盐酸的浓度逐渐减小,所以Zn与盐酸反应的速率逐渐减慢,故原因可能是盐酸浓度
减小使反应速率减慢;
②金属与酸反应放热,温度升高反应速率加快,所以第4~6s的反应速率高于第2~4s的反应速率,原因可
能是盐酸与Zn反应放热,使反应速率加快;
(5)依据上述实验及数据推测,温度越高,反应速率越快;氢离子浓度越大,反应速率越快;盐酸与硫酸氢离子浓度相同时,阴离子不同,反应速率不同,所以影响锌与酸反应生成氢气的快慢的因素有氢离子的浓
度、温度以及Cl-、SO 等。
【点睛】本题考查反应速率的计算和影响化学反应速率的因素,会根据图形进行分析,结合影响反应速率
的因素进行解题。