文档内容
北京市昌平区 2019-2020 学年高一上学期期末考试
化学试题
1.下列化学家与其所作的突出贡献不匹配的是( )
门捷列夫 拉瓦锡 阿伏伽德罗 道尔顿
提出化学元素的概念
提出氧化学说 提出分子学说 提出原子论
A B C D
A. A B. B C. C D. D
2. 下列气体是黄绿色的是
A. Cl B. N C. SO D. NO
2 2 2 2
3.以下仪器中,名称为“容量瓶”的是( )
A. B. C. D.
4.碳酸钠的物质类别是( )
A. 酸 B. 碱 C. 盐 D. 酸性氧化物
5.下列物质中属于碱性氧化物的是( )
A. NaO B. SO C. NH D. KOH
2 2 3
6.下列化学符号可以表示硫酸根离子的是( )
A. S2- B. SO C. SO 2- D. SO 2-
4 3 4
7.常温下,下列物质中易溶于水的是( )
A. MgSO B. AgCl C. Al (OH) D. BaCO
4 3 38.Na在空气中加热的产物是( )
A. Na O B. Na O C. NaOH D. NaHCO
2 2 2 3
9.以下物质中,不具备消毒作用的是( )
A. 84消毒液 B. 氯水 C. Ca(ClO) D. N
2 2
10.下列化学反应中,不是氧化还原反应的是( )
A. 3NO + H O = 2HNO + NO B. 2 H +O 2HO
2 2 3 2 2 2
C. Cl +HO=HClO+HCl D. CuCl +Ba(OH) =Cu(OH) +BaCl
2 2 2 2 2 2
11.下列物质分别加入水中,主要以离子形式存在的是( )
A. CaCO B. Zn C. Fe O D. Mg(NO )
3 2 3 3 2
12.下列物质在水中发生电离的电离方程式书写正确的是( )
A. HNO = H-+ NO + B. Ba(OH) =Ba2++ OH2-
3 3 2
C. NH NO =NH ++NO- D. CaO= Ca2+ + O2-
4 3 4 3
13.下列离子方程式书写正确的是( )
A. 氢氧化钾溶液与盐酸:K ++OH-+H+ +Cl-=KCl+H O
2
B. 碳酸钙与稀盐酸:CO2-+2H+=H O+CO↑
3 2 2
C. 氧化铁与盐酸: Fe O+6H+ =2Fe3++3HO
2 3 2
D. 钠与水反应:Na+HO=Na++OH-+H ↑
2 2
14.在离子方程式2Fe3++Fe=3Fe2+中,Fe3 +可能代表的物质是( )
A. FeSO B. FeCl C. Fe O D. Fe(OH)
4 3 2 3 3
15.下列各组离子在溶液中能大量共存的是( )
A. Na+、H+、SO 2-、HCO - B. NO -、OH-、Na+、NH +
4 3 3 4
C. Mg2+、Na+、Cl-、OH- D. OH-、Na+、SO 2-、Cl-
4
16.从20 mL如图所示NaCO 溶液中取出10 mL,取出溶液中Na+的物质的量为( )
2 3
A. 0.005 mol B. 0.01 mol C. 0.5 mol/L D. 1 mol/L
17.下列说法正确 的是( )
A. Cl 的摩尔质量为35.5 g/mol
2
B. 2 mol H 含有N 个原子
2 AC. 任意温度和压强下,2 mol NH 的质量都是34g
3
D. 标准状况下,1 mol O 和1 mol O 的体积不相等
2 3
18.下列现象或事实与物质性质对应关系不正确的是( )
现象或事实 物质性质
干燥的氯气不能使有色干布条褪色,氯气能使湿润的有 氯气与水反应产生的某种新物质具有漂
A
色布条褪色 白性
碳酸氢钠可单独用作蒸馒头的膨松剂,但效果不太好, 碳酸氢钠加热可产生气体;
B
同时加入食醋,效果则更为理想 碳酸氢钠与酸反应可产生气体
C NO遇空气变为红棕色 NO具有还原性
D FeCl 溶液可与Cu反应 Cu在一定条件下可置换铁
3
A. A B. B C. C D. D
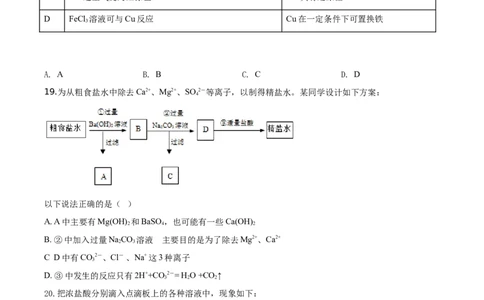
19.为从粗食盐水中除去Ca2+、Mg2+、SO 2-等离子,以制得精盐水。某同学设计如下方案:
4
以下说法正确的是( )
A. A中主要有Mg(OH) 和BaSO,也可能有一些Ca(OH)
2 4 2
B. ②中加入过量NaCO 溶液 的主要目的是为了除去Mg2+、Ca2+
2 3
.
C D中有CO2-、Cl- 、Na+ 这3种离子
3
D. ③中发生的反应只有2H++CO 2-= H O +CO ↑
3 2 2
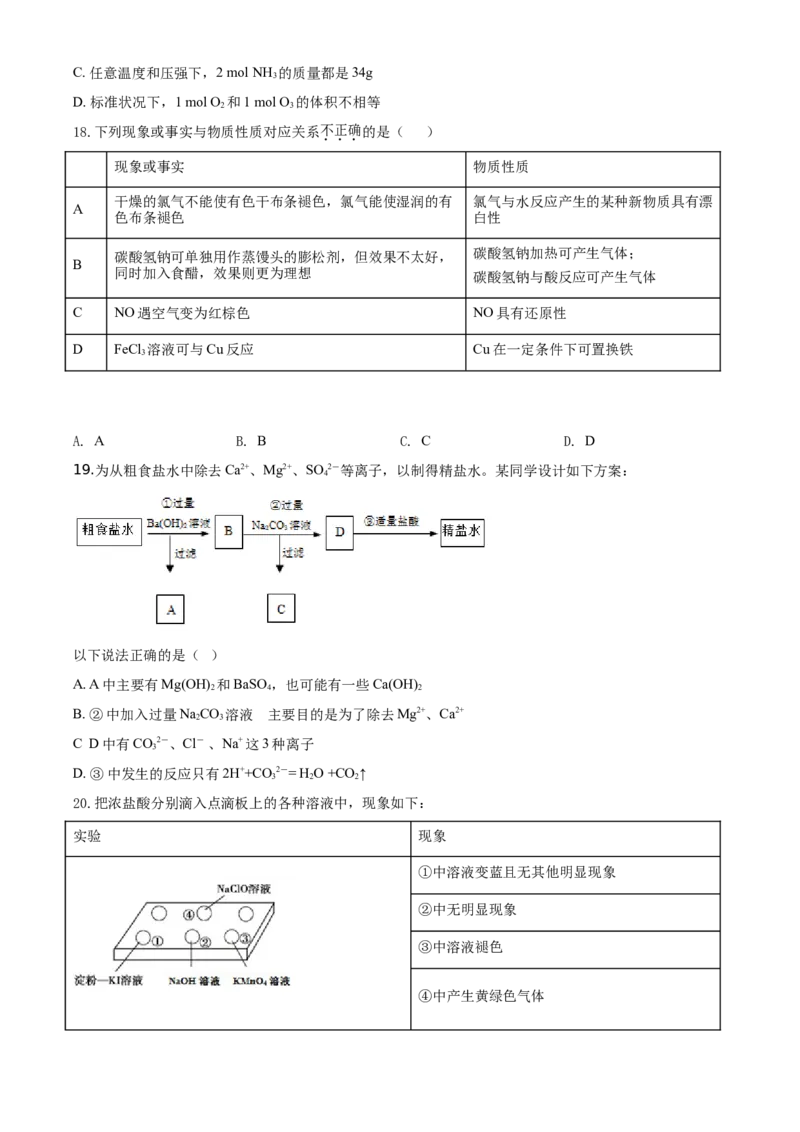
20.把浓盐酸分别滴入点滴板上的各种溶液中,现象如下:
实验 现象
①中溶液变蓝且无其他明显现象
②中无明显现象
③中溶液褪色
④中产生黄绿色气体下列分析正确 的是( )
A. ①中现象体现了浓盐酸的氧化性
B. ②中现象说明未发生反应
C. ③中反应后氯元素全部以KCl形式存在
D. ④中产生黄绿色气体的反应是:ClO-+ Cl-+ 2H+ = Cl ↑+ H O
2 2
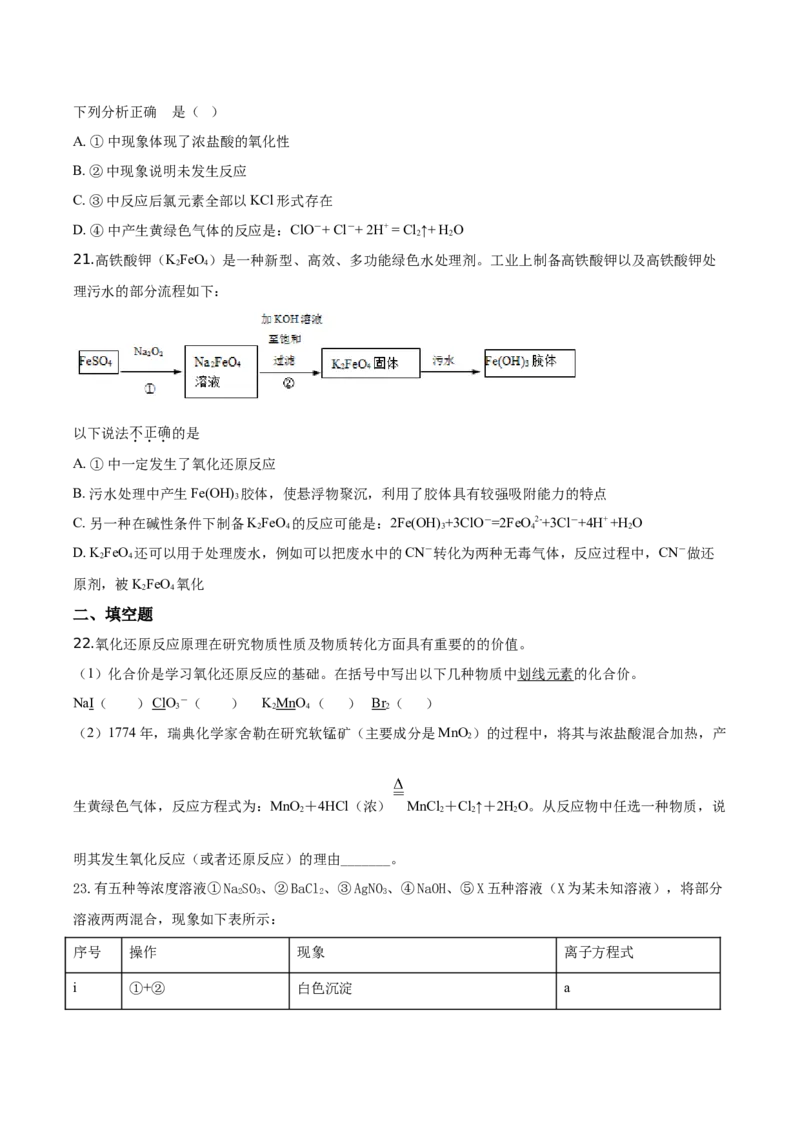
21.高铁酸钾(KFeO)是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处
2 4
理污水的部分流程如下:
以下说法不正确的是
A. ①中一定发生了氧化还原反应
B. 污水处理中产生Fe(OH) 胶体,使悬浮物聚沉,利用了胶体具有较强吸附能力的特点
3
C. 另一种在碱性条件下制备KFeO 的反应可能是:2Fe(OH) +3ClO-=2FeO 2-+3Cl-+4H+ +H O
2 4 3 4 2
D. K FeO 还可以用于处理废水,例如可以把废水中的CN-转化为两种无毒气体,反应过程中,CN-做还
2 4
原剂,被KFeO 氧化
2 4
二、填空题
22.氧化还原反应原理在研究物质性质及物质转化方面具有重要的的价值。
(1)化合价是学习氧化还原反应的基础。在括号中写出以下几种物质中划线元素的化合价。
NaI( )ClO-( ) KMnO ( ) Br ( )
3 2 4 2
(2)1774年,瑞典化学家舍勒在研究软锰矿(主要成分是MnO )的过程中,将其与浓盐酸混合加热,产
2
生黄绿色气体,反应方程式为:MnO +4HCl(浓) MnCl +Cl↑+2HO。从反应物中任选一种物质,说
2 2 2 2
明其发生氧化反应(或者还原反应)的理由_______。
23.有五种等浓度溶液①NaSO、②BaCl、③AgNO、④NaOH、⑤X五种溶液(X为某未知溶液),将部分
2 3 2 3
溶液两两混合,现象如下表所示:
序号 操作 现象 离子方程式
i ①+② 白色沉淀 aii ②+③ b c
iii ①+⑤ 无色气体 d
(1)将表格补充完整。a.______;b._____;c. ______。
(2)预测②与④不能发生反应,预测依据是__________。
(3)猜测⑤是HSO , 因此在实验iii的基础上增加实验iv,证明了猜测。实验iv的操作及现象是(所需
2 4
试剂任选)____________ 。
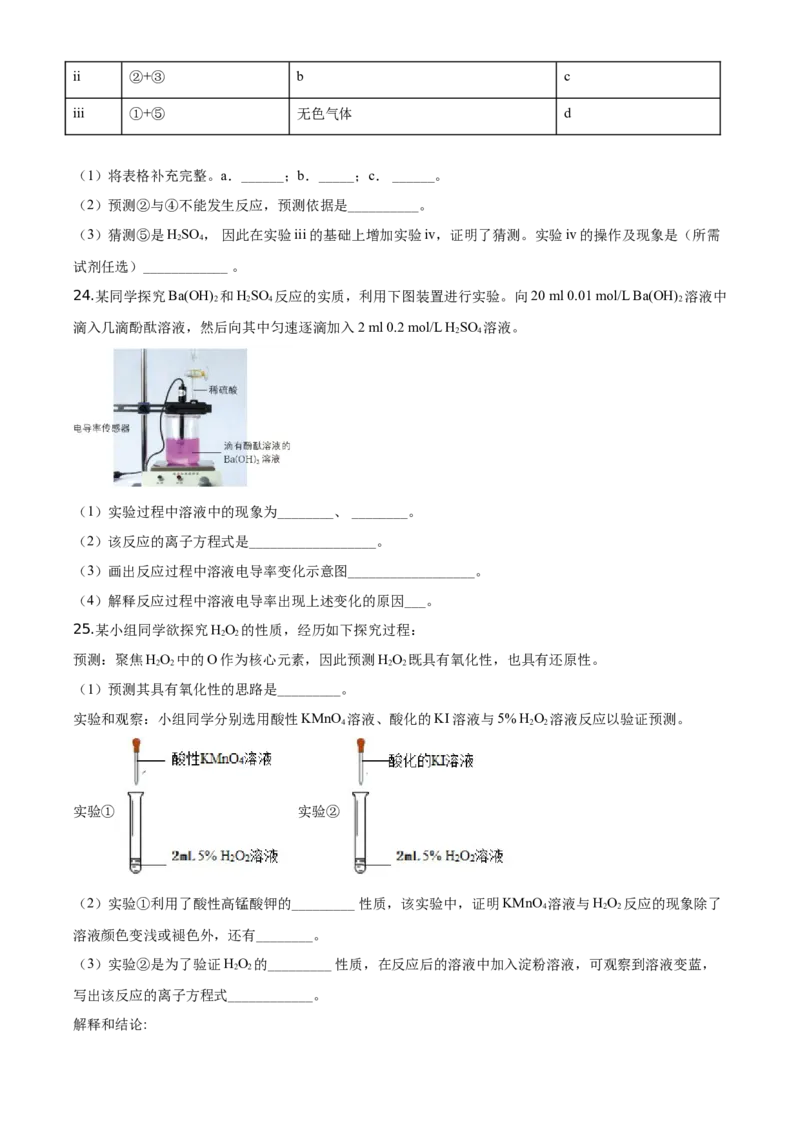
24.某同学探究Ba(OH) 和HSO 反应的实质,利用下图装置进行实验。向20 ml 0.01 mol/L Ba(OH) 溶液中
2 2 4 2
滴入几滴酚酞溶液,然后向其中匀速逐滴加入2 ml 0.2 mol/L H SO 溶液。
2 4
(1)实验过程中溶液中的现象为________、 ________。
(2)该反应的离子方程式是__________________。
(3)画出反应过程中溶液电导率变化示意图__________________。
(4)解释反应过程中溶液电导率出现上述变化的原因___。
25.某小组同学欲探究HO 的性质,经历如下探究过程:
2 2
预测:聚焦HO 中的O作为核心元素,因此预测HO 既具有氧化性,也具有还原性。
2 2 2 2
(1)预测其具有氧化性的思路是_________。
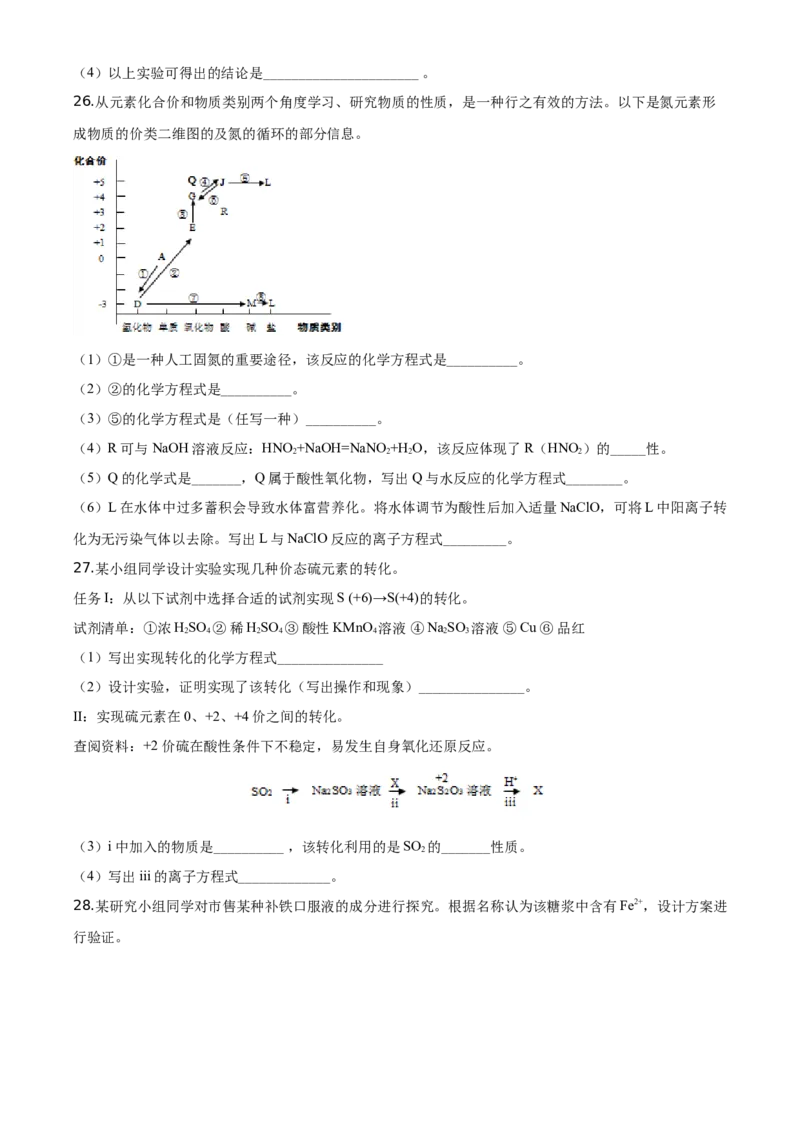
实验和观察:小组同学分别选用酸性KMnO 溶液、酸化的KI溶液与5% H O 溶液反应以验证预测。
4 2 2
实验① 实验②
(2)实验①利用了酸性高锰酸钾的_________ 性质,该实验中,证明KMnO 溶液与HO 反应的现象除了
4 2 2
溶液颜色变浅或褪色外,还有________。
(3)实验②是为了验证HO 的_________ 性质,在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,
2 2
写出该反应的离子方程式____________。
解释和结论:(4)以上实验可得出的结论是______________________ 。
26.从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法。以下是氮元素形
成物质的价类二维图的及氮的循环的部分信息。
(1)①是一种人工固氮的重要途径,该反应的化学方程式是__________。
(2)②的化学方程式是__________。
(3)⑤的化学方程式是(任写一种)__________。
(4)R可与 NaOH溶液反应:HNO+NaOH=NaNO +H O,该反应体现了R(HNO)的_____性。
2 2 2 2
(5)Q的化学式是_______,Q属于酸性氧化物,写出Q与水反应的化学方程式________。
(6)L在水体中过多蓄积会导致水体富营养化。将水体调节为酸性后加入适量NaClO,可将L中阳离子转
化为无污染气体以去除。写出L与NaClO反应的离子方程式_________。
27.某小组同学设计实验实现几种价态硫元素的转化。
任务I:从以下试剂中选择合适的试剂实现S (+6)→S(+4)的转化。
试剂清单:①浓HSO ②稀HSO ③酸性KMnO 溶液 ④NaSO 溶液 ⑤Cu ⑥品红
2 4 2 4 4 2 3
(1)写出实现转化的化学方程式_______________
(2)设计实验,证明实现了该转化(写出操作和现象)_______________。
II:实现硫元素在0、+2、+4价之间的转化。
查阅资料:+2价硫在酸性条件下不稳定,易发生自身氧化还原反应。
(3)i中加入的物质是__________ ,该转化利用的是SO 的_______性质。
2
(4)写出iii的离子方程式_____________。
28.某研究小组同学对市售某种补铁口服液的成分进行探究。根据名称认为该糖浆中含有Fe2+,设计方案进
行验证。I.设计方案如下:
方案 试剂X 预期现象
方案i 1mL 1 mol/L NaOH溶液 a
方案ii 1mL 1 mol/L 酸性KMnO 溶液 b
4
依次加入5滴KSCN溶液、1mL氯
方案iii c
水
(1)方案i的预期现象是产生白色沉淀,逐渐变为灰绿色,最终变为红褐色。产生白色沉淀的离子方程式
是_________,最终变为红褐色的化学方程式是________。
(2)方案ii的预期现象是_________。
(3)方案iii的预期现象是________,反应中氯水参与反应的的离子方程式是____。
II.进行实验操作,得到的实际现象如下:
方案 实际现象 是否与预期现象相同
方案i 产生灰绿色浑浊,长时间不变红褐色 不同
方案ii 相同
方案iii 自始至终无明显现象 不同
(4)为探究实验中出现异常现象的原因,该小组同学查看说明书,得知有关补铁口服液成分的如下:
本品每毫升含主要成分葡萄糖酸亚铁30毫克,
辅料为:蔗糖、香精、枸檬酸、羟苯乙酯。
结合资料对异常现象产生的原因进行猜想:______________;为验证其猜想,在方案iii的基础上继续加入
过量的氯水,得到了预期的现象。
(5) 实验反思:方案ii中预期现象与实验现象相同,并不能证明补铁口服液中一定含有Fe2+,理由是
______。
(6)小组同学进一步提出研究问题:仍选用之前用过的试剂,设计实验验证某久置的补铁口服液(计为
Y)已部分变质。以下是小组同学的实验方案:实验序号 操作 现象
ⅳ 取2 mL溶液Y,加入1滴KSCN,再加入1 mL水 溶液显红色
V
实验V的操作及现象是_____________。