文档内容
北京市房山区 2019-2020 学年度高一上学期期末检测试卷
化学试题
1.纪录片《我在故宫修文物》表现了文物修复者穿越古今与百年之前的人进行对话的职业体验,让我们领
略到历史与文化的传承。下列文物修复和保护的过程中涉及化学变化的是( )
A B C D
银器用除锈剂除锈 变形的金属香炉复原 古画水洗除尘 木器表面擦拭烫蜡
A. A B. B C. C D. D
2.下列物质中,属于电解质的是
A. Cu B. KSO C. MgCl 溶液 D. NaOH溶液
2 4 2
3.当光束通过下列分散系时,能观察到丁达尔效应的是
A. KCl溶液 B. 蔗糖溶液 C. Fe(OH) 胶体 D. NaOH溶液
3
4.下列关于物质分类的叙述中,不正确的是
A. 硝酸属于酸 B. 液氯属于纯净物
C. 碳酸钠属于碱 D. 二氧化硫属于氧化物
5.下图为某城市某日空气质量报告,下列叙述与报告内容不相符的是
A. 该日空气首要污染物是PM2.5 B. 该市空气质量等级属于重度污染
C. 污染物NO 可能主要来源于机动车尾气 D. CO、SO 均可导致酸雨
2 2
6.常温下,下列溶液可用铁质容器盛装的是A. 稀硝酸 B. 稀硫酸 C. 浓硝酸 D. 浓盐酸
7.下列关于二氧化氮性质的描述中,不正确的是
A. 无色气体 B. 有刺激性气味
C. 相同条件下密度比空气的大 D. 能与水反应
8.水饺是中华传统美食。下列制作水饺的主要过程中,包含过滤操作的是
A.和面、饧面 B.剁馅、拌馅 C.擀皮、包饺子 D.煮熟、捞饺子
A. A B. B C. C D. D
9.下列说法不正确的是:
A. 遇空气变为红棕色的是NO
B. NH HCO 不稳定 受热易分解
4 3 ,
C. Cl 能使湿润的红色布条褪色
2
D. 浓HSO 能使蔗糖变黑并有刺激性气味的气体生成,只体现了浓硫酸的脱水性
2 4
10.实验室中,下列行为不符合安全要求的是
A. 在通风橱内制备有毒气体
B. 氯气泄漏的时候,人顺风向低处跑
C. 闻气体时用手轻轻扇动,使少量气体飘进鼻孔
D. 稀释浓硫酸时,将浓硫酸沿器壁缓慢倒入水中并用玻璃棒不断搅拌
11.下列有关试剂保存的说法中,不正确的是
A. 新制氯水需要避光保存 B. Na可保存在煤油中
C. 浓硝酸要保存在棕色瓶中 D. 保存FeCl 溶液时需加入少量Fe粉
3
12.下列各组离子在溶液中能大量共存的是
A. Ca2+、Na+、CO2-、NO - B. Na+、Cl-、H+、OH-
3 3
C. Na+、Fe3+、Cl-、SO 2- D. H+、K+、CO2-、SO 2-
4 3 4
13.吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含
硒元素(Se)的化合物亚硒酸钠(NaSeO),能消除人体内的活性氧,由此判断NaSeO 的作用是
2 3 2 3A. 作还原剂 B. 作氧化剂
C. 既作氧化剂又作还原剂 D. 作催化剂
14.下列反应的离子方程式书写正确的是
A. 碳酸钙与稀盐酸反应:CO2-+2H+ =CO ↑+HO
3 2 2
B. 氯化亚铁溶液与氯水反应:Fe2++ Cl=Fe3++2Cl-
2
C. 氯化铁溶液与氢氧化钠溶液反应:Fe3++3OH-=Fe(OH) ↓
3
D. 铜与稀硝酸反应:Cu+4H+ +2NO -=Cu2++2NO ↑+2HO
3 2 2
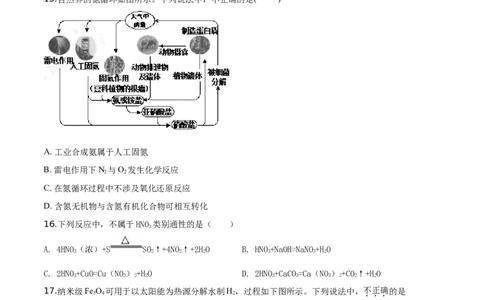
15.自然界的氮循环如图所示。下列说法中,不正确的是( )
A. 工业合成氨属于人工固氮
B. 雷电作用下N 与O 发生化学反应
2 2
C. 在氮循环过程中不涉及氧化还原反应
D. 含氮无机物与含氮有机化合物可相互转化
16.下列反应中,不属于HNO 类别通性的是( )
3
A. 4HNO(浓)+S SO↑+4NO↑+2HO B. HNO+NaOH=NaNO+HO
3 2 2 2 3 3 2
C. 2HNO+CuO=Cu(NO)+HO D. 2HNO+CaCO=Ca(NO)+CO↑+HO
3 3 2 2 3 3 3 2 2 2
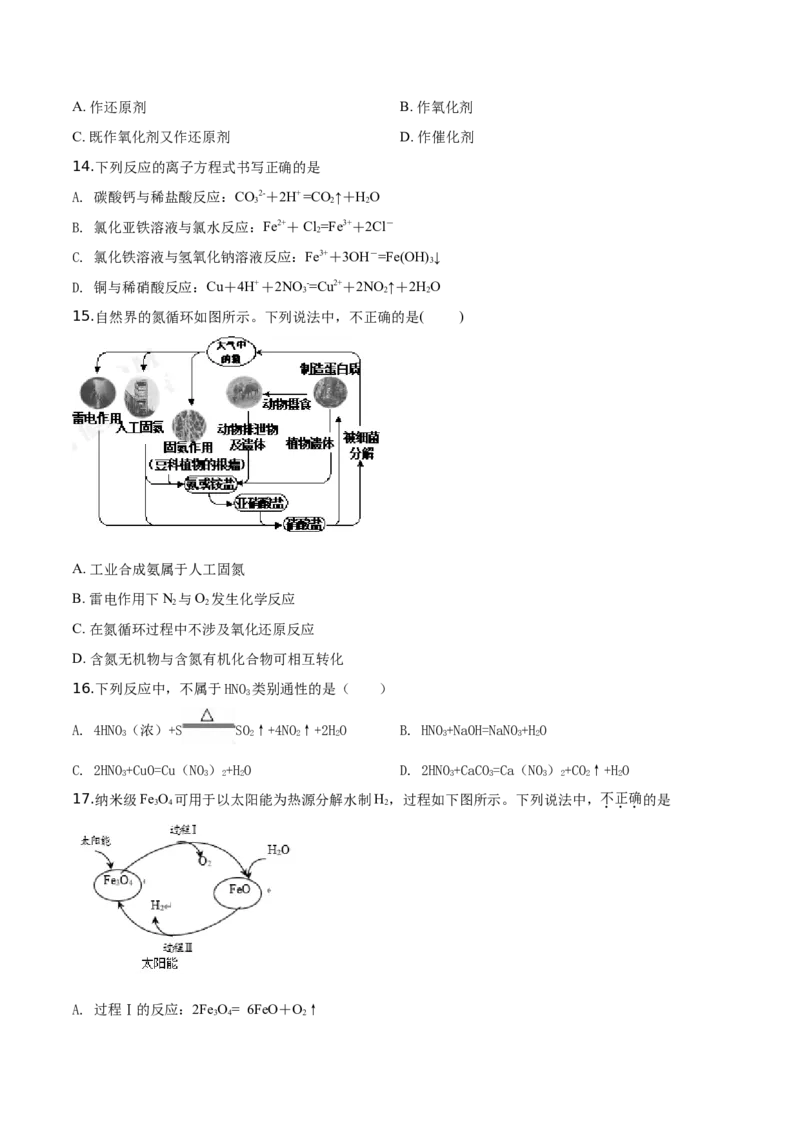
17.纳米级Fe O 可用于以太阳能为热源分解水制H,过程如下图所示。下列说法中,不正确的是
3 4 2
A. 过程Ⅰ的反应:2Fe O= 6FeO+O↑
3 4 2B. 过程Ⅱ的反应:2HO =2H ↑+O↑
2 2 2
C. 两个转化过程都发生了氧化还原反应
D. 整个过程实现了太阳能向化学能的转化
18.下列说法中,正确的是
A. 36 g HO的物质的量为1 mol
2
B. 常温常压下,1mol Cl 的体积是22.4 L
2
C. 0.5mol·L-1NaCl溶液中含有0.5mol Na+
D. 1molCO 中含有的分子数约为6.02×1023
2
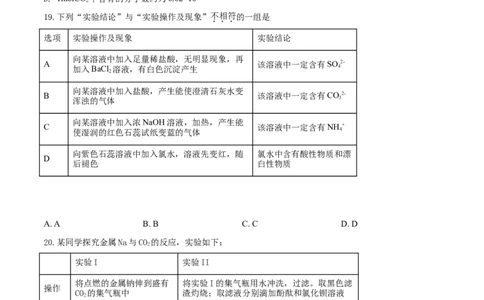
19.下列“实验结论”与“实验操作及现象”不相符的一组是
选项 实验操作及现象 实验结论
向某溶液中加入足量稀盐酸,无明显现象,再
A 该溶液中一定含有SO 2-
加入BaCl 溶液,有白色沉淀产生 4
2
向某溶液中加入盐酸,产生能使澄清石灰水变
B 该溶液中一定含有CO2-
浑浊的气体 3
向某溶液中加入浓NaOH溶液,加热,产生能
C 该溶液中一定含有NH +
使湿润的红色石蕊试纸变蓝的气体 4
向紫色石蕊溶液中加入氯水,溶液先变红,随 氯水中含有酸性物质和漂
D
后褪色 白性物质
A. A B. B C. C D. D
20.某同学探究金属Na与CO 的反应,实验如下:
2
实验I 实验II
将点燃的金属钠伸到盛有 将实验I的集气瓶用水冲洗,过滤。取黑色滤
操作
CO 的集气瓶中 渣灼烧;取滤液分别滴加酚酞和氯化钡溶液
2
①火焰呈黄色 ①黑色滤渣可燃
现象 ②底部有黑色固体,瓶壁 ②滤液能使酚酞溶液变红,滴加氯化钡溶液有
上附有白色固体 白色沉淀生成
下列说法不正确的是
A. 生成的黑色固体中含有C B. 白色固体是NaO
2C. 实验说明CO 具有氧化性 D. 金属Na着火不能用CO 灭火
2 2
21.下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是
物质(括号内为杂质) 除杂试剂
A FeCl 溶液(FeCl ) Fe粉
2 3
B NaCl溶液(MgCl ) NaOH溶液、稀HCl
2
C Cl(HCl) HO、浓HSO
2 2 2 4
D NO(NO ) HO、无水CaCl
2 2 2
A. A B. B C. C D. D
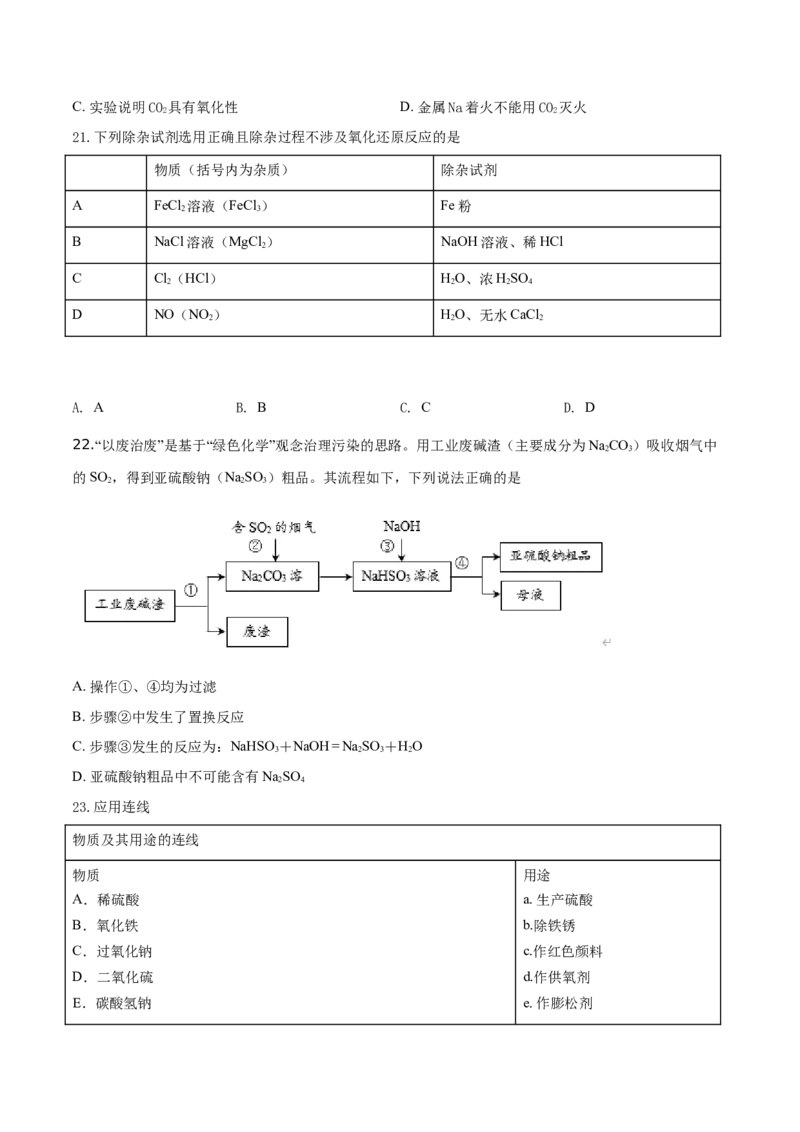
22.“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为NaCO)吸收烟气中
2 3
的SO ,得到亚硫酸钠(NaSO )粗品。其流程如下,下列说法正确的是
2 2 3
A. 操作①、④均为过滤
B. 步骤②中发生了置换反应
C. 步骤③发生的反应为:NaHSO+NaOH=NaSO +HO
3 2 3 2
D. 亚硫酸钠粗品中不可能含有NaSO
2 4
23.应用连线
物质及其用途的连线
物质 用途
A.稀硫酸 a. 生产硫酸
B.氧化铁 b.除铁锈
C.过氧化钠 c.作红色颜料
D.二氧化硫 d.作供氧剂
E.碳酸氢钠 e. 作膨松剂F.亚铁盐 f. 作补铁剂
___________、___________、___________、 ___________、 ___________
24.阅读短文,回答问题。
燃放烟花爆竹是我国的传统习俗,烟花爆竹的主要成分有黑火药、特效药剂等。
黑火药由硝酸钾(KNO)、硫黄(S)和木炭组成,
3
燃烧时,瞬间产生大量气体,同时释放大量热,在有限的空间里,气体受热迅速膨胀引起爆炸。特效药剂
常含一些金属元素,燃烧时会产生五彩缤纷的火焰。(如右图所示)
下表为几种金属元素的化合物燃烧时的火焰颜色:
所含金属元素 钠 钙 钡 铯
火焰颜色 黄 砖红色 黄绿 蓝
然而,传统 的烟花爆竹不仅会污染环境,也会造成各种伤残及火灾事故。为了改善传统烟花爆竹的不足,
又能为人们的佳节祝兴,电子鞭炮应运而生。目前,常见的电子鞭炮有三种形式。
第一,雷电式仿真电子鞭炮,不仅能发出普通鞭炮的模拟声,而且还能发出闪光,以假乱真。无火药、无
污染,不会发生伤残及火灾事故。能重复使用,大大减少经济支出。其局限性是需要使用家用电源,不方
便移动。
第二,电子鞭炮机,是一种使用煤气和氧气混合气体作为燃料的设备,声响大,与火药鞭炮无异,但缺陷
是点燃混合气体时存在一定的安全隐患。
第三,录音鞭炮,通过音频解码播放存储于芯片中的鞭炮录音,声音与功率大小有关。这种鞭炮的优点是
纯电能、可移动、造价低廉。缺点是仿真和氛围感度稍差。
新型电子鞭炮正在不断地被研发出来,更好地促进民俗与科技的融合。
依据上文,回答问题:
(1)若燃放烟花的火焰呈现黄绿色,则烟花中可能含有______元素。(2)雷电式仿真电子鞭炮的优点有______(填序号)。
A.无火药、无污染
B.不会发生伤残及火灾事故
C.能重复使用,减少经济支出
(3)判断下列说法是否正确(填“对”或“错”)。
①燃放烟花爆竹时产生不同颜色的火焰,是因为药剂中含有不同的金属元素。______
②燃放烟花爆竹后会闻到刺激性的气味,是因为生成了二氧化碳。______
③电子鞭炮机在点燃混合气体时存在一定的安全隐患。______
④录音鞭炮的声音大小与功率无关。______
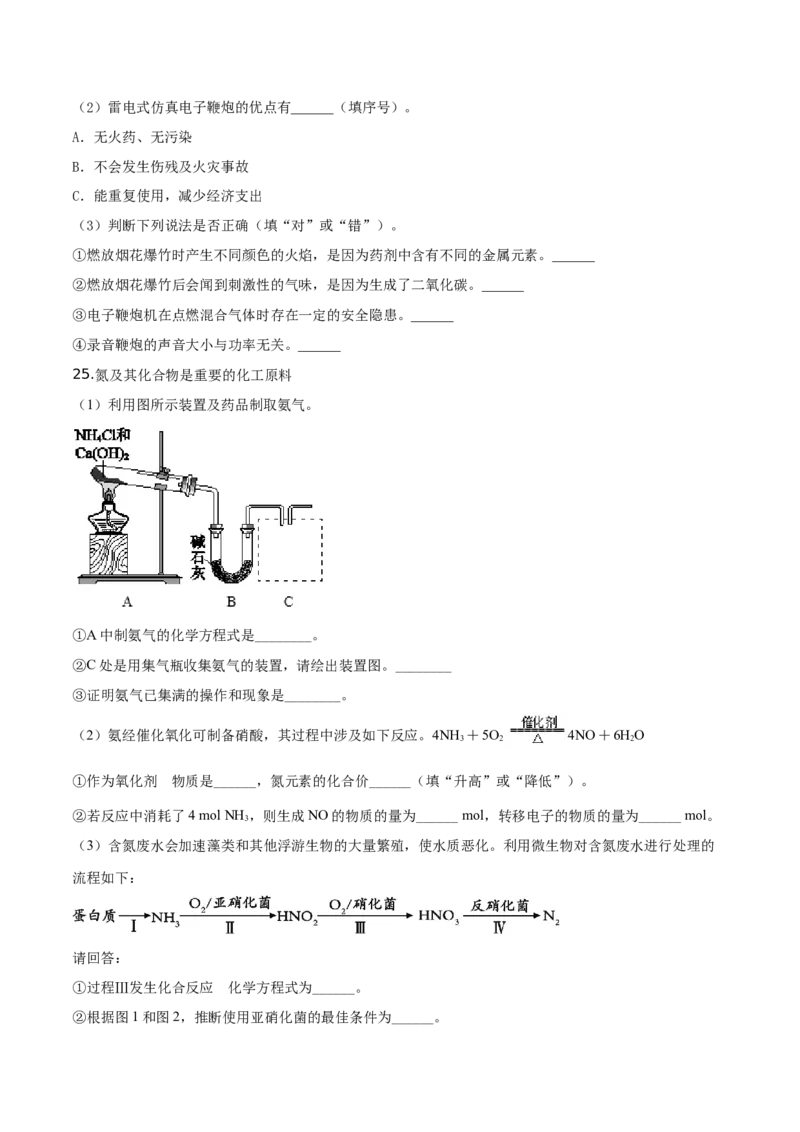
25.氮及其化合物是重要的化工原料
(1)利用图所示装置及药品制取氨气。
①A中制氨气的化学方程式是________。
②C处是用集气瓶收集氨气的装置,请绘出装置图。________
③证明氨气已集满的操作和现象是________。
(2)氨经催化氧化可制备硝酸,其过程中涉及如下反应。4NH +5O 4NO+6HO
3 2 2
①作为氧化剂 的物质是______,氮元素的化合价______(填“升高”或“降低”)。
②若反应中消耗了4 mol NH ,则生成NO的物质的量为______ mol,转移电子的物质的量为______ mol。
3
(3)含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的
流程如下:
请回答:
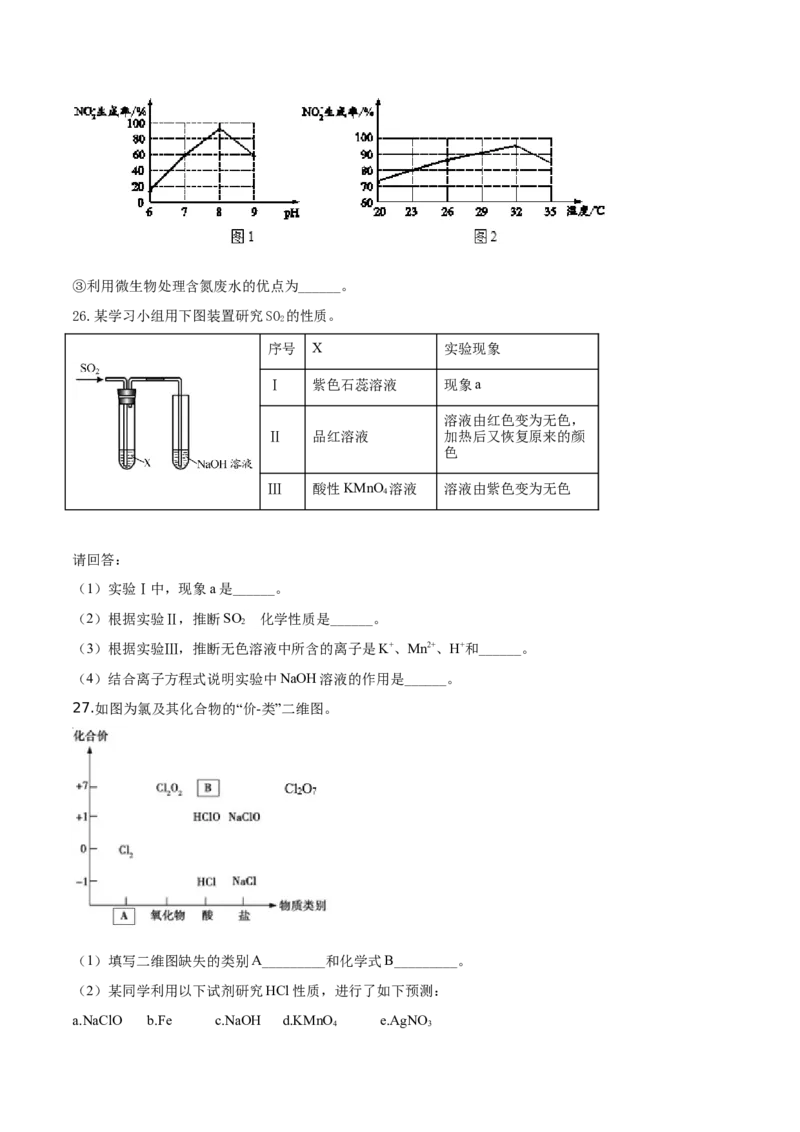
①过程Ⅲ发生化合反应 的化学方程式为______。
②根据图1和图2,推断使用亚硝化菌的最佳条件为______。③利用微生物处理含氮废水的优点为______。
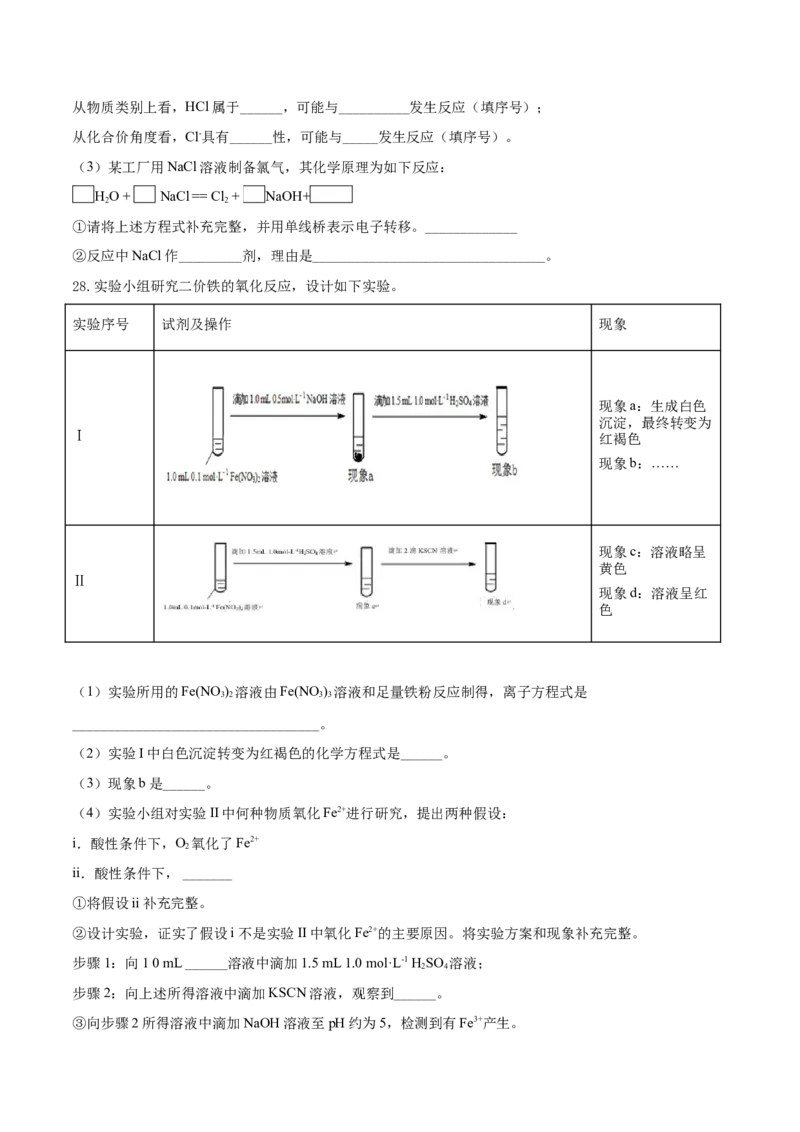
26.某学习小组用下图装置研究SO 的性质。
2
序号 X 实验现象
Ⅰ 紫色石蕊溶液 现象a
溶液由红色变为无色,
Ⅱ 品红溶液 加热后又恢复原来的颜
色
Ⅲ 酸性KMnO 溶液 溶液由紫色变为无色
4
请回答:
(1)实验Ⅰ中,现象a是______。
(2)根据实验Ⅱ,推断SO 的化学性质是______。
2
(3)根据实验Ⅲ,推断无色溶液中所含的离子是K+、Mn2+、H+和______。
(4)结合离子方程式说明实验中NaOH溶液的作用是______。
27.如图为氯及其化合物的“价-类”二维图。
(1)填写二维图缺失的类别A_________和化学式B_________。
(2)某同学利用以下试剂研究HCl性质,进行了如下预测:
a.NaClO b.Fe c.NaOH d.KMnO e.AgNO
4 3从物质类别上看,HCl属于______,可能与__________发生反应(填序号);
从化合价角度看,Cl-具有______性,可能与_____发生反应(填序号)。
(3)某工厂用NaCl溶液制备氯气,其化学原理为如下反应:
HO + NaCl== Cl + NaOH+
2 2
①请将上述方程式补充完整,并用单线桥表示电子转移。_____________
②反应中NaCl作_________剂,理由是_________________________________。
28.实验小组研究二价铁的氧化反应,设计如下实验。
实验序号 试剂及操作 现象
现象a:生成白色
沉淀,最终转变为
Ⅰ 红褐色
现象b:……
现象c:溶液略呈
黄色
Ⅱ
现象d:溶液呈红
色
(1)实验所用的Fe(NO ) 溶液由Fe(NO ) 溶液和足量铁粉反应制得,离子方程式是
3 2 3 3
___________________________________。
(2)实验I中白色沉淀转变为红褐色的化学方程式是______。
(3)现象b是______。
(4)实验小组对实验II中何种物质氧化Fe2+进行研究,提出两种假设:
i.酸性条件下,O 氧化了Fe2+
2
ii.酸性条件下, _______
①将假设ii补充完整。
②设计实验,证实了假设i 不是实验II中氧化Fe2+的主要原因。将实验方案和现象补充完整。
.
步骤1:向10 mL ______溶液中滴加1.5 mL 1.0 mol·L-1 H SO 溶液;
2 4
步骤2:向上述所得溶液中滴加KSCN溶液,观察到______。
③向步骤2所得溶液中滴加NaOH溶液至pH约为5,检测到有Fe3+产生。(5)综合上述实验,说明二价铁的氧化反应与______因素有关。