文档内容
2024 年秋期高中一年级期终质量评估
化学试题答案
题号 1 2 3 4 5 6 7 8 9 10
答案 C D C C D B B C A D
题号 11 12 13 14 15
答案 D D B A B
1.C
【详解】A.雾是一种气溶胶,能产生丁达尔效应,A 项正确;
B.SO 有还原性还能抑制葡萄酒中某些细菌的生长,葡萄酒中常添加一定量的 SO 用来抗
2 2
氧化和杀菌,B 项正确;
C.《天工开物》中有“凡石灰经火焚炼为用”,其中涉及的有碳酸钙的分解反应,没有化合价
的变化,不是氧化还原反应,C 项错误;
D.因为 Fe2+极易被氧化,而维生素 C 具有较强还原性,可防止二价铁被氧化,琥珀酸亚铁
缓释片与维生素 C 同服,可增强该药物的吸收,D 项正确;
答案选 C。
2.D
【详解】A.CO 和 NO 的相对分子质量都是 44,混合气体的平均摩尔质量为 44g/mol,A
2 2
不正确;
B.没有明确溶液体积,不能计算 0.5mol/L 的 AlCl 溶液中含有的 Cl-数目,B 错误;
3
C.没有温度和压强条件,30mLNH 和 60mLO 的物质的量关系不明,所含分子个数无法计
3 2
算,C 错误;
D.相同质量的 CO 和 CO 的物质的量之比为 44:28,所含原子个数比为(44×2):(28×3)
2
=22:21,D 正确;
1
学科网(北京)股份有限公司故选 D。
3.C
【详解】A.Cl 与水反应 Cl+H O HClO+HCl,盐酸为强酸,HClO 具有漂白性,因此氯
2 2 2
气遇到湿润的蓝色石蕊试纸,试纸先变红后褪色,故 A 说法正确;
B.浸有淀粉-KI 的试纸变蓝,发生离子方程式为 Cl+2I-=2Cl-+I ,反应中氯气表现强氧化性,
2 2
故 B 说法正确;
C.氯气将 Fe2+氧化成 Fe3+,Fe3+与 SCN-反应生成血红色 Fe(SCN) ,该过程中体现氯气的强
3
氧化性,故 C 说法错误;
D.氯水中含有 HClO,HClO 具有漂白性,湿润的红色布条褪色,体现氯水的漂白性,故 D
说法正确;
答案为 C。
4.C
【详解】根据氧化还原反应的电子得失守恒定律,KI 作还原剂失去电子, 、HNO、
3
、 作氧化剂得到电子,1mol 得电子形成 Cr3+得到 6mol e-,则可以产生 3mol
I;1mol HNO 得电子形成 NO,得到 3mol e-,可以产生 1.5mol I ;1mol 得电子形成
2 3 2
Mn2+得到 5mol e-,可以产生 2.5mol I ;1mol 得电子形成 I,得到 5mol e-,可以产生 2.5mol
2 2
I,由于该反应还原产物是 I,还原产物的 I 有 0.5mol,故该反应总共产生 3mol I ,即得到
2 2 2 2
I 由多到少的顺序为④=①>③>②,故 C 正确。
2
5.D
【详解】由氧化还原反应规律可知,还原性强于铜的铁会优先与硫酸铁溶液反应,所以在硫
酸铁溶液中同时加入铁粉和铜粉,若硫酸铁溶液过量,加入的铁粉和铜粉全部参加反应,不
会有剩余;若硫酸铁溶液不足量,加入的铁粉和铜粉可能都剩余,也可能是铁粉全部反应而
铜粉有剩余,但不可能是铜粉全部反应而铁粉有剩余,故选 D。
6.B
2
学科网(北京)股份有限公司【分析】二氧化硫是酸性氧化物,具有漂白性、还原性、氧化性。实验时,湿润的 pH 试纸
只变红色,不褪色;而鲜花、品红溶液;KMnO 溶液均褪色,NaS 溶液出现淡黄色 S 沉淀。
4 2
SO 是有毒气体,最后用 NaOH 溶液吸收尾气。
2
【详解】A.挤压注射器的活塞,试管①中发生反应 NaSO +H SO =Na SO +SO↑+H O,
2 3 2 4 2 4 2 2
硫酸中元素化合价不变,只体现硫酸的酸性,故 A 正确;
B.二氧化硫是酸性气体,实验时,湿润的 pH 试纸变红,但不褪色,故 B 错误;
C.湿润的 pH 试纸变红证明 SO 水溶液显酸性,NaS 溶液出现淡黄色沉淀证明 SO 具有氧
2 2 2
化性,KMnO 溶液均褪色证明二氧化硫具有还原性、品红褪色证明二氧化硫具有漂白性,
4
故 C 正确;
D.点燃酒精灯进行加热,褪色后的品红溶液又恢复红色,证明 SO 使品红溶液褪色具有可
2
逆性,故 D 正确;
选 B。
7.B
【详解】A.二氧化硫与酸性高锰酸钾反应,生成硫酸锰和硫酸:
,故 A 正确;
B.向 FeBr 溶液中通入足量氯气:2Fe2++4Br-+3Cl == 2Fe3++2Br +6Cl-
2 2 2
故 B 错误;
C. 酸性碘化钾溶液中滴加适量双氧水:2I-+2H++HO == I+2HO,故 C 正确;
2 2 2 2
D.向铜粉中滴加稀硝酸产生气体:3Cu+ +8H+== 3Cu2++2NO↑+4HO, 故 D 正
2
确;
故选 B。
8.C
【详解】A.制取 Fe(OH) 胶体应向沸水中加入饱和 FeCl 溶液,继续加热至溶液呈红褐色,
3 3
A 项错误;
3
学科网(北京)股份有限公司B.检验 ,应先加入盐酸,若无明显现象,再加入氯化钡溶液,B 项错误;
C.氨气极易溶于水,挤压胶头滴管后,可以形成红色喷泉,C 项正确;
D.氨气易溶于水,可用水吸收,但应用四氯化碳防倒吸,D 项错误;
答案选 C。
9.A
【分析】根据 N、S 原子结构及形成的物质化合价,可知 a 是 NH ,b 是 N,c 是 NO,d 是
3 2
NO ,e 是 HNO 或硝酸盐;a'是 HS,b'是 S,c'是 SO ,d'是 SO ,e'是亚硫酸或
2 3 2 2 3
亚硫酸盐;f'是硫酸或硫酸盐,然后根据问题分析解答。
【详解】A.根据上述分析可知:a 是 NH ,可以用湿润的红色石蕊试纸检验,A 错误;
3
B.a 是 NH ,c'是 SO ,二者在溶液中发生反应可能形成(NH )SO ,也可能形成 NH HSO
3 2 4 2 3 4 3
,或者生成二者的混合物,B 正确;
C.d 是 NO ,NO 与 HO 反应会产生 HNO;d'是 SO ,SO 与 HO 反应会产生 HSO 。
2 2 2 3 3 3 2 2 4
HSO 、HNO 都是强酸,C 正确;
2 4 3
D.在工业上制取 HSO 的一种途径,可以是 S 与 O 反应产生 SO ,SO 催化氧化产生 SO
2 4 2 2 2 3
,SO 与 HO 反应产生 HSO ,D 正确;
3 2 2 4
故合理选项是 A。
10.D
【详解】A.当铜丝与浓硫酸接触时才能反应,当往上抽动铜丝时,铜丝与硫酸不接触,反
应停止,可通过上下移动①中铜丝可控制 SO 的量,A 项正确;
2
B.该反应为 ,浓硫酸在该反应中表现了酸性和强
氧化性,氧化剂与还原剂的物质的量之比为 1:1,B 项正确;
C.SO 为酸性气体,具有污染性,可与碱发生反应,用 NaOH 溶液吸收多余的 SO ,C 项
2 2
正确;
D.铜与浓硫酸反应后①中溶液中混有剩余的浓硫酸,稀释时,应该将试管①中的溶液加入
4
学科网(北京)股份有限公司水中,玻璃棒不断搅拌,可以得到蓝色硫酸铜溶液,不能直接向反应后的溶液中加水,因浓
硫酸溶于水放出大量的热,会造成溶液四溅,发生危险,D 项错误;
答案选 D。
11.D
【详解】A.NH4
+
、Cu2+都能与 OH-反应,不能共存,A 错误;
B.SO23-、S2-都可以和 H
+
反应,且酸性条件下可以二者可以发生归中反应,不能共存,B
错误;
C.Fe2+、 NH4 都能与 OH-反应,不能共存;酸性条件下,Fe2+可被 NO3-氧化不能共
+
存,C 错误;
D. 、 、 Na+、 与 OH-及 H+ 都不反应,可以共存,D 正确;
故选 D。
12.D
【详解】A.过程Ⅰ、Ⅱ中,SO 中 S 元素化合价升高,SO 均发生氧化反应,故 A 正确;
2 2
B.根据图示过程Ⅱ中,二氧化硫被 Fe3+氧化为 ,发生反应的离子方程式为 2Fe3
++SO
2
+2H
2
O=2Fe2++ +4H+ ,故 B 正确;
C.根据图示,SO 最终转化成 ,故 C 正确;
2
D.Fe2+是该反应的催化剂,Fe3+是中间产物,故 D 错误;
答案选 D。
13.B
【详解】A.在室温下浓硝酸遇 Fe 时,浓硝酸会将 Fe 表面氧化,而在 Fe 表面产生一层致
密的氧化物保护膜而阻止金属进一步发生反应,因此不能看到产生 NO 红棕色气体,A 不
2
符合题意;
5
学科网(北京)股份有限公司B.二氧化硫水溶液具有还原性,酸性 KMnO 溶液具有强氧化性,酸性 KMnO 溶液能够将
4 4
SO 氧化而使溶液紫色褪色,因此会看到溶液紫色褪色,B 符合题意;
2
C.FeSO 溶液具有还原性,氯水具有强氧化性,二者混合会发生氧化还原反应产生 FeCl 、
4 3
Fe (SO ),使溶液变为黄色,而不是溶液褪色,C 不符合题意;
2 4 3
D.由于酸性:HCl>HSO ,所以将二氧化硫水溶液加入 BaCl 溶液,不能发生反应,因此
2 3 2
不能产生白色沉淀,D 不符合题意;
故合理选项是 B。
14.A
【详解】溶液为无色溶液肯定不含 Fe3+,向部分溶液中加入少量溴水,振荡,溶液呈无色,
说明溶液中一定含有还原性离子 ,不能确定是否存在 I-;由于 被溴水氧化生成
,则向①的溶液中加入过量 BaCl 溶液,产生不溶于稀硝酸的白色沉淀,不能确定是
2
否含有 ;向溶液加入少量溴水时,Br 被还原为 Br-,向①的溶液中加入过量 BaCl 溶
2 2
液时,引入了氯离子,则少量②的溶液滴入足量 AgNO 溶液,有溴化银沉淀和氯化银沉淀
3
生成,由电荷守恒可知,溶液中一定存在 K+ 。综上可知,溶液中一定存在 K+ 和 ,肯
定不存在 Fe3+,可能存在 I-和 ,A 项符合题意,答案选 A。
15.B
【解析】混合气体 100mL,通过浓硫酸洗气瓶气体减少了 30mL,氨气被吸收,则氨气体积
为 30mL;剩余气体通过过氧化钠,与二氧化碳反应:2CO+2Na O=2Na CO+O ,生成的
2 2 2 2 3 2
氧气与一氧化氮化合产生红棕色气体二氧化氮,再将该气体通入装满水的试管,最后无气体
剩余,4NO+ 3O+2H O= 4HNO ,由 CO 产生的 O 和 NO 应该按照 3:4 恰好完全反应才符
2 2 3 2 2
合题意,故 CO:NO=6:4,最简比 3:2(共 70mL),那么 CO 体积应为 42 mL,NO 体积应为
2 2
28 mL,则原混合气体中 NH 、NO、CO 气体的体积比为 15 14 21。
3 2
∶ ∶
答案选B。
II 卷 (方程式反应物生成物写正确没配平给 1 分,物质没写全 0 分)
6
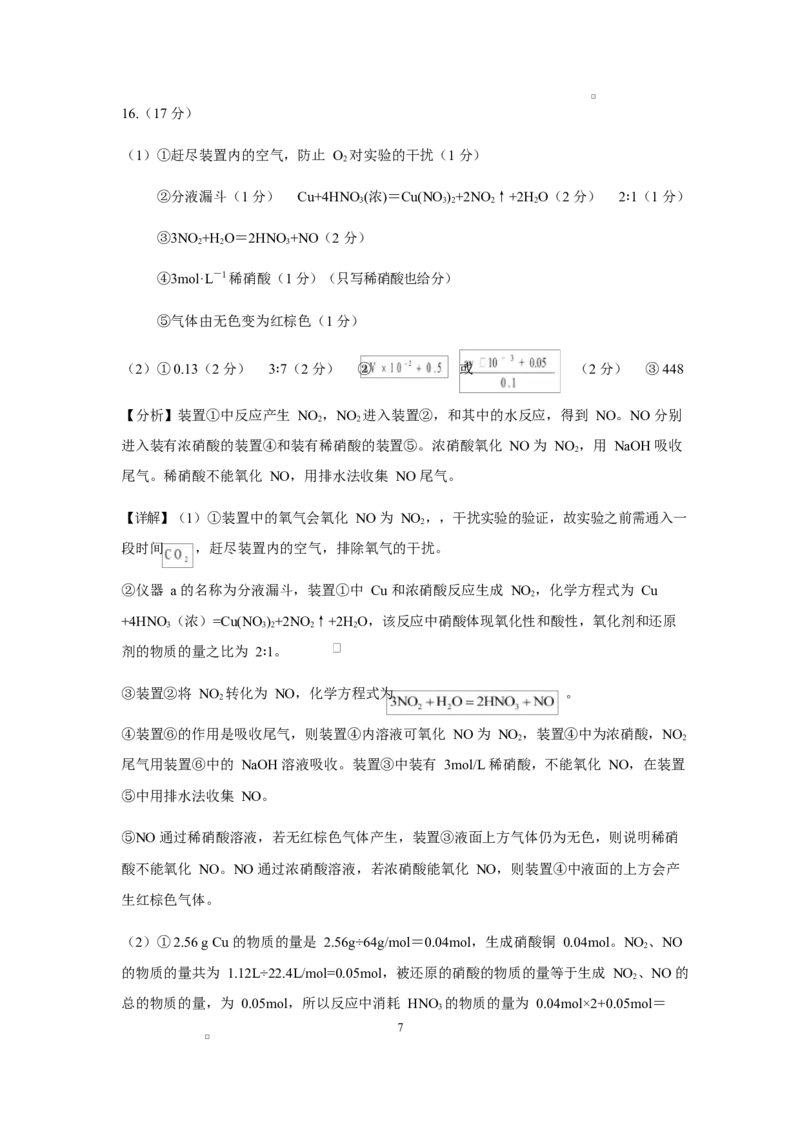
学科网(北京)股份有限公司16.(17 分)
(1)①赶尽装置内的空气,防止 O 对实验的干扰(1 分)
2
②分液漏斗(1 分) Cu+4HNO (浓)=Cu(NO )+2NO↑+2H O(2 分) 2 1(1 分)
3 3 2 2 2
∶
③3NO +H O=2HNO+NO(2 分)
2 2 3
④3mol·L-1 稀硝酸(1 分)(只写稀硝酸也给分)
⑤气体由无色变为红棕色(1 分)
(2)①0.13(2 分) 3 7(2 分) ② 或 (2 分) ③448
∶
【分析】装置①中反应产生 NO ,NO 进入装置②,和其中的水反应,得到 NO。NO 分别
2 2
进入装有浓硝酸的装置④和装有稀硝酸的装置⑤。浓硝酸氧化 NO 为 NO ,用 NaOH 吸收
2
尾气。稀硝酸不能氧化 NO,用排水法收集 NO 尾气。
【详解】(1)①装置中的氧气会氧化 NO 为 NO ,,干扰实验的验证,故实验之前需通入一
2
段时间 ,赶尽装置内的空气,排除氧气的干扰。
②仪器 a 的名称为分液漏斗,装置①中 Cu 和浓硝酸反应生成 NO ,化学方程式为 Cu
2
+4HNO (浓)=Cu(NO)+2NO↑+2H O,该反应中硝酸体现氧化性和酸性,氧化剂和还原
3 3 2 2 2
剂的物质的量之比为 2 1。
∶
③装置②将 NO 转化为 NO,化学方程式为 。
2
④装置⑥的作用是吸收尾气,则装置④内溶液可氧化 NO 为 NO ,装置④中为浓硝酸,NO
2 2
尾气用装置⑥中的 NaOH 溶液吸收。装置③中装有 3mol/L 稀硝酸,不能氧化 NO,在装置
⑤中用排水法收集 NO。
⑤NO 通过稀硝酸溶液,若无红棕色气体产生,装置③液面上方气体仍为无色,则说明稀硝
酸不能氧化 NO。NO 通过浓硝酸溶液,若浓硝酸能氧化 NO,则装置④中液面的上方会产
生红棕色气体。
(2)①2.56 g Cu 的物质的量是 2.56g÷64g/mol=0.04mol,生成硝酸铜 0.04mol。NO 、NO
2
的物质的量共为 1.12L÷22.4L/mol=0.05mol,被还原的硝酸的物质的量等于生成 NO 、NO 的
2
总的物质的量,为 0.05mol,所以反应中消耗 HNO 的物质的量为 0.04mol×2+0.05mol=
3
7
学科网(北京)股份有限公司0.13mol;设混合气体 NO 、NO 的物质的量分别是 xmol、ymol,则 x+y=0.05,依据电子
2
得失守恒可知 x+3y=0.04×2,解得 x=0.015、y=0.035,所以产生 NO 和 NO 的体积比为 3:
2
7;
②恰好使溶液中的 Cu2+全部转化成沉淀,溶液中的溶质是硝酸钠,物质的量等于氢氧化钠
的物质的量,为 0.001aVmol,根据氮原子守恒可知原硝酸的物质的量是 0.05mol
+0.001aVmol,则原硝酸溶液的浓度为 mol·L-1;
③欲使铜与硝酸反应生成的气体在 NaOH 溶液中全部转化为 NaNO ,则 NO 、NO 与氧气和
3 2
水完全反应生成硝酸,由此可得出硝酸与铜反应得到电子的物质的量应等于氧气氧化 NO 、
2
NO 生成硝酸得到电子的物质的量,等于铜失去电子的物质的量,则由电子守恒可得需要氧
气的物质的量是 0.08mol÷4=0.02mol,在标准状况下的体积为 0.02mol×22.4L/mol=0.448L
=448mL。
17.(1)干燥管(或球形干燥管)(1 分)
(2)NaOH 溶液(1 分) (3)③④①②(2 分) (4)D(1 分)
(5)吸收复合膨松剂分解产生的 HO 和 CO,便于准确测定 NH 的质量。(2 分)(合理即
2 2 3
可,若只回答吸收 CO 不给分)
2
(6)防止倒吸(1 分)
(7)①NH HCO NH ↑+H O↑+CO ↑(2 分) ②1 2(2 分)
4 3 3 2 2
∶
【分析】碳酸氢钠受热分解生成碳酸钠、二氧化碳、水,通过浓硫酸装置吸收水,碳酸氢铵
分解生成氨气、二氧化碳、水,通过装置 C 吸收水蒸气和氨气,通过碱石灰装置 D 吸收二
氧化碳,装置 E 盛有碱石灰可以排除空气中水和二氧化碳的干扰;使用装置 A 吸收空气中
二氧化碳,用空气排出滞留在装置中二氧化碳气体;
【详解】(1)由图可知,仪器 E 的名称为干燥管(或球形干燥管);
(2)空气中含有二氧化碳,则试剂 A 可以除去空气中的二氧化碳,则试管 A 中所装试剂是
NaOH 溶液;
(3)装置要连好后再测试(如气密性等),因此排除装置内的 需要连好装置后再通入空
8
学科网(北京)股份有限公司气。但本装置中的空气含有的 会影响测定结果,造成 U 形管吸收的 增加,会造成
测定结果偏大,因此需要先对已连接好的装置 A、B 和 C 通入一段时间的空气,排除后
再连接上装置 D、E,故答案为:③④①②;
(4)根据分析可知装置 D 的质量的变化为反应生成的二氧化碳的质量,故答案为 D;
(5)由第四问可知,装置 D 的作用为:吸收复合膨松剂分解产生的 HO 和 CO 气体,便
2 2
于准确测定 NH 的质量;
3
(6)②氨气易溶于水,则实验过程中必须持续通入空气的目的有:产生的 便于被浓硫
酸完全吸收;防止倒吸;
(7)①m(CO )=5.5g,n(CO)=0.125mol,m(NH )=1.7g,n(NH )=0.1mol,根据方程式
2 2 3 3
, ;
②可知 n( )=n(NH )=0.1mol,所以碳酸氢铵分解产生的二氧化碳为 0.1mol,所以碳
3
酸氢钠分解产生的 n(CO)=0.125mol-0.1mol=0.025mol,根据方程式可知,需要碳酸氢钠的物
2
质的量为 0.05mol,故碳酸氢钠和碳酸氢铵的物质的量之比为 1:2。
18.(1)Fe2+、Fe3+
(2)FeO+2H+=Fe2+ + H
2
O
(3)将 Fe2+全部氧化为 Fe3+
(4) 2Fe3+ + 3SO + 3Ba2+ +6OH-=2Fe(OH) ↓+ 3BaSO ↓ 2 : 1 b≥2a
3 4
(5) 5Fe2++MnO
4
-+8H+ =5Fe3++Mn2++4H
2
O
【分析】铁矿石主要成分是 FeO、Fe O,加入稀硫酸,FeO、Fe O 与稀硫酸反应生成
2 3 2 3
Fe2+、Fe3+,加入足量 HO,HO 将 Fe2+氧化成 Fe3+,据此分析;
2 2 2 2
(1) FeO、Fe O 为碱性氧化物,加入稀硫酸发生 FeO+HSO =FeSO+HO、Fe O+
2 3 2 4 4 2 2 3
3HSO =Fe (SO )+3HO,溶液 A 中所含金属阳离子有 Fe2+、Fe3+;故答案为 Fe2+、
2 4 2 4 3 2
Fe3+;
9
学科网(北京)股份有限公司(2)FeO 为碱性氧化物,与稀硫酸反应的离子方程式为 FeO+2H+=Fe2++HO;故答案为 FeO
2
+2H+=Fe2++HO;
2
(3)NH Fe(SO ) 中 Fe 的价态为+3 价,利用 HO 的氧化性将 Fe2+氧化成 Fe3+,故答案为
4 4 2 2 2
将 Fe2+全部氧化为 Fe3+;
(4)根据题意反应顺序是 Fe3++3OH-=Fe(OH) ↓、NH +OH-=NH·H O,当 a=b 时,OH
3 3 2
-不足,Fe3+过量,令 a=b=1,1molBa(OH) 能电离出 1molBa2+和 2molOH-,1molBa2+能
2
消耗 1molSO ,2molOH-消耗 molFe3+,因此离子方程式为 2Fe3++3SO +3Ba2++
6OH-=2Fe(OH) ↓+3BaSO↓;b=1.5a,令 a=1,b=1.5,1.5molBa(OH) 能电离产生 1.5molBa2
3 4 2
+和 3molOH-,3molOH-恰好与 1molFe3+完全反应,NH 物质的量为 1mol,1.5molBa2+
能与 1.5molSO 反应生成 BaSO,还剩下 0.5mol SO ,同一溶液物质的量之比等于物质的
4
量浓度之比,c(NH ) c(SO )=1 0.5=2 1;BaSO 的摩尔质量为 233g·mol-1,Fe(OH) 的摩
4 3
尔质量为 107g·mol-1∶,因此 Ba∶2+全部∶转化成沉淀时,沉淀的质量最大,因此有 b≥2a 时,
沉淀达到最大;故答案为 2Fe3++3SO +3Ba2++6OH-=2Fe(OH) ↓+3BaSO↓;2 1;b
3 4
≥2a。 ∶
(5) 写出溶液 A 中具有还原性的含铁离子是 Fe2+,与酸性 KMnO 溶液反应的离子方程式
4
5Fe2++MnO
4
-+8H+ =5Fe3++Mn2++4H
2
O
19.(1) 、
(2)取少量溶液于试管中,向其中加入过量稀盐酸,再滴加 溶液,如果产生白色沉淀,
证明混有 。
(3)
(4)
(5)
【详解】(1)由图 2 可知,M、N 分别代表+6 价的和-2 价的含硫元素的盐类物质,在图 1
中,对应的是 CaSO•2H O、NaSO •10H O 与 CuFeS;
4 2 2 4 2 2
10
学科网(北京)股份有限公司(2)NaSO 溶液易被空气中的氧气氧化为 NaSO ,实验室检验 NaSO 溶液是否变质的基
2 3 2 4 2 3
本操作是取少量溶液于试管中,向其中加入过量稀盐酸,再滴加 BaCl 溶液,如果产生白色
2
沉淀,证明混有 NaSO ;
2 4
(3)令 Cr 元素在产物中的化合价为 a 价,根据电子转移守恒,则:24×103L×0.05mol/L×(6-4)
=20×10-3L×0.02mol/L×2×(6-a),即还原产物为 Cr3+,根据电荷守恒与元素守恒,写出该反应
的离子方程式为: ;
(4) 中含有过氧键,在碱性条件下 溶液能将 氧化成 ,且反应后的溶
液滴入 溶液生成不溶于稀盐酸的白色沉淀,说明有硫酸根生成,根据电子守恒、电荷
守恒以及元素守恒可以写出该反应的离子方程式为:
;
(5)①As S 和 SnCl 在盐酸中反应转化为 As S 和 SnCl 并放出 HS 气体,则反应为 2As S
2 3 2 4 4 4 2 2 3
+2SnCl +4HCl=As S+2SnCl +2H S,故答案为:1:1;
2 4 4 4 2
②As S 中 As 为+2 价、S 为-2 价,且生成 As O,1molAs S(其中 As 元素的化合价为+2 价)
4 4 2 3 4 4
参加反应时,As 失去 4mol 电子,转移 28mole-,则 4molS 元素化合价从-2 价升高,一共升
高 6 价,则生成物化合价为+4 价,应为 SO ,转移 28mole-,消耗氧气 7mol。
2
11
学科网(北京)股份有限公司