文档内容
专题六 原子结构 元素周期侓 专题检验
选择题(20×5=100分)
1.(2022·四川省成都市高三检测)已知A、B、C、D、E是五种短周期主族元素,其原子半
径与原子序数的关系如图,且B、C、D原子最外层电子数之和等于D的质子数,D的
简单离子半径在同周期元素中最小,只有C与E同主族。下列说法错误的是
A.简单氢化物的沸点:C>E
B.简单离子的半径:D>C
C.A、B可形成多种二元化合物
D.电解熔融C、D形成化合物冶炼D的单质
【答案】B
【解析】同周期自左至右原子序数增大,原子半径减小,所以B、C为同一周期元素,D、
E为同一周期元素,A单独一个周期,且原子半径、序数最小,所以A为H元素;D的
简单离子半径在同周期元素中最小,D应为第三周期元素,所以D为Al元素;B、C、
D原子最外层电子数之和等于D的质子数,则B、C的最外层电子数之和为13-3=10,C
与E同主族,E的原子序数大于Al,则C、E的最外层电子数大于3,而C的最外层电
子数大于B,所以C的最外层电子数为6或7,而C为7时,B为3,此时B和Al同主
族,不符合题意,所以C的最外层电子数为6,B为4,所以C为O元素,B为碳元
素,E为S元素。
A项:C、E的简单氢化物分别为H O和H S,H O分子间存在氢键,沸点较高,A正确;
2 2 2
B项:D、C的简单离子半径分别为Al3+、O2-,二者电子层数相同,但O的核电荷数更小,
所以O2-的半径更大,B错误;
C项:H和C元素可以形成多种烃类,均为二元化合物,C正确;
D项:O和Al形成的化合物为氧化铝,电解熔融氧化铝可以得到铝单质,D正确;
综上所述答案为B。2.(2023届·湖南省益阳市高三质量检测)某化合物结构如图所示,其中X。Y、W、Z是原子
序数依次增大的短周期元素,且四种元素分布在三个周期,W的最外层电子数是Y的
最外层电子数的2倍,Z和X同主族。下列说法正确的是
A.W与Z形成的化合物中只含离子键
B.该化合物中Y都满足8电子稳定结构
C.X YW 是弱酸
3 3
D.离子半径:Z>W>Y
【答案】C
【解析】X、Y、W、Z是原子序数依次增大的短周期元素,且四种元素分布在三个周期,则
X为H元素;Z和X同主族,且Z的原子序数最大,则Z为Na元素;W的最外层电子
数是Y的最外层电子数的2倍,且Y能形成4个共价键,W能形成2个共价键,则Y为
B元素,W为O元素。
A项:O和Na可以形成化合物Na O ,含有离子键和共价键,A错误;
2 2
B项:Y为B元素,该结构中形成3个共价键的B原子最外层只有6个电子,B错误;
C项:X YW 即H BO ,为一种弱酸,C正确;
3 3 3 3
D项:电子层数越多离子半径越大,电子层数相同时,核电荷数越小半径越大,所以离子
半径O2->Na+,即W>Z,D错误;
答案为C。
3.(2022·陕西汉中·二模)一种矿石[YZX(XW)]的组成元素W、X、Y、Z为原子序数依次
3 2 5 4
增大的短周期元素,其中W、X、Z分别位于不同周期,Z核外最外层电子数是X核外电
子数的一半,1个WX分子含有10个电子。下列说法正确的是
2
A.原子半径:Y>Z>X>W
B.Y与X形成的化合物可与NaOH溶液反应C.简单氢化物的沸点:Z>X
D.Z的最高价氧化物不能与酸、碱反应
【答案】A
【解析】W、X、Y、Z为原子序数依次增大的短周期元素,其中W、X、Z分别位于不同周
期,则W为H元素;X位于第2周期,Z位于第3周期,1个WX分子含有10个电子,
2
则X为O元素;Z核外最外层电子数是X核外电子数的一半,Z最外层有4个电子,Z
为Si元素;矿石[YZX(XW)]的化学式为YSiO(OH),根据化合物中元素正负化合价
3 2 5 4 3 2 5 4
的代数和为0可知,Y显+2价,为Mg元素,然后根据物质的形状及元素周期律分析解
答。
根据分析可知,W为H,X为O,Y为Mg,Z为Si元素。
A项:同一周期元素,从左到右原子半径逐渐减小,同一主族,从上到下,原子半径逐渐
增大,则原子半径:Y>Z>X>W,A正确;
B项:X为O,Y为Mg元素,二者形成的化合物MgO是碱性氧化物,不能够与碱NaOH溶液发
生反应,B错误;
C项:X为O,Z为Si元素,二者的简单氢化物分别是HO、SiH,它们都属于分子晶体,分
2 4
子之间以微弱的分子间作用力结合,因此物质熔沸点都比较低,但HO分子之间除存
2
在分子间作用力外还存在氢键,增加了分子之间的吸引作用,导致HO的沸点比SiH
2 4
的高,故简单氢化物的沸点:Z<X,C错误;
D项:Z为Si元素,其最高价氧化物SiO 是酸性氧化物,能够与碱NaOH反应产生NaSiO
2 2 3
和HO,也能够与HF反应产生SiF、HO,D错误;
2 4 2
故合理选项是A。
4.(2022·辽宁沈阳·一模)X、Y、Z、W为原子序数依次增大的短周期主族元素。Y
的单质常温下为气体,W的单质可用于饮用水消毒。由X、Y、Z、W组成的某化合物
结构如图所示,分子中所有原子均达到8电子稳定结构。下列说法正确的是
A.原子半径:X>Y>ZB.氧化物对应的水化物的酸性:W>Y>X
C.氢元素与X、Y、Z均能形成两种或两种以上的二元化合物
D.Y的单质与镁反应的产物既含离子键、又含共价键
【答案】C
【解析】根据题意,W的单质可用于饮用水消毒,且形成1个共价键,则应是Cl元素;该
分子中所有原子均达到8电子稳定结构,Y可以形成3个共价键,则Y原子最外层应
有5个电子,其单质常温下为气体,则Y为N元素;X可以形成4个共价键,且原子
序数小于N元素,则X为C元素,Z可以形成2个共价键,原子序数大于N小于Cl,
则为O或S元素。
A项:若Z为S元素,则原子半径:S>C>N,A错误;
B项:最高价氧化物对应的水化物的酸性:W>Y>X,然题中没有注明“最高价”,无法比
较酸性强弱,B错误;
C项:H元素可以和C元素形成CH、C H 等多种烃类化合物,H元素可以和N元素形成
4 2 6
NH 、NH 等化合物,H元素可以和O元素形成HO、HO 两种化合物,可以和S元
3 2 4 2 2 2
素形成HS、HS 两种化合物,C正确;
2 2 2
D项:Y的单质为N,与Mg反应生成MgN,只含离子键,不含共价键,D错误;故选
2 3 2
C。
5.(2022·吉林延边·一模)短周期元素W、R、X、Y、Z原子序数依次增大,可形成甲、
乙两种具有强还原性的物质(结构如下图),基态X原子的2p能级上只有1个电子,Z
原子的最外层电子数与电子层数相同。下列说法中错误的是( )
甲: 乙:
A.W、R、Y在元素周期表中位于同一主族
B.甲、乙两物质中W都显-1价
C.电负性:Y<Z
D.Z元素最高价氧化物对应的水化物只能与酸反应,不能与碱反应
【答案】D
【解析】基态X原子的2p能级上只有1个电子,则X为B;Z原子的最外层电子数与电子
层数相同,且其原子序数比X大,则Z为Al;R、Y分别能形成R+、Y+,且R的原子
序数小于B,Y的原子序数在B和Al之间,故R为Li,Y为Na;W和B、Al分别构成两种阴离子[BW ]-和[AlW ]-,且W的原子序数比B小,则W为H;综上所述,W
4 4
为H,R为Li,X为B,Y为Na,Z为Al,甲为NaBH ,乙为LiAlH 。
4 4
A项:W为H,R为Li,Y为Na,三者均位于元素周期表中IA族,A正确;
B项:W为H,甲为NaBH ,乙为LiAlH ,两种物质中,H都显-1价,B正确;
4 4
C项:Y为Na,Z为Al,Al的非金属性比Na强,所以Al的电负性大于Na,C正确;
D项:Z为Al,其最高价氧化物对应的水化物Al(OH) ,是两性氢氧化物,既可以和酸反
3
应,也能与碱反应,D错误;故选D。
6.(2022·江西九江·一模)短周期主族元素X、Y、Z、W、R的原子序数依次增加,X、
Y、W位于不同周期,原子序数:3Y=Z+R,常温下X与Y可组成两种液态二元化合
物。某种缓冲溶液的主要成分结构如图。下列说法错误的是( )
A.R的最高价氧化物对应的水化物为强酸
B.简单氢化物的稳定性:YZ>W
【答案】A
【解析】短周期主族元素X、Y、Z、W、R的原子序数依次增加,X、Y、W位于不同周
期,常温下X与Y可组成两种液态二元化合物,则X为H元素、Y为O元素;由缓冲
溶液的主要成分结构中W为正一价阳离子、R形成5个共价键可知,W为Na元素、R
为P元素;由原子序数:3Y=Z+R可知,Z为F元素。
A项:磷元素的最高价氧化物对应的水化物磷酸为中强酸,故A错误;
B项:元素的非金属性越强,简单氢化物的稳定性越强,氧元素的非金属性弱于氟元素,
所以水的稳定性弱于氟化氢,故B正确;
C项:过氧化氢和过氧化钠都具有强氧化性,都是具有漂白性的化合物,故C正确;
D项:电子层结构相同的离子,核电荷数越大,离子半径越小,所以简单离子的离子半径
为O2—>F—>Na+,故D正确;故选A。
7.(2022·河南商丘·三模)2021年,英国剑桥大学Dominic S.Wright课题组设计了一种新型电池中电解质(结构如图所示)的合成路线。已知X、Y、Z为原子序数依次增大的短
周期主族元素,三者的核外电子数之和等于35,Y与Z位于同一周期,则下列说法正
确的是
A.简单离子的半径:X>Y
B.Z的最高价氧化物对应水化物是强酸
C.工业上常采用电解Y的氧化物冶炼单质Y
D.该化合物阴离子中各原子均满足8电子稳定结构
【答案】A
【解析】X、Y、Z为原子序数依次增大的短周期主族元素,三者的核外电子数之和等于
35,Y与Z位于同一周期,从结构图Z形成6个共价键,X为1价,若X为H,Y为Li,
Z为31号,不合理,若X为H,Y为Na,则Z为23号元素,不合理,若X为F,Y为
Na,Z为35-9-11=15,Z为P。
A项: F-、Na+电子层结构相同,核电荷大的半径小,简单离子的半径:F->Na+,故A正
确;
B项: Z的最高价氧化物对应水化物H PO 是弱酸,故B错误;
3 4
C项: 工业上常采用电解熔融氯化钠冶炼单质钠,故C错误;
D项: 该化合物阴离子中F原子满足8电子稳定结构,但P最外层有12个电子,故D错
误;
故选A。
8.(2022·四川省成都市一模)麻黄素是中枢神经兴奋剂,结构式如图。其组成元素Y、X、
W、Z为原子序数依次增大的前两周期主族元素。下列说法正确的是( )A.Y、W、Z三元素形成的化合物一定能抑制水的电离
B.氢化物沸点:Z>W>X
C.X、W、Z分别与Y 均可形成既含极性键又含非极性键的化合物
D.X与钙形成的化合物的电子式:
【答案】C
【解析】由麻黄素的结构式可知,Y周围只形成了1个共价键,X周围形成了4个共价
键,W周围形成了3个发共价键,Z周围形成了2个共价键,且组成元素Y、X、W、
Z为原子序数依次增大的前两周期主族元素,则可知Y为H、X为C、W为N、Z为
O。
A项:Y、W、Z三元素分别为H、N、O,则三种元素形成的化合物不一定能抑制水的电
离,如NH NO ,NH NO 由于NH +发生水解而促进水的电离,NH ·H O由于电离出的
4 3 4 2 4 3 2
OH-而抑制水的电离,A错误;
B项:Z、W、X为O、N、C,由于C的氢化物种类很多,沸点相差较大,则氢化物沸点
大小无法比较,B错误;
C项:X、W、Z分别为C、N、O与Y即 H均可形成既含极性键又含非极性键的化合物如
CHCH、CH=CH 、NH、HO 等,C正确;
3 3 2 2 2 4 2 2
D项:X即C与钙形成的化合物即CaC ,则其电子式为: ,D错误;故
2
选C。
9.(2022·江西南昌·一模)物质M可用作调味剂、乳化剂、抗氧化增效剂、吸湿剂、pH调
节剂、增香剂、缓冲剂,其结构式如图所示。M的组成元素X、Y、Z、Q为原子序数依
次增大的短周期主族元素,且Y的一种核素常用于检测文物的年代。下列说法错误的是( )
A.物质M与稀硫酸反应生成的一种化合物中含有两种官能团
B.Y与Z分别形成的简单氢化物的沸点:Z>Y
C.Z、Q两种元素的简单离子半径:Q>Z
D.Y、Z两种元素形成化合物时,Z总显负价,说明非金属性:Z>Y
【答案】C
【解析】M的组成元素X、Y、Z、Q为原子序数依次增大的短周期主族元素,且Y的一种核
素常用于检测文物的年代,可知Y为C元素;结合M中X形成1个共价单键,且X的原
子序数最小,可知X为H元素;Z形成2个共价键,Z为O元素;Q可形成带1个单位
正电荷的阳离子,结合原子序数可知Q为Na元素,根据上述分析可知:X为H、Y为
C、Z为O、Q为Na元素。
A项:物质M与稀硫酸反应生成的有机物为CHCHOHCOOH,分子物质中含羟基、羧基两种官
3
能团,A正确;
B项:Y为C、Z为O,元素的非金属性:O>C,元素的非金属性越强,其简单氢化物的稳定
性就越强,所以Y与Z分别形成的简单氢化物的沸点:Z>Y,B正确;
C项:Z为O、Q为Na,二者形成的简单离子O2-、Na+核外电子排布都是2、8,离子的核外
电子层结构相同,离子的核电荷数越大,离子半径就越小,所以离子半径:Q<Z,C
错误;
D项:Y为C、Z为O,二者都是非金属元素,原子之间通过共价键结合形成化合物。元素非
金属性越强,在形成化合物时,共用电子对就偏向吸引电子能力强的O元素,该元素
化合价就显负价,吸引电子能力弱的形成化合物时元素显正价,因此可根据Y、Z两种
元素形成化合物时,Z总显负价,判断元素的非金属性:Z>Y,D正确;故选C。
10.(2022·陕西西安·二模)有一种化合物是很多表面涂层的重要成分,其结构如图所示.
其中W、X、Y、Z为原子序数依次增大的短周期元素,只有X、Y在同一周期,Z的
单质是黄绿色气体;下列有关说法不正确的是( )A.非金属性强弱比较:Y>X
B.XW 的沸点高于WY的沸点
4 2
C.X的含氧酸有一元弱酸、二元弱酸等
D.ZY中所有原子最外层都满足8电子结构
2
【答案】B
【解析】根据题意,W、X、Y、Z为原子序数依次增大的短周期元素,Z的单质是黄绿色
气体,Z为氯;只有X、Y在同一周期, 则W为氢,位于第一周期,XY位于第二周
期;由结构可知,XY形成共价键数分别为4、2,则XY分别为碳、氧。
A项:同周期从左到右,金属性减弱,非金属性变强,非金属性强弱比较:Y>X,A正
确;
B项:氧电负性较强,水分子中可以形成氢键,故CH 的沸点低于HO的沸点,B错误;
4 2
C项:碳的含氧酸有一元弱酸醋酸、二元弱酸碳酸等,C正确;
D项:ClO 中氯、氧原子的最外层都满足8电子结构,D正确;故选B。
2
11.(2022·浙江省稽阳联谊学校高三下学期4月联考)短周期元素X、Y、Z、W的原子序数依
次增大,X的单质是空气中含量最高的气体,Y原子最外层电子数是内层电子数的3
倍,短周期主族元素中Z原子的半径最大,W原子的最外层电子数等于X、Y、Z原子的
最外层电子数的平均值。下列推断错误的是
A.X、Y、Z、W四种元素最多组成两种正盐
B.Z对应的氢化物中存在离子键
C.简单离子半径X>Z
D.最高价氧化物对应水化物的酸性X>W
【答案】A
【解析】由题干信息可知,短周期元素X、Y、Z、W的原子序数依次增大,X的单质是空气
中含量最高的气体,则X为N,Y原子最外层电子数是内层电子数的3倍,则Y为O,
短周期主族元素中Z原子的半径最大,则Z为Na,W原子的最外层电子数等于X、Y、Z
原子的最外层电子数的平均值,即W的最外层上电子数为4,则W为Si,据此分析解题。
A项:由分析可知,X、Y、Z、W分别为N、O、Na、Si,则四种元素可组成NaNO、NaNO、
2 3
NaSiO 等正盐,A错误;
2 3
B项:由分析可知,Z为Na,则Z对应的氢化物即NaH中存在离子键,B正确;
C项:由分析可知,X为N,Z为Na,N3-和Na+具有相同的核外电子排布,核电荷数越大微
粒半径越小,则简单离子半径N3->Na+即X>Z,C正确;
D项:已知N的非金属性比Si的强,则最高价氧化物对应水化物的酸性HNO>HSiO 即X>
3 2 3
W,D正确;
故答案为:A。
12.(2022·吉林长春·三模)主族元素W、X、Y、Z的原子序数依次增大,且均不大于
20, W与Y原子的最外层电子数之和等于X原子的最外层电子数。这四种元素形成的
一种食品添加剂的结构如图所示。下列说法正确的是
A.原子半径: WY>Q B.简单氢化物的沸点:W>E>Z>Y
C.简单离子半径:Q>E>W>Z D.Z、W组成的化合物共有三种
【答案】B
【解析】X、Y、Z、W、E、Q均为短周期主族非金属元素,且原子序数依次增大,由离子液
体的结构式可知,X和E原子形成1个共价键、Y原子形成4个共价键、Z原子形成3
个共价键、W原子形成2个共价键、Q原子形成6个共价键,则X为H元素、Y为C元
素、Z为N元素、W为O元素、E为F元素、Q为S元素。
A项:元素的非金属性越强,最高价氧化物对应水化物的酸性越强,硫元素的非金属性强
于碳元素,则硫酸的酸性强于碳酸,故A错误;
B项:氟化氢和水都能形成分子间氢键,水分子形成氢键的数目多于氟化氢,分子间作用
力强于氟化氢,沸点高于氟化氢,氨气可以形成分子间氢键,但是作用力较弱,故其
沸点比氟化氢低,甲烷不能形成分子间氢键,沸点最低,故简单氢化物的沸点:
W>E>Z>Y,故B正确;
C项:电子层结构相同的离子,核电荷数越大,离子的离子半径越小,则电子层结构相同
的氮离子、氧离子和氟离子中,氮离子的离子半径最大,故C错误;D项:由分析可知Z为N元素、W为O元素,它们之间形成化合物有一氧化二氮(NO)、一氧
2
化氮(NO)、二氧化氮(NO)、三氧化二氮(NO)、四氧化二氮(NO)和五氧化二氮(NO)
2 2 3 2 4 2 5
等,故D错误;
故选B。
15.(2022·山西临汾·三模)中国地质科学院地质研究所对嫦娥五号月球玄武岩开展了
年代学、元素、同位素分析,证明月球在19.6亿年前仍存在岩浆活动。X、Y、Z、V、
W 是月核中含有的五种原子序数依次增大的前20号元素,X原子的最外层电子数是其
电子总数的 ,V的单质常在地球火山口附近沉积, Y的氧化物常用作耐高温材料,
Y、W原子的最外层电子数相等且之和等于Z原子的最外层电子数,下列说法正确的是
A.Y的氧化物是两性氧化物
B.最高价含氧酸的酸性:X>V>Z
C.简单离子半径:W>V>Y
D.X、Z形成的化合物是制备玻璃的原料之一
【答案】D
【解析】X原子的最外层电子数是其电子总数的 ,若电子总数是4,最外层电子数为3,
不符合,若电子总数是8,最外层电子数为6,排布为2、6,则X是O元素;V单质常
在火山口附近沉积,则V为S元素;Y的氧化物常用作耐高温材料,氧化镁因为其熔点
高常用作耐火材料,则Y为Mg元素; Y、W原子的最外层电子数相等且之和等于Z原
子的最外层电子数,Y最外层电子数是2,W原子序数比S大,Z在Mg和S之间,则W
最外层电子数不可能为7,若W为K时Z为Al元素,若W为Ca时Z为Si元素;
根据分析知,X是O,Y为Mg,V为S,若Z为Al时W为K,若Z为Si时W为Ca;
A项:Y为Mg,MgO只能与酸反应生成正盐和水,属于碱性氧化物,A错误;
B项:X是O,没有最高正价,不存在最高价含氧酸,B错误;
C项:电子层数越多离子半径越大,电子层数相同原子序数越大半径越小,则
V(S2-)>W(K+或Ca2+)> Y(Mg2+),C错误;
D项:X是O,Z为Si,形成的化合物SiO,制玻璃的原料:石灰石、纯碱、二氧化硅,则
2
SiO 制备玻璃的原料之一,D正确;
2
故选:D。
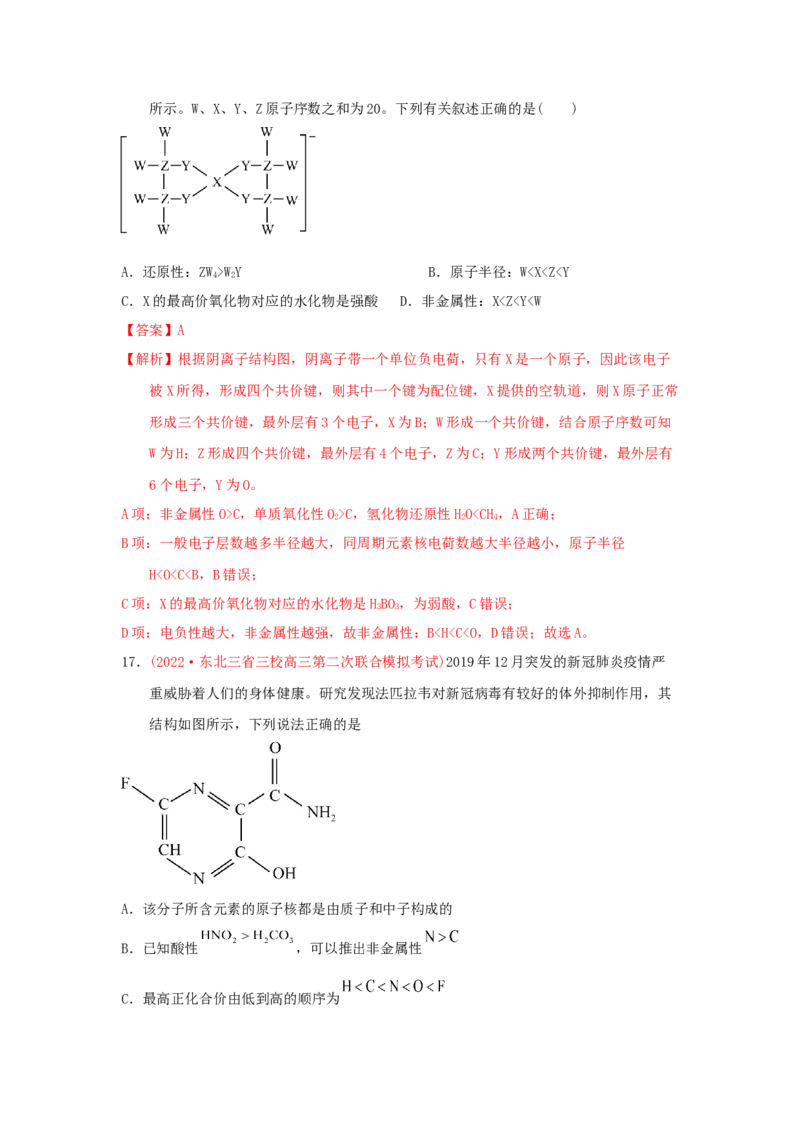
16.(2022·山西太原·二模)一种由短周期主族元素组成的化合物,其阴离子结构如图所示。W、X、Y、Z原子序数之和为20。下列有关叙述正确的是( )
A.还原性:ZW>WY B.原子半径:WC,单质氧化性O>C,氢化物还原性HOW
C.该物质具有强氧化性,可以用作漂白剂
D.该物质中,Y、X原子的最外层均满足8电子结构
【答案】A
【解析】W、Y、Z属于不同周期、不同主族的短周期元素,说明有一种元素为H,根据图示
结构可知,W形成+2价阳离子,X形成2个共价键,Z形成1个共价键,则Z为H元
素,W位于IIA族,X位于VIA族,W、X对应的简单离子核外电子排布相同,则W为
Mg,X为O元素,W、Y、Z的最外层电子数之和等于X的核外层电子数,Y的最外层电
子数为6-2-1=3,Y与H、Mg不同周期,则 Y为B元素,据此解答。A项:由分析可知, Y为B元素,原子序数为5,位于第二周期IIIA族,故A错误;
B项:由分析可知, X为O元素,W为Mg元素,电子层数相同时,核电荷数越大离子半径
越小,则离子半径X>W,故B正确;
C项:该物质中含有O-O键,具有强氧化性,可以用作漂白剂,故C正确;
D项:该化合物中O形成2个共价键,且有2个孤电子对,两个B都形成4个共价键且得两
个电子,则O、B原子均满足8电子稳定结构,故D正确;
故答案选A。
20.(2022·河南郑州·三模)某化合物可用作发酵助剂,结构如图所示。图中X、Y、
Z、W为元素周期表中前20号元素,且位于不同周期,它们的原子序数依次增大,其
中Y为地壳中含量最高的元素。下列有关说法正确的是
A.该化合物中除X外,其他原子最外层不一定均为8
B.Z元素形成的单质均为白色固体
C.X分别与Y、Z、W形成的简单化合物中均含有共价键
D.Z的最高价氧化物的水化物的酸性强于硫酸
【答案】A
【解析】X、Y、Z、W为元素周期表中前20号元素,且位于不同周期,它们的原子序数依
次增大,其中Y为地壳中含量最高的元素,则X为H元素、Y为O元素;由化合物中Z
形成5个共价键可知,Z为P元素,所以W为K元素。
A项:由化合物的结构式可知,化合物中磷原子的最外层电子数为10,钾离子和氧原子的
最外层电子数为8,故A正确;
B项:红磷为磷元素形成的红色单质,故B错误;
C项:氢元素和钾元素形成的化合物氢化钾为离子化合物,故C错误;
D项:磷元素的最高价氧化物的水化物为磷酸,酸性弱于硫酸,故D错误;
故选A。