文档内容
专题突破卷 07 化学反应与能量
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.下列有关电化学知识的描述正确的是
A.锌、铜与稀硫酸组成的原电池,在工作过程中,电解质溶液的pH保持不变
B.用足量锌粒与稀硫酸反应制取 ,若要增大反应速率,可以滴入几滴 溶液
C.将铁、铜用导线连接后放入浓硝酸中组成原电池,铁作负极,铜作正极,其负极反应式为
D.燃料电池是利用燃料和氧化剂之间的氧化还原反应,将化学能转化为热能,然后再转化为电能的化学
电源
【答案】B
【详解】A.锌、铜与稀硫酸组成的原电池,在工作过程中,H+在正极上放电生成H,电解质溶液的pH
2
增大,A错误;
B.用足量锌粒与稀硫酸反应制取 ,滴入几滴 溶液,Zn与Cu2+发生置换反应,锌粒表面由Cu生
成,在稀硫酸形成原电池,能增大反应速率,B正确;
C.将铁、铜用导线连接后放入浓硝酸中组成原电池,常温下铁遇浓硝酸发生钝化,因此铜作负极,铁作
正极,其负极反应式为: ,C错误;
D.燃料电池是利用燃料和氧化剂之间的氧化还原反应,将化学能转化电能的化学电源,D错误;
故选B。
2.钢铁在中性条件下发生电化学腐蚀时,正极上的电极反应式为
A. B.
C. D.
【答案】B
【详解】钢铁在中性条件下发生电化学腐蚀时,正极上氧气得电子生成OH-,正极的电极反应式为O+4e
2
-+2HO=4OH-,B项正确。
2
答案选B。3.下列反应属于氧化还原反应,且能量变化如图所示的是
A.甲烷在空气中燃烧的反应 B.灼热的木炭与CO 反应
2
C.锌粒和稀硫酸反应 D.Ba(OH) ·8H O晶体与NH Cl晶体的反应
2 2 4
【答案】B
【分析】根据图像可知,反应物总能量小于生成物总能量,属于吸热反应。
【详解】A.甲烷在空气中燃烧属于放热反应,A不符合题意;
B.灼热的木炭与CO 反应生成CO,有化合价变化,是氧化还原反应且该反应吸热,B符合题意;
2
C.锌粒和稀硫酸是放热反应,C不符合题意;
D.Ba(OH) ·8H O晶体与NH Cl晶体的反应生成氯化钡、氨气和水,没有化合价的变化,是非氧化还原反
2 2 4
应,D不符合题意;
故选B。
4.X、Y、Z、M代表四种金属元素,金属X和Z用导线连接放入稀硫酸中时,Z极上有 放出;单质Z
可以从Y的盐溶液中置换出单质Y;又知 的氧化性强于 。则这四种金属的活动性由强到弱的顺序
为
A. B.
C. D.
【答案】A
【详解】金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出,所以X是负极,Z是正
极,故金属的活动性: ;单质Z可以从Y的盐溶液中置换出Y,说明金属的活动性: ; 离
子的氧化性强于 离子,所以金属的活动性 ;综上可知四种金属的活动性由强到弱的顺序为
,A项正确。
5.如图所示装置中,试管A、B中电极为多孔石墨电极,C、D为铂夹。断开 ,闭合 、 一段时间
后,A、B中气体的量之间的关系如图所示:下列说法正确的是
A.a为正极,b为负极
B.滤纸上紫红色液滴向C端移动
C.断开 、 ,闭合 ,A极电极反应式为
D.断开 、 ,闭合 ,水槽中溶液的pH增大
【答案】C
【详解】A.断开 ,闭合 、 ,水槽中电解氢氧化钾溶液,相当于电解水,总反应为
,结合题图试管中气体的量之间的关系可知,A中生成气体是氧气,A为阳极,B
中多孔石墨为阴极,阳极与电源正极相连,则a为负极,b为正极,故A错误;
B.滤纸上C为阴极,D为阳极,电解池中阴离子向阳极移动,显紫色的离子为 ,则紫红色液滴向D
端移动,故B错误;
C.断开 、 ,闭合 ,构成氢氧燃料电池,A中为氧气,A是正极,B中为氢气,B为负极,A极电
极反应式为 ,故C正确;
D.断开 、 ,闭合 ,构成氢氧燃料电池,电池总反应为 ,则溶液中水增多,氢氧
根离子的浓度减小,溶液的碱性减弱,pH减小,故D错误;
选C。
6.下列热化学方程式正确的是选
已知条件 热化学方程式
项
A H 的燃烧热为a kJ∙mol−1 H(g)+Cl (g) 2HCl(g) ΔH=−a kJ∙mol−1
2 2 2
1molSO 、0.5molO 完全反应后,放出热
B 2 2 2SO (g)+O(g) 2SO (g) ΔH=−98.3 kJ∙mol−1
量98.3kJ 2 2 3
H+(aq)+OH-(aq)=HO(l) ΔH=−57.3 HSO (aq)+Ba(OH)(aq)=BaSO(s)+2HO(l) ΔH=−114.6
C 2 2 4 2 4 2
kJ∙mol−1 kJ∙mol−1
D 31g白磷比31g红磷能量多bkJ P(白磷,s) = 4P(红磷,s) ΔH=−4b kJ∙mol−1
4
A.A B.B C.C D.D
【答案】D
【详解】A.燃烧热是指1mol可燃物完全燃烧生成稳定氧化物所释放的热量,应是1mol气态H 和气态O
2 2
反应生成1mol液态水放出的热量,故A错误;
B.根据1molSO 、0.5molO 完全反应后,放出热量98.3kJ可知,则2molSO 、1molO 完全反应后,放出
2 2 2 2
热量196.6kJ,因此2SO (g)+O(g) 2SO (g) ΔH=−196.6 kJ∙mol−1,故B错误;
2 2 3
C.根据H+(aq)+OH-(aq)=HO(l) ΔH=−57.3 kJ∙mol−1,生成BaSO 沉淀,放出的热量大于114.6 kJ ,故
2 4
HSO (aq)+Ba(OH)(aq)=BaSO(s)+2HO(l) ΔH<−114.6 kJ∙mol−1,故C错误;
2 4 2 4 2
D.根据31g即0.25mol白磷比31g即1mol红磷能量多bkJ,白磷转化为红磷会释放能量,1mol白磷固体
变为4mol红磷固体释放4bkJ的热量,因此P(白磷,s)=4P(红磷,s) ΔH=−4b kJ∙mol−1,故D正确。
4
综上所述,答案为D。
【点睛】无论化学反应是否可逆,热化学方程式中的反应热 Δ H 都表示反应进行到底 ( 完全转化 ) 时
的能量变化。
7.某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。下列叙述中不正确的是
A.a极是负极,该电极上发生氧化反应
B.b极反应式是O+4OH--4e-=2H O
2 2C.总反应方程式为2H+O =2H O
2 2 2
D.氢氧燃料电池是一种具有应用前景的绿色电源
【答案】B
【详解】A.a极通入氢气,氢气失电子发生氧化反应,a是负极,故A正确;
B.b极通入氧气,氧气得电子发生还原反应生成氢氧根离子,反应式是O+2H O +4e-=4OH-,故B错误;
2 2
C.氢氧燃料电池,总反应方程式为2H+O =2H O,故C正确;
2 2 2
D.氢氧燃料电池反应产物是水,氢氧燃料电池是一种具有应用前景的绿色电源,故D正确;
选B。
8.用惰性电极电解CuSO 和NaCl 的混合溶液,开始时阴极和阳极上分别析出的物质是
4
A.H 和Cl B.Cu和Cl C.H 和O D.Cu和O
2 2 2 2 2 2
【答案】B
【详解】根据电解原理,阳离子放电顺序是Cu2+>H+>Na+,阴离子放电顺序是Cl->OH-> ,所以开始
时阴极反应式Cu2++2e-=Cu,阳极反应式:2Cl--2e-=Cl↑,故选B。
2
9.下面有关电化学的图示,完全正确的是
A.Cu-Zn原电池 B.粗铜的精炼
C.铁片镀锌 D.验证NaCl溶液(含酚酞)电解产物【答案】D
【详解】A.在Cu-Zn原电池中,Zn电极可以被稀硫酸氧化,Zn作负极,Cu作正极,H 在正极产生,A
2
错误;
B.粗铜精炼时,粗铜作阳极,发生氧化反应生成Cu2+,精铜作阴极,CuSO 溶液作电解液,B错误;
4
C.电镀时,应待镀件铁片作阴极,镀层金属Zn作阳极,ZnCl 溶液作电解液,C错误;
2
D.电解NaCl溶液的装置中,碳棒作阳极,Cl-在阳极发生电极反应,生成Cl,可以将其通入碘化钾淀粉
2
溶液中,若溶液变蓝,即可证明此产物为Cl;阴极由溶液中的HO反应生成H 和OH-,可以将生成的气
2 2 2
体收集后点燃,以进行验证,D正确。
本题选D。
10.肼( )是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1mol化学键所需的能量
(kJ):N=N键为942、O=O键为500、N-N键为154,则断裂1molN-H键所需的能量是
A.194kJ B.391kJ C.516kJ D.658kJ
【答案】B
【详解】根据图中内容可知, ,化学反应的焓变等于产物的能量与反应
物能量的差值,旧键断裂吸收能量,新建形成释放能量,设断裂1molN-H键所需的能量为K,所以有
154+4K+500=2218;解得K=391;
故答案选B。11.双极膜亦称双极性膜,是特种离子交换膜,它是由阳离子交换膜和阴离子交换膜复合而成。双极膜内
层为水层,工作时水层中的HO解离成H+和OH-,并分别通过离子交换膜向两侧发生迁移。三碘甲烷
2
(CHI )又名碘仿,在医药和生物化学中用作防腐剂和消毒剂。电解法制取碘仿的工作原理如图所示,生成
3
三碘甲烷的反应原理为C HOH+5IO-=CHI + +2I-+OH-+2H O。下列说法正确的是
2 5 3 2
A.电极X连接直流电源的正极
B.电极Y上的主要反应为I--2e-+2OH-=IO-+H O
2
C.电解一段时间后,硫酸溶液浓度升高
D.每制备0.25mol三碘甲烷,理论上双极膜内解离90gHO
2
【答案】B
【详解】A.电极X上H+放电生成H,发生还原反应,该电极为阴极,应连接直流电源的负极,故A错
2
误;
B.电极M为阳极,电极上I-被氧化成IO-,电极反应式为I--2e-+2OH-=IO-+H O,故B正确;
2
C.电解过程中阴极区每消耗lmolH+,双极膜内就向阴极区转移lmolH+,所以硫酸浓度不变,故C错误;
D.每制备0.25mol三碘甲烷,需要消耗1.25mol IO-,导线上转移2.5mole-,分别有2.5molOH-和
2.5molH+移出双极膜,所以理论上双极膜内解离45gHO,故D错误;
2
故选B。
12.光催化微生物燃料电池的工作原理如图所示:已知:电极a在光激发条件下会产生电子(e-)—空穴(h+)。下列说法错误的是
A.电极电势:电极a>电极b
B.电极b发生的电极反应式为(C H O)-24e-+7H O=6CO↑+24H+
6 10 5 n 2 2
C.光激发时,光生电子会与O 结合,光生空穴会与电极b产生的电子结合
2
D.电池工作一段时间后,右侧溶液pH保持不变(不考虑CO 的溶解)
2
【答案】B
【详解】A.根据题图信息判断,(C H O) 在电极b上失电子,转化为CO,则电极b为负极,电极a为
6 10 5 n 2
正极,原电池中,正极的电极电势高于负极的电极电势,则电极电势:电a>电极b,故A正确;
B.根据得失电子守恒判断,电极b发生的电极反应式为(C H O)-24ne-+7nH O=6nCO↑+24nH+,故B错
6 10 5 n 2 2
误;
C.根据题图信息判断,电极a在光激发条件下会产生电子(e-)、空穴(h+),光生电子会与O 结合,光生空
2
穴会与电极b产生的电子结合,故C正确;
D.根据电极反应判断,每转移24nmol电子时,右侧溶液中生成24nmolH+,同时会有24n mol H+通过阳离
子交换膜移向左侧溶液,则右侧溶液的pH保持不变,故D正确;
故选B。
13.电解食盐水间接氧化法去除工业废水中氨氮的原理如图所示,通过电解氨氮溶液(含有少量的NaCl),
将 转化为 (无 逸出),下列说法正确的是A.M为负极 B.N极附近pH值不变化
C. D.电解后 上升
【答案】C
【分析】该装置为电解池装置,在M电极上氯离子失去电子生成氯气(无 Cl 逸出),然后氯气将氨氧化为
2
氮气,氯气又被还原为氯离子,在这过程中氯离子做了催化剂,M电极为阳极,阳极区的总反应为
;N电极为阴极,电极反应为2HO+2e-=H ↑+2OH-。
2 2
【详解】A.由分析可知,M电极为阳极,A错误;
B.由分析可知,N电极为阴极,电极反应为2HO+2e-=H ↑+2OH-,故该电极附近pH增大,B错误;
2 2
C.M电极为阳极,阳极区的总反应为 ,阴极的电极反应为2HO+2e-=H ↑+2OH-,根
2 2
据电路中电子转移守恒可知,生成的氢气更多,C正确;
D.由分析可知,在阳极上氯离子失去电子生成氯气,然后氯气又被氨还原为氯离子,电解后氯离子浓度
不可能上升,D错误;
故选C。
14.甲、乙、丙三个电解槽如图所示(其中电极的大小、形状、间距均相同)。乙、丙中AgNO 溶液浓度和
3
体积均相同,通电一段时间后,若甲中铜电极的质量增加0.128g,则乙中电极上银的质量增加
A.0.054g B.0.108g C.0.216g D.0.432g
【答案】C
【详解】甲中铜电极增重0.128g,说明析出铜为0.002mol。由图示可知,乙、丙并联后与甲串联,又因
乙、丙两槽中的电极反应相同,故乙、丙中的电子转移分别是甲中的一半。甲中转移电子为0.004mol,则
乙中转移的电子为0.002mol,故乙中析出的银为0.002mol,质量为 。故选
C。15.三碘甲烷( )又名碘仿,在医药和生物化学中用作防腐剂和消毒剂。电解法制取碘仿的工作原理如
图所示,其中电解液为KI、 的碱性溶液。已知反应中生成等物质的量的 与 。下列说法
错误的是
A.电极N连接直流电源的负极
B.电极M上的电极反应式为
C.阳极区发生反应的离子方程式为
D.电解一段时间后,电解液的pH减小
【答案】D
【分析】电极N上, 放电生成 ,发生还原反应,该电极为阴极,电极M为阳极。
【详解】A.电极N上, 放电生成 ,发生还原反应,该电极为阴极,应连接直流电源的负极,A正
确;
B.电极M为阳极,电极上 被氧化成 ,电极反应式为 ,B正确;
C.阳极生成的 将 氧化成 和 ,配平可得反应的离子方程式为
,C正确;
D.该电解池工作的总反应为 ,反应中生成 ,则电解一段时间后,电解液的pH增大,D错误;
故选D。
二、填空题(本题包括4小题,共55分)
16.(12分)回答下列问题:
(1)已知 和 反应生成1mol 过程中能量变化如图所示。根据下列已知键能数据计算A—B
键键能为 kJ/mol。
化学键 B—B
键能(kJ/mol) 946 436
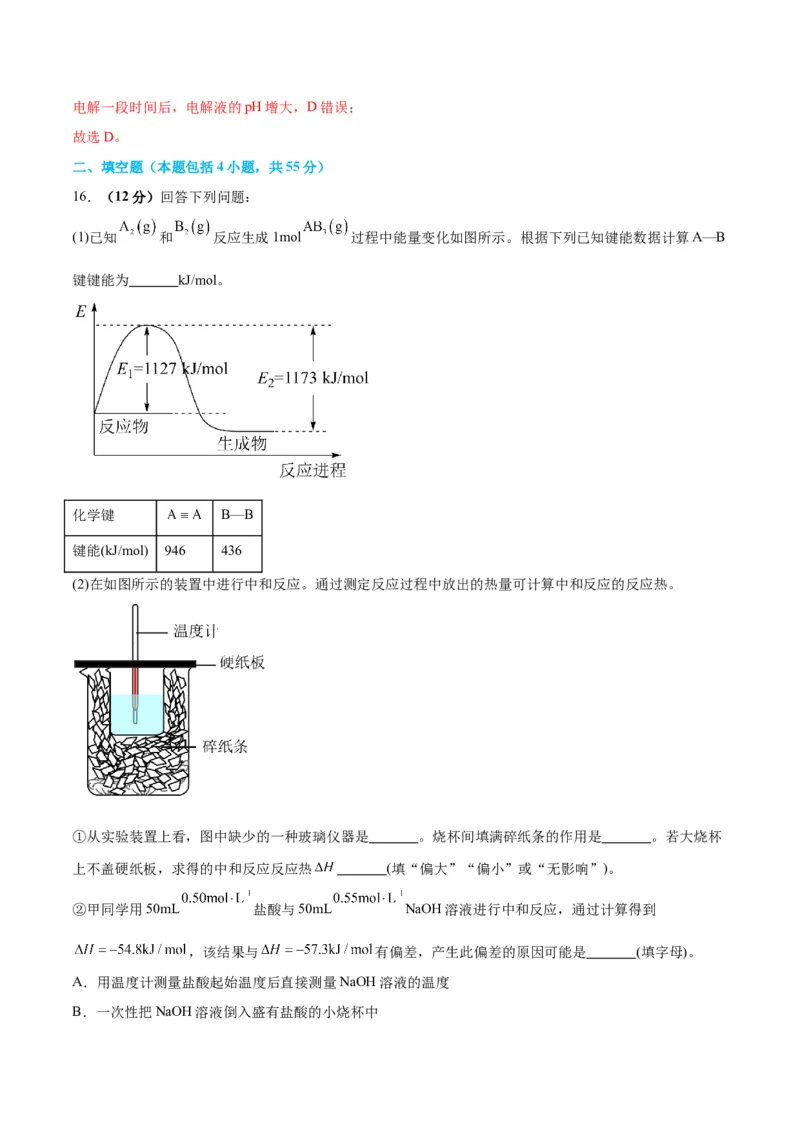
(2)在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和反应的反应热。
①从实验装置上看,图中缺少的一种玻璃仪器是 。烧杯间填满碎纸条的作用是 。若大烧杯
上不盖硬纸板,求得的中和反应反应热 (填“偏大”“偏小”或“无影响”)。
②甲同学用50mL 盐酸与50mL NaOH溶液进行中和反应,通过计算得到
,该结果与 有偏差,产生此偏差的原因可能是 (填字母)。
A.用温度计测量盐酸起始温度后直接测量NaOH溶液的温度
B.一次性把NaOH溶液倒入盛有盐酸的小烧杯中C.实验装置保温、隔热效果差
③若改用60mL 盐酸与60mL NaOH溶液进行反应,与②中实验相比,所放出的热量
(填“相等”或“不相等”);若用50mL 溶液代替盐酸进行②中实验,测得反应前后
温度的变化值 (填“偏大”“偏小”或“不受影响”)。
【答案】(1)391
(2) 环形玻璃搅拌器 保温(或隔热或减少实验过程中热量损失) 偏大 AC 不相等
偏小
【详解】(1)由题干图示信息可知, 为放热反应,
。设A—B键键能为x, 反应物的键能总和-生成
物的键能总和 , ,故答案为:391;
(2)①该实验装置是中和反应反应热的测定装置,图中缺少的一种玻璃仪器是环形玻璃搅拌器,为了减
少实验过程中热量损失,烧杯间填满碎纸条,若大烧杯上不盖硬纸板,会有热量散失,测得的中和反应反
应热的数值偏小, 偏大,故答案为:环形玻璃搅拌器;保温(或隔热或减少实验过程中热量损失);偏
大;
②用温度计测量盐酸起始温度后,没有冲洗、冷却温度计,直接测量NaOH溶液的温度导致测量温度偏
高,使得 偏小,求得的中和反应反应热 偏大,A符合题意;一次性把NaOH溶液倒入盛有盐酸的小
烧杯中,符合操作要求,B不符合题意;实验装置保温、隔热效果差,造成热量损失,使求得的中和反应
反应热 偏大,C符合题意,故答案为:AC;
③所放出的热量与反应物的物质的量有关,若改用60mL 盐酸与60mL NaOH溶液进
行反应,参加反应的HCI和NaOH的物质的量比②中实验的大,放出的热量比②中实验多;醋酸为弱酸,
电离要吸热,若用50mL 溶液代替②中盐酸进行实验,测得反应前后温度的变化值会
偏小,故答案为:不相等;偏小。
17.(15分)某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到
电流表的指针发生了偏转。请回答下列问题:
(1)甲池为 (填“原电池”“电解池”或“电镀池”),通入CHOH电极的电极反应式为 。
3
(2)乙池中A(石墨)电极的名称为 (填“正极”“负极”“阴极”或“阳极”),乙池总反应式为 。
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗O 的体积为 mL(标准状况下),丙池中 极析
2
出 g铜。
(4)若丙中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲中溶液的pH将 (填“增大”
“减小”或“不变”);丙中溶液的pH将 (填“增大”“减小”或“不变”)。
【答案】(1) 原电池 CHOH-6e-+8OH-=CO +6H O
3 2
(2) 阳极 4AgNO+2H O 4Ag+O↑+4HNO
3 2 2 3
(3) 280 D 1.60
(4) 减小 增大
【分析】由题干图示信息可知,甲池为甲醇燃料电池,通CHOH的一极为负极,电极反应为:
3
CHOH+8OH--6e-= +6H O,通O 的一极为正极,电极反应为:O+2H O+4e-=4OH-;乙池为电解池,石
3 2 2 2 2
墨电极A为阳极,电极反应为:2HO-4e-=4H++O ↑,Ag电极B为阴极,电极反应为:Ag++e-=Ag;丙池为
2 2
电解池,电极C为阳极,电极反应为:2Cl- -2e-=Cl↑,电极D为阴极,电极反应为:Cu2++2e-=Cu,据此分
2
析解题。
【详解】(1)①由分析可知,甲池为原电池;
②通入CHOH 电极的电极反应式为CHOH+8OH--6e-= +6H O;
3 3 2
(2)①由分析可知,乙池A(石墨)电极的名称为阳极;②电极反应为:2HO-4e-=4H++O ↑,Ag电极B为阴极,电极反应为:Ag++e-=Ag,则乙池中总反应式为:
2 2
4AgNO+2H O 4Ag+4HNO +O ↑;
3 2 3 2
(3)①由分析可知,当乙池中B极质量增加 5.40g ,即析出5.40g的Ag时,n(Ag)=
=0.05mol,则电路中转移的电子的物质的量为0.05mol,故甲池中理论上消耗 O 的体积为
2
=0.28L=280mL;
②丙池中阴极(即D极);
③析出铜的质量为 =1.60g;
(4)①若丙中电极不变,将其溶液换成 NaCl 溶液,电键闭合一段时间后,甲池为甲醇燃料电池,通
CHOH的一极为负极,电极反应为:CHOH+8OH--6e-= +6H O,通O 的一极为正极,电极反应为:
3 3 2 2
O+2H O+4e-=4OH-则溶液的 pH 将减小;
2 2
②若丙中电极不变,将其溶液换成 NaCl 溶液,电键闭合一段时间后,即用惰性电极电解NaCl溶液,丙
中D极即阴极,电极反应为:2HO+2e-=H ↑+2OH-,则阴极的产物为NaOH、H,由于生成了NaOH,则溶
2 2 2
液的 pH 将增大。
18.(14分)载人航天工程对科学研究及太空资源开发具有重要意义,其发展水平是衡量一个国家综合国
力的重要指标。中国正在逐步建立自己的载人空间站“天宫”,神舟十三号载人飞船在北京时间10月16
日0时23分点火发射,又一次正式踏上飞向浩渺星辰的征途。
(1)氢氧燃料电池(构造示意图如图)单位质量输出电能较高,反应生成的水可作为航天员的饮用水,氧气可
以作为备用氧源供给航天员呼吸。由此判断X极为电池的 极,OH-向 (填“正”或“负”)极作
定向移动,Y极的电极反应式为 。(2)“神舟”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。
①飞船在光照区运行时,太阳能电池帆板将 能转化为 能,除供给飞船使用外,多余部分用镉
镍蓄电池储存起来。其工作原理为:Cd+2NiOOH+2H O Cd(OH) +2Ni(OH) ,充电时,阳极的电极反应式
2 2 2
为 ;当飞船运行到地影区时,镉镍蓄电池开始为飞船供电,此时负极附近溶液的碱性 (填
“增强”“减弱”或“不变”)。
②紧急状况下,应急电池会自动启动,工作原理为Zn+Ag O+HO 2Ag+Zn(OH) ,其负极的电极反应式
2 2 2
为 。
【答案】(1) 负 负 O+2HO+4e-=4OH-
2 2
(2) 太阳 电 Ni(OH) -e-+OH-=NiOOH+H O 减弱 Zn-2e-+2OH-=Zn(OH)
2 2 2
【详解】(1)根据电子流向可知,X电极是电子流出的一极,由此判断X极为电池的负极,原电池中阴
离子向负极移动,则OH-向负极作定向移动,Y极是正极,氧气得到电子,电极反应式为O+2HO+4e-
2 2
=4OH-。
(2)①飞船在光照区运行时,太阳能电池帆板将太阳能转化为电能,除供给飞船使用外,多余部分用镉
镍蓄电池储存起来。其工作原理为Cd+2NiOOH+2H O Cd(OH) +2Ni(OH) ,充电时相当于是电解池,阳
2 2 2
极Ni失去电子,其电极反应式为Ni(OH) -e-+OH-=NiOOH+H O;当飞船运行到地影区时,镉镍蓄电池开
2 2
始为飞船供电,此时相当于是原电池,Cd失去电子结合氢氧根离子生成Cd(OH) ,因此负极附近溶液的碱
2
性减弱。
②紧急状况下,应急电池会自动启动,工作原理为Zn+Ag O+HO 2Ag+Zn(OH) ,其负极是Zn失去电
2 2 2
子,其电极反应式为Zn-2e-+2OH-=Zn(OH) 。
219.(14分)电解原理在化学工业中有广泛应用。
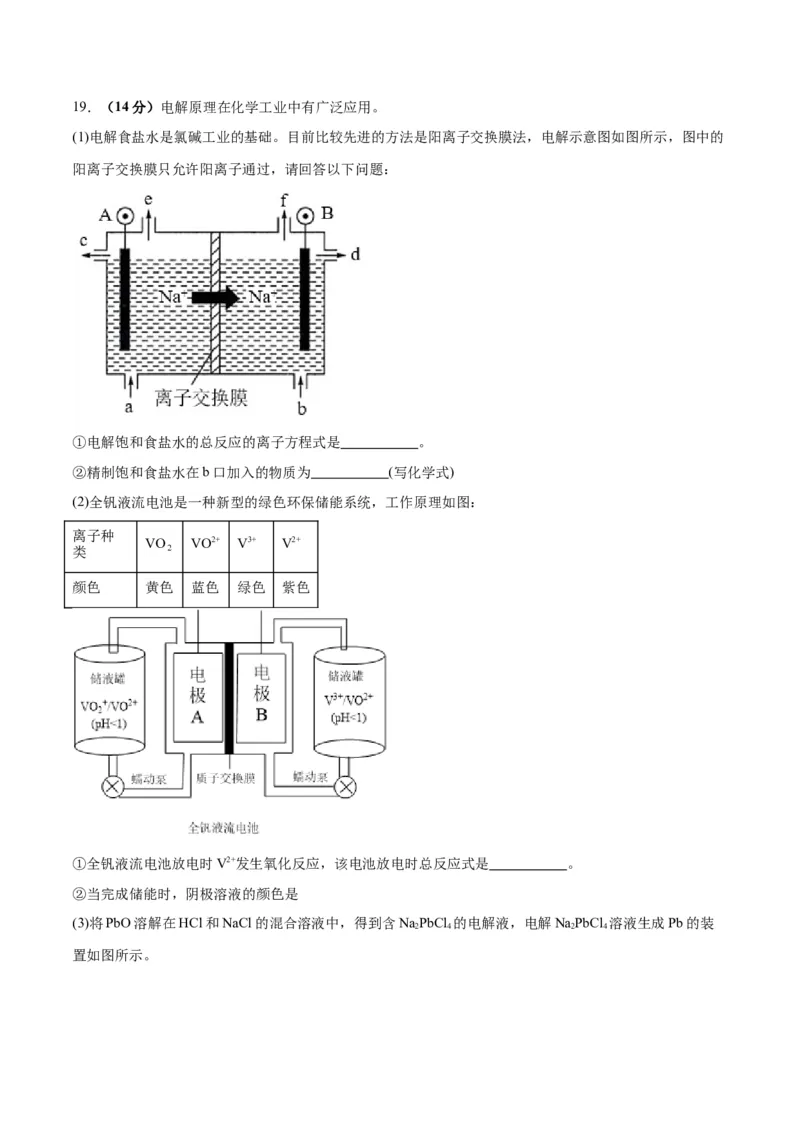
(1)电解食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的
阳离子交换膜只允许阳离子通过,请回答以下问题:
①电解饱和食盐水的总反应的离子方程式是 。
②精制饱和食盐水在b口加入的物质为 (写化学式)
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图:
离子种
VO VO2+ V3+ V2+
类
颜色 黄色 蓝色 绿色 紫色
①全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是 。
②当完成储能时,阴极溶液的颜色是
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含NaPbCl 的电解液,电解NaPbCl 溶液生成Pb的装
2 4 2 4
置如图所示。①写出电解时阴极的电极反应式
②电解过程中通过阳离子交换膜的离子主要为
③电解过程中,NaPbCl 电解液浓度不断减小,为了恢复其浓度,应该向 极室(填“阴”或者
2 4
“阳”)加入 (填化学式)。
【答案】(1) 2Cl-+2H O 2OH-+Cl↑+H ↑ NaOH
2 2 2
(2) V2++VO +2H+=V3++VO2++H O 紫色
2
(3) PbCl +2e−=Pb+4Cl− H+ 阴 PbO
【分析】由电解食盐水装置图可知,钠离子移向右边,则左边电极为阳极,右边电极为阴极,据此分析解
答;全钒液流电池放电时V2+发生氧化反应生成V3+,则 VO 离子发生还原反应生成VO2+,据此书写反应
的总方程式,电池储能时为电解池,电解的总反应为放电总反应的逆反应,据此分析解答;将PbO溶解在
HCl和NaCl的混合溶液中,得到含NaPbCl 的电解液,电解NaPbCl 溶液生成Pb,阴极发生还原反应生
2 4 2 4
成Pb,阳极发生氧化反应生成氧气,据此分析解答。
【详解】(1)①电解饱和食盐水总反应的离子方程式是2Cl-+2H O Cl ↑+H ↑+2OH-,故答案为:2Cl-
2 2 2
+2H O Cl ↑+H ↑+2OH-;
2 2 2②由电解食盐水的装置图可知,钠离子移向右边,则左边电极为阳极,A连接电源正极,电极反应式为
2Cl--2e-=Cl↑,所以精制饱和食盐水从图中a位置补充,右边电极为阴极,B连接电源负极,电极反应式为
2
2HO+2e-=H ↑+2OH- 或2H++2e-=H ↑,生成氢氧化钠从图中d位置流出,b口加入的物质是稀氢氧化钠溶
2 2 2
液,故答案为:NaOH;
(2)①全钒液流电池放电时V2+发生氧化反应,则 VO 离子发生还原反应,反应的总方程式为V2++VO
═V3++VO2++H O,故答案为:V2++VO +2H+=V3++VO2++H O;
2 2
②电池储能时为电解池,电解的总反应为V3++VO2++H O= V2++VO +2H+,阴极发生还原反应,阴极反应式
2
为V3++e-═V2+,阴极溶液颜色变为紫色,故答案为:紫色;
(3)①阴极发生还原反应,NaPbC1 被还原生成Pb,阴极反应式为PbCl +2e-=Pb+4Cl-,故答案为:PbCl
2 4
+2e-=Pb↓+4Cl-;
②电解时阳离子向阴极移动,通过阳离子交换膜的离子主要为氢离子,故答案为:H+;
③电解过程中,NaPbCl 在阴极发生还原反应,阴极发生还原反应生成Pb,阳极发生氧化反应生成氧气,
2 4
NaPbCl 浓度不断减小,为恢复浓度,则应在阴极加入PbO,溶解在HCl和NaCl的混合溶液中,得到含
2 4
NaPbCl 的电解液,故答案为:阴;PbO。
2 4