文档内容
专题讲座(一) 陌生化学方程式书写
1.由于氰化钠有剧毒,因此需要对“废液”中的氰化钠进行处理,通常选用漂白粉或漂白液在碱性
条件下将其氧化,其中一种产物为空气的主要成分,则在碱性条件下漂白液与氰化钠反应的离子方程式为
_______。
【答案】5ClO-+2CN-+2OH-=5Cl-+2CO 2- +N ↑+H O
3 2 2
【解析】碱性条件下,漂白液NaClO氧化NaCN生成氮气和Cl-、CO2-,离子方程式:5ClO-+2CN-
3
+2OH-=5Cl-+2CO 2- +N ↑+H O,答案:5ClO-+2CN-+2OH-=5Cl-+2CO 2- +N ↑+H O。
3 2 2 3 2 2
2.从工业废钒中回收金属钒既避免污染环境又有利于资源综合利用。某工业废钒的主要成分为
VO、VOSO 和SiO 等,如图是从废钒中回收钒的一种工艺流程:
2 5 4 2
(1)“氧化”工序中反应的离子方程式为___________。
(2)写出流程中铝热反应的化学方程式:___________。
【答案】(1)ClO +6VO2++3HO=Cl-+6VO +6H+
2
(2)3V O+10Al 6V+5Al O
2 5 2 3
【分析】从废钒催化剂中回收VO,由流程可知,“酸浸”时VO 转化为VO +,VOSO 转成VO2+,只
2 5 2 5 2 4
有SiO 不溶,然后加草酸还原发生2VO ++ H C O+2H+=2VO2++2CO ↑+2H O,将VO +变为VO2+,除杂后加
2 2 2 2 4 2 2 2
入氯酸钾氧化生成VO +,加入氨水生成偏钒酸铵( NHVO )沉淀,煅烧生成VO,用铝热反应生成粗钒,
2 4 3 2 5
经电解精炼得到钒,以此解答该题。
【解析】(1)氧化时反应物为ClO -和VO2+,生成物为Cl- 和VO +,配平得方程式为:ClO +6VO2
3 2
++3HO=Cl-+6VO ++6H+。
2 2(2)该铝热反应为氯和五氧化二钒的置换反应,方程式为:3VO+10Al 6V+5Al O。
2 5 2 3
3.以硫铁矿烧渣(主要成分Fe O、SiO,少量的Fe O、Al O、MgO)生产安全高效的水处理剂高铁酸
2 3 2 3 4 2 3
钾(K FeO)的工艺流程如下:
2 4
“氧化”时发生反应的离子方程式为___________
【答案】2Fe3++3ClO-+10OH-=2FeO 2-+3Cl-+5HO
4 2
【解析】硫铁矿烧渣中加入硫酸,金属氧化物能溶解,二氧化硅不溶解,再加入过氧化氢将亚铁离子
氧化生成铁离子,再加入次氯酸钠溶液进行氧化,根据最后的产物分析,该过程应将+3铁氧化成高铁酸根
离子,次氯酸根离子被还原为氯离子,离子方程式为:2Fe3++3ClO-+10OH-=2FeO 2-+3Cl-+5HO。该过
4 2
程加入氢氧化钠调节pH,将镁离子或铝离子沉淀,过滤后滤液中加入饱和氢氧化钾溶液,得到高铁酸钾固
体。据此解答。氧化过程中是将铁离子氧化成高铁酸根离子,离子方程式为:2Fe3++3ClO-+10OH-
=2FeO 2-+3Cl-+5HO。
4 2
4.以黄铜矿(CuFeS)、FeCl 和乳酸[CHCH(OH)COOH]为原料可制备有机合成催化剂CuCl和补铁剂
2 3 3
乳酸亚铁{[CH CH(OH)COO] Fe}。其主要实验流程如下:
3 2
FeCl 溶液与黄铜矿发生反应的离子方程式为___________
3
【答案】CuFeS+3Fe3++Cl-=4Fe2++CuCl+2S
2
【解析】CuFeS 与FeCl 反应生成CuCl和S以及Fe2+,Fe元素由+3价下降到+2价,S元素由-2价上
2 3
升到0价,Cu元素由+2价下降到+1价,根据得失电子守恒配平离子方程式为:CuFeS+3Fe3++Cl-=4Fe2+
2
+CuCl+2S。
5.高锰酸钾生产过程中产生的废锰渣(主要成分为MnO 、KOH、MgO和Fe O)可用于制备MnSO 晶
2 2 3 4
体,工艺流程如下:“反应Ⅲ”的离子方程式为___________
【答案】2Fe2++MnO +4H+=2Fe3++Mn2++2HO
2 2
【分析】废锰渣主要成分为MnO 、KOH、MgO和Fe O,KOH、MgO和Fe O 与硫酸反应生成硫酸
2 2 3 2 3
钾、硫酸镁、硫酸铁,MnO 和硫酸不反应,加硫酸溶解、过滤,废渣A是MnO ,MnO 、过量FeS 在酸
2 2 2 2
性条件下反应得到MnSO 、S、FeSO ,滤液中的Fe2+被加入的MnO 氧化为Fe3+,加碳酸钙调pH生成氢氧
4 4 2
化铁沉淀除去Fe3+。
【解析】“反应Ⅲ”是溶液中的Fe2+被加入的MnO 氧化为Fe3+,MnO 被还原为Mn2+,根据得失电子
2 2
守恒、电荷守恒,反应的离子方程式为2Fe2++MnO +4H+=2Fe3++Mn2++2HO。
2 2
6.氧化铁黄(化学式为FeOOH)是一种黄色颜料,工业上以废铁为主要原料生产氧化铁黄的一种工艺
流程如下:
氧化过程生成氧化铁黄的化学方程式是___________
【答案】4FeSO +O+8NaOH=4FeOOH↓+4NaSO +2HO
4 2 2 4 2
【解析】过量铁与硫酸反应生成FeSO ,而空气中的O 将Fe2+氧化为FeOOH,根据质量守恒
4 2
(SO 2-),有NaSO 生成,进一步推出NaOH参加反应,根据电子得失守恒配平后可知,生成物还有水。
4 2 4
据此可写出:4FeSO +O+8NaOH=4FeOOH↓+4NaSO +2HO。
4 2 2 4 2
7.以红土镍矿(主要含有Fe O、FeO、NiO、SiO 等)为原料,获取净水剂黄钠铁矾[NaFe (SO )(OH) ]
2 3 2 3 4 2 6
和纳米镍粉的部分工艺流程如下:(1)“氧化”过程发生的离子方程式为___________
(2)向“过滤Ⅱ”所得滤液(富含Ni2+)中加入NH·H O,在碱性条件下制备纳米镍粉同时生成N 的离
2 4 2 2
子方程式:___________
【答案】(1)2H++2Fe2++ClO-=2Fe3++Cl-+HO
2
(2)N H·H O+2Ni2++4OH-=2Ni↓+N↑+5HO
2 4 2 2 2
【解析】(1)FeO被酸溶解生成Fe2+,用NaClO氧化Fe2+,前面加入了HSO ,故为酸性条件下,
2 4
ClO-将Fe2+氧化生成Fe3+,ClO-自身被还原为Cl-,根据Cl和Fe得失电子守恒配平反应,用H+平衡电荷。
故离子方程式为2H++2Fe2++ClO-=2Fe3++Cl-+HO。NH·H O+2Ni2++4OH-=2Ni↓+N↑+5HO。
2 2 4 2 2 2
(2)Ni2+氧化NH·H O,生成N,自身被还原为Ni,根据N和Ni得失电子守恒配平反应,用OH-平
2 4 2 2
衡电荷。故离子方程式为NH·H O+2Ni2++4OH-=2Ni↓+N↑+5HO。
2 4 2 2 2
8.某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物
质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO ·7H O):
4 2
(1)“碱浸”中NaOH的两个作用分别是_______;为回收金属,用稀硫酸将“滤液①”调为中性,生成
沉淀,写出该反应的离子方程式:_______。
(2)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH,写出该反应的
离子方程式:_______。
【答案】(1) 除去油脂,溶解Al、A1 O、SiO AlO +H++HO=Al(OH) ↓
2 3 2 2 3
(2)2Ni2++ClO—+4OH—=2NiOOH↓+Cl—+HO
2
【分析】由题给流程可知,向废镍催化剂中加入氢氧化钠溶液进行碱浸,可除去油脂,且Al、Al O
2 3
和NaOH发生反应生成NaAlO ,SiO 和NaOH反应生成NaSiO,过滤得到含有NaAlO 、NaSiO 的滤液
2 2 2 3 2 2 3
①和含有Ni、Fe及其氧化物和少量不溶性杂质的滤饼①;向滤饼中加入稀硫酸酸浸时,金属氧化物溶于稀
硫酸得到可溶性硫酸盐,过滤除去不溶性杂质,得到可溶性硫酸盐的滤液;向滤液中加入双氧水溶液将
Fe2+氧化为Fe3+,再加入NaOH调节溶液pH使Fe3+转化为Fe(OH) 沉淀,过滤除去氢氧化铁,得到含有硫
3
酸镍溶液,控制溶液pH浓缩结晶得到硫酸镍晶体。【解析】(1)由分析可知,“碱浸”中NaOH的作用是除去油脂,溶解Al、A1 O、SiO;用稀硫酸
2 3 2
将“滤液①”调为中性时,溶液中偏铝酸钠与稀硫酸反应生成硫酸钠和氢氧化铝沉淀,而硅酸钠不能与稀
硫酸反应生成硅酸沉淀,则生成沉淀的离子方程式为AlO +H++HO=Al(OH) ↓;
2 3
(2)由题意可知,生成碱式氧化镍的反应为碱性溶液中,镍离子与次氯酸根离子反应生成碱式氧化
镍沉淀、氯离子和水,反应的离子方程式为2Ni2++ClO—+4OH—=2NiOOH↓+Cl—+HO。
2
9.以某工业铜渣(主要成分为Cu、Cu Se、Cu Te,还有少量Ag)为原料制备胆矾、硒、碲的一种工艺
2 2
流程如下:
(1)“浆化、焙烧”后,铜渣中金属元素均转化为硫酸盐,碲元素转化为不溶于水的TeO 。Cu Se与浓
2 2
硫酸反应的化学方程式为___________
(2)“浸取Ⅱ”后,TeO 转化为TeCl ,则“还原”过程反应的离子方程式为___________
2
【答案】(1)Cu Se+6HSO (浓) 2CuSO +SeO↑+4SO ↑+6HO
2 2 4 4 2 2 2
(2)TeCl 2-+2SO +4HO=Te+2SO 2-+6Cl-+8H+
6 2 2 4
【解析】(1)根据题意,“浆化、焙烧”过程中生成物有SeO,CuSO ,SO ,而硫酸中的H元素转
2 4 2
化为水,反应为:Cu Se+6HSO (浓) 2CuSO +SeO↑+4SO ↑+6HO。
2 2 4 4 2 2 2
(2)“还原”时,SO 将TeCl 2-还原为Te,本身氧化成SO 2-,结合三大守恒(质量守恒,电子得失
2 6 4
守恒及电荷守恒)可得反应:TeCl 2-+2SO +4HO=Te+2SO 2-+6Cl-+8H+。
6 2 2 4
10.绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备
高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了Cr
—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:回答下列问题:
(1)工序③中发生反应的离子方程式为_______。
(2)物质V可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为_______。
【答案】(1)2Na++2 +2CO +H O= +2NaHCO↓
2 2 3
(2)4Fe(CrO )+ 7O +16NaHCO 8NaCrO+2 Fe O+ 16CO+8H O
2 2 2 3 2 4 2 3 2 2
【分析】由题给流程可知,铬铁矿、氢氧化钠和空气在高温下连续氧化发生的反应,在熔融氢氧化钠
作用下,Fe(CrO ) 被氧气高温氧化生成铬酸钠和氧化铁,氧化铝与熔融氢氧化钠反应转化为偏铝酸钠,氧
2 2
化镁不反应;将氧化后的固体加水溶解,过滤得到含有氧化镁、氧化铁的滤渣1和含有过量氢氧化钠、铬
酸钠、偏铝酸钠的滤液;将滤液在介稳态条件下分离得到铬酸钠溶液、氢氧化钠溶液和偏铝酸钠溶液;向
铬酸钠溶液中通入过量的二氧化碳得到重铬酸钠和碳酸氢钠沉淀;向偏铝酸钠溶液中通入过量的二氧化碳
气体得到氢氧化铝沉淀和碳酸氢钠;向滤渣1中通入二氧化碳和水蒸气,氧化镁与二氧化碳和水蒸气反应
转化为碳酸氢镁溶液;碳酸氢镁溶液受热分解得到碳酸镁固体和二氧化碳、水蒸气,二氧化碳、水蒸气可
以在工序②循环使用;碳酸镁高温煅烧得到氧化镁。
【解析】(1)工序③中发生的反应为铬酸钠溶液与过量的二氧化碳反应生成重铬酸钠和碳酸氢钠沉
淀,反应的离子方程式为2Na++2 +2CO +H O= +2NaHCO↓;
2 2 3
(2)碳酸氢钠代替高温连续氧化工序中的氢氧化钠发生的主要反应为高温下,Fe(CrO ) 与氧气和碳
2 2
酸氢钠反应生成铬酸钠、氧化铁、二氧化碳和水,反应的化学方程式为4Fe(CrO )+ 7O +16NaHCO
2 2 2 3
8NaCrO+2 Fe O+ 16CO+8H O;若将碳酸氢钠换为碳酸钠也能发生类似的反应。
2 4 2 3 2 2
11.一种制取电池级二氧化锰的工艺流程如下图:“浸取”过程有硫单质生成,写出该过程中主要反应的化学方程式_______。
【答案】
【解析】浸取过程中,FeS 和MnO 在酸性溶液中反应,生成S,则FeS 中-1价S的化合价升高,FeS
2 2 2 2
做还原剂,MnO 做氧化剂,Mn的化合价从+4价降低到+2价,同时FeS 中的+2价铁也被MnO 氧化为+3
2 2 2
价,所以生成物有硫酸锰、硫酸铁、硫,根据电子守恒和质量守恒写出该反应的化学方程式为:
。
12.1797年,法国化学家Vauquelin发现了一种新元素。由于包含这种元素的矿物呈现出多种颜色,
因此称之为Chromium,元素符号为Cr。一些含Cr元素的物质或微粒的性质如表。
物质 Cr(OH) HCrO HCr O
3 2 4 2 2 7
灰蓝色固体,难溶 红色固体,水溶液 无纯净物,只存在于
性质
于水两性氢氧化物 为黄色中强酸 水溶液中,强酸
、
微粒 Cr3+ Cr(OH) 、HCrO
HCr O
2
颜色 蓝紫色 绿色 黄色 橙红色
(1)取少量Cr(OH) 于试管中,逐滴加入稀硫酸,直至过量,可观察到的现象为___________。
3
(2)请结合平衡移动原理,解释(1)中现象___________。
(3)将Cr(OH) 加热可得到Cr O 固体,将稍过量的Cr O 固体与NaCO 固体混合均匀,在空气中高温
3 2 3 2 3 2 3
煅烧,可得到黄色的NaCrO 固体,请写出该反应的化学方程式___________。
2 4
(4)Na CrO 部分水合物溶解度如图1。
2 4将(3)中所得固体溶解于水中,过滤,得到NaCrO 溶液。从该溶液中获得NaCrO•6H O的方法为
2 4 2 4 2
___________。
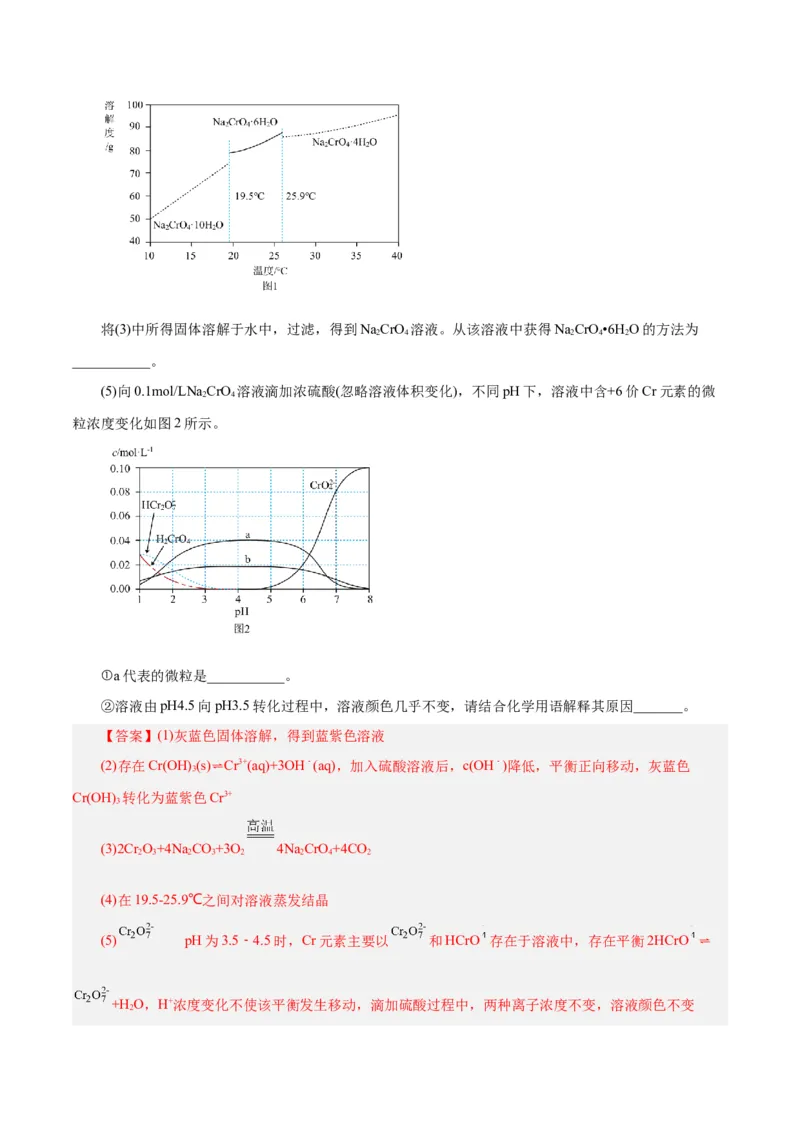
(5)向0.1mol/LNa CrO 溶液滴加浓硫酸(忽略溶液体积变化),不同pH下,溶液中含+6价Cr元素的微
2 4
粒浓度变化如图2所示。
①a代表的微粒是___________。
②溶液由pH4.5向pH3.5转化过程中,溶液颜色几乎不变,请结合化学用语解释其原因_______。
【答案】(1)灰蓝色固体溶解,得到蓝紫色溶液
(2)存在Cr(OH)
3
(s)⇌Cr3+(aq)+3OH﹣(aq),加入硫酸溶液后,c(OH﹣)降低,平衡正向移动,灰蓝色
Cr(OH) 转化为蓝紫色Cr3+
3
(3)2Cr O+4Na CO+3O 4NaCrO+4CO
2 3 2 3 2 2 4 2
(4)在19.5-25.9℃之间对溶液蒸发结晶
(5) pH为3.5﹣4.5时,Cr元素主要以 和HCrO 存在于溶液中,存在平衡2HCrO ⇌
+H O,H+浓度变化不使该平衡发生移动,滴加硫酸过程中,两种离子浓度不变,溶液颜色不变
2【解析】(1)Cr(OH) 两性氢氧化物,2Cr(OH) +3H SO =Cr (SO )+3H O,所以现象为Cr(OH) 灰蓝色
3 3 2 4 2 4 3 2 3
固体溶解,得到Cr3+蓝紫色溶液。
(2)在水溶液中Cr(OH)
3
存在沉淀溶解平衡,Cr(OH)
3
(s)⇌Cr3+(aq)+3OH﹣(aq),加入硫酸溶液后,
c(OH﹣)降低,平衡正向移动,灰蓝色固体溶解,转化为蓝紫色溶液。
(3)由题意知,Cr O 与NaCO 在空气中高温煅烧得到NaCrO 固体,Cr元素化合价升高,O 参与反
2 3 2 3 2 4 2
应,Cr O+Na CO+O ﹣NaCrO+CO ,Cr元素化合价升高3×2,O元素化合价降低2×2,再结合原子个数
2 3 2 3 2 2 4 2
守恒可配平化学方程式2Cr O+4Na CO+3O 4NaCrO+4CO 。
2 3 2 3 2 2 4 2
(4)由图像可得,欲从溶液中获得NaCrO•6H O,需在19.5﹣25.9℃之间蒸发结晶。
2 4 2
(5)由图像可知,pH在3.3﹣4.5时Cr元素主要以 和HCrO ﹣形式存在,根据图示量的关系确
4
定a为 ,b为 。由图知溶液由pH4.5向pH3.5转化过程中, 和 浓度几乎不变,说明
溶液颜色不变。
13.钴具有广泛用途,其正三价化合物具有强氧化性。利用含钴废料(主要成分为Co O,还含有少量
3 4
的铝箔、LiCoO 等杂质)制备碳酸钴的工艺流程如下图所示:
2
(1)“碱浸”过程中,可以加快反应速率和提高原料利用率的方法是__________(任写两点)。
(2)“滤液①”主要成分是__________;“操作②”的分离方法是__________。
(3)“酸溶”时,Co、Li元素的浸出率随温度的变化如图所示:“酸溶”的适宜温度是__________;“酸溶”时有无色气体产生,该气体为__________;若用
NaSO 代替HO 则有两种硫酸盐生成,写出NaSO 在“酸溶”时发生的化学方程式:__________。
2 2 3 2 2 2 2 3
【答案】(1)升高温度、粉碎废料、适当增大NaOH溶液的浓度等(任写两点)
(2) NaAlO 萃取分液或分液
2
(3)80℃或80℃左右 O 4Co O+Na SO+11H SO =12CoSO+Na SO +11H O
2 3 4 2 2 3 2 4 4 2 4 2
【分析】“碱浸”过程中,Co O 和LiCoO 不与碱反应存在于滤渣中,Al在碱性溶液中发生反应生成
3 4 2
NaAlO ,滤液①主要成分为NaAlO ,滤渣中加入硫酸和过氧化氢发生反应使滤渣溶解,过滤后加入有机
2 2
磷萃取,得到有机相和无机相,有机相反萃取后加入NaCO 沉钴,得到CoCO,以此解答。
2 3 3
(1)“碱浸”过程中可以加快反应速率和提高原料利用率的方法是升高温度、粉碎矿石、适当增加
NaOH的浓度等;
(2)由分析知,滤液①主要成分为NaAlO ;操作②为萃取分液或分液;
2
(3)由图可知,当温度过高时,钴元素的浸出率降低,则酸浸的适宜温度是80℃;由分析知,“酸
溶”时HO 的作用为还原剂,则产生的气体为O;若用NaSO 代替HO,根据题意知,生成CoSO 和
2 2 2 2 2 3 2 2 4
NaSO ,结合得失电子守恒、元素守恒配平的化学方程式为
2 4
4Co O+Na SO+11H SO =12CoSO+Na SO +11H O。
3 4 2 2 3 2 4 4 2 4 2
14.工业上用粗铜电解精炼所产生的阳极泥[主要含硒化亚铜(Cu Se)和碲化亚铜(Cu Te)]为原料,进行
2 2
综合回收利用的某种工艺流程如下:
已知:①TeO 是两性氧化物,微溶于水。
2
②25℃时,亚碲酸(H TeO )的 , 。
2 3
(1)“烧结”时的固体产物主要为NaSeO、NaTeO 和Cu O,该过程中Cu Se反应的化学方程式为
2 3 2 4 2 2
_______。
(2)还原过程的主要目的是将“烧结”时生成的少部分NaTeO 进行转化,写出“还原”时反应的离子
2 4
方程式_______。【答案】(1)2Cu Se+2Na CO+3O 2Cu O+2Na SeO+2CO
2 2 3 2 2 2 3 2
(2)2Fe2++TeO +2H+ = 2Fe3++TeO +H O
2
【分析】阳极泥主要含硒化亚铜(Cu Se )和碲化亚铜(Cu Te),通过在氧气和NaCO 固体中烧结,生成
2 2 2 3
NaSeO、NaTeO 和Cu O;水浸后过滤,滤渣中Cu O加入氧化剂和硫酸溶液生成硫酸铜溶液,滤液通过
2 3 2 3 2 2
稀硫酸调整pH后 转化为TeO 沉淀,过滤后,通过HCl和SO 转化为Te,剩下的滤液加入FeSO 将
2 2 4
溶液中少量的 还原为 除杂,最后通入SO 进行还原得到粗硒。
2
(1)阳极泥主要含硒化亚铜Cu Se 和碲化亚铜Cu Te,通过在氧气和NaCO 固体中烧结,生成
2 2 2 3
NaSeO、NaTeO 和Cu O,通过元素守恒和电子转移守恒,得到Cu Se发生的化学方程式为:
2 3 2 3 2 2
2Cu Se+2Na CO+3O 2Cu O+2Na SeO+2CO ;
2 2 3 2 2 2 3 2
(2)根据流程烧结是产生的少量NaTeO 被FeSO 还原为NaTeO 除去,根据电子转移守恒和元素守
2 4 4 2 3
恒,反应的离子方程式为2Fe2++ +2H+ = 2Fe3++ +H O。
2
15.以碳酸锰铜矿(主要成分为MnCO 、CuCO,还含有Fe O 杂质)为原料制备硫酸锰并回收铜的一种
3 3 3 4
工艺流程如图:
已知:Ksp[Fe(OH) ]=4.0×10-38,Ksp[Cu(OH) ]=2.2×10-20,Ksp[Fe(OH) ]=8.0×10-16,
3 2 2
Ksp[Mn(OH) ]=2.1×10-13
2
(1)写出“酸浸”时,杂质Fe O 与稀硫酸反应的化学方程式:_______
3 4
(2)“沉锰”时,发生反应的离子方程式为_______【答案】Fe O+4H SO =Fe (SO )+FeSO+4H O Mn2++2HCO =MnCO↓+CO ↑+H O
3 4 2 4 2 4 3 4 2 3 2 2
【分析】碳酸锰铜矿主要成分为MnCO 、CuCO,还含有Fe O 杂质,用硫酸酸浸,得到硫酸锰、硫
3 3 3 4
酸铜、硫酸铁、硫酸亚铁的混合溶液,加入二氧化锰,Fe2+被氧化为Fe3+;加入MnCO 调节pH生成氢氧化
3
铁沉淀;过滤后向溶液中通入氨气生成氢氧化铜沉淀,过滤,向滤液中加入NH HCO ,生成MnCO 沉
4 3 3
淀,MnCO 沉淀中加硫酸,得到硫酸锰溶液。
3
【解析】(1)“酸浸”时,Fe O 与稀硫酸反应生成硫酸铁、硫酸亚铁和水,反应的化学方程式是
3 4
Fe O+4H SO =Fe (SO )+FeSO+4H O;
3 4 2 4 2 4 3 4 2
(2)“沉锰”时,锰离子和碳酸氢根离子反应生成碳酸锰沉淀、二氧化碳、水,发生反应的离子方程式
为Mn2++2HCO =MnCO↓+CO ↑+H O。
3 2 2
16.利用“价类二维图”研究物质的性质是化学研究的重要手段。下图是氯元素的化合价与部分物质
类别的对应关系。
(1)A、B、C三种物质中,属于电解质的是_______ (填化学式)。
(2)写出 的电离方程式_______。
(3)C可与HCl反应生成A,写出该反应的化学方程式_______。
(4)已知D可用于实验室制 ,其焰色试验为紫色。D可以用A与某强碱溶液在加热下反应制得,除
生成D外,还生成一种无氧酸盐和水,写出该反应的化学方程式_______。
【答案】(1)HClO (2)
(3) (4)
【分析】由图可知,A为氯元素的单质,即Cl,B为+1价的氯的氧化物,即ClO,C为+1价的含氧
2 2酸,即HClO,D为+5价的含氧酸盐,如氯酸盐。
【解析】(1)A、B、C三种物质中,A为氯元素的单质,即Cl,B为+1价的氯的氧化物,即ClO,
2 2
C属于酸,属于电解质的是HClO。
(2) 由钠离子和亚氯酸根离子构成,电离方程式 。
(3)C为HClO,可与HCl反应生成氯气和水,该反应的化学方程式 。
(4)已知D可用于实验室制 ,其焰色试验为紫色,D为钾盐。D可以用氯气与某强碱溶液在加热
下反应制得,除生成D外,还生成一种无氧酸盐KCl和水,该反应的化学方程式
。
17.铁酸HFeO 是一种多功能、高效无毒的新型绿色水处理剂,投入水中会迅速发生反应。
2 4
(1)H FeO 中Fe的化合价为________。
2 4
(2)已知:常温下高铁酸为紫黑色固体,将HFeO 投入水中,有气体生成,同时有红褐色沉淀产生,
2 4
则HFeO 与水反应的化学方程式为________。
2 4
(3)在工业上制备HFeO 的方法有多种。
2 4
Ⅰ.干法制备的反应原理如下:2FeSO +6Na O=aNa FeO+bM↑+2Na O+2Na SO
4 2 2 2 4 2 2 4
①b=________。
②每生成1molM,该反应转移电子的物质的量为________mol。
Ⅱ.湿法制备的工艺流程如下;
已知:HFeO 在强碱性溶液中的溶解度较小,高温易分解。
2 4
③反应a中,生成物除了HFeO 外,另一种盐的化学式为________。
2 4
④一系列操作包括过滤、________、________。
【答案】+6 4H FeO+2H O=4Fe(OH) +3O ↑ 1 10 NaCl 洗涤 低温干燥
2 4 2 3 2
【分析】常温下高铁酸为紫黑色固体,将HFeO 投入水中,有气体生成,同时有红褐色沉淀产生,说
2 4
明反应产生Fe(OH) 和O;根据干法制备的原理方程式2FeSO +6Na O=aNa FeO+bM↑+2Na O+2Na SO ,
3 2 4 2 2 2 4 2 2 4
反应产生气体M应为O,根据元素守恒和氧化还原反应的规律分析解答。
2【解析】(1)根据正负化合价的代数和为0,HFeO 中H为+1价,O为-2价,则Fe的化合价应为+6
2 4
价;
(2)常温下,高铁酸为紫黑色固体,将HFeO 投入水中,有气体生成,同时有红褐色沉淀产生,说明
2 4
反应产生Fe(OH) 和O,则HFeO 与水反应的化学方程式为4HFeO+2H O=4Fe(OH) +3O ↑;
3 2 2 4 2 4 2 3 2
(3) ①根据干法制备的原理方程式2FeSO +6Na O=aNa FeO+bM↑+2Na O+2Na SO 分析,反应产生气
4 2 2 2 4 2 2 4
体M,应为O,根据Fe元素守恒,a应为2,再根据O元素守恒,b应为1;
2
②M为O,化合价升高的元素有Fe和O,Fe从+2价升高为+6价,O从-1价升高为0价,根据电子得
2
失守恒,则每生成1mol M时,转移的电子数为2×(6-2)+2×[0-(-1)]=10;
③反应a中,FeCl 、NaOH和NaClO发生反应生成NaFeO,从元素角度分析另一种盐,ClO-被还原
3 2 4
为Cl-,则另一种盐应为NaCl;
④H FeO 高温易分解,得到NaFeO 溶液后,后续操作需要经过过滤,洗涤,低温干燥,最终得到高
2 4 2 4
纯NaFeO 晶体。
2 4
18.某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量,体积均为
1L),当闭合该装置的开关K时,观察到电流计的指针发生了偏转。请回答下列问题:
(1)甲、乙、丙三池中为原电池的是______(填“甲池”、“乙池”或“丙池”),A电极的电极反应式
为______,C电极的电极反应式为______。
(2)丙池总反应的离子方程式为______。
(3)当甲池中B电极上消耗O 的体积为560mL(标准状况)时,理论上通过乙池的电量为______(法拉第
2
常数F=9.65×104C•mol-1,列式并计算),丙池溶液的pH为______(忽略溶液体积的变化)。
【答案】(1) 甲池 CHOCH -12e-+16OH-=2 +11H O Ag-e-=Ag+
3 3 2
(2)2Cu2++2H O 2Cu+O ↑+4H+ (3) 9.65×103C 1
2 2
【解析】(1)从图中可以看出,甲池为燃料电池,乙池和丙池为电解池。则甲、乙、丙三池中为原
电池的是甲池,A电极的电极反应式为CHOCH -12e-+16OH-=2 +11H O;乙池中,C电极与燃料电池
3 3 2的正极相连,则C电极为阳极,Ag失电子生成Ag+,电极反应式为Ag-e-=Ag+。
(2)丙池中,阴极Cu2+得电子生成Cu,阳极HO失电子生成O 和H+,总反应的离子方程式为2Cu2+
2 2
+2H O 2Cu+O ↑+4H+。
2 2
(3)当甲池中B电极上消耗O 的体积为560mL(标准状况)时,线路中通过电子的物质的量n(e-)=
2
=0.1mol,理论上通过乙池的电量为0.1mol×9.65×104C•mol-1=9.65×103C;丙池中,可建立关
系式:H+——e-,则溶液中生成H+的物质的量为0.1mol,溶液的pH为1。
19.回答下列问题:
(1)下图是某化学兴趣小组探究化学能转变为电能的装置。
①若电极a为Zn、电极b为Ag、c为CuSO 溶液,开始时a电极与b电极质量相等,当电路中转移
4
0.2mol电子时,a电极与b电极质量差为_______g。
②若电极a为Mg、电极b为Al、c为NaOH溶液,则负极电极反应式为:_______。
③若电极a为Fe、电极b为Cu、c为浓硝酸,则正极电极反应式为:_______。
(2)燃料电池的工作原理是将燃料和氧化剂(如O)反应所放出的化学能直接转化为电能。现设计如图为
2
CH 燃料电池示意图,工作时电子流向如图所示。
4
写出电极A的电极方程式_______,电极A附近pH如何变化?_______ (填“变大”或“变小”)。
(3)Li-SOCl 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解质溶液是LiAlCl - SOCl
2 4 2.
电池的总反应可表示为:4Li+2SOCl = 4LiCl+S+ SO 。已知SOCl 会与水反应有刺激性气味的气体生成:
2 2 2
SOCl + H O=2HCl↑+ SO ↑。电池正极发生的电极反应式为_______;组装该电池必须在无水、无氧的条件
2 2 2
下进行,原因是_______。【答案】(1)12.9 Al-3e-+4OH-=[Al(OH) ]- NO +e-+2H+=NO↑+H O
4 2 2
(2)CH -8e-+10OH-= +7H O 减小
4 2
(3)SOCl +4e-=4Cl-+S+SO ↑ 锂是活泼金属,易与水和O 反应,SOCl 也可与水反应
2 2 2 2
【解析】(1)①若电极a为Zn、电极b为Ag、c为CuSO 溶液,Zn为负极,电极反应式为Zn-2e-
4
=Zn2+,Ag为正极,电极反应式为Cu2++2e-=Cu,当电路中转移0.2mol电子时,负极溶解0.1molZn,正极析
出0.1molCu,则a电极与b电极质量差为 ;
②若电极a为Mg、电极b为Al、c为NaOH溶液,Mg不与NaOH溶液反应,Al能与NaOH溶液反
应,则Al作负极,负极发生氧化反应,电极反应式为Al-3e-+4OH-=[Al(OH) ]-;
4
③若电极a为Fe、电极b为Cu、c为浓硝酸,Fe在浓硝酸中钝化,Cu能与浓硝酸反应,则Cu为负
极,Fe为正极,正极发生还原反应,电极反应式为NO +e-+2H+=NO↑+H O;
2 2
(2)甲烷燃料电池中,通入甲烷的一极为负极,负极发生氧化反应,通入氧气的一极为正极,正极
发生还原反应,原电池工作时,阴离子向负极移动,根据电子流向可知,电极A为负极,则X为甲烷,电
极B为正极,Y为氧气,电极A上甲烷发生氧化反应,电解质溶液为碱性,则电极反应式为CH-8e-
4
+10OH-= +7H O;电极A负极消耗氢氧根,溶液pH减小;
2
(3)根据4Li+2SOCl = 4LiCl+S+ SO 可知,锂失电子,化合价升高,发生氧化反应,锂是负极,
2 2
SOCl 在正极得到电子被还原为S,同时生成二氧化硫,电极反应式为SOCl +4e-=4Cl-+S+SO ↑;锂和钠是
2 2 2
同一主族的元素,性质相似,钠和空气中的氧气、水蒸气反应,所以锂和空气中的氧气、水蒸气也能反
应;SOCl 也可与水反应,所以组装该电池必须在无水、无氧的条件下进行,故答案为:SOCl +4e-=4Cl-
2 2
+S+SO ↑;锂是活泼金属,易与水和O 反应,SOCl 也可与水反应。
2 2 2
20.I.如图是利用电化学装置将SO 转化为重要的化工原料HSO 的原理示意图。
2 2 4请回答下列问题:
(1)该装置将_______能转化为______能。
(2)催化剂b表面O 发生_______反应,其附近溶液酸性______(填“增强”、“不变”或“减弱”)。
2
(3)催化剂a表面的电极反应式:_______。
II.某废料铁泥主要成分是Fe O、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe O,设
2 3 2 3
计实验流程如图:
(4)步骤(I)充分反应后进行的实验操作名称是______。
(5)步骤(II)中加入HO 溶液后需要适当加热但温度不能过高,原因是______。
2 2
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢
氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由______。
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH) 沉淀,反应的离子方程式为______。
3
【答案】(1)化学 电 (2) 还原减弱 (3)SO +2H O-2e-=SO +4H+
2 2
(4)过滤 (5)适当加热可加快反应速率,温度不能过高避免双氧水受热分解
(6)不可行,溶液B中存在大量Fe3+,往该溶液中滴加氢氧化钠溶液会产生红褐色的Fe(OH) 沉淀,干
3
扰Fe2+的检验
(7)3NH +3H O+Fe3+=Fe(OH) ↓+3NH
3 2 3
【分析】II.铁泥中的Fe O、FeO和Fe和足量硫酸反应得含Fe3+、Fe2+、H+的溶液A,用HO 将Fe2+氧
2 3 2 2
化成Fe3+所得溶液B含Fe3+,加NaOH溶液将Fe3+沉淀,过滤得Fe(OH) 沉淀,将Fe(OH) 沉淀洗涤、加热
3 3
得Fe O 固体,据此解答。
2 3
【解析】(1)该装置没有外加电源,是一个原电池,把化学能转化为电能。
(2)由图示可看出,电子由a表面转移到b表面,因此b表面发生还原反应,催化剂b处的反应为:
O+2H++2e-=H O,酸性减弱。
2 2
(3)催化剂a表面是SO 失去电子生成硫酸,电极方程式为:SO +2H O−2e−== +4H+。
2 2 2
(4)将溶液和沉淀分离的操作名称为过滤,故答案为:过滤。(5)适当加热可加快反应速率,温度不能过高避免双氧水受热分解。
(6)不可行,溶液B中存在大量Fe3+,往该溶液中滴加氢氧化钠溶液会产生红褐色的Fe(OH) 沉淀,
3
干扰Fe2+的检验。
(7)氨水和Fe3+反应生成氢氧化铁的离子方程式为3NH +3H O+Fe3+=Fe(OH) ↓+3NH 。
3 2 3