文档内容
专题讲座(二) 整合有效信息书写陌生化学方程
式
第一部分:高考真题感悟
1.(2021·全国·高考真题(节选))碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回
答下列问题:
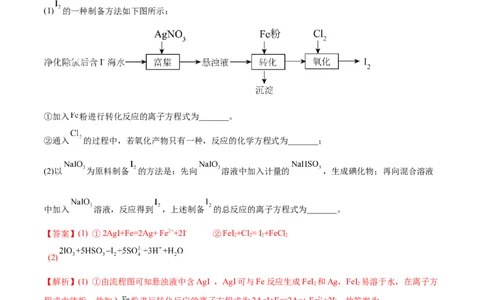
(1) 的一种制备方法如下图所示:
①加入 粉进行转化反应的离子方程式为_______。
②通入 的过程中,若氧化产物只有一种,反应的化学方程式为_______;
(2)以 为原料制备 的方法是:先向 溶液中加入计量的 ,生成碘化物;再向混合溶液
中加入 溶液,反应得到 ,上述制备 的总反应的离子方程式为_______。
【答案】(1) ①2AgI+Fe=2Ag+ Fe2++2I- ②FeI+Cl= I+FeCl
2 2 2 2
(2)
【解析】(1) ①由流程图可知悬浊液中含AgI ,AgI可与Fe反应生成FeI 和Ag,FeI 易溶于水,在离子方
2 2
程式中能拆,故加入 粉进行转化反应的离子方程式为2AgI+Fe=2Ag+ Fe2++2I-,故答案为:
2AgI+Fe=2Ag+ Fe2++2I-;
②通入 的过程中,因I-还原性强于Fe2+, 先氧化还原性强的I-,若氧化产物只有一种,则该氧化产
物只能是I,故反应的化学方程式为FeI+Cl= I+FeCl ,故答案为:FeI+Cl= I+FeCl ;
2 2 2 2 2 2 2 2 2
(2)先向 溶液中加入计量的 ,生成碘化物即含I-的物质;再向混合溶液中(含I-)加入溶液,反应得到 ,上述制备 的两个反应中I-为中间产物,总反应为 与 发生氧化还原反应,生
成 和 ,根据得失电子守恒、电荷守恒]及元素守恒配平离子方程式即可得:
,故答案为: ;
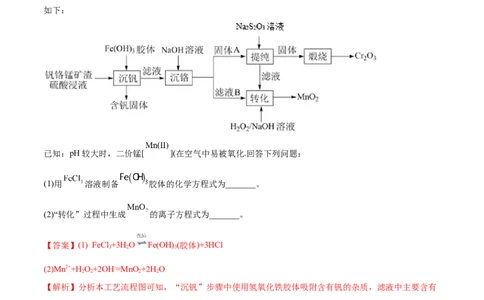
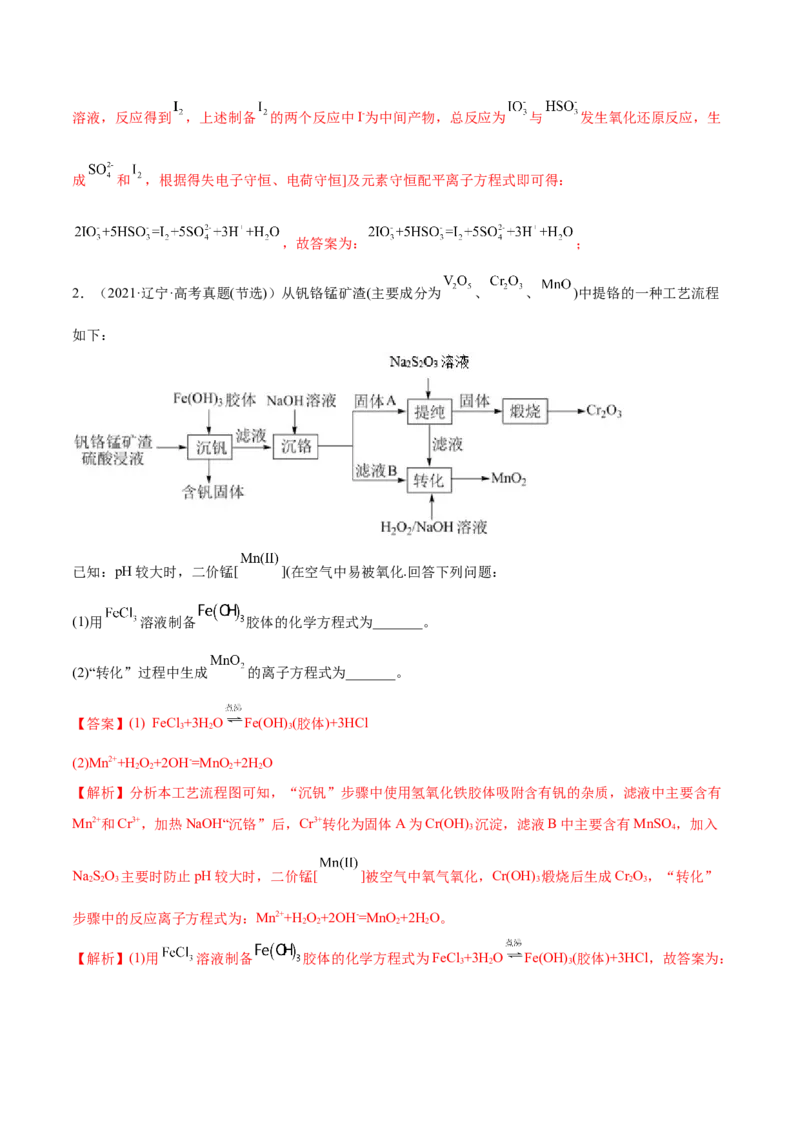
2.(2021·辽宁·高考真题(节选))从钒铬锰矿渣(主要成分为 、 、 )中提铬的一种工艺流程
如下:
已知:pH较大时,二价锰[ ](在空气中易被氧化.回答下列问题:
(1)用 溶液制备 胶体的化学方程式为_______。
(2)“转化”过程中生成 的离子方程式为_______。
【答案】(1) FeCl +3H O Fe(OH) (胶体)+3HCl
3 2 3
(2)Mn2++H O+2OH-=MnO+2H O
2 2 2 2
【解析】分析本工艺流程图可知,“沉钒”步骤中使用氢氧化铁胶体吸附含有钒的杂质,滤液中主要含有
Mn2+和Cr3+,加热NaOH“沉铬”后,Cr3+转化为固体A为Cr(OH) 沉淀,滤液B中主要含有MnSO ,加入
3 4
NaSO 主要时防止pH较大时,二价锰[ ]被空气中氧气氧化,Cr(OH) 煅烧后生成Cr O,“转化”
2 2 3 3 2 3
步骤中的反应离子方程式为:Mn2++H O+2OH-=MnO+2H O。
2 2 2 2
【解析】(1)用 溶液制备 胶体的化学方程式为FeCl +3H O Fe(OH) (胶体)+3HCl,故答案为:
3 2 3FeCl +3H O Fe(OH) (胶体)+3HCl;
3 2 3
(2)由分析可知,“转化”过程中生成 的离子方程式为Mn2++H O+2OH-=MnO+2H O,故答案为:
2 2 2 2
Mn2++H O+2OH-=MnO+2H O;
2 2 2 2
3.(2022·全国·高考真题(节选))废旧铅蓄电池的铅膏中主要含有 、 、 和Pb。还有少量
Ba、Fe、Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。
回答下列问题:
(1)在“脱硫”中 转化反应的离子方程式为________。
(2) 促进了金属Pb在醋酸中转化为 ,其化学方程式为________;
【答案】(1) PbSO (s)+CO (aq)= PbCO (s)+SO (aq)
4 3
(2)Pb+HO+2HAc=Pb(Ac) +2H O
2 2 2 2
【解析】铅膏中主要含有PbSO 、PbO 、PbO和Pb,还有少量Ba、Fe、Al的盐或氧化物等,向铅膏中加
4 2
入碳酸钠溶液进行脱硫,硫酸铅转化为碳酸铅,过滤,向所得固体中加入醋酸、过氧化氢进行酸浸,过氧
化氢可将溶液中的亚铁离子氧化为铁离子,酸浸后溶液的pH约为4.9,依据金属氢氧化物沉淀时的pH可
知,滤渣主要成分为氢氧化铝、氢氧化铁,过滤后,向滤液中加入氢氧化钠溶液进行沉铅,得到氢氧化铅
沉淀,滤液中的金属阳离子主要为钠离子和钡离子,氢氧化铅再进行处理得到PbO。
(1)“脱硫”中,碳酸钠溶液与硫酸铅反应生成碳酸铅和硫酸钠,反应的离子方程式为:PbSO (s)+CO (aq)=
4
PbCO (s)+SO (aq)。
3
(2)过氧化氢促进金属Pb在醋酸溶液中转化为Pb(Ac) ,过氧化氢与Pb、HAc发生氧还原反应生成Pb(Ac)
2 2
和HO,依据得失电子守恒和原子守恒可知,反应的化学方程式为:Pb+HO+2HAc=Pb(Ac) +2H O。
2 2 2 2 2
4.(2022·全国·高考真题(节选))硫酸锌( )是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为 ,杂质为 以及Ca、Mg、Fe、Cu等的
化合物。其制备流程如下:
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______。
(2)为了提高锌的浸取效果,可采取的措施有_______、_______。
(3)加入物质X调溶液 ,最适宜使用的X是_______(填标号)。
A. B. C.
滤渣①的主要成分是_______、_______、_______。
(4)向 的滤液①中分批加入适量 溶液充分反应后过滤,滤渣②中有 ,该步反应的离
子方程式为_______。
(5)滤液②中加入锌粉的目的是_______。
(6)滤渣④与浓 反应可以释放HF并循环利用,同时得到的副产物是_______、_______。
【答案】(1)ZnCO ZnO+CO ↑
3 2
(2)3Fe2++ +7H O=3Fe(OH) ↓+MnO↓+5H+
2 3 2
【解析】由题干信息,菱锌矿的主要成分为ZnCO ,杂质为SiO 以及Ca、Mg、Fe、Cu等的化合物,结合
3 2
流程图分析,菱锌矿焙烧,主要发生反应ZnCO ZnO+CO ↑,再加入HSO 酸浸,得到含Zn2+、Ca2+、
3 2 2 4
Mg2+、Fe2+、Fe3+、Cu2+的溶液,加入物质X调节pH=5,结合表格数据,过滤得到Fe(OH) 、CaSO、SiO
3 4 2
的滤渣①,滤液①中主要含有Zn2+、Cu2+、Mg2+、Ca2+、Fe2+,再向滤液①中加入KMnO 溶液氧化Fe2+,过
4
滤得到Fe(OH) 和MnO 的滤渣②,滤液②中加入锌粉,发生反应Zn+Cu2+=Zn2+=Cu,过滤后得到滤渣③为
3 2Cu,再向滤液③中加入HF脱钙镁,过滤得到滤渣④为CaF 、MgF ,滤液④为ZnSO 溶液,经一系列处理
2 2 4
得到ZnSO·7H O。
4 2
(1)由分析,焙烧时,生成ZnO的反应为:ZnCO ZnO+CO ↑;
3 2
(2)向80~90℃滤液①中加入KMnO 溶液,可氧化Fe2+,得到Fe(OH) 和MnO 的滤渣②,反应的离子方程
4 3 2
式为3Fe2++ +7H O=3Fe(OH) ↓+MnO↓+5H+;
2 3 2
5.(2021·河北·高考真题(节选))绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了
一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,
不产生废弃物,实现了Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:
回答下列问题:
(1)工序③中发生反应的离子方程式为_______。
(2)物质V可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为__。
【答案】(1)2Na++2 +2CO +H O= +2NaHCO↓
2 2 3
(2)4Fe(CrO )+ 7O +16NaHCO 8NaCrO+2 Fe O+ 16CO+8H O
2 2 2 3 2 4 2 3 2 2
【解析】由题给流程可知,铬铁矿、氢氧化钠和空气在高温下连续氧化发生的反应为,在熔融氢氧化钠作
用下,Fe(CrO ) 被氧气高温氧化生成铬酸钠和氧化铁,氧化铝与熔融氢氧化钠反应转化为偏铝酸钠,氧化
2 2
镁不反应;将氧化后的固体加水溶解,过滤得到含有氧化镁、氧化铁的滤渣1和含有过量氢氧化钠、铬酸
钠、偏铝酸钠的滤液;将滤液在介稳态条件下分离得到铬酸钠溶液、氢氧化钠溶液和偏铝酸钠溶液;向铬
酸钠溶液中通入过量的二氧化碳得到重铬酸钠和碳酸氢钠沉淀;向偏铝酸钠溶液中通入过量的二氧化碳气
体得到氢氧化铝沉淀和碳酸氢钠;向滤渣1中通入二氧化碳和水蒸气,氧化镁与二氧化碳和水蒸气反应转
化为碳酸氢镁溶液;碳酸氢镁溶液受热分解得到碳酸镁固体和二氧化碳、水蒸气,二氧化碳、水蒸气可以在工序②循环使用;碳酸镁高温煅烧得到氧化镁。
(1)工序③中发生的反应为铬酸钠溶液与过量的二氧化碳反应生成重铬酸钠和碳酸氢钠沉淀,反应的离子方
程式为2Na++2 +2CO +H O= +2NaHCO↓,故答案为:2Na++2 +2CO +H O=
2 2 3 2 2
+2NaHCO↓;
3
(2)碳酸氢钠代替高温连续氧化工序中的氢氧化钠发生的主要反应为高温下,,Fe(CrO ) 与氧气和碳酸氢钠
2 2
反应生成铬酸钠、氧化铁、二氧化碳和水,反应的化学方程式为4Fe(CrO )+ 7O +16NaHCO
2 2 2 3
8NaCrO+2 Fe O+ 16CO+8H O;若将碳酸氢钠换为碳酸钠也能发生类似的反应,故答案为:4Fe(CrO )+
2 4 2 3 2 2 2 2
7O+16NaHCO 8NaCrO+2 Fe O+ 16CO+8H O;
2 3 2 4 2 3 2 2
6.(2021·福建·高考真题(节选))四钼酸铵是钼深加工的重要中间产品具有广泛的用途。一种以钼精矿(主
要含 ,还有 、 的化合物及 等)为原料制备四钼酸铵的工艺流程如下图所示。
回答下列问题:
(1)“净化”后,溶液中若有低价钼(以 表示),可加入适量 将其氧化为 ,反应的离子方程式
为_______。
(2)高温下用 还原(NH )MoO 可制得金属钼,反应的化学方程式为_______。【已知:(NH )MoO 受
4 2 4 13 4 2 4 13
热分解生成 】
【答案】(1)(2)
【解析】钼精矿(主要含 ,还有 、 的化合物及 等)通入氧气焙烧得到 、CuO、Fe O、
2 3
SiO 和SO ,焙烧产生的气体主要为SO ; 、CuO、Fe O、SiO 加NaCO、HO浸出, 转化为
2 2 2 2 3 2 2 3 2
,铜、铁大多转化为氢氧化物,SiO 不反应,浸渣为SiO、氢氧化铁、氢氧化铜等,浸出液含
2 2
和少量Cu2+、Fe2+,加(NH )S净化,Cu2+、Fe2+转化CuS、FeS沉淀,滤渣为CuS、FeS,滤液主要含 ,
4 2
滤液中加NH NO 、HNO 进行沉淀得到(NH )MoO ·2H O。
4 3 3 4 2 4 13 2
(1)溶液中若有低价钼(以 表示),可加入适量 将其氧化为 ,则氧化剂为 ,还原产物
为-2价的O,还原剂为 ,氧化产物为 ,则反应的离子方程式为 ;
(2)高温下用 还原(NH )MoO 可制得金属钼,结合得失电子守恒、原子守恒可知反应的化学方程式为
4 2 4 13
。
第二部分:最新模拟精练
完卷时间:50分钟
1.(2021·四川南充市·阆中中学高三月考(节选))(10分)镉(Cd)可用于制作某些发光电子组件,一种以镉
废渣(含CdO及少量ZnO、CuO、MnO、FeO杂质)为原料制备镉的工艺流程如图:
回答下列问题:
(1)“氧化”步骤是为了除铁、除锰,其中 的还原产物是 ,该步骤中除锰的离子方程式分别为_______。
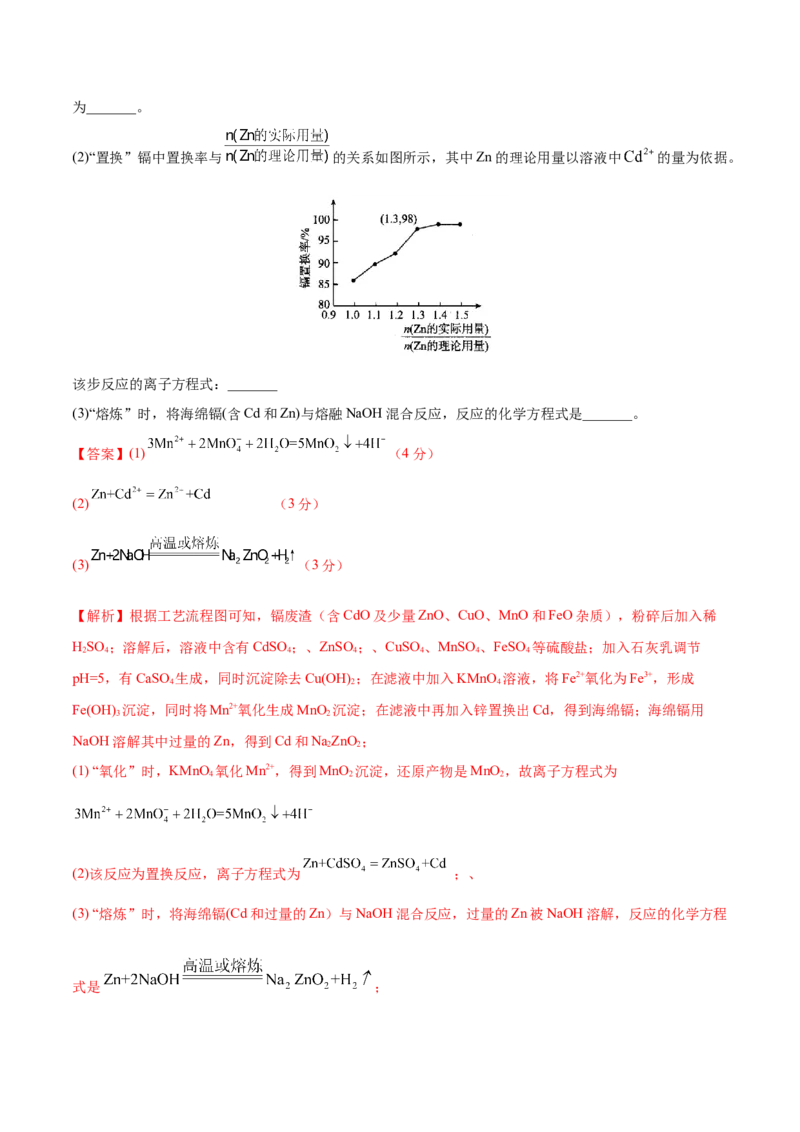
(2)“置换”镉中置换率与 的关系如图所示,其中Zn的理论用量以溶液中 的量为依据。
该步反应的离子方程式:_______
(3)“熔炼”时,将海绵镉(含Cd和Zn)与熔融NaOH混合反应,反应的化学方程式是_______。
【答案】(1) (4分)
(2) (3分)
(3) (3分)
【解析】根据工艺流程图可知,镉废渣(含CdO及少量ZnO、CuO、MnO和FeO杂质),粉碎后加入稀
HSO ;溶解后,溶液中含有CdSO ;、ZnSO;、CuSO 、MnSO 、FeSO 等硫酸盐;加入石灰乳调节
2 4 4 4 4 4 4
pH=5,有CaSO 生成,同时沉淀除去Cu(OH) ;在滤液中加入KMnO 溶液,将Fe2+氧化为Fe3+,形成
4 2 4
Fe(OH) 沉淀,同时将Mn2+氧化生成MnO 沉淀;在滤液中再加入锌置换出Cd,得到海绵镉;海绵镉用
3 2
NaOH溶解其中过量的Zn,得到Cd和NaZnO;
2 2
(1) “氧化”时,KMnO 氧化Mn2+,得到MnO 沉淀,还原产物是MnO ,故离子方程式为
4 2 2
(2)该反应为置换反应,离子方程式为 ;、
(3) “熔炼”时,将海绵镉(Cd和过量的Zn)与NaOH混合反应,过量的Zn被NaOH溶解,反应的化学方程
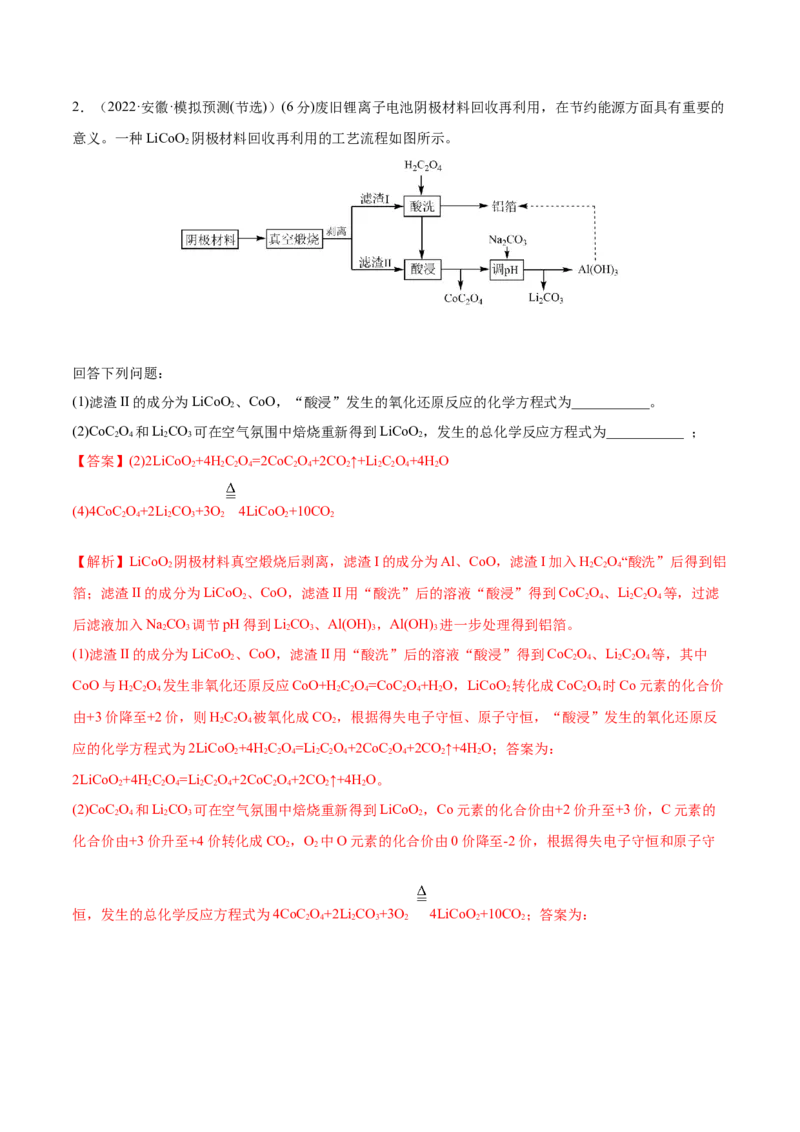
式是 ;2.(2022·安徽·模拟预测(节选))(6分)废旧锂离子电池阴极材料回收再利用,在节约能源方面具有重要的
意义。一种LiCoO 阴极材料回收再利用的工艺流程如图所示。
2
回答下列问题:
(1)滤渣II的成分为LiCoO 、CoO,“酸浸”发生的氧化还原反应的化学方程式为___________。
2
(2)CoC O 和LiCO 可在空气氛围中焙烧重新得到LiCoO ,发生的总化学反应方程式为___________ ;
2 4 2 3 2
【答案】(2)2LiCoO +4H C O=2CoC O+2CO ↑+Li C O+4H O
2 2 2 4 2 4 2 2 2 4 2
(4)4CoC O+2Li CO+3O 4LiCoO +10CO
2 4 2 3 2 2 2
【解析】LiCoO 阴极材料真空煅烧后剥离,滤渣I的成分为Al、CoO,滤渣I加入HC O“酸洗”后得到铝
2 2 2 4
箔;滤渣II的成分为LiCoO 、CoO,滤渣II用“酸洗”后的溶液“酸浸”得到CoC O、LiC O 等,过滤
2 2 4 2 2 4
后滤液加入NaCO 调节pH得到LiCO、Al(OH) ,Al(OH) 进一步处理得到铝箔。
2 3 2 3 3 3
(1)滤渣II的成分为LiCoO 、CoO,滤渣II用“酸洗”后的溶液“酸浸”得到CoC O、LiC O 等,其中
2 2 4 2 2 4
CoO与HC O 发生非氧化还原反应CoO+HC O=CoC O+H O,LiCoO 转化成CoC O 时Co元素的化合价
2 2 4 2 2 4 2 4 2 2 2 4
由+3价降至+2价,则HC O 被氧化成CO,根据得失电子守恒、原子守恒,“酸浸”发生的氧化还原反
2 2 4 2
应的化学方程式为2LiCoO +4H C O=Li C O+2CoC O+2CO ↑+4H O;答案为:
2 2 2 4 2 2 4 2 4 2 2
2LiCoO +4H C O=Li C O+2CoC O+2CO ↑+4H O。
2 2 2 4 2 2 4 2 4 2 2
(2)CoC O 和LiCO 可在空气氛围中焙烧重新得到LiCoO ,Co元素的化合价由+2价升至+3价,C元素的
2 4 2 3 2
化合价由+3价升至+4价转化成CO,O 中O元素的化合价由0价降至-2价,根据得失电子守恒和原子守
2 2
恒,发生的总化学反应方程式为4CoC O+2Li CO+3O 4LiCoO +10CO ;答案为:
2 4 2 3 2 2 24CoC O+2Li CO+3O 4LiCoO +10CO ;
2 4 2 3 2 2 2
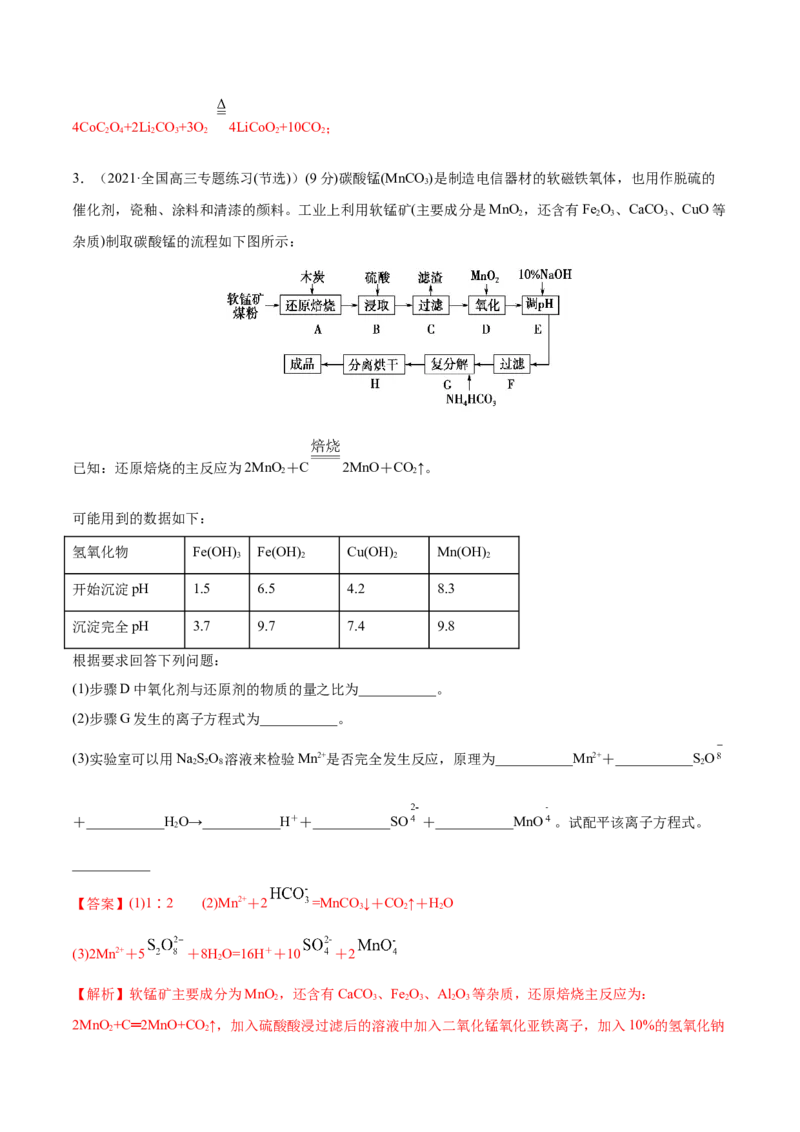
3.(2021·全国高三专题练习(节选))(9分)碳酸锰(MnCO )是制造电信器材的软磁铁氧体,也用作脱硫的
3
催化剂,瓷釉、涂料和清漆的颜料。工业上利用软锰矿(主要成分是MnO ,还含有Fe O、CaCO 、CuO等
2 2 3 3
杂质)制取碳酸锰的流程如下图所示:
已知:还原焙烧的主反应为2MnO +C 2MnO+CO↑。
2 2
可能用到的数据如下:
氢氧化物 Fe(OH) Fe(OH) Cu(OH) Mn(OH)
3 2 2 2
开始沉淀pH 1.5 6.5 4.2 8.3
沉淀完全pH 3.7 9.7 7.4 9.8
根据要求回答下列问题:
(1)步骤D中氧化剂与还原剂的物质的量之比为___________。
(2)步骤G发生的离子方程式为___________。
(3)实验室可以用NaSO 溶液来检验Mn2+是否完全发生反应,原理为___________Mn2++___________SO
2 2 8 2
+___________HO→___________H++___________SO +___________MnO 。试配平该离子方程式。
2
___________
【答案】(1)1∶2 (2)Mn2++2 =MnCO↓+CO↑+HO
3 2 2
(3)2Mn2++5 +8HO=16H++10 +2
2
【解析】软锰矿主要成分为MnO ,还含有CaCO 、Fe O、Al O 等杂质,还原焙烧主反应为:
2 3 2 3 2 3
2MnO +C═2MnO+CO ↑,加入硫酸酸浸过滤后的溶液中加入二氧化锰氧化亚铁离子,加入10%的氢氧化钠
2 2溶液调节溶液pH=4.5使铁离子全部沉淀,过滤后的滤液中加入NaS沉淀重金属离子可以除去Pb2+、Al3+等
2
离子,滤液中加入碳铵发生复分解反应生成碳酸锰,分离烘干得到成品。
(1)步骤D中加入MnO 氧化溶液中的Fe2+,其中Mn从+4价降为+2价,Fe从+2价升高为+3价,Fe2+是
2
还原剂,根据电子守恒,氧化剂与还原剂的物质的量之比为1∶2;
(2)在含有Mn2+的溶液中加入NH HCO 生成MnCO 沉淀,发生反应的离子方程式为Mn2++2
4 3 3
=MnCO↓+CO↑+HO;
3 2 2
(3)Mn从+2价升高为+7价,S从+7价降为+6价,根据电子守恒,Mn2+前系数为2, 前系数为5,再
结合电荷守恒和原子守恒得此反应的离子方程式2Mn2++5 +8HO=16H++10 +2 。
2
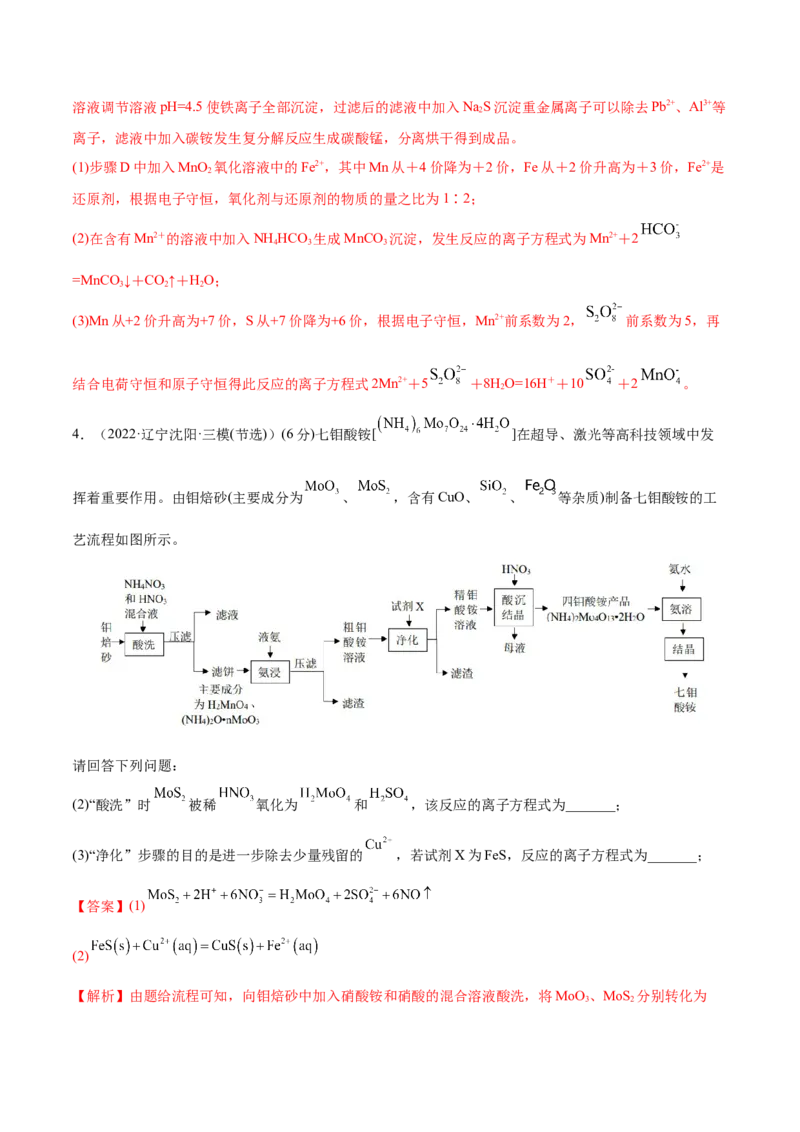
4.(2022·辽宁沈阳·三模(节选))(6分)七钼酸铵[ ]在超导、激光等高科技领域中发
挥着重要作用。由钼焙砂(主要成分为 、 ,含有CuO、 、 等杂质)制备七钼酸铵的工
艺流程如图所示。
请回答下列问题:
(2)“酸洗”时 被稀 氧化为 和 ,该反应的离子方程式为_______;
(3)“净化”步骤的目的是进一步除去少量残留的 ,若试剂X为FeS,反应的离子方程式为_______;
【答案】(1)
(2)
【解析】由题给流程可知,向钼焙砂中加入硝酸铵和硝酸的混合溶液酸洗,将MoO 、MoS 分别转化为
3 2(NH )O·MoO、HMoO ,二氧化硅不反应,氧化铁、氧化铜溶于硝酸得到可溶性硝酸盐,过滤得到滤液
4 2 3 2 4
和滤饼;向滤饼中液氨氨浸,将钼元素转化为粗钼酸铵溶液,过滤得到粗钼酸铵溶液和滤渣;向粗钼酸铵
溶液中加入硫化亚铁净化,将溶液中残留的铜离子转化为硫化铜,过滤得到精钼酸铵溶液和滤渣;向精钼
酸铵溶液中加入硝酸酸沉结晶、过滤得到四钼酸铵,向四钼酸铵中加入氨水,在料液比为0.25g/mL、搅拌
转速为160r/min、冷却温度10℃的条件下氨溶、结晶得到七钼酸铵。
(1)酸洗时发生的反应为MoS 与稀HNO 反应生成HMoO 、NO和HSO ,反应的离子方程式为
2 3 2 4 2 4
,故答案为:
;
(2)由题意可知,向粗钼酸铵溶液中加入硫化亚铁净化的目的是将溶液中残留的铜离子转化为硫化铜,反应
的离子方程式为 故答案为: ;
5.(9分)现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系
如图所示(图中有些反应的生成物和反应的条件没有标出)。
请根据以上信息完成下列各题:
(1)写出实验室制备黄绿色气体乙的化学方程式:_______,
(2)反应③中的离子方程式是_______
(3)反应⑤的离子方程式是_______
【答案】(1)4HCl(浓)+MnO Cl↑+MnCl +2H O
2 2 2 2
(2) 2Al+2OH-+2H O=2AlO +3H ↑
2 2
(3)2Fe2++Cl=2Fe3++2Cl-
2
【解析】金属单质A焰色反应呈黄色,则A是Na,Na与HO反应产生气体甲是H,D溶液为NaOH,金
2 2属B和氢氧化钠溶液反应,说明B为Al,黄绿色气体乙为Cl,气体甲和氯气反应生成丙为HCl,物质E
2
为盐酸溶液,物质D是氢氧化钠,D和物质G反应生成红褐色沉淀H为Fe(OH) ,盐酸与金属C反应产生
3
金属氯化物,该氯化物与NaOH溶液反应产生Fe(OH) ,则C是Fe,F为FeCl 、G为FeCl 。
3 2 3
(1)气体乙为氯气,实验室利用二氧化锰和浓盐酸共热制取氯气,化学方程式为4HCl(浓)+MnO
2
Cl↑+MnCl +2H O;
2 2 2
(2)反应③为铝和NaOH溶液的反应,生成偏铝酸钠、氢气,离子方程式为2Al+2OH-+2H O= +3H ↑;
2 2
(3)结合分析可知,反应⑤为FeCl 与Cl 反应生成FeCl ,其离子方程式是2Fe2++Cl=2Fe3++2Cl-;
2 2 3 2
6.(2021·福建三明市·高三二模)(9分)从分金渣(主要成分为:AgCl、Ag S、PbSO 、BaSO)中获取高纯
2 4 4
银的流程如图所示:
已知:K (AgCl)=1.8×10-10,K (Ag S)=6.3×10-50。
sp sp 2
(1)“预处理”时主要反应的化学方程式为_______。
(2)“分银”时AgCl与NaSO 反应生成Ag(SO ) 的离子方程式为_______。
2 3 3
(3)“还原”时HCHO转化为HCOOH,其化学方程式为_______。
【答案】(1)2FeCl +Ag S=2FeCl +S+2AgCl
3 2 2
(2) AgCl+2SO = Ag(SO ) +Cl-
3
(3)2AgCl+HCHO+H O=2Ag+HCOOH+2HCl
2
【解析】分金渣加入氯化铁进行预处理,氯化铁与硫酸银反应生成氯化亚铁、单质硫;分银时,加入亚硫
酸钠,AgCl与NaSO 反应生成Ag(SO ) ,而PbSO 、BaSO 及生成的单质S不溶于水,则分银渣为
2 3 3 4 4
PbSO 、BaSO 及生成的单质S;过滤加入盐酸,使Ag(SO ) 生成氯化银沉淀,过滤氯化银与甲醛反应生
4 4 3
成甲酸、单质银和氯化氢。
(1)根据分金渣的成分,加入氯化铁时,氯化铁具有强氧化性,则只能与硫化银发生氧化还原反应,方程式
为2FeCl +Ag S=2FeCl +S+2AgCl;
3 2 2(2) “分银”时AgCl与NaSO 反应生成Ag(SO ) 和氯离子,离子方程式为AgCl+2SO = Ag(SO ) +Cl-;
2 3 3 3
(3)“还原”时HCHO与氯化银、水反应生成HCOOH、单质银,化学方程式为
2AgCl+HCHO+H O=2Ag+HCOOH+2HCl;
2
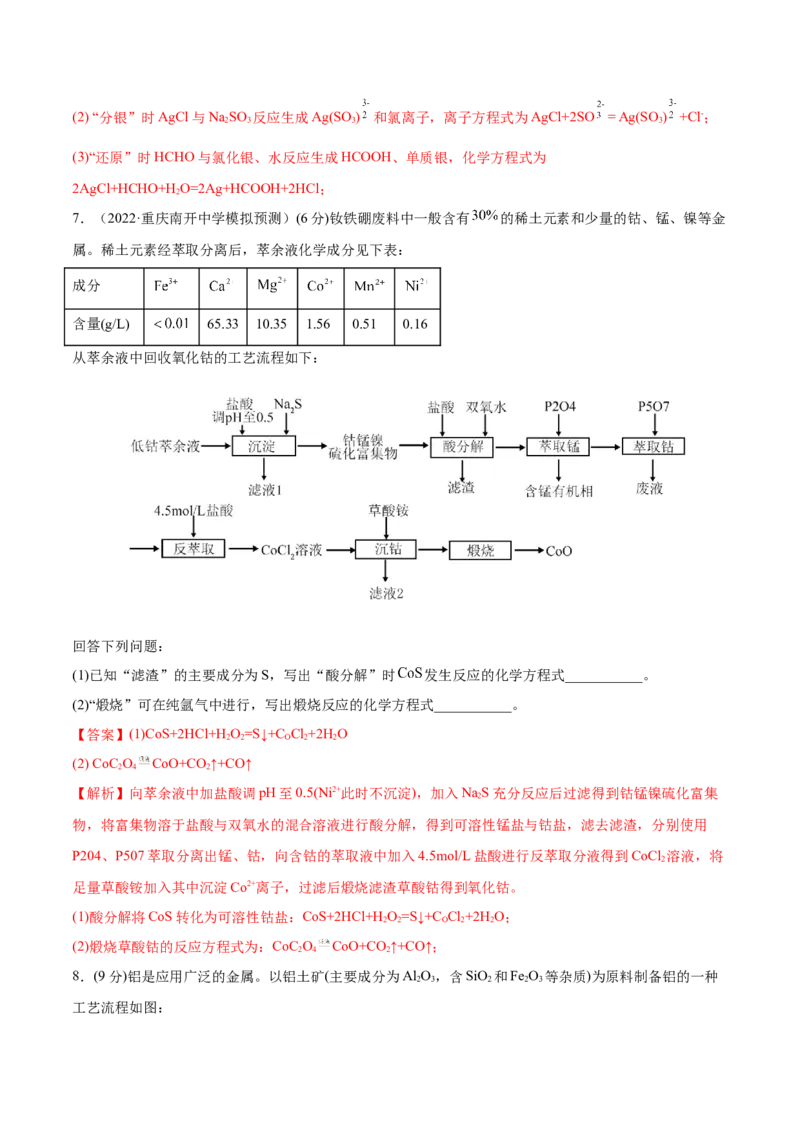
7.(2022·重庆南开中学模拟预测)(6分)钕铁硼废料中一般含有 的稀土元素和少量的钴、锰、镍等金
属。稀土元素经萃取分离后,萃余液化学成分见下表:
成分
含量(g/L) 65.33 10.35 1.56 0.51 0.16
从萃余液中回收氧化钴的工艺流程如下:
回答下列问题:
(1)已知“滤渣”的主要成分为S,写出“酸分解”时 发生反应的化学方程式___________。
(2)“煅烧”可在纯氩气中进行,写出煅烧反应的化学方程式___________。
【答案】(1)CoS+2HCl+H O=S↓+C Cl+2H O
2 2 O 2 2
(2) CoC O CoO+CO↑+CO↑
2 4 2
【解析】向萃余液中加盐酸调pH至0.5(Ni2+此时不沉淀),加入NaS充分反应后过滤得到钴锰镍硫化富集
2
物,将富集物溶于盐酸与双氧水的混合溶液进行酸分解,得到可溶性锰盐与钴盐,滤去滤渣,分别使用
P204、P507萃取分离出锰、钴,向含钴的萃取液中加入4.5mol/L盐酸进行反萃取分液得到CoCl 溶液,将
2
足量草酸铵加入其中沉淀Co2+离子,过滤后煅烧滤渣草酸钴得到氧化钴。
(1)酸分解将CoS转化为可溶性钴盐:CoS+2HCl+H O=S↓+C Cl+2H O;
2 2 O 2 2
(2)煅烧草酸钴的反应方程式为:CoC O CoO+CO↑+CO↑;
2 4 2
8.(9分)铝是应用广泛的金属。以铝土矿(主要成分为Al O,含SiO 和Fe O 等杂质)为原料制备铝的一种
2 3 2 2 3
工艺流程如图:注:SiO 在“碱溶”时转化为铝硅酸钠沉淀。
2
(1)“碱溶”时生成偏铝酸钠的离子方程式为_______
(2)“电解Ⅰ”是电解熔融Al O,写出阳极的电极反应式_______。
2 3
(3)“电解Ⅱ”是电解NaCO 溶液,原理如图所示。阳极的电极反应式为_______。
2 3
【答案】(1)AlO+2OH-=2 +H O
2 3 2
(2) 2O2--4e-=O ↑
2
(3)4 +2H O-4e-=4 +O ↑
2 2
【解析】铝土矿在碱溶时,其中的Al O 和SiO 可与强碱溶液反应,二氧化硅和强碱溶液反应后转化为沉
2 3 2
淀,氧化铝和氢氧化钠反应后得到可溶于水的偏铝酸钠,Fe O 不与强碱反应,则滤渣为Fe O;过滤后,
2 3 2 3
滤液中的NaAlO 与NaHCO 反应生成氢氧化铝沉淀和NaCO,氢氧化铝经灼烧后得到Al O,最后电解熔
2 3 2 3 2 3
融的Al O 得到铝。NaCO 溶液经电解后可以再生成NaHCO 和NaOH进行循环利用。
2 3 2 3 3
(1)“碱溶”时,铝土矿中的Al O 和SiO 能够与氢氧化钠反应,其中生成偏铝酸钠的离子方程式为
2 3 2
Al O+2OH-=2 +H O;
2 3 2
(2)“电解Ⅰ”是电解熔融Al O,电解过程中,阳极上生成氧气,能够氧化石墨生成二氧化碳,因此阳极的
2 3
电极反应为2O2--4e-=O ↑;
2
(3)“电解Ⅱ”是电解NaCO 溶液,阳极上是溶液中的水失电子生成氧气,产生的氢离子与碳酸根离子反应
2 3
生成碳酸氢根离子,电极反应为4 +2H O-4e-=4 +O ↑;
2 2
9.(2022·云南·昆明一中模拟预测)(6分)银催化剂在石油化工生产中应用广泛,但使用一段时间后催化
活性降低或失效。从失效的废银催化剂中回收银具有极高的社会、经济价值。废银催化剂主要由银和α-氧化铝及少量二氧化硅组成,其回收工艺流程如下:
回答下列问题:
(1)酸浸时,反应的离子方程式为 _______。
(2)AgCl沉淀还可以在氨水中用水合肼 还原为海绵状单质银,氧化产物为氮气,反应的化学方程式为
_______。
【答案】(1) 3Ag + +4H+=3Ag+ + NO↑+ 2H O
2
(2)4AgCl+N H·H O+4NH ·H O=4Ag+N↑+4NHCl+5H O
2 4 2 3 2 2 4 2
【解析】用硝酸溶解废银催化剂,过滤除去不溶于水和硝酸的二氧化硅和α-氧化铝,所得滤液中含有硝酸
银和过量的稀硝酸,向滤液中加入氯化钠生成氯化银沉淀,将过滤得到的氯化银和氧化铁反应生成氧化银,
再熔炼铸锭得到银锭。
(1)酸浸时,银河硝酸反应生成硝酸银和一氧化氮和水,反应的离子方程式为3Ag + +4H+=3Ag+ +
NO↑+ 2HO。
2
(2)AgCl在氨水中用水合肼 还原为海绵状单质银,氧化产物为氮气,根据氧化还原反应的电子守恒配平方
程式为:4AgCl+N H·H O+4NH ·H O=4Ag+N↑+4NHCl+5H O;
2 4 2 3 2 2 4 2
10.(2021·四川遂宁市·高三三模)(9分)以含锂的电解铝废渣(主要含AlF、NaF、LiF、CaO)和浓硫酸为
3
原料,制备电池级碳酸锂,同时得到副产品冰晶石的工艺流程如下:
已知:LiOH易溶于水,LiCO 微溶于水。回答下列问题:
2 3
(1)碱解反应中,同时得到气体和沉淀,反应的离子方程式为___________。
(2)上述流程得到的副产品冰晶石的化学方程式___________
(3)电池级LiCO 可由高纯度LiOH转化而来。将电池级LiCO 和C、FePO 高温下反应,生成LiFePO 和
2 3 2 3 4 4
一种可燃性气体,该反应的化学方程式为___________。【答案】(1)2Al3++3CO +3H O=2Al(OH) ↓+3CO ↑
2 3 2
(2)6HF+Na SO +NaAlO=NaAlF +H SO +2H O
2 4 2 6 2 4 2
(3)Li CO+2C+2Fe PO 2LiFePO +3CO↑
2 3 4 4
【解析】AlF、NaF、LiF、CaO和浓硫酸反应生成硫酸铝、硫酸钠、硫酸锂、硫酸钙和HF气体,硫酸钙
3
微溶于水,水浸得到硫酸铝、硫酸钠、硫酸锂溶液,滤渣1是硫酸钙;向溶液中加入碳酸钠溶液,生成氢
氧化铝沉淀、LiCO 沉淀、二氧化碳气体,过滤,得硫酸钠溶液和固体氧化铝、LiCO,氧化铝、LiCO
2 3 2 3 2 3
固体加水调浆,加入氧化钙将碳酸锂转化为氢氧化锂溶液,过滤,滤渣2是氢氧化铝,氢氧化锂溶液中通
入二氧化碳生成LiCO 产品;氢氧化铝加入氢氧化钠生成偏铝酸钠,偏铝酸钠、HF、硫酸钠反应生成
2 3
NaAlF 和HSO 。
3 6 2 4
(1)碱解反应中,硫酸铝与碳酸钠反应生成氢氧化铝沉淀、二氧化碳气体,反应的离子方程式为2Al3++3CO
+3H O=2Al(OH) ↓+3CO ↑;
2 3 2
(2) 偏铝酸钠、HF、硫酸钠反应生成NaAlF 和HSO ,反应的化学方程式为
3 6 2 4
6HF+Na SO +NaAlO=NaAlF +H SO +2H O;
2 4 2 6 2 4 2
(3)将电池级LiCO 和C、FePO 高温下反应,生成LiFePO 和一种可燃性气体,根据化合价升降规律,可
2 3 4 4
知生成的可燃性气体是CO,该反应的化学方程式为LiCO+2C+2Fe PO 2LiFePO +3CO↑。
2 3 4 4
11.(2022·陕西·西北工业大学附属中学模拟预测)(6分)铈的氧化物在半导体材料、高级颜料及汽车尾气
的净化器方面有广泛应用。以氟碳酸铈(主要含CeFCO)为原料制备CeO 的工艺流程如下:
3 2
已知:①CeO 具有较强的氧化性,难溶于一般的酸或碱。
2
②F-能和很多金属离子形成较为稳定的配合物,如Ce4+能与F-结合成CeF3+,Al3+也能与F-结合成AlF ;它的这种性质有利于酸浸步骤,却不利于后续的沉淀步骤。
③Ce4+能被萃取剂TBP萃取,而Ce3+不能。
回答下列问题:
(1)“氧化焙烧”后的固体产物中含有CeO 和CeF ,CeO 和CeF 的物质的量之比为3:1,“酸浸”时发生
2 4 2 4
反应的离子方程式为_______。
(2)“反萃取”步骤中发生反应的离子方程式为_______。
【答案】(2) 3CeO+CeF +12H+=4CeF3++6H O
2 4 2
(4)2CeTBP4+ +H O=2Ce3+ +O ↑+2H++TBP
2 2 2
【解析】二氧化铈通过氧气氧化焙烧获得CeO 和CeF ,再加入硫酸酸浸,形成CeF3+,反应为
2 4
3CeO+CeF +12H+=4CeF3++6H O,随后加入萃取剂TBP,形成CeTBP4+,在萃取过程中氟洗液中添加Al3+
2 4 2
,促进CeF3+ +TBP CeTBP4++F-正向进行然后进行反萃取, 发生反应2CeTBP4+ +H O=2Ce3+
2 2
+O ↑+2H++TBP ,形成Ce3+,通过加入氢氧化钠调节pH,先使A13+沉淀分离出Ce3+,随后再调节pH,使
2
Ce3+完全沉淀,再加次氨酸钠氧化形成Ce (OH) ,反应为: 2Ce (OH ) +NaClO+H O=2Ce (OH) ↓+NaCl,
4 3 2 4
最后煅烧生成CeO。
2
(1)已知题意中氧化焙烧后的固体产物中含有CeO 和CeF 物质的量之比为3 : 1,随后开始用硫酸酸浸,则
2 4
CeO 和硫酸反应生成Ce4 +,则Ce4+能与F结合成CeF3+,故而反应依据电荷守恒和原子守恒可得:
2
3CeO+CeF +12H+=4CeF3+ +6H O;
2 4 2
(2)“反萃取”步骤中加入了硫酸和双氧水,最终水层中有Ce3+产生, CeTBP4+中Ce为+4价,化合价降低,
说明发生了氧化还原,即双氧水做了还原剂,价态升高。故推测产物中有氧气产生,依据电子守恒、电荷守
恒和原子守恒,即可得反应方程式为:2CeTBP4+ +H O=2Ce3+ +O ↑+2H++TBP。
2 2 2
12.(2021·山东高三模拟)(6分)三氧化二钴(Co O)主要用作颜料、釉料、磁性材料、催化剂和氧化剂等。
2 3
以含钴废料(主要成分为Co O,含有少量MnO 、NiO、Fe O)为原料制备Co O 的流程如图所示。
2 3 2 3 4 2 3
已知:
Ⅰ.“酸浸”后的浸出液中含的阳离子有H+、Co2+、Fe3+、Ni2+等。
Ⅱ.部分阳离子以氢氧化物形式沉淀时溶液的pH如表。
沉淀物 Fe(OH) Co(OH) Ni(OH)
3 2 2完全沉淀时的pH 3.7 9.0 9.2
①“酸浸”时发生的主要反应是___(写离子方程式)。
②写出高温煅烧时发生的化学反应方程式___。
【答案】①Co O+H O+4H+=2Co2++3H O+O↑ ②2Co (OH) CO+O 2Co O+2H O+2CO
2 3 2 2 2 2 2 2 3 22 2 3 2 2
【解析】由题给流程可知,向研磨后的含钴废料中加入硫酸和双氧水,酸性条件下,氧化钴与双氧水发生
氧化还原反应生成亚钴离子,四氧化三铁与双氧水发生氧化还原反应生成铁离子,氧化亚镍溶于硫酸生成
亚镍离子,二氧化锰不溶解,过滤得到含有氢离子、亚钴离子、铁离子、亚镍离子的酸浸液和二氧化锰;
调节酸浸液的pH为3.7,铁离子转化为氢氧化铁沉淀,过滤得到含有亚钴离子、亚镍离子的滤液和滤渣1
氢氧化铁;向滤液中加入萃取剂,萃取分液得到含有亚钴离子的水相和含有亚镍离子的有机相;向水相中
加入氨水和碳酸氢铵溶液,亚钴离子离子转化为Co (OH) CO 沉淀,过滤得到含有硫酸铵的滤液和
2 2 3
Co (OH) CO 沉淀;高温煅烧,Co (OH)CO 与空气中的氧气发生氧化还原反应生成氧化钴、二氧化碳
2 2 3 2 2 3
和水。
①含钴废料中含有Co O、NiO、Fe O,“酸浸”后的溶液中含有Co2+,“酸浸”时发生的主要反应为
2 3 3 4
Co O 氧化HO,生成O 和Co2+,反应的离子方程式为Co O+H O+4H+=2Co2++3H O+O↑;
2 3 2 2 2 2 3 2 2 2 2
②高温煅烧时,Co (OH) CO 被氧化为Co O,所以反应的化学方程式为2Co (OH) CO+O
2 2 3 2 3 2 2 3 22
2Co O+2H O+2CO;
2 3 2 2
13.(2021·福建高三模拟)(10分)工业上制取硝酸铵的流程图如图,回答下列问题:
(1)设备Ⅱ发生反应的化学方程式为___。
(2)设备Ⅲ中生成HNO 化学方程式为____。
3
(3)设备Ⅳ中的尾气主要为NO,可以用NaClO溶液吸收,其他条件相同,NO转化为NO 的转化率随NaClO溶液初始pH的变化如图所示。
在酸NaClO性溶液中,HClO氧化NO生成Cl-和NO ,其离子方程式为__。
【答案】(1)4NH +5O 4NO+6H O (3分)
3 2 2
(2)4NO+3O +2H O=4HNO 或2NO+O =2NO,3NO +H O=2HNO +NO (3分)
2 2 3 2 2 2 2 3
(3)3HClO+2NO+H O=3Cl-+2NO +5H+或3ClO-+2NO+HO=3Cl-+2NO +2H+ (4分)
2 2
【解析】(1)由框图可知:设备Ⅱ是氨气和氧气在催化剂的条件下发生反应生成一氧化氮和水,其反应的化
学方程式为4NH +5O 4NO+6H O 。
3 2 2
(2) 由框图可知:设备Ⅲ中是一氧化氮和氧气反应生成二氧化氮,二氧化氮在和水反应生成一氧化氮和
HNO,该反应的化学方程式为2NO+O =2NO,3NO +H O=2HNO +NO,或4NO+3O +2H O=4HNO 。设
3 2 2 2 2 3 2 2 3
备Ⅲ在工作时不断通入空气的目的是使NO循环利用,最终全部转化成HNO,故答案:2NO+O =2NO,
3 2 2
3NO +H O=2HNO +NO,或4NO+3O +2H O=4HNO ;可使NO循环利用,全部转化成HNO。
2 2 3 2 2 3 3
(3)在酸性NaClO溶液中,HClO氧化NO生成Cl-和NO ,其离子方程式为3HClO+2NO+H O=3Cl-+2NO
2
+5H+或3ClO-+2NO+HO=3Cl-+2NO +2H+。
2