文档内容
专题 10 热化学方程式的书写与盖斯定律
1.已知:Rln K =-+C(C为常数),根据下图,该反应的反应热ΔH=______ kJ·mol-1。
p
2.CO 与CH 经催化重整,制得合成气:CH(g)+CO(g)2CO(g)+2H(g)。已知上述
2 4 4 2 2
反应中相关的化学键键能数据如下:
化学键 C—H C==O H—H C≡O(CO)
键能/ (kJ·mol-1) 413 745 436 1 075
则该反应的ΔH=____________。
3.近几年,大气污染越来越严重,雾霾天气对人们的生活、出行、身体健康产生了许多不
利的影响。汽车尾气是主要的大气污染源。降低汽车尾气危害的方法之一是在排气管上安装
催化转化器,发生的反应为2CO(g)+2NO(g)2CO(g)+N(g)。已知:
2 2
则2CO(g)+2NO(g)2CO(g)+N(g) ΔH=_____________(用含a、b、c、d的式子表示)。
2 2
4.工业上利用甲酸的能量关系转换图如图所示:
反应CO(g)+H(g)HCOOH(g)的ΔH=________ kJ·mol-1。
2 2
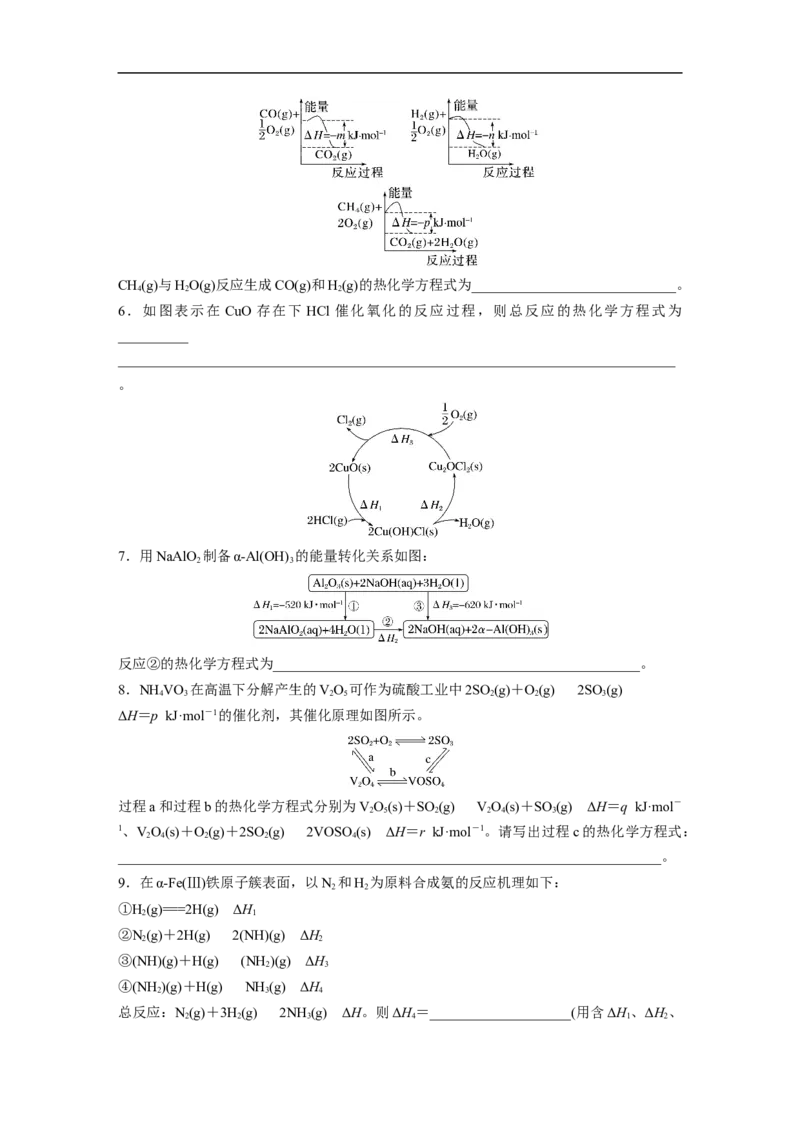
5.CO和H 是工业上最常用的合成气,制备该合成气的一种方法是以 CH 和HO为原料,
2 4 2
有关反应的能量变化如图所示。CH(g)与HO(g)反应生成CO(g)和H(g)的热化学方程式为_____________________________。
4 2 2
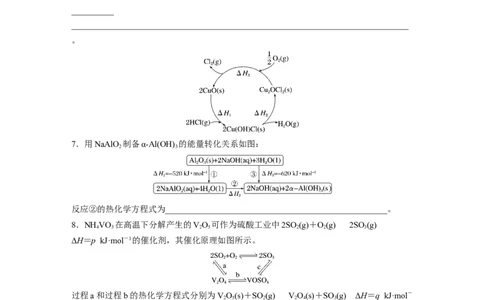
6.如图表示在 CuO 存在下 HCl 催化氧化的反应过程,则总反应的热化学方程式为
__________
_______________________________________________________________________________
。
7.用NaAlO 制备α-Al(OH) 的能量转化关系如图:
2 3
反应②的热化学方程式为____________________________________________________。
8.NH VO 在高温下分解产生的VO 可作为硫酸工业中2SO (g)+O(g)2SO (g)
4 3 2 5 2 2 3
ΔH=p kJ·mol-1的催化剂,其催化原理如图所示。
过程a和过程b的热化学方程式分别为VO(s)+SO (g)VO(s)+SO (g) ΔH=q kJ·mol-
2 5 2 2 4 3
1、VO(s)+O(g)+2SO (g)2VOSO(s) ΔH=r kJ·mol-1。请写出过程c的热化学方程式:
2 4 2 2 4
_____________________________________________________________________________。
9.在α-Fe(Ⅲ)铁原子簇表面,以N 和H 为原料合成氨的反应机理如下:
2 2
①H(g)===2H(g) ΔH
2 1
②N(g)+2H(g)2(NH)(g) ΔH
2 2
③(NH)(g)+H(g)(NH )(g) ΔH
2 3
④(NH )(g)+H(g)NH (g) ΔH
2 3 4
总反应:N(g)+3H(g)2NH (g) ΔH。则ΔH =____________________(用含ΔH 、ΔH 、
2 2 3 4 1 2ΔH、ΔH的式子表示)。
3
10.氨基甲酸铵(H NCOONH )为尿素生产过程的中间产物,易分解,某小组对氨基甲酸铵
2 4
的分解实验进行探究。已知:
Ⅰ.N (g)+3H(g)2NH (g)
2 2 3
ΔH=-92.4 kJ·mol-1
1
Ⅱ.C(s)+O(g)CO(g)
2 2
ΔH=-393.8 kJ·mol-1
2
Ⅲ.N (g)+3H(g)+C(s)+O(g)HNCOONH (s) ΔH=-645.7 kJ·mol-1
2 2 2 2 4 3
写出HNCOONH 分解生成NH 与CO 气体的热化学方程式:__________________________
2 4 3 2
_______________________________________________________________________________
。
11.甲醇(CHOH)可替代汽油作为公交车的燃料,写出由CO和H 生产甲醇的化学方程式:
3 2
________________________________________________________________________。
用该反应合成1 mol液态甲醇放出热量128.1 kJ。
又知2H(g)+CO(g)+O(g)===CO(g)+2HO(g) ΔH=-766.6 kJ·mol-1,HO(g)===HO(l)
2 2 2 2 2 2
ΔH=-44 kJ·mol-1。
请写出表示甲醇燃烧热的热化学方程式:__________________________________________。
12.科研工作者目前正在尝试以二氧化钛(TiO)催化分解汽车尾气的研究。已知:反应Ⅰ:
2
2NO(g)+O(g)===2NO (g) ΔH=-113.0 kJ·mol-1
2 2 1
反应Ⅱ:2SO (g)+O(g)===2SO (l)
2 2 3
ΔH=-288.4 kJ·mol-1
2
反应Ⅲ:3NO (g)+HO(l)===2HNO(l)+NO(g) ΔH=-138.0 kJ·mol-1
2 2 3 3
则反应NO (g)+SO (g)===NO(g)+SO (l)
2 2 3
ΔH=__________________。
4
13.实验室可用KClO 分解制取O,KClO 受热分解的反应分两步进行:
3 2 3
①4KClO(s)===3KClO(s)+KCl(s)
3 4
②KClO(s)===KCl(s)+2O(g)
4 2
已知:
K(s)+Cl(g)===KCl(s)
2
ΔH=-437 kJ·mol-1
K(s)+Cl(g)+O(g)===KClO(s)
2 2 3
ΔH=-398 kJ·mol-1
K(s)+Cl(g)+2O(g)===KClO(s)
2 2 4
ΔH=-433 kJ·mol-1
则反应4KClO(s)===3KClO(s)+KCl(s)的ΔH=__________ kJ·mol-1。
3 4
14.下图是 2LiBH /MgH 体系放氢焓变示意图,则:Mg(s)+2B(s)===MgB (s) ΔH=
4 2 2________
_______________________________________________________________________________
。
15.氮和碳的氧化物分别是造成大气污染、温室效应的主要物质。
请回答下列问题:
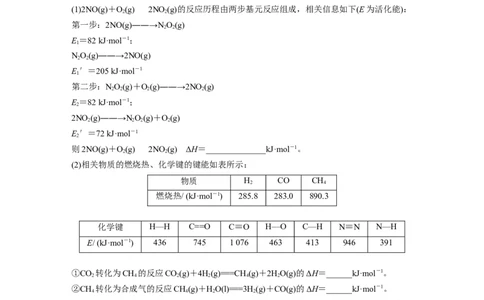
(1)2NO(g)+O(g)2NO (g)的反应历程由两步基元反应组成,相关信息如下(E为活化能):
2 2
第一步:2NO(g)――→NO(g)
2 2
E=82 kJ·mol-1;
1
NO(g)――→2NO(g)
2 2
E′=205 kJ·mol-1
1
第二步:NO(g)+O(g)――→2NO (g)
2 2 2 2
E=82 kJ·mol-1;
2
2NO (g)――→NO(g)+O(g)
2 2 2 2
E′=72 kJ·mol-1
2
则2NO(g)+O(g)2NO (g) ΔH=______________kJ·mol-1。
2 2
(2)相关物质的燃烧热、化学键的键能如表所示:
物质 H CO CH
2 4
燃烧热/ (kJ·mol-1) 285.8 283.0 890.3
化学键 H—H C==O C≡O H—O C—H N≡N N—H
E/ (kJ·mol-1) 436 745 1 076 463 413 946 391
①CO 转化为CH 的反应CO(g)+4H(g)===CH(g)+2HO(g)的ΔH=______kJ·mol-1。
2 4 2 2 4 2
②CH 转化为合成气的反应CH(g)+HO(l)===3H(g)+CO(g)的ΔH=______kJ·mol-1。
4 4 2 2
16.如图是发射卫星时用肼(N H)作燃料,用NO 作氧化剂(反应生成N 、水蒸气)和用F 作
2 4 2 2 2
氧化剂(反应生成N、HF)的反应原理。
2通过计算,可知原理 Ⅰ 和原理 Ⅱ 氧化气态肼生成氮气的热化学方程式分别为
___________
____________________________、_________________________,
消耗等量的NH(g)时释放能量较多的是原理__________(填“Ⅰ”或“Ⅱ”)。
2 4