文档内容
★ 启用前·绝密★
吉林市普通高中 2022—2023 学年度高中毕业年级第二次调研测试
化 学
说明:本试卷分Ⅰ卷、Ⅱ卷两部分。将第Ⅰ、Ⅱ卷的答案填在答题卡中。考试结束时上交
答题卡。考试时间90分钟,满分100分。
可能用到的相对原子质量:H1 C12 O16 Na23 Fe56
第Ⅰ卷 选择题(共50分)
一、选择题(每小题只有一个正确答案,1-10每题2分,11-20每题3分,共50分)
1. 开发和利用自然资源,必须遵循减量化、再利用和再循环的原则,践行绿色发展理念。
下列做法不值得提倡的是
A.选用一次性筷子、纸杯和塑料袋
B.选用回收废纸制造的纸箱
C.将生活垃圾进行分类处理
D.选乘公共交通工具出行
2. 氢能是公认的低碳、绿色清洁能源,氢能开发中一个重要问题是如何制取氢气。以下
研究方向你认为不可行的是
A.建设水电站,用电力分解水制取氢气
B.寻找更多的化石燃料,利用其燃烧放热,使水分解产生氢气
C.设法将太阳光聚焦,产生高温,使水分解产生氢气
D.寻找特殊的化学物质作催化剂,用于分解水制取氢气
3. 下列物质中,水解的最终产物可以发生银镜反应的是
A.油脂 B.蔗糖 C.蛋白质 D.乙酸乙酯
4. 下列化学用语表示错误的是
A.次氯酸的电子式: B.丙烷的球棍模型:
C.钠原子的原子结构示意图: D.原子核内有10个中子的氧原子:
5.下列气体中,既可用浓硫酸干燥,又可用碱石灰固体干燥的是
A.Cl B.NH C.SO D.H
2 3 2 2
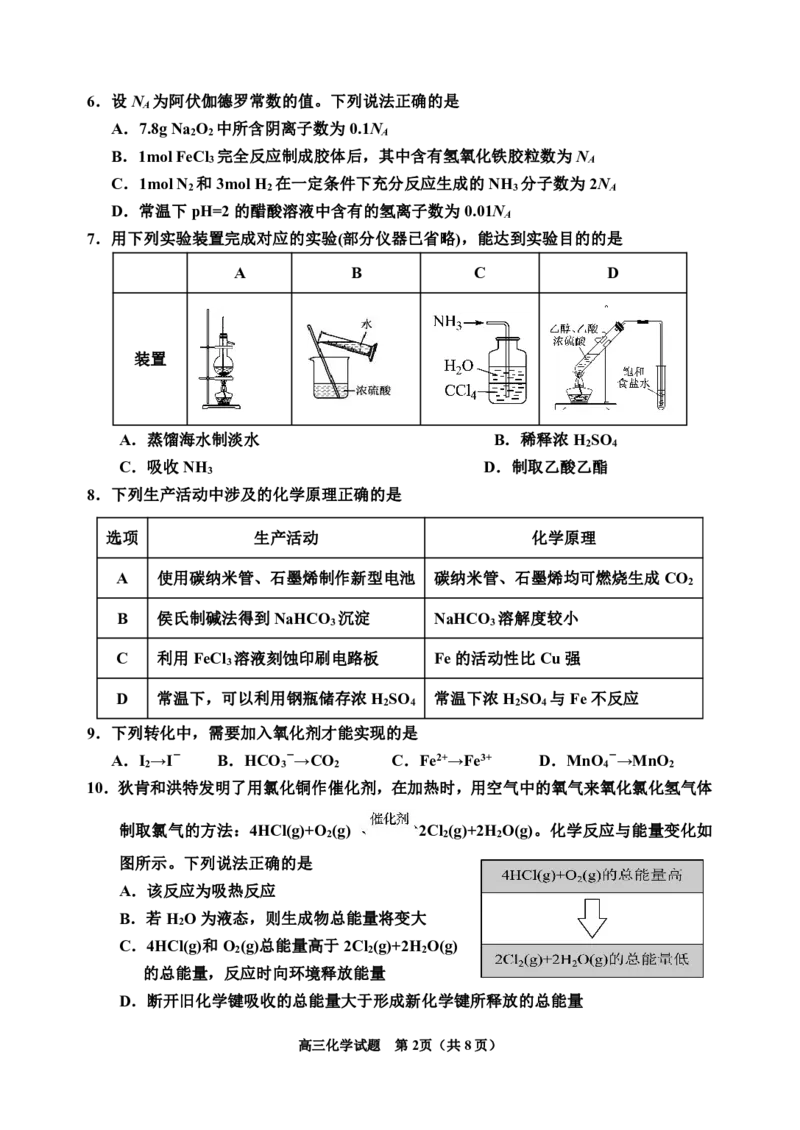
高三化学试题 第1页(共8页)6.设N 为阿伏伽德罗常数的值。下列说法正确的是
A
A.7.8gNa O 中所含阴离子数为0.1N
2 2 A
B.1molFeCl 完全反应制成胶体后,其中含有氢氧化铁胶粒数为N
3 A
C.1molN
2
和3molH
2
在一定条件下充分反应生成的NH
3
分子数为2N
A
D.常温下pH=2的醋酸溶液中含有的氢离子数为0.01N
A
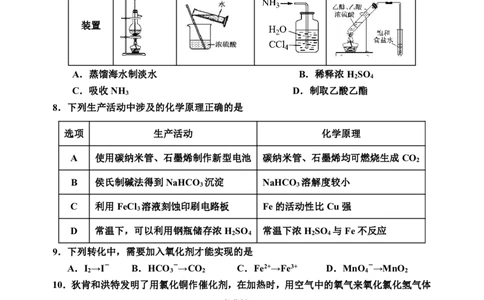
7.用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的的是
A B C D
装置
A.蒸馏海水制淡水 B.稀释浓H SO
2 4
C.吸收NH D.制取乙酸乙酯
3
8.下列生产活动中涉及的化学原理正确的是
选项 生产活动 化学原理
A 使用碳纳米管、石墨烯制作新型电池 碳纳米管、石墨烯均可燃烧生成CO
2
B 侯氏制碱法得到NaHCO 沉淀 NaHCO 溶解度较小
3 3
C 利用FeCl 溶液刻蚀印刷电路板 Fe的活动性比Cu强
3
D 常温下,可以利用钢瓶储存浓H SO 常温下浓H SO 与Fe不反应
2 4 2 4
9.下列转化中,需要加入氧化剂才能实现的是
A.I →I- B.HCO -→CO C.Fe2+→Fe3+ D.MnO -→MnO
2 3 2 4 2
10.狄肯和洪特发明了用氯化铜作催化剂,在加热时,用空气中的氧气来氧化氯化氢气体
制取氯气的方法:4HCl(g)+O (g) 2Cl (g)+2H O(g)。化学反应与能量变化如
2 2 2
图所示。下列说法正确的是
A.该反应为吸热反应
B.若H O为液态,则生成物总能量将变大
2
C.4HCl(g)和O (g)总能量高于2Cl (g)+2H O(g)
2 2 2
的总能量,反应时向环境释放能量
D.断开旧化学键吸收的总能量大于形成新化学键所释放的总能量
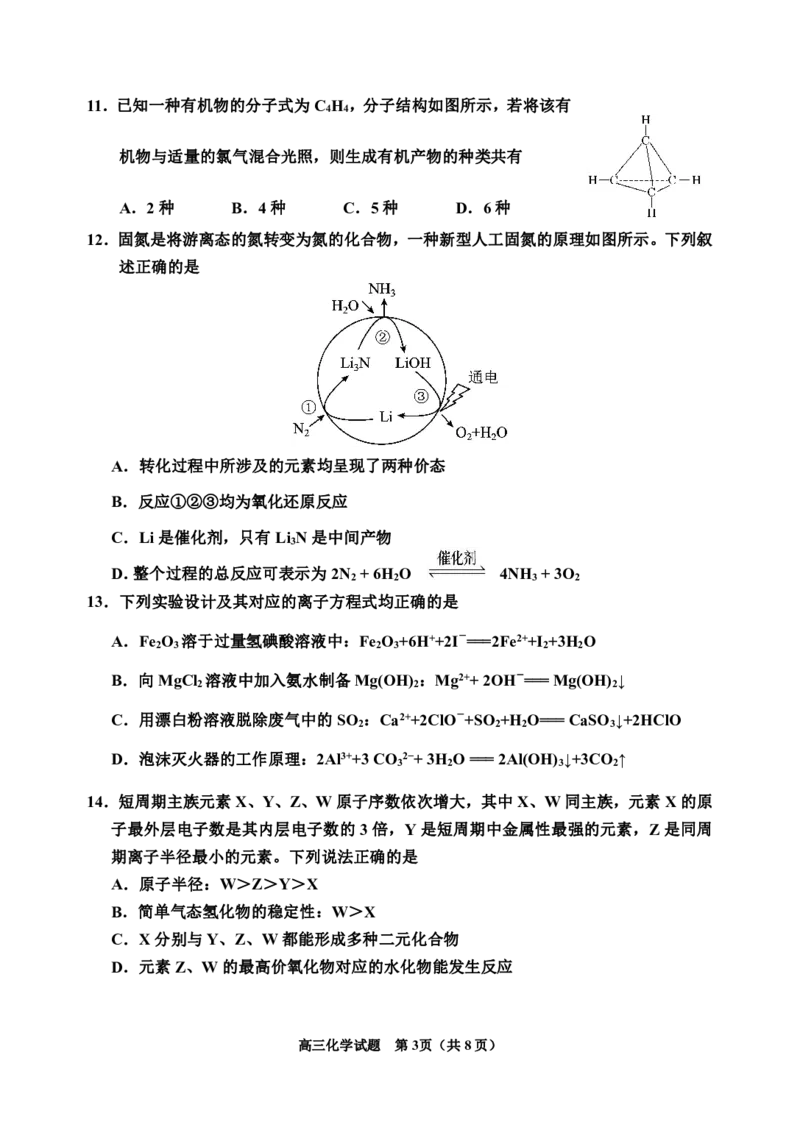
高三化学试题 第2页(共8页)11.已知一种有机物的分子式为C H ,分子结构如图所示,若将该有
4 4
机物与适量的氯气混合光照,则生成有机产物的种类共有
A.2种 B.4种 C.5种 D.6种
12.固氮是将游离态的氮转变为氮的化合物,一种新型人工固氮的原理如图所示。下列叙
述正确的是
A.转化过程中所涉及的元素均呈现了两种价态
B.反应①②③均为氧化还原反应
C.Li是催化剂,只有Li N是中间产物
3
D.整个过程的总反应可表示为2N +6H O 4NH +3O
2 2 3 2
13.下列实验设计及其对应的离子方程式均正确的是
A.Fe O 溶于过量氢碘酸溶液中:Fe O +6H++2I-===2Fe2++I +3H O
2 3 2 3 2 2
B.向MgCl 溶液中加入氨水制备Mg(OH) :Mg2++2OH-===Mg(OH) ↓
2 2 2
C.用漂白粉溶液脱除废气中的SO :Ca2++2ClO-+SO +H O===CaSO ↓+2HClO
2 2 2 3
D.泡沫灭火器的工作原理:2Al3++3CO 2−+3H O===2Al(OH) ↓+3CO ↑
3 2 3 2
14.短周期主族元素X、Y、Z、W原子序数依次增大,其中X、W同主族,元素X的原
子最外层电子数是其内层电子数的3倍,Y是短周期中金属性最强的元素,Z是同周
期离子半径最小的元素。下列说法正确的是
A.原子半径:W>Z>Y>X
B.简单气态氢化物的稳定性:W>X
C.X分别与Y、Z、W都能形成多种二元化合物
D.元素Z、W的最高价氧化物对应的水化物能发生反应
高三化学试题 第3页(共8页)15.常温下,下列各组离子在指定溶液中能大量共存的是
A.pH=1的溶液中:Fe2+、NO -、SO 2−、K +
3 4
B.由水电离的c(H + )=1×10−14mol/L的溶液中:Al3+、K +、Cl-、HCO -
3
C.
c(H+)
=1012的溶液中:NH +、Al3+、NO -、Cl-
c(OH-) 4 3
D.c(Fe3+ )=0.1mol/L的溶液中:K +、ClO-、SO 2−、SCN-
4
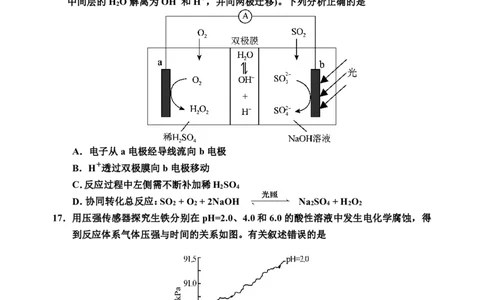
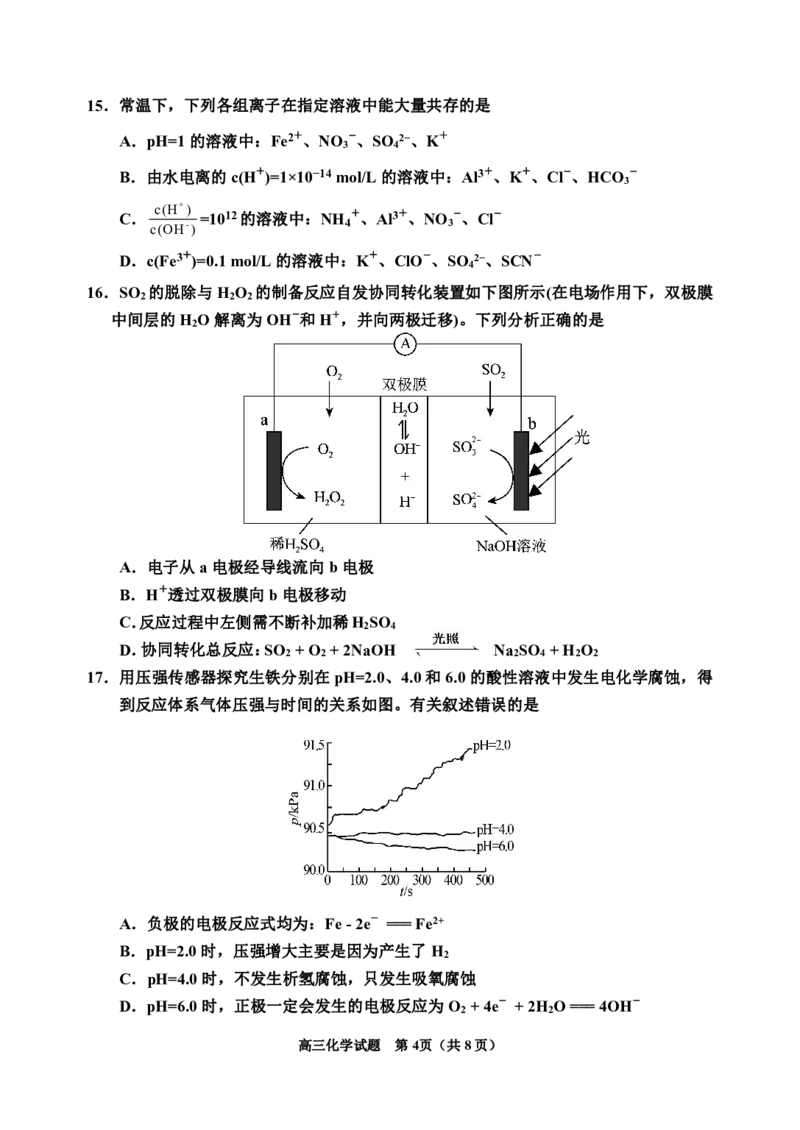
16.SO 的脱除与H O 的制备反应自发协同转化装置如下图所示(在电场作用下,双极膜
2 2 2
中间层的H O解离为OH-和H+,并向两极迁移)。下列分析正确的是
2
A.电子从a电极经导线流向b电极
B.H +透过双极膜向b电极移动
C.反应过程中左侧需不断补加稀H SO
2 4
D.协同转化总反应:SO +O +2NaOH Na SO +H O
2 2 2 4 2 2
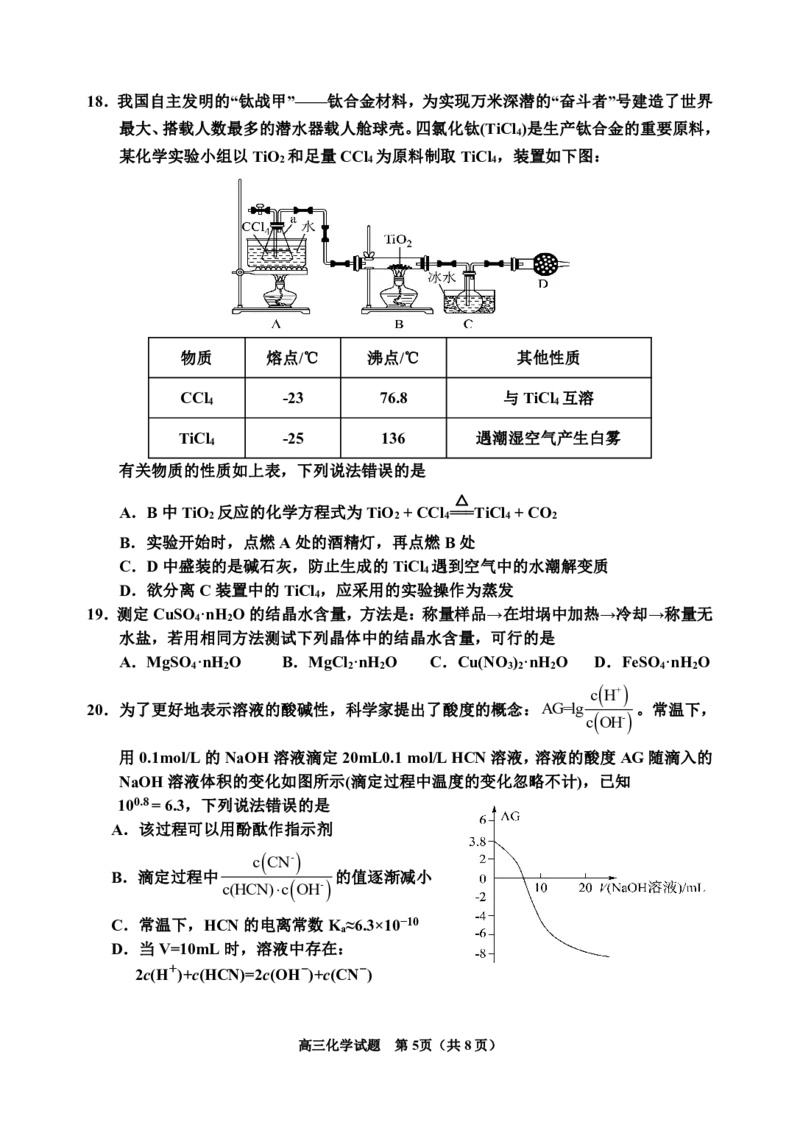
17.用压强传感器探究生铁分别在pH=2.0、4.0和6.0的酸性溶液中发生电化学腐蚀,得
到反应体系气体压强与时间的关系如图。有关叙述错误的是
A.负极的电极反应式均为:Fe-2e- ===Fe2+
B.pH=2.0时,压强增大主要是因为产生了H
2
C.pH=4.0时,不发生析氢腐蚀,只发生吸氧腐蚀
D.pH=6.0时,正极一定会发生的电极反应为O +4e- +2H O===4OH-
2 2
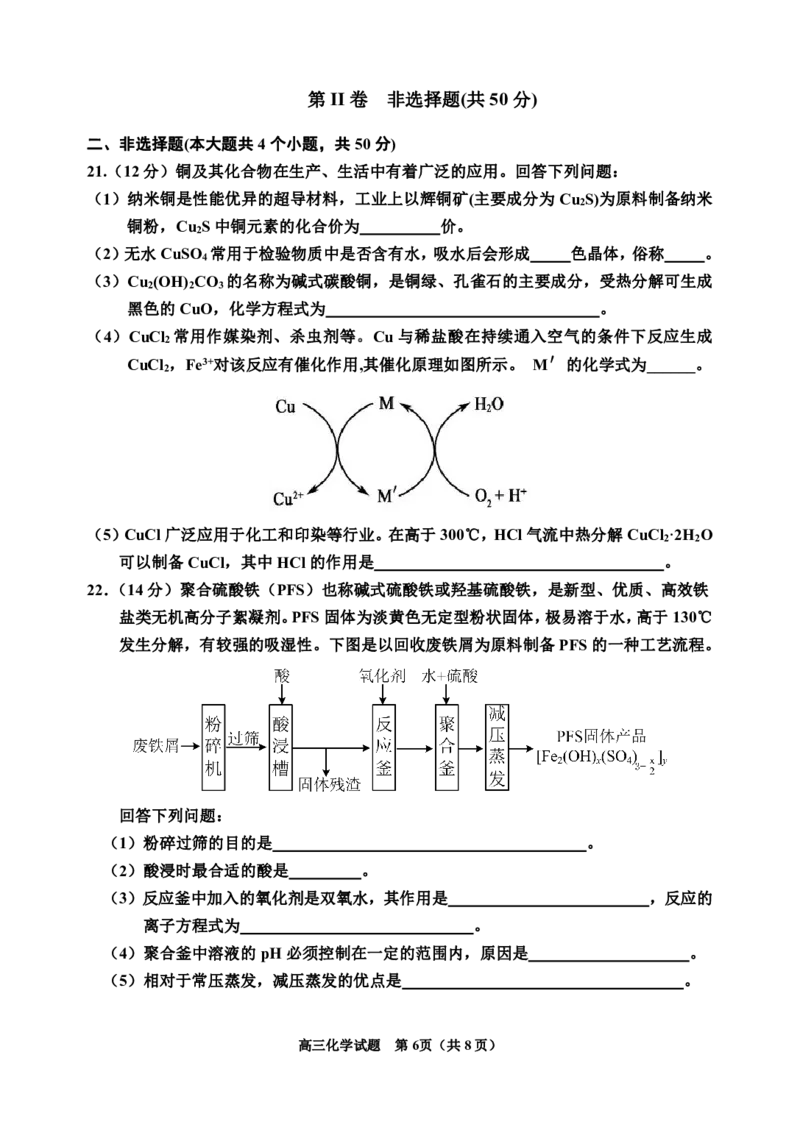
高三化学试题 第4页(共8页)18.我国自主发明的“钛战甲”——钛合金材料,为实现万米深潜的“奋斗者”号建造了世界
最大、搭载人数最多的潜水器载人舱球壳。四氯化钛(TiCl )是生产钛合金的重要原料,
4
某化学实验小组以TiO 和足量CCl 为原料制取TiCl ,装置如下图:
2 4 4
物质 熔点/℃ 沸点/℃ 其他性质
CCl -23 76.8 与TiCl 互溶
4 4
TiCl -25 136 遇潮湿空气产生白雾
4
有关物质的性质如上表,下列说法错误的是
A.B中TiO 反应的化学方程式为TiO +CCl ===TiCl +CO
2 2 4 4 2
△
B.实验开始时,点燃A处的酒精灯,再点燃B处
C.D中盛装的是碱石灰,防止生成的TiCl 遇到空气中的水潮解变质
4
D.欲分离C装置中的TiCl ,应采用的实验操作为蒸发
4
19.测定CuSO ·nH O的结晶水含量,方法是:称量样品→在坩埚中加热→冷却→称量无
4 2
水盐,若用相同方法测试下列晶体中的结晶水含量,可行的是
A.MgSO ·nH O B.MgCl ·nH O C.Cu(NO ) ·nH O D.FeSO ·nH O
4 2 2 2 3 2 2 4 2
c
H+
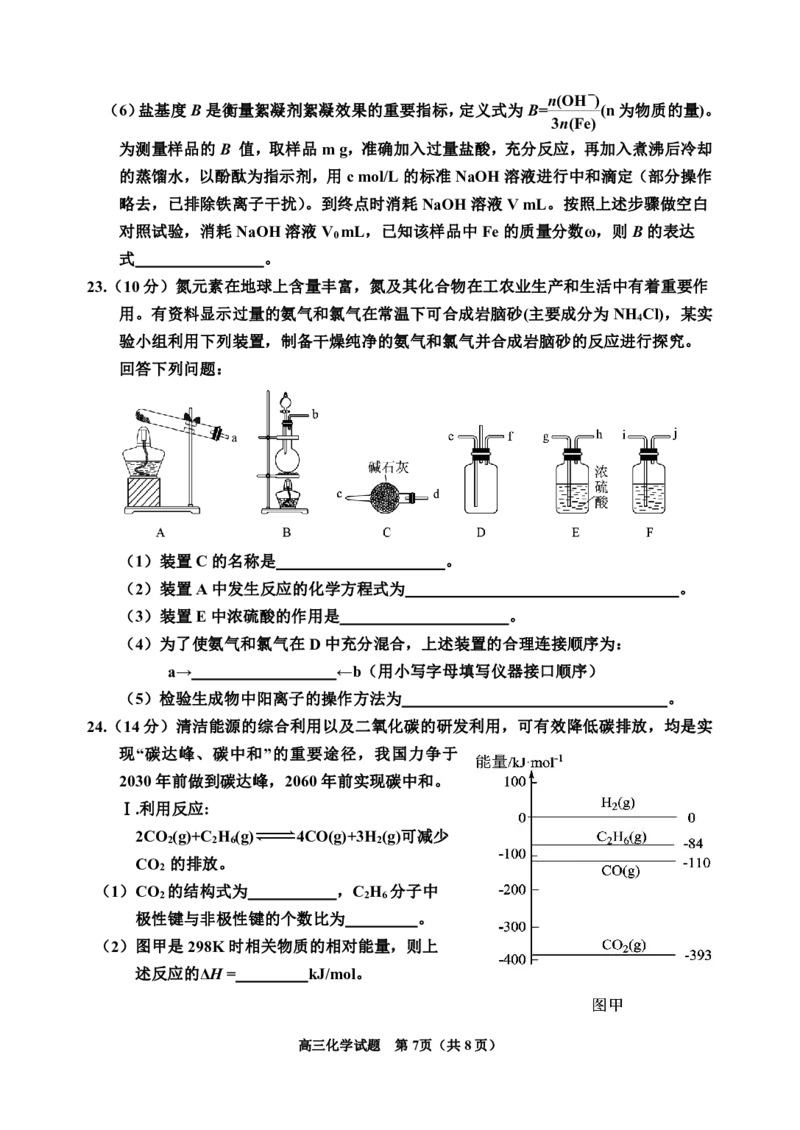
20.为了更好地表示溶液的酸碱性,科学家提出了酸度的概念:AG=lg 。常温下,
c
OH-
用0.1mol/L的NaOH溶液滴定20mL0.1mol/LHCN溶液,溶液的酸度AG随滴入的
NaOH溶液体积的变化如图所示(滴定过程中温度的变化忽略不计),已知
100.8=6.3,下列说法错误的是
A.该过程可以用酚酞作指示剂
c
CN-
B.滴定过程中 的值逐渐减小
c(HCN)c
OH-
C.常温下,HCN的电离常数K ≈6.3×10−10
a
D.当V=10mL时,溶液中存在:
2c(H + )+c(HCN)=2c(OH-)+c(CN-)
高三化学试题 第5页(共8页)第II 卷 非选择题(共50分)
二、非选择题(本大题共4个小题,共50分)
21.(12分)铜及其化合物在生产、生活中有着广泛的应用。回答下列问题:
(1)纳米铜是性能优异的超导材料,工业上以辉铜矿(主要成分为Cu S)为原料制备纳米
2
铜粉,Cu S中铜元素的化合价为 价。
2
(2)无水CuSO 常用于检验物质中是否含有水,吸水后会形成 色晶体,俗称 。
4
(3)Cu (OH) CO 的名称为碱式碳酸铜,是铜绿、孔雀石的主要成分,受热分解可生成
2 2 3
黑色的CuO,化学方程式为 。
(4)CuCl 常用作媒染剂、杀虫剂等。Cu与稀盐酸在持续通入空气的条件下反应生成
2
CuCl ,Fe3+对该反应有催化作用,其催化原理如图所示。 M ′的化学式为______。
2
(5)CuCl广泛应用于化工和印染等行业。在高于300℃,HCl气流中热分解CuCl ·2H O
2 2
可以制备CuCl,其中HCl的作用是 。
22.(14分)聚合硫酸铁(PFS)也称碱式硫酸铁或羟基硫酸铁,是新型、优质、高效铁
盐类无机高分子絮凝剂。PFS固体为淡黄色无定型粉状固体,极易溶于水,高于130℃
发生分解,有较强的吸湿性。下图是以回收废铁屑为原料制备PFS的一种工艺流程。
回答下列问题:
(1)粉碎过筛的目的是 。
(2)酸浸时最合适的酸是 。
(3)反应釜中加入的氧化剂是双氧水,其作用是 ,反应的
离子方程式为 。
(4)聚合釜中溶液的pH必须控制在一定的范围内,原因是 。
(5)相对于常压蒸发,减压蒸发的优点是 。
高三化学试题 第6页(共8页)n(OH-)
(6)盐基度B是衡量絮凝剂絮凝效果的重要指标,定义式为B= (n为物质的量)。
3n(Fe)
为测量样品的B 值,取样品mg,准确加入过量盐酸,充分反应,再加入煮沸后冷却
的蒸馏水,以酚酞为指示剂,用cmol/L的标准NaOH溶液进行中和滴定(部分操作
略去,已排除铁离子干扰)。到终点时消耗NaOH溶液VmL。按照上述步骤做空白
对照试验,消耗NaOH溶液V mL,已知该样品中Fe的质量分数ω,则B的表达
0
式 。
23.(10分)氮元素在地球上含量丰富,氮及其化合物在工农业生产和生活中有着重要作
用。有资料显示过量的氨气和氯气在常温下可合成岩脑砂(主要成分为NH Cl),某实
4
验小组利用下列装置,制备干燥纯净的氨气和氯气并合成岩脑砂的反应进行探究。
回答下列问题:
(1)装置C的名称是 。
(2)装置A中发生反应的化学方程式为 。
(3)装置E中浓硫酸的作用是 。
(4)为了使氨气和氯气在D中充分混合,上述装置的合理连接顺序为:
a→ ←b(用小写字母填写仪器接口顺序)
(5)检验生成物中阳离子的操作方法为 。
24.(14分)清洁能源的综合利用以及二氧化碳的研发利用,可有效降低碳排放,均是实
现“碳达峰、碳中和”的重要途径,我国力争于
2030年前做到碳达峰,2060年前实现碳中和。
Ⅰ.利用反应:
2CO (g)+C H (g) 4CO(g)+3H (g)可减少
2 2 6 2
CO 的排放。
2
(1)CO 的结构式为 ,C H 分子中
2 2 6
极性键与非极性键的个数比为 。
(2)图甲是298K时相关物质的相对能量,则上
述反应的ΔH= kJ/mol。
高三化学试题 第7页(共8页)(3)下列关于该反应的说法错误的是
a. 在恒容绝热的条件下,温度不再改变,说明该反应已达平衡状态
b. 在恒温恒压的条件下,充入稀有气体氦气,平衡不移动
c. 平衡向右移动,平衡常数K一定增大
d. 该反应在高温条件下自发
(4)该反应的净反应速率方程: v=k c2(CO )·c(C H )-k c4(CO)·c3(H )
正 2 2 6 逆 2
(k 、k 为速率常数,只与温度、催化剂、接触面积有关,与浓度无关)。温度为
正 逆
T ℃时,k =0.4k ,温度为T ℃时,k =1.6k ,则T _______T (填“>”、“<”或
1 正 逆 2 正 逆 1 2
“=”) 。
Ⅱ. 乙烯的产量是衡量一个国家石油化工发展水平的标准。国内第一套自主研发的乙烷
裂解制乙烯的大型生产装置建成。已知该项目中乙烷制乙烯的反应原理为:
主反应:C H (g) CH =CH (g)+H (g)
2 6 2 2 2
副反应:2C H (g) CH =CH (g)+2CH (g)
2 6 2 2 4
在一定温度下,在2L恒容密闭容器中充入7molC H 进行反应,达到平衡时CH
2 6 4
和H 的体积分数均为20%,则
2
(5)乙烷的总转化率为 (保留4位有效数字)。
(6)该温度下主反应的平衡常数K为 mol/L 。
命题、校对:化学学科核心组
高三化学试题 第8页(共8页)