文档内容
专项训练 化学反应原理综合题
1.(2023·全国·统考高考真题)甲烷选择性氧化制备甲醇是一种原子利用率高的方法。
回答下列问题:
(1)已知下列反应的热化学方程式:
①
②
反应③ 的 _______ ,平衡常数
_______(用 表示)。
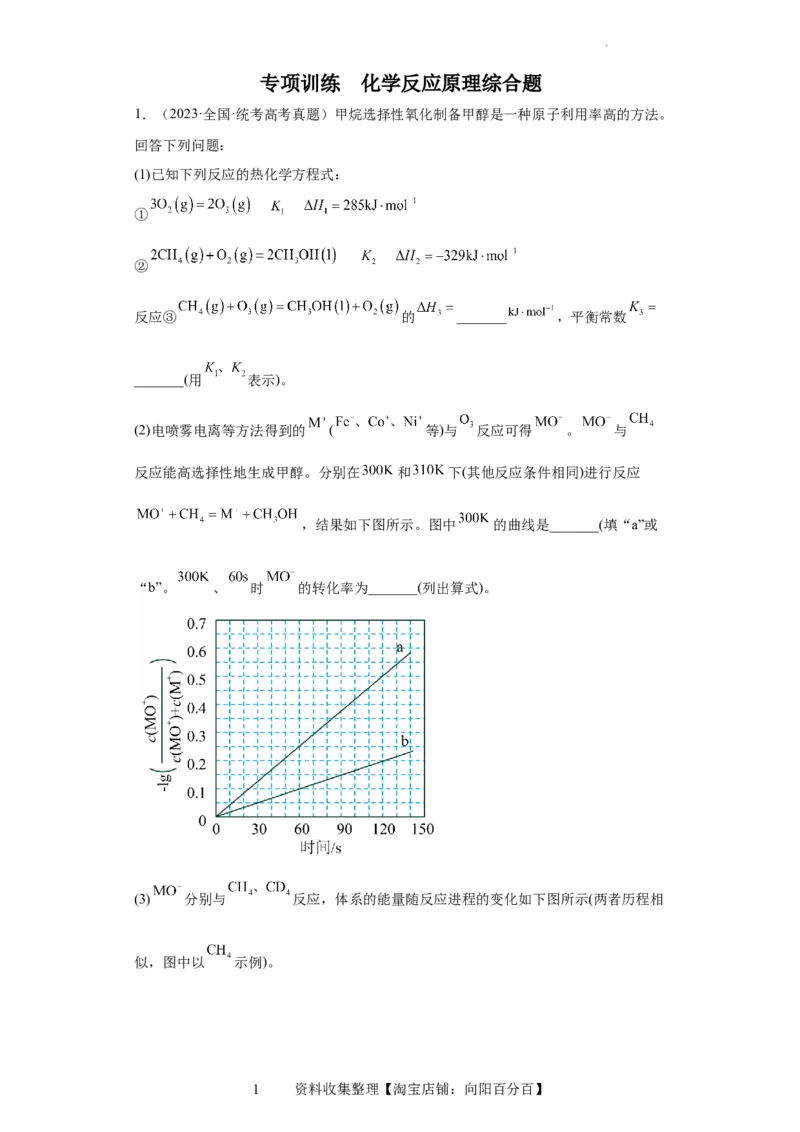
(2)电喷雾电离等方法得到的 ( 等)与 反应可得 。 与
反应能高选择性地生成甲醇。分别在 和 下(其他反应条件相同)进行反应
,结果如下图所示。图中 的曲线是_______(填“a”或
“b”。 、 时 的转化率为_______(列出算式)。
(3) 分别与 反应,体系的能量随反应进程的变化如下图所示(两者历程相
似,图中以 示例)。
1 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司(ⅰ)步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是_______(填“Ⅰ”或“Ⅱ”)。
(ⅱ)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则
与 反应的能量变化应为图中曲线_______(填“c”或“d”)。
(ⅲ) 与 反应,氘代甲醇的产量 _______ (填“>”“<”
或“=”)。若 与 反应,生成的氘代甲醇有_______种。
2.(2023·全国·统考高考真题)氨是最重要的化学品之一,我国目前氨的生产能力位
居世界首位。回答下列问题:
(1)根据图1数据计算反应 的 _______ 。
(2)研究表明,合成氨反应在 催化剂上可能通过图2机理进行(*表示催化剂表面吸附
位, 表示被吸附于催化剂表面的 )。判断上述反应机理中,速率控制步骤(即速
率最慢步骤)为_______(填步骤前的标号),理由是_______。
试卷第2页,共20页(3)合成氨催化剂前驱体(主要成分为 )使用前经 还原,生成 包裹的 。
已知 属于立方晶系,晶胞参数 ,密度为 ,则 晶胞中含有
的原子数为_______(列出计算式,阿伏加德罗常数的值为 )。
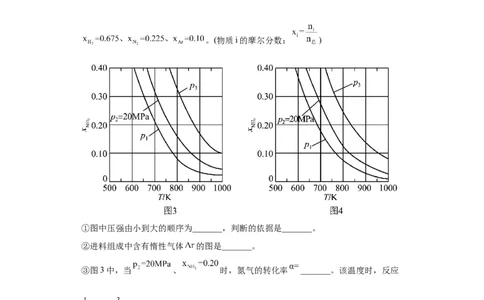
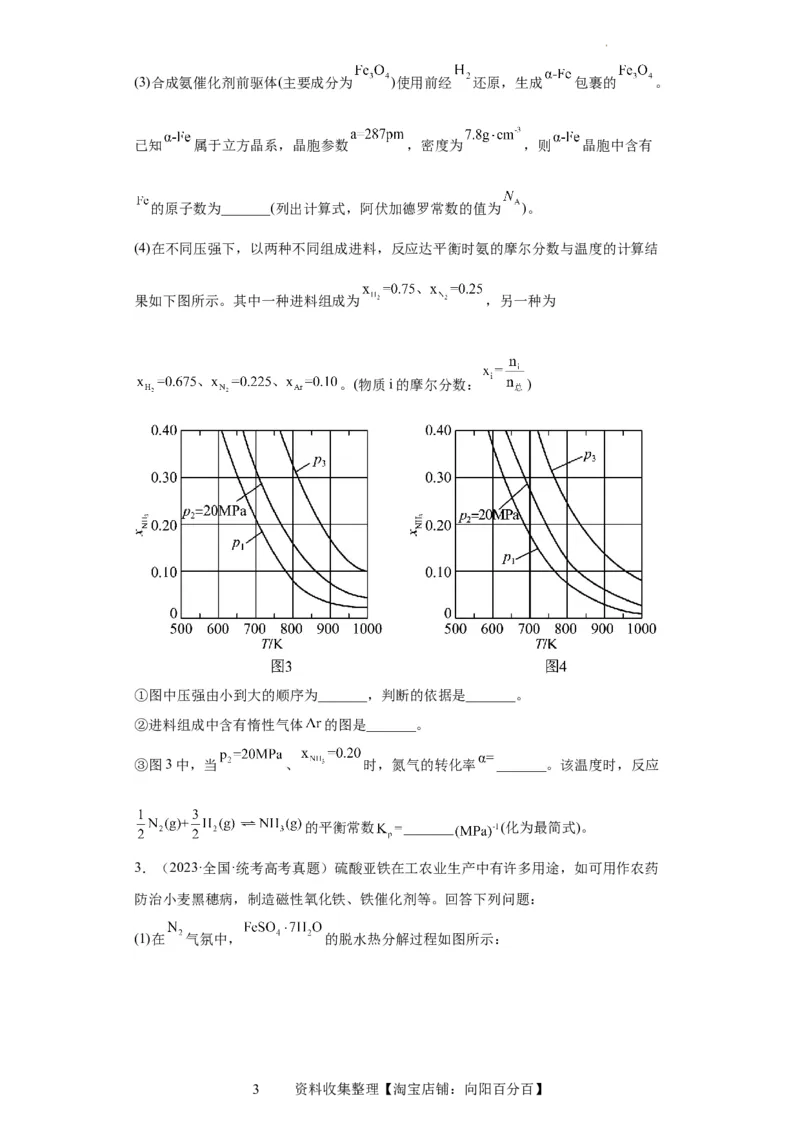
(4)在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结
果如下图所示。其中一种进料组成为 ,另一种为
。(物质i的摩尔分数: )
①图中压强由小到大的顺序为_______,判断的依据是_______。
②进料组成中含有惰性气体 的图是_______。
③图3中,当 、 时,氮气的转化率 _______。该温度时,反应
的平衡常数 _______ (化为最简式)。
3.(2023·全国·统考高考真题)硫酸亚铁在工农业生产中有许多用途,如可用作农药
防治小麦黑穗病,制造磁性氧化铁、铁催化剂等。回答下列问题:
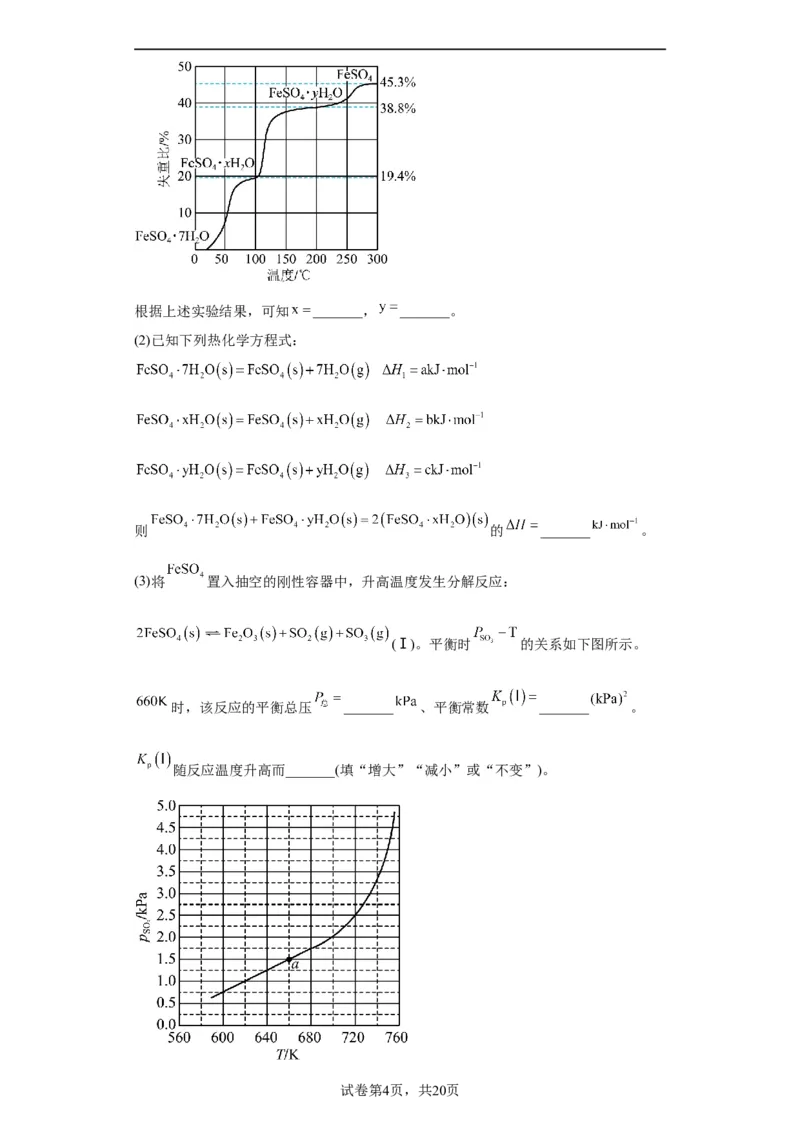
(1)在 气氛中, 的脱水热分解过程如图所示:
3 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司根据上述实验结果,可知 _______, _______。
(2)已知下列热化学方程式:
则 的 _______ 。
(3)将 置入抽空的刚性容器中,升高温度发生分解反应:
(Ⅰ)。平衡时 的关系如下图所示。
时,该反应的平衡总压 _______ 、平衡常数 _______ 。
随反应温度升高而_______(填“增大”“减小”或“不变”)。
试卷第4页,共20页(4)提高温度,上述容器中进一步发生反应 (Ⅱ),平衡时
_______(用 表示)。在 时, ,则
_______ , _______ (列出计算式)。
4.(2023·辽宁·统考高考真题)硫酸工业在国民经济中占有重要地位。
(1)我国古籍记载了硫酸的制备方法——“炼石胆(CuSO ·5H O)取精华法”。借助现代
4 2
仪器分析,该制备过程中CuSO ·5H O分解的TG曲线(热重)及DSC曲线(反映体系热
4 2
量变化情况,数值已省略)如下图所示。700℃左右有两个吸热峰,则此时分解生成的
氧化物有SO 、_______和_______(填化学式)。
2
(2)铅室法使用了大容积铅室制备硫酸(76%以下),副产物为亚硝基硫酸,主要反应如下:
NO +SO+H O=NO+H SO
2 2 2 2 4
2NO+O =2NO
2 2
(ⅰ)上述过程中NO 的作用为_______。
2
(ⅱ)为了适应化工生产的需求,铅室法最终被接触法所代替,其主要原因是_______(答
出两点即可)。
(3)接触法制硫酸的关键反应为SO 的催化氧化:
2
SO (g)+ O(g) SO (g) ΔH=-98.9kJ·mol-1
2 2 3
(ⅰ)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速
率(数值已略去)与温度的关系如下图所示,下列说法正确的是_______。
5 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司a.温度越高,反应速率越大
b.α=0.88的曲线代表平衡转化率
c.α越大,反应速率最大值对应温度越低
d.可根据不同 下的最大速率,选择最佳生产温度
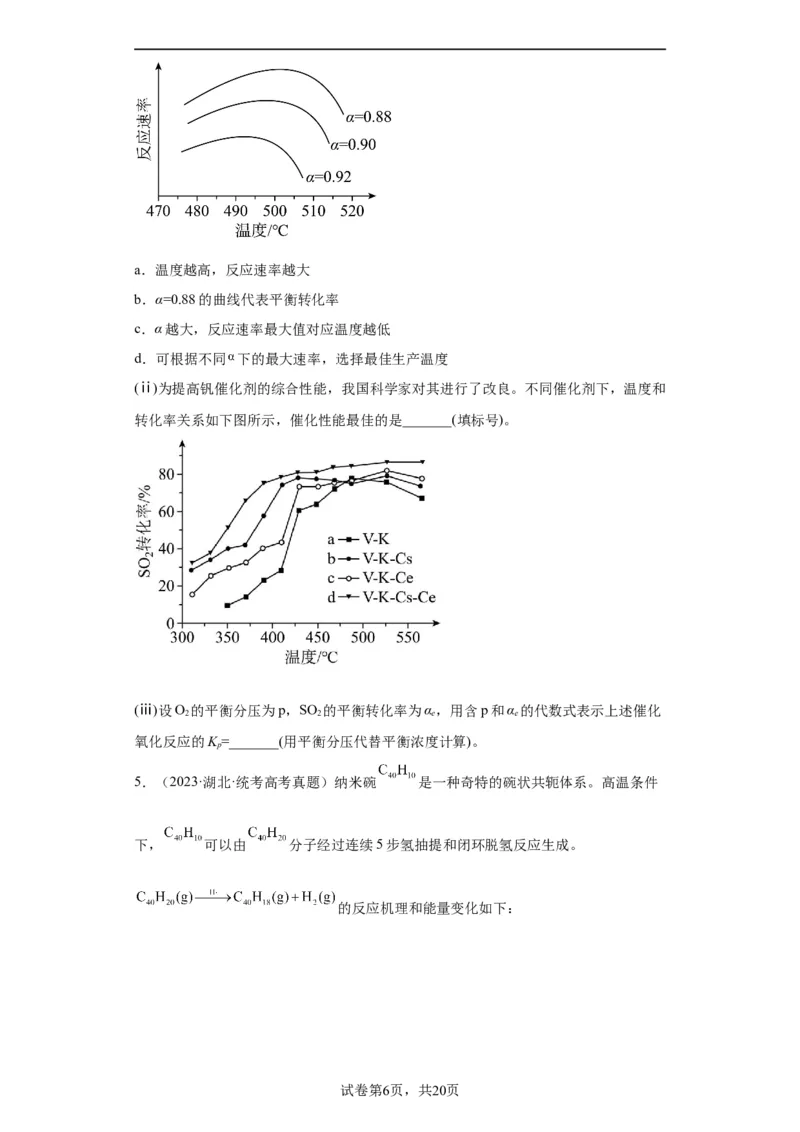
(ⅱ)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和
转化率关系如下图所示,催化性能最佳的是_______(填标号)。
(ⅲ)设O 的平衡分压为p,SO 的平衡转化率为α,用含p和α 的代数式表示上述催化
2 2 e e
氧化反应的K =_______(用平衡分压代替平衡浓度计算)。
p
5.(2023·湖北·统考高考真题)纳米碗 是一种奇特的碗状共轭体系。高温条件
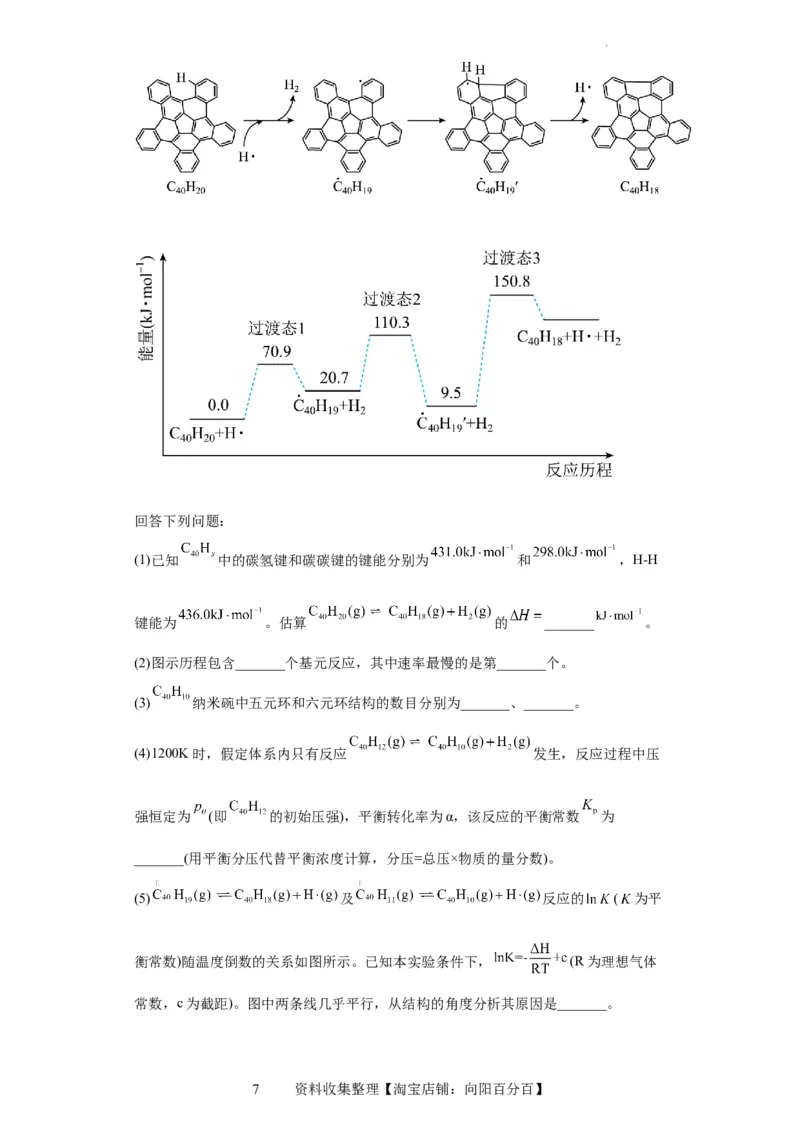
下, 可以由 分子经过连续5步氢抽提和闭环脱氢反应生成。
的反应机理和能量变化如下:
试卷第6页,共20页回答下列问题:
(1)已知 中的碳氢键和碳碳键的键能分别为 和 ,H-H
键能为 。估算 的 _______ 。
(2)图示历程包含_______个基元反应,其中速率最慢的是第_______个。
(3) 纳米碗中五元环和六元环结构的数目分别为_______、_______。
(4)1200K时,假定体系内只有反应 发生,反应过程中压
强恒定为 (即 的初始压强),平衡转化率为α,该反应的平衡常数 为
_______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5) 及 反应的 ( 为平
衡常数)随温度倒数的关系如图所示。已知本实验条件下, (R为理想气体
常数,c为截距)。图中两条线几乎平行,从结构的角度分析其原因是_______。
7 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司(6)下列措施既能提高反应物的平衡转化率,又能增大生成 的反应速率的是
_______(填标号)。
a.升高温度 b.增大压强 c.加入催化剂
6.(2023·湖南·统考高考真题)聚苯乙烯是一类重要的高分子材料,可通过苯乙烯聚
合制得。
Ⅰ.苯乙烯的制备
(1)已知下列反应的热化学方程式:
①
②
③
计算反应④ 的 _______ ;
(2)在某温度、 下,向反应器中充入 气态乙苯发生反应④,其平衡转化率
为50%,欲将平衡转化率提高至75%,需要向反应器中充入_______ 水蒸气作为稀
释气(计算时忽略副反应);
(3)在 、 下,以水蒸气作稀释气。 作催化剂,乙苯除脱氢生成苯乙烯
外,还会发生如下两个副反应:
⑤
⑥
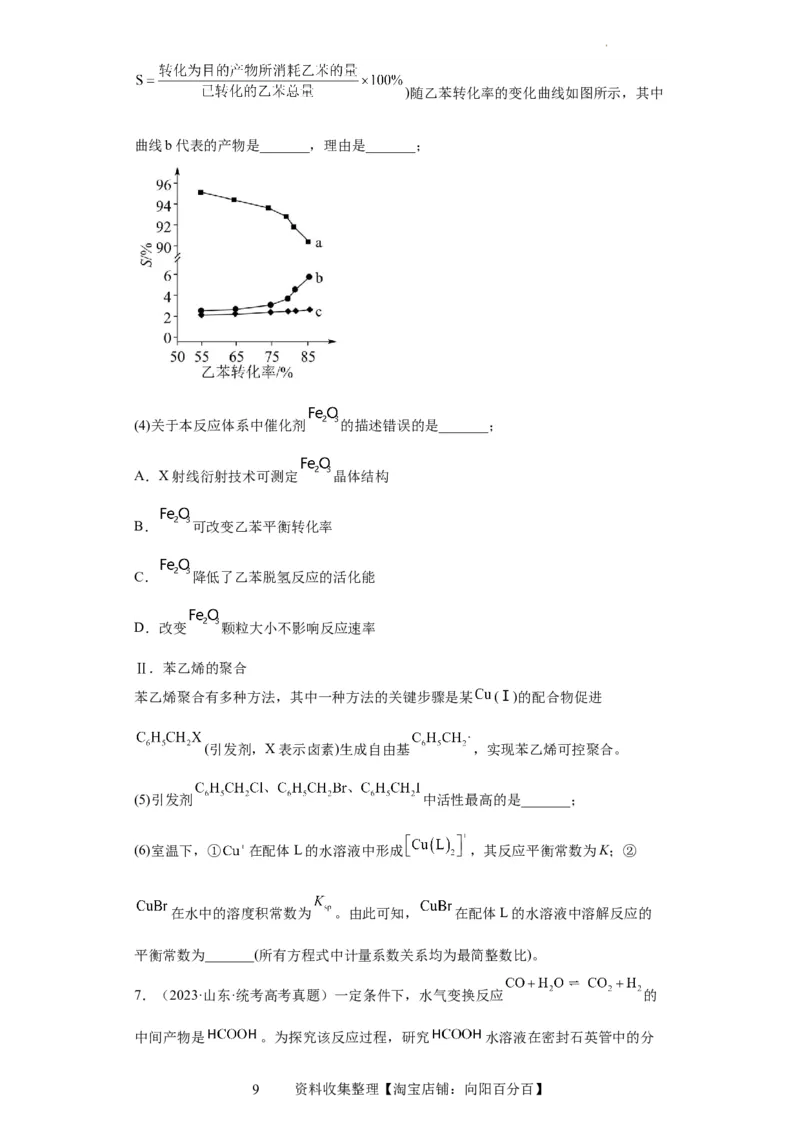
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性S(
试卷第8页,共20页)随乙苯转化率的变化曲线如图所示,其中
曲线b代表的产物是_______,理由是_______;
(4)关于本反应体系中催化剂 的描述错误的是_______;
A.X射线衍射技术可测定 晶体结构
B. 可改变乙苯平衡转化率
C. 降低了乙苯脱氢反应的活化能
D.改变 颗粒大小不影响反应速率
Ⅱ.苯乙烯的聚合
苯乙烯聚合有多种方法,其中一种方法的关键步骤是某 (Ⅰ)的配合物促进
(引发剂,X表示卤素)生成自由基 ,实现苯乙烯可控聚合。
(5)引发剂 中活性最高的是_______;
(6)室温下,① 在配体L的水溶液中形成 ,其反应平衡常数为K;②
在水中的溶度积常数为 。由此可知, 在配体L的水溶液中溶解反应的
平衡常数为_______(所有方程式中计量系数关系均为最简整数比)。
7.(2023·山东·统考高考真题)一定条件下,水气变换反应 的
中间产物是 。为探究该反应过程,研究 水溶液在密封石英管中的分
9 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司子反应:
Ⅰ.
Ⅱ.
研究发现,在反应Ⅰ、Ⅱ中, 仅对反应Ⅰ有催加速作用;反应Ⅰ速率远大于反应Ⅱ,
近似认为反应Ⅰ建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答
下列问题:
(1)一定条件下,反应Ⅰ、Ⅱ的焓变分别为 、 ,则该条件下水气变换反应的焓
变 _____(用含 的代数式表示)。
(2)反应Ⅰ正反应速率方程为: ,k为反应速率常数。 温度下,
电离平衡常数为 ,当 平衡浓度为 时, 浓度为_____
,此时反应Ⅰ应速率 _____ (用含 和k的代数式表示)。
(3) 温度下,在密封石英管内完全充满 水溶液,使 分解,
分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的
其他存在形式)。 时刻测得 的浓度分别为 ,反应Ⅱ
达平衡时,测得 的浓度为 。体系达平衡后 _____(用含y的代数式
表示,下同),反应Ⅱ的平衡常数为_____。
相同条件下,若反应起始时溶液中同时还含有 盐酸,则图示点
试卷第10页,共20页中, 的浓度峰值点可能是_____(填标号)。与不同盐酸相比, 达浓度峰值时,
浓度_____(填“增大”“减小”或“不变”), 的反应_____(填“增
大”“减小”或“不变”)。
8.(2023·浙江·统考高考真题)水煤气变换反应是工业上的重要反应,可用于制氢。
水煤气变换反应:
该反应分两步完成:
请回答:
(1) _______ 。
(2)恒定总压 和水碳比[ ]投料,在不同条件下达到平衡时
和 的分压(某成分分压=总压×该成分的物质的量分数)如下表:
条件1 0.40 0.40 0
条件2 0.42 0.36 0.02
①在条件1下,水煤气变换反应的平衡常数 ___________。
②对比条件1,条件2中 产率下降是因为发生了一个不涉及 的副反应,写出该
反应方程式____。
(3)下列说法正确的是______。
A.通入反应器的原料气中应避免混入
B.恒定水碳比 ,增加体系总压可提高 的平衡产率
C.通入过量的水蒸气可防止 被进一步还原为
D.通过充入惰性气体增加体系总压,可提高反应速率
11 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司(4)水煤气变换反应是放热的可逆反应,需在多个催化剂反应层间进行降温操作以“去
除”反应过程中的余热(如图1所示),保证反应在最适宜温度附近进行。
①在催化剂活性温度范围内,图2中b-c段对应降温操作的过程,实现该过程的一种操
作方法是______。
A.按原水碳比通入冷的原料气 B.喷入冷水(蒸气) C.通过热交换器换热
②若采用喷入冷水(蒸气)的方式降温,在图3中作出 平衡转化率随温度变化的曲线
____。
(5)在催化剂活性温度范围内,水煤气变换反应的历程包含反应物分子在催化剂表面的
吸附(快速)、反应及产物分子脱附等过程。随着温度升高,该反应的反应速率先增大后
减小,其速率减小的原因是________。
9.(2023·广东深圳·翠园中学校考模拟预测)我国在应对气候变化工作中取得显著成
效,并向国际社会承诺2030年实现“碳达峰”,2060年实现“碳中和”。因此将
转化为高附加值化学品成为科学家研究的重要课题。异丁烯 作为汽
油添加剂的主要成分,可利用异丁烷与 反应来制备。
反应I:
反应II:
已知:
回答下列问题:
(1)已知:异丁烷,异丁烯,CO的燃烧热热化学方程式的焓变分别为 , ,
试卷第12页,共20页,则 ___________(用题目给的反应焓变来表示)
(2)向 恒容密闭容器中加入 和 ,利用反应Ⅰ
制备异丁烯。已知 。已知正反应速率表示为
,逆反应速率表示为
,其中 、 为速率常数。
①图中能够代表 的曲线为___________(填“ ”“ ”“ ”或“ ”)。
②温度为 时,该反应化学平衡常数 ___________,平衡时 转化
率___________50%(填“>”、“=”、“<”)。
(3) 重整技术是实现“碳中和”的一种理想的 利用技术,反应为:
。在 时,将 和 按物质的量之为
充入密闭容器中,分别在无催化剂及 催化下反应相同时间,测得 的转化
率与温度的关系如图所示:
①a点 转化率相等的原因是___________。
13 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司②在 、900℃、 催化条件下,将 、 、 按物质的量之比为
充入密闭容器, 的平衡转化率为 ,此时平衡常数 ___________(以分压
表示,分压=总压×物质的量分数;写出含 、n、p的计算表达式)。
(4)相比于反应II直接脱氢,有人提出加入适量空气。采用异丁烷氧化脱氢的方法制备
异丁烯,发生反应
相比于异丁烷直按脱氢制备丁烯。从产率角度分析该方法的优点
是___________。
(5)利用电化学可以将 有效转化为 ,装置如图所示。
装置工作时,阴极除有 生成外,还可能生成副产物降低电解效率。阴极生成的
副产物可能是___________,标准状况下,当阳极生成 的体积为 时,测得阴
极区内的 ,则电解效率为___________。(忽略电解前后液体
积的变化)
已知:电解效率= ×100%。
10.(2023·云南楚雄·统考模拟预测)O 具有杀菌消毒作用,但是O 含量过大时对人
3 3
体有害。已知O 的氧化能力比O 的强,O 氧化2-甲基-2-丁烯(C H )的有关反应如下:
3 2 3 5 10
①C H (g) +2O (g) CHCOCH (g)+CH CHO(g)+2O (g) ΔH<0
5 10 3 3 3 3 2 1
②CH CHO(g) +O(g) CHCOOH(g)+O(g) ΔH<0
3 3 3 2 2
试卷第14页,共20页(1)C H (g) + 3O(g) CHCOCH (g) +CH COOH(g) +3O (g) ΔH=
5 10 3 3 3 3 2
___________。(用含ΔH 和ΔH 的代数式表示)
1 2
(2)在一定温度下,向刚性密闭容器中充入1 mol C H (g)和4 mol O (g),发生反应:
5 10 3
C H (g) +3O (g) CHCOCH (g) +CH COOH(g)+ 3O (g)。下列叙述正确的是
5 10 3 3 3 3 2
___________。( 填标号)
A.达到平衡时,O 的体积分数小于50%
2
B.混合气体的密度不随时间变化时达到平衡状态
C.加入催化剂,不能提高单位时间内2-甲基- 2-丁烯的转化率
D.平衡后,及时分离出CHCOOH,能提高CHCOCH 的平衡产率
3 3 3
(3)在密闭容器中充入C H (g)和O(g), 发生反应C H (g) + 3O(g) CHCOCH
5 10 3 5 10 3 3 3
(g) +CH COOH(g) +3O (g) ΔH,测得 C H 的平衡转化率[α (C H )]与温度。压强的
3 2 5 10 5 10
关系如图1所示。
①一定压强下,随着温度升高, C H 的平衡转化率降低,原因是___________。
5 10
②根据图1可知,p___________ (填“>”、 “<”或“=”)p ,判断依据是___________。
1 2
(4)在一定温度下,向一恒容密闭容器中充入一定量O,发生反应2O 3O,气体总
3 3 2
压强与时间关系如图2所示。0~10 min时,O 分压变化率为___________kPa·min-1
2
(5)一定温度、总压强保持在96.0 kPa下,向一密闭容器中充入1 mol C H (g)和3 mol
5 10
O(g)发生反应①和反应②,一段时间后达到平衡,测得C H 的转化率为80%,
3 5 10
CHCOOH的物质的量与C H 相同。计算反应①的平衡常数K=___________ kPa.
3 5 10 p
15 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司(用分压计算的平衡常数为K,分压等于总压 ×物质的量分数)
p
(6)最新技术是以固体聚合物电解质(SPE)膜为复合电极,酸性溶液为电解质溶液,电解
水制备臭氧。阳极上的电极反应式为___________。
11.(2023·海南海口·海南华侨中学校考模拟预测)油气开采、石油化工、煤化工等行
业废气普遍含有的硫化氢,需要回收处理并加以利用。回答下列问题:
(1)已知下列反应的热化学方程式:
① kJ·mol
② kJ·mol
计算反应③ 的 _______kJ·mol ;反应③能够
自发的条件是_______(填“低温”或“高温”或“任何温度”)。
(2)在1000℃时,反应①的 kJ·mol ,反应③的 kJ·mol 。已
知 (R为常数,T为温度,K为平衡常数),据此分析反应③处理 的工
艺方法的优点是_______。
(3)在不同温度、反应压强为100 kPa,进料比 分别为a、b、c的条件下,反应
③ 平衡转化率如下图所示,则a、b、c由大到小的顺序为_______;
温度越高,反应③ 平衡转化率越大的原因是_______。
(4)在T℃、p kPa条件下,将 的混合气进行反应③,同时发生副
反应 ,达到平衡时, 的转化率为80%, 的转化率为
试卷第16页,共20页90%,则反应③的 _______ (列出计算式即可)。
12.(2023·辽宁沈阳·辽宁实验中学校考模拟预测)国家提出2030年前实现碳达峰、
2060年前实现碳中和的目标,利用 加氢制甲醇将成为实现目标的最佳路径.利用
加氢制甲醇的有关反应如下:
(1)已知:反应中相关的化学键键能数据如下.
化学键
键能
803 436 414 326 464
则 ____________ kJ∙mol−1。
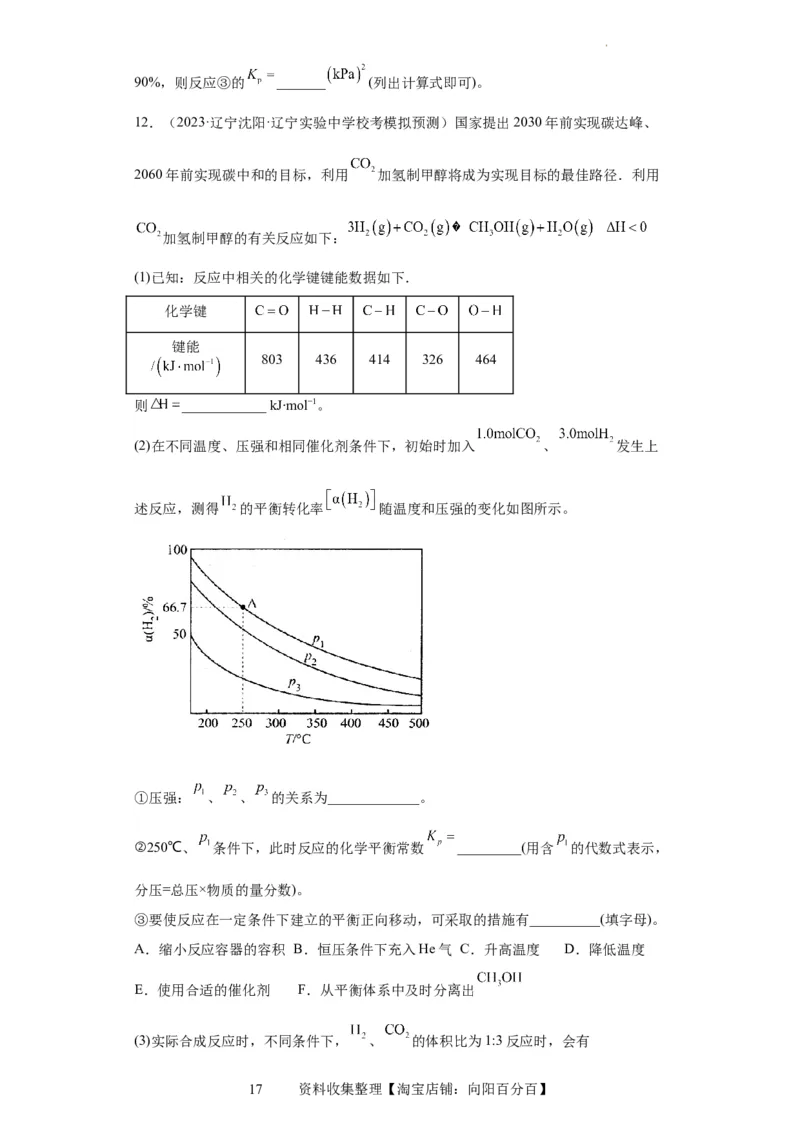
(2)在不同温度、压强和相同催化剂条件下,初始时加入 、 发生上
述反应,测得 的平衡转化率 随温度和压强的变化如图所示。
①压强: 、 、 的关系为_____________。
②250℃、 条件下,此时反应的化学平衡常数 _________(用含 的代数式表示,
分压=总压×物质的量分数)。
③要使反应在一定条件下建立的平衡正向移动,可采取的措施有__________(填字母)。
A.缩小反应容器的容积 B.恒压条件下充入He气 C.升高温度 D.降低温度
E.使用合适的催化剂 F.从平衡体系中及时分离出
(3)实际合成反应时,不同条件下, 、 的体积比为1:3反应时,会有
17 资料收集整理【淘宝店铺:向阳百分百】
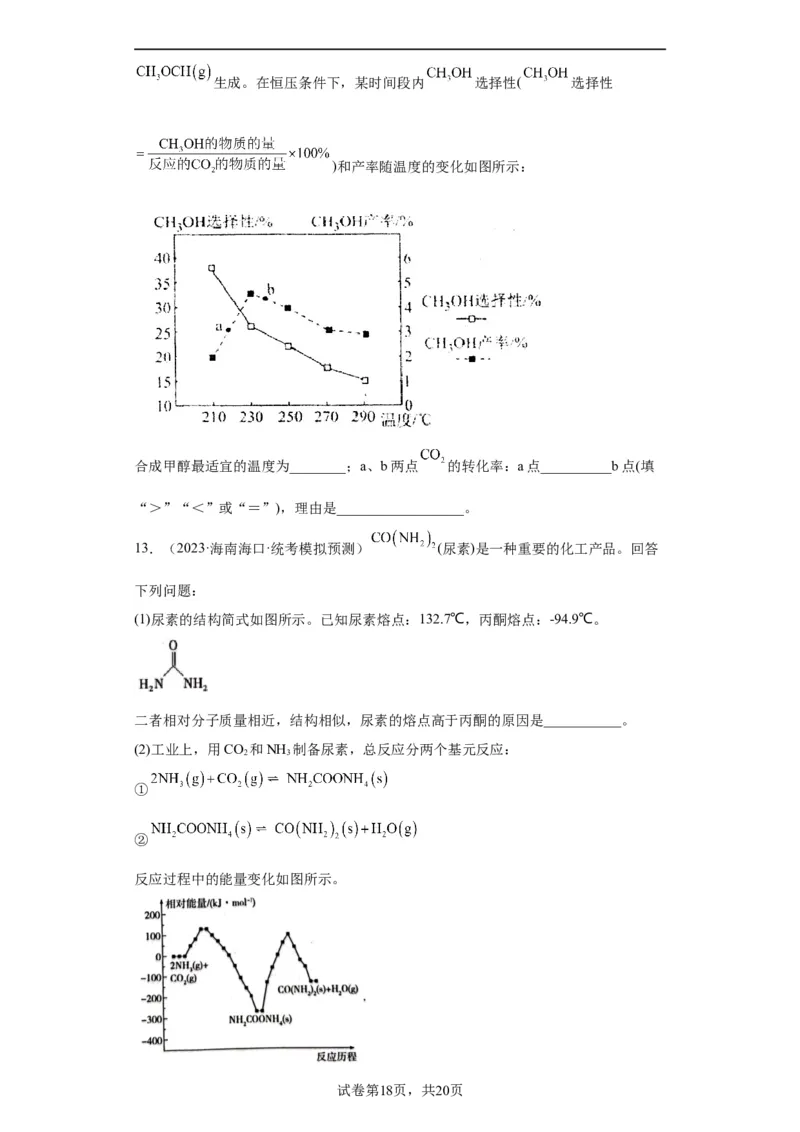
学科网(北京)股份有限公司生成。在恒压条件下,某时间段内 选择性( 选择性
)和产率随温度的变化如图所示:
合成甲醇最适宜的温度为________;a、b两点 的转化率:a点__________b点(填
“>”“<”或“=”),理由是__________________。
13.(2023·海南海口·统考模拟预测) (尿素)是一种重要的化工产品。回答
下列问题:
(1)尿素的结构简式如图所示。已知尿素熔点:132.7℃,丙酮熔点:-94.9℃。
二者相对分子质量相近,结构相似,尿素的熔点高于丙酮的原因是___________。
(2)工业上,用CO 和NH 制备尿素,总反应分两个基元反应:
2 3
①
②
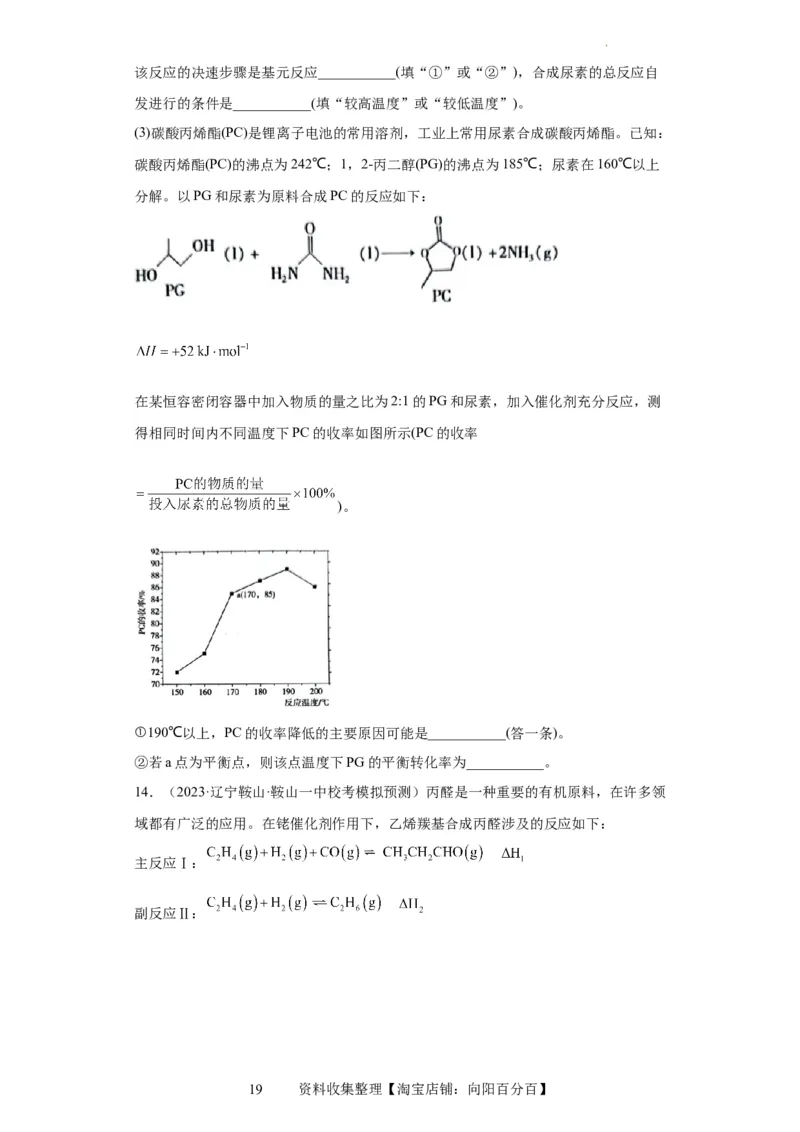
反应过程中的能量变化如图所示。
试卷第18页,共20页该反应的决速步骤是基元反应___________(填“①”或“②”),合成尿素的总反应自
发进行的条件是___________(填“较高温度”或“较低温度”)。
(3)碳酸丙烯酯(PC)是锂离子电池的常用溶剂,工业上常用尿素合成碳酸丙烯酯。已知:
碳酸丙烯酯(PC)的沸点为242℃;1,2-丙二醇(PG)的沸点为185℃;尿素在160℃以上
分解。以PG和尿素为原料合成PC的反应如下:
在某恒容密闭容器中加入物质的量之比为2:1的PG和尿素,加入催化剂充分反应,测
得相同时间内不同温度下PC的收率如图所示(PC的收率
)。
①190℃以上,PC的收率降低的主要原因可能是___________(答一条)。
②若a点为平衡点,则该点温度下PG的平衡转化率为___________。
14.(2023·辽宁鞍山·鞍山一中校考模拟预测)丙醛是一种重要的有机原料,在许多领
域都有广泛的应用。在铑催化剂作用下,乙烯羰基合成丙醛涉及的反应如下:
主反应Ⅰ:
副反应Ⅱ:
19 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司回答下列问题:
(1)T℃时,向恒压容器中充入0.2mol 、0.2mol 和0.2molCO(g),若在该
条件下只发生主反应Ⅰ:
①达平衡时,放出15.48kJ的能量;若向相同容器中充入0.4mol ,在
相同条件下达到平衡时,吸收20.64kJ的能量,则反应Ⅰ的 ___________kJ/mol。
②下列说法能说明反应I达到平衡的是( )
A、CO的消耗速率等于 的生成速率
B、气体的密度不再随时间改变
C、平衡常数K不再随时间改变
D、气体平均摩尔质量不再随时间改变
(2)在恒压密闭容器中,通入1mol 、1molCO和一定物质的量的 ,在一定温度
和铑催化剂作用下,发生上述反应,测得 的转化率(α)和丙醛选择性(x)
随 变化关系如图1所示。
表示乙烯转化率的曲线是___________(填a或b)
(3)保持温度不变,在恒容反应器中,按照 投料,发生
Ⅰ、Ⅱ反应,起始总压为3pkPa,反应达到平衡时 的转化率为80%, 的选择
性为25%,则 的转化率为___________%,反应Ⅰ的 ___________ (用含p
试卷第20页,共20页的代数式表示)。
(4)在恒压条件下,按照 投料,匀速通入装有催化剂的
反应器中发生反应Ⅰ和Ⅱ,相同时间内,测得不同温度下 的转化率(α)如图2中曲
线n所示(图2中,曲线m表示相同条件下 的平衡转化率随温度的变化)。测得
___________ (填“>”、“=”、“<”),产生这一结果的原因可能是
___________。
15.(2023·湖南长沙·长沙市明德中学校考模拟预测)氮及其化合物是科学家们一直在
探究的问题,它们在工农业生产和生命活动中起着重要的作用。回答下列问题:
(1)查阅资料:标准摩尔生成焓是指在25℃和101kPa时,由元素最稳定的单质生成
1mol纯化合物时的焓变,符号为 。已知以下物质的标准摩尔生成焓如下表所示。
物质 NH (g) HO(g)
3 2
由此可得 ___________kJ/mol。
(2)氨气的催化氧化是工业制取硝酸的重要步骤,假设只会发生以下两个竞争反应Ⅰ、
Ⅱ。
反应Ⅰ:
反应Ⅱ:
为分析某催化剂对该反应的选择性,将1molNH 和2molO 充入1L密闭容器中,在不
3 2
同温度相同时间下,测得有关物质的量关系如图。
①该催化剂在低温时对反应___________(填“Ⅰ”或“Ⅱ”)的选择性更好。
②520℃时,容器中NH 的转化率=___________
3
21 资料收集整理【淘宝店铺:向阳百分百】
学科网(北京)股份有限公司③高于840℃时,NO的产率降低的可能原因是___________(填选项字母)。
A.NH 溶于水 B.NH 的浓度降低
3 3
C.反应I的平衡常数变小 D.催化剂活性降低
(3)已知反应 ,某研究小组研究不同温度
T℃、T℃下的平衡状态中lgp(NO )和lgp(SO)两个压强对数的关系如图所示,实验初
1 2 2 3
始时体系中的p(NO )和p(SO )相等、p(NO)和p(SO )相等。
2 2 3
①a、b两点体系压强p 与p 的比值 ___________;同一温度下图像呈线性变化的
a b
理由是___________
②温度为T 时化学平衡常数K=___________
1 p
(4)某同学设计用NO—空气质子交换膜燃料电池探究将雾霾中的SO 、NO转化为
2
(NH )SO 的原理。
4 2 4
①燃料电池放电过程中负极的电极反应式为___________。
②若甲装置中消耗22.4LO (标况),则乙装置中SO 和NO转化的物质的量共有
2 2
___________mol。
试卷第22页,共20页