专项训练 化学平衡图像分析(解析版)
1.已知反应 。图①表示反应物的平衡转化率与投料比
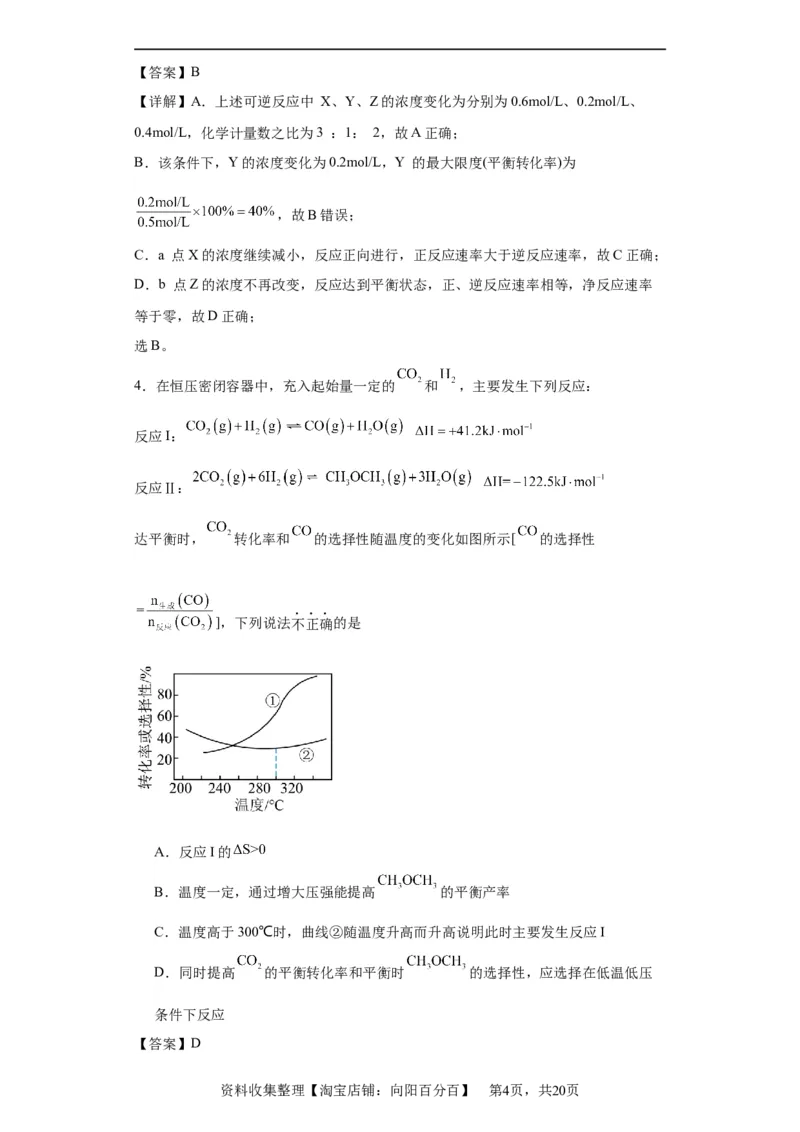
的关系;图②表示一定量的 和 在密闭容器中反应时, 的百分含
量与温度和时间的关系。下列判断错误的是
A.曲线a表示 的平衡转化率与投料比 的关系
B.M点时,投料比
C.
D.保持其他条件不变,对M点的体系压缩体积,平衡向正反应方向移动
【答案】B
【详解】A.投料比 越大,X的转化率越小,Y的转化率越大,结合图像可知曲
线a表示 的平衡转化率与投料比 的关系,故A正确;
B.M点时,X、Y的转化率相等,则 满足化学计量数之比,即 =2,故B
错误;
C.由图②可知温度升高时,X的百分含量增加,则平衡逆向移动,逆向为吸热反应,
正向为放热反应, ,故C正确;
D.该反应正向气体分子数减少,保持其他条件不变,对M点的体系压缩体积,平衡
1
学科网(北京)股份有限公司向气体分子数减小的方向进行,即向正反应方向移动,故D正确;
故选:B。
2.碳热还原氧化锌反应可用于循环制氢。碳热还原氧化锌的主要反应如下:
反应Ⅰ: ;反应Ⅱ: ,在不同容器中分别发生
反应Ⅰ、反应Ⅱ,不同压强( 或 )下分别达平衡时,两个反应中
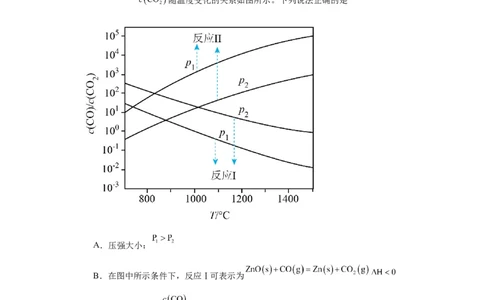
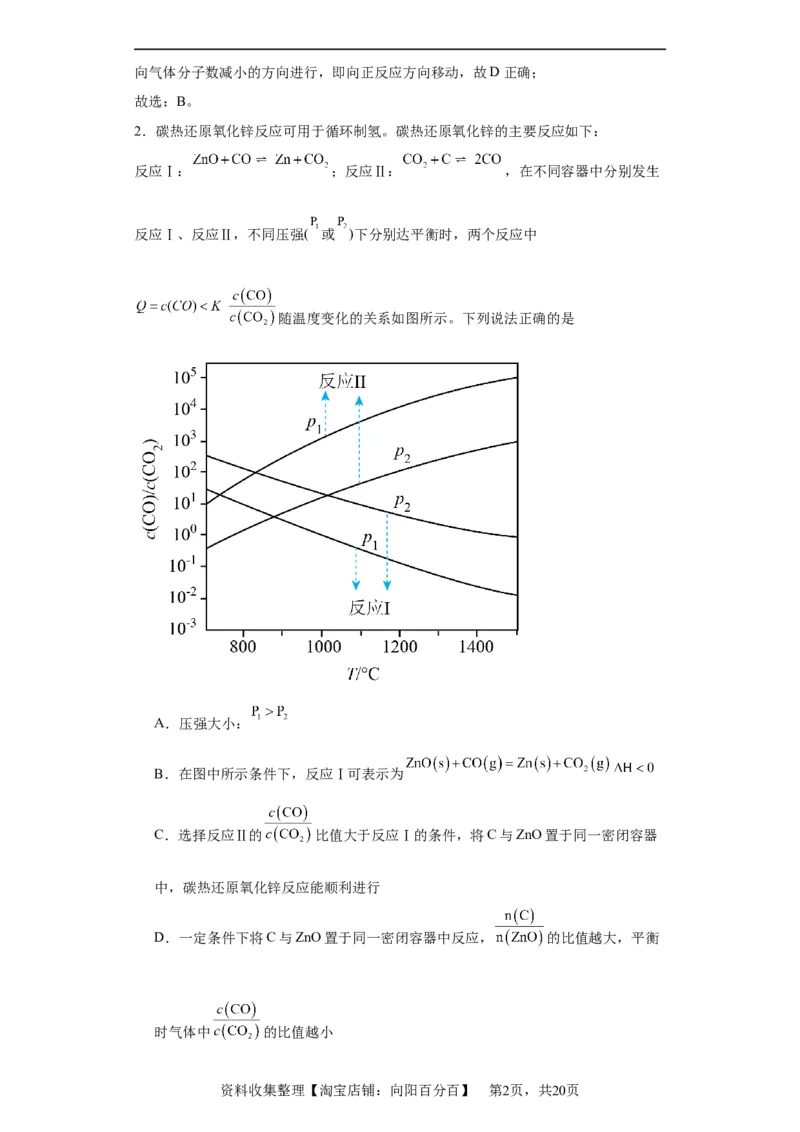
随温度变化的关系如图所示。下列说法正确的是
A.压强大小:
B.在图中所示条件下,反应Ⅰ可表示为
C.选择反应Ⅱ的 比值大于反应Ⅰ的条件,将C与ZnO置于同一密闭容器
中,碳热还原氧化锌反应能顺利进行
D.一定条件下将C与ZnO置于同一密闭容器中反应, 的比值越大,平衡
时气体中 的比值越小
资料收集整理【淘宝店铺:向阳百分百】 第2页,共20页【答案】C
【详解】A.反应Ⅱ是一个气体分子数增大的反应,压强应为P
K
5
学科网(北京)股份有限公司C.升高温度, 、 增大倍数:
D. ℃时发生反应,测得 ,则
【答案】C
【详解】A.M和N点反应未达到平衡,则 (正) (逆), (正) (逆),反应过
程中v(正)不断减小,则 (正)> (正),则 (正) (逆),故A错误;
B.L点时,顺1,2-二甲基环丙烷和逆1,2-二甲基环丙烷的质量分数相等,由方程式
(顺式) (反式)可知,此时顺1,2-二甲基环丙烷转化了一半,
转化率为50%,此时反应未达到平衡,平衡正向进行,Q(浓度商)K,平衡向逆反应方向移动,则CO
c
的消耗速率大于其生成速率,选项A正确;
B.由分析可知,该反应为吸热反应,反应的ΔH>0,选项B错误;
C.温度是 K即 时,根据图像可知,lgc(CO)=1,c(CO)=10mol/L,
K=c4(CO)=10000,选项C错误;
9
学科网(北京)股份有限公司D.反应的化学平衡常数K=c4(CO),平衡常数为温度函数,温度不变,平衡常数不变,
则温度不变时,将R点状态的容器体积扩大,重新达到平衡时,c(CO)不变,则气体的
压强不变,选项D错误;
故选A。
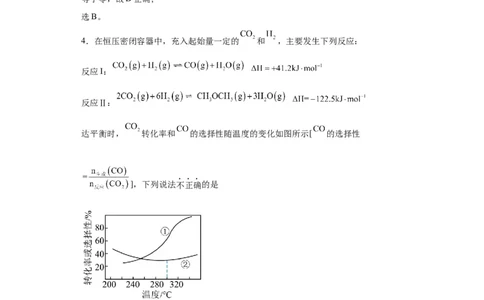
9.在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式如下:
反应I:CO(g)+4H(g) CH(g)+2HO(g) ΔH=-164.7 kJ·mol-1
2 2 4 2
反应Ⅱ:CO(g)+H(g) CO(g)+HO(g) ΔH=+41.2 kJ·mol-1
2 2 2
反应Ⅲ:2CO(g)+2H(g) CO(g)+CH (g) ΔH=-247.1 kJ·mol-1
2 2 4
向恒压、密闭容器中通入1 mol CO 和4 mol H ,平衡时CH、CO、CO 的物质的量随
2 2 4 2
温度的变化曲线如图所示。则图中曲线A表示的物质是
A.CO B.CH C.CO D.无法确定
4 2
【答案】B
【详解】随着温度的升高,对于反应Ⅰ,平衡逆向移动,c(CH)减小,c(CO)增大;对
4 2
于反应Ⅱ,平衡正向移动,c(CO)增大,c(CO)减小;对于反应Ⅲ,平衡逆向移动,
2
c(CH)、c(CO)减小,c(CO)增大,从图看,温度升高,A的物质的量减小,由此判断
4 2
曲线A为CH,C的物质的量随温度升高而增大,则曲线C为CO,反应Ⅰ、Ⅲ为放热
4
反应,反应Ⅱ为吸热反应,升高温度时,要看温度对三个反应的影响程度,所以
n(CO)可以增大,可以减小,对应图中曲线B,故选B。
2
10.向刚性容器中,按物质的量之比为3:1充入H 和CO 发生反应:2CO(g)+
2 2 2
6H(g) C H(g)+4HO(g)。反应相同时间,CO(g)的转化率随温度的变化关系如图
2 2 4 2 2
所示,下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】 第10页,共20页A.H(g)的转化率随温度的变化关系图与上图完全相同
2
B.该反应在低温下能自发进行
C.T℃时容器内压强为p,该反应的K=( )3
2 0 p
D.M、N两点时容器内压强相等
【答案】D
【详解】A.反应的投料比恰好等于系数比,所以H(g)转化率随温度的变化关系图与
2
CO(g)转化率随温度的变化关系图完全相同,A项正确;
2
B.反应开始时,CO(g)转化率随温度升高而增大,反应达到平衡后,随温度升高,
2
CO 转化率减小,所以该反应的焓变ΔH<0,B项正确;
2
C.N点容器内压强为p,T℃平衡时CO(g)转化率为50%,假设起始时充入
0 2 2
3molH ,列三段式如下:
2
平衡时分压分别为: p、 p、 p、 p
0 0 0 0
反应的Kp= ,C项正确;
D.M、N两点对应的温度不同,所以两容器内压强不相等,D项错误;
故选:D
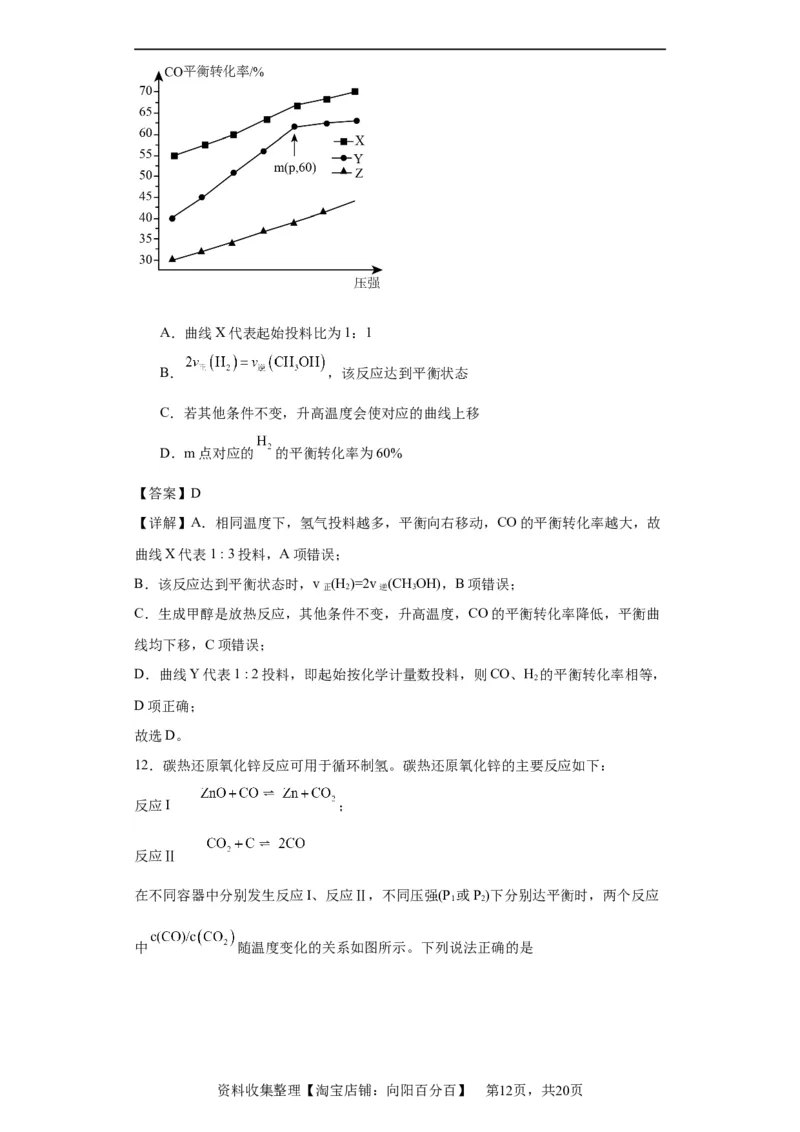
11.在600K下,按初始投料比 分别为1:1、1:2、1:3投料,发生反
应为 。测得不同压强下,CO平衡转化率如图
所示。下列叙述正确的是
11
学科网(北京)股份有限公司A.曲线X代表起始投料比为1:1
B. ,该反应达到平衡状态
C.若其他条件不变,升高温度会使对应的曲线上移
D.m点对应的 的平衡转化率为60%
【答案】D
【详解】A.相同温度下,氢气投料越多,平衡向右移动,CO的平衡转化率越大,故
曲线X代表1 : 3投料,A项错误;
B.该反应达到平衡状态时,v (H )=2v (CHOH),B项错误;
正 2 逆 3
C.生成甲醇是放热反应,其他条件不变,升高温度,CO的平衡转化率降低,平衡曲
线均下移,C项错误;
D.曲线Y代表1 : 2投料,即起始按化学计量数投料,则CO、H 的平衡转化率相等,
2
D项正确;
故选D。
12.碳热还原氧化锌反应可用于循环制氢。碳热还原氧化锌的主要反应如下:
反应I ;
反应Ⅱ
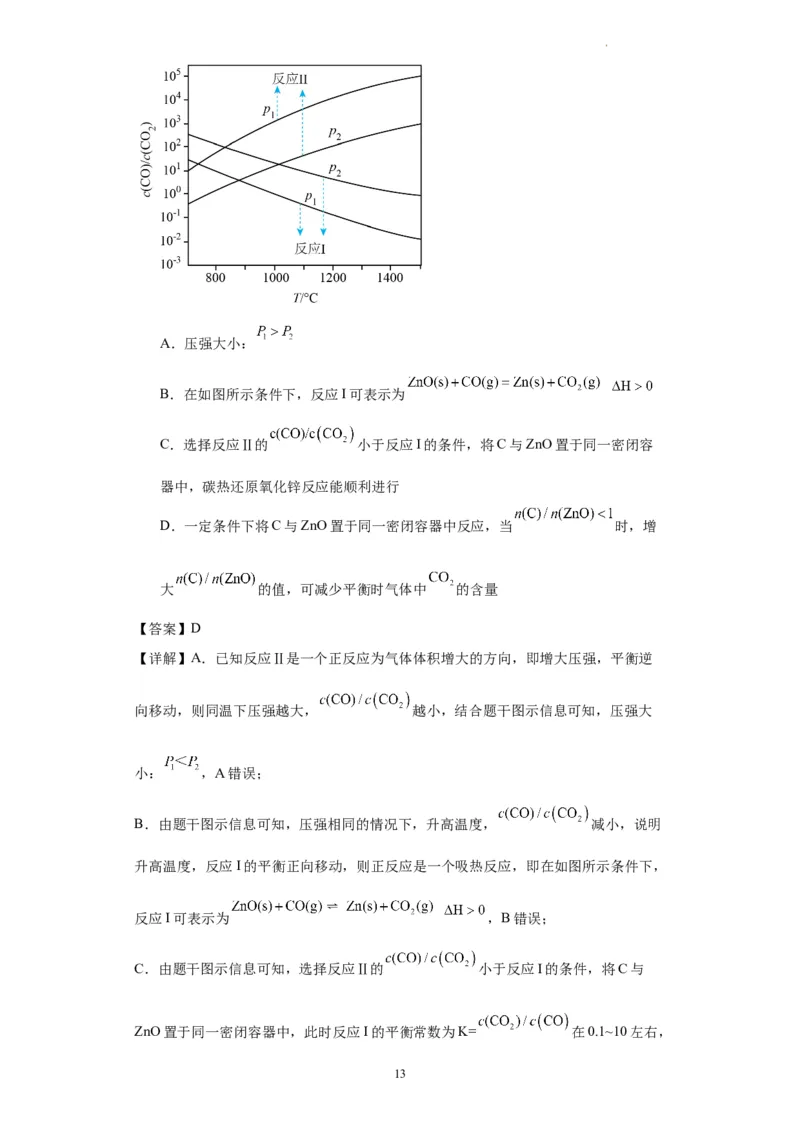
在不同容器中分别发生反应I、反应Ⅱ,不同压强(P 或P)下分别达平衡时,两个反应
1 2
中 随温度变化的关系如图所示。下列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】 第12页,共20页A.压强大小:
B.在如图所示条件下,反应I可表示为
C.选择反应Ⅱ的 小于反应I的条件,将C与ZnO置于同一密闭容
器中,碳热还原氧化锌反应能顺利进行
D.一定条件下将C与ZnO置于同一密闭容器中反应,当 时,增
大 的值,可减少平衡时气体中 的含量
【答案】D
【详解】A.已知反应Ⅱ是一个正反应为气体体积增大的方向,即增大压强,平衡逆
向移动,则同温下压强越大, 越小,结合题干图示信息可知,压强大
小: ,A错误;
B.由题干图示信息可知,压强相同的情况下,升高温度, 减小,说明
升高温度,反应I的平衡正向移动,则正反应是一个吸热反应,即在如图所示条件下,
反应I可表示为 ,B错误;
C.由题干图示信息可知,选择反应Ⅱ的 小于反应I的条件,将C与
ZnO置于同一密闭容器中,此时反应I的平衡常数为K= 在0.1~10左右,
13
学科网(北京)股份有限公司平衡常数很小,即碳热还原氧化锌反应不能顺利进行,C错误;
D.一定条件下将C与ZnO置于同一密闭容器中反应,当 时,增大
的值,即增大C的用量,促使进行反应Ⅱ,故可减少平衡时气体中
的含量,D正确;
故答案为:D。
13.在 刚性密闭容器中充入 气体,容器内反应为
,在 和 时,测得 的物质的量随时间的变化如图所示,
下列说法错误的是
A. 时, 内 的平均反应速率为
B.温度
C.若增大 的起始浓度,平衡时 比原平衡小
D.M点和N点的平衡常数
【答案】B
【详解】A. 时, 内 的平均反应速率为
,A项正确;
B.由图可知,反应在 温度下比 温度下先达到平衡状态,所以 ,由于 平衡
时 比 平衡时的少,故升高温度,平衡向生成 的方向移动,即向吸热反
资料收集整理【淘宝店铺:向阳百分百】 第14页,共20页应方向移动,所以 ,B项错误;
C.增大 的起始浓度相当于增大压强,平衡向左移动, 减小,C项正确;
D.正反应是吸热反应,M点的温度高于N点,温度越高,平衡常数越大,平衡常数
,D项正确;
故选B。
14. 时,存在如下平衡: 。该反应正、逆反应速率与
的浓度关系为: , ( 是速率常数),
且 与 的关系如图所示,下列说法正确的是
A.图中表示 的是线Ⅱ
B. 时,往刚性容器中充入一定量 ,平衡后测得 为 ,
则平衡时
C. 时,该反应的平衡常数
D. 时向 恒容密闭容器中充入 ,某时刻
,则此时 的转化率为
【答案】C
15
学科网(北京)股份有限公司【分析】因 ,则 ;
,同理可得: ,由函数关系可知 的斜率大
于 ,结合图像可知线Ⅰ应为 ,线Ⅱ应为 ,据此
分析解答。
【详解】A.由以上分析可知线Ⅰ应为 ,故A错误;
B.由以上分析可知线Ⅱ应为 ,又 ,结合图像
可知当 =0时, =a,则 ,平衡后测得 为 ,则
平衡时 ,故B错误;
C.线Ⅰ应为 , ,当 =0时,
=a+2,则 ,反应达到平衡状态时:
, = =100,故C正确;
D.某时刻 ,此时 ,则此
时 的转化率= ,故D错误;
故选:C。
15.CO 催化加氢合成二甲醚是一种CO 转化方法,其过程中主要发生下列反应:
2 2
反应Ⅰ:CO(g)+H(g) CO(g)+HO(g) H
2 2 2 1
反应Ⅱ:2CO
2
(g)+6H
2
(g) CH
3
OCH
3
(g)+△3H
2
O(g) H
2
恒压,投入1 mol CO
2
和适当过量的H
2
,CO
2
平衡转△化率和平衡时CH
3
OCH
3
的选择性
随温度的变化如图。其中:
资料收集整理【淘宝店铺:向阳百分百】 第16页,共20页CHOCH 的选择性= ×100%
3 3
下列说法中不正确的是
A. H>0, H<0
1 2
B.温△度高于3△00℃,反应Ⅰ正移程度超过反应Ⅱ逆移程度
C.220℃时,反应一段时间后,测得CHOCH 的选择性为48%(即图中A点)。此
3 3
时反应Ⅰ和Ⅱ均未达到平衡状态
D.若平衡时CHOCH 的选择性为48%,则体系中c(CHOCH )∶c(CO)=48∶52
3 3 3 3
【答案】D
【详解】A.根据图像分析可知:反应达到平衡状态后,升高温度,CHOCH (g)的选
3 3
择性减小,CO(g)转化率增大,说明升温反应Ⅰ正向进行,反应为吸热反应, H>
2 1
0,反应Ⅱ逆向进行,正反应为放热反应, H<0,A正确; △
2
B.温度高于300℃,CO
2
平衡转化率随温度△升高而上升的原因是:反应Ⅰ的 H
1
>0,
反应Ⅱ的 H<0,温度升高使CO 转化为CO的平衡转化率上升,使CO 转化△为
2 2 2
CHOCH△的平衡转化率下降,且上升幅度超过下降幅度,B正确;
3 3
C.2CO(g)+6H(g) CHOCH (g)+3HO(g) H<0,CHOCH 的选择性=
2 2 3 3 2 2 3 3
△
,化学平衡正向进行,二甲醚物质的量增大,二氧化碳物质的
量减小,二甲醚选择性增大,A点对于反应Ⅱ是未达到平衡,反应Ⅰ是吸热反应,随
着温度升高,平衡正向进行,二氧化碳转化率增大,则A点对于反应Ⅰ也未达到平衡
状态,C正确;
D.CHOCH 的选择性= 分析,设生成CHOCH 物质的量为x
3 3 3 3
17
学科网(北京)股份有限公司mol,生成CO物质的量为y mol,反应的二氧化碳为(2x+y) mol,得到
=48%, ,则体系中c(CHOCH )∶c(CO)=6∶13,D错误;
3 3
故合理选项是D。
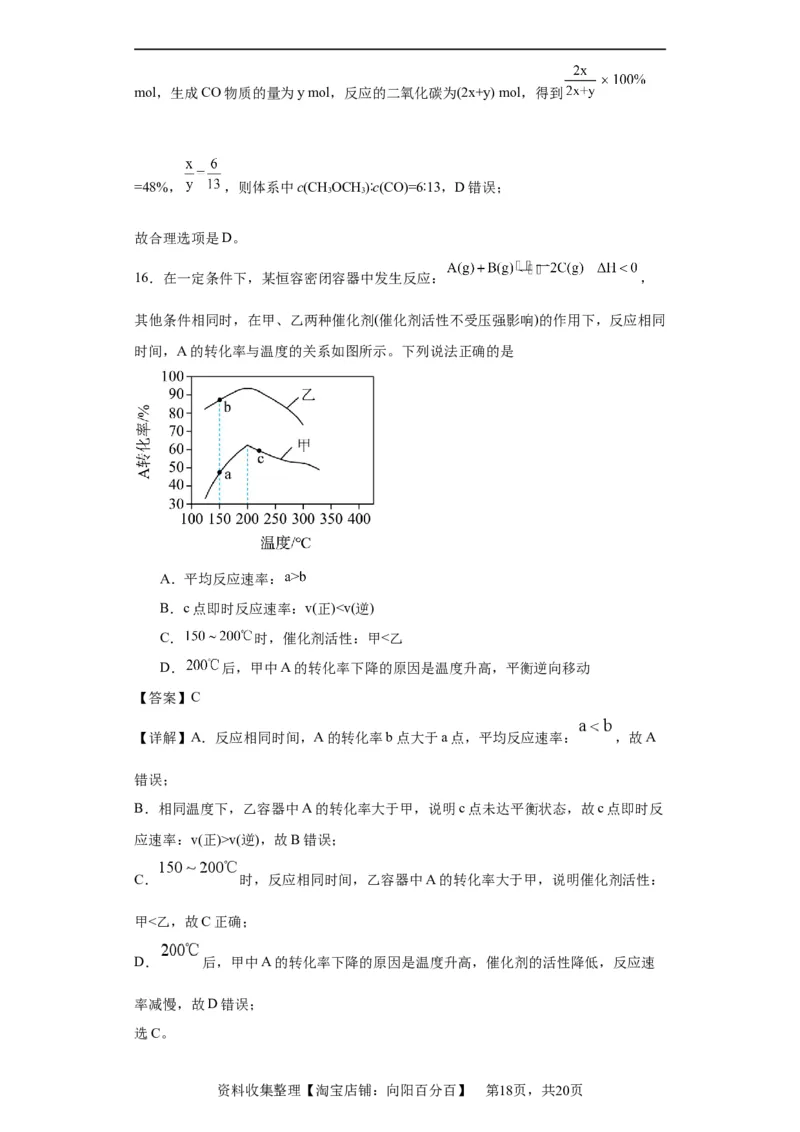
16.在一定条件下,某恒容密闭容器中发生反应: ,
其他条件相同时,在甲、乙两种催化剂(催化剂活性不受压强影响)的作用下,反应相同
时间,A的转化率与温度的关系如图所示。下列说法正确的是
A.平均反应速率:
B.c点即时反应速率:v(正)v(逆),故B错误;
C. 时,反应相同时间,乙容器中A的转化率大于甲,说明催化剂活性:
甲<乙,故C正确;
D. 后,甲中A的转化率下降的原因是温度升高,催化剂的活性降低,反应速
率减慢,故D错误;
选C。
资料收集整理【淘宝店铺:向阳百分百】 第18页,共20页17.在盛有 载氧体的恒容密闭容器中充入空气,发生反应:
。平衡时 的体积分数 随反应温度 变化
的曲线如图所示。下列说法错误的是
A.
B.该反应的平衡常数表达式为
C.在 时加入催化剂,平衡时
D. 达到平衡状态后,充入纯氧,再次达到平衡后,
【答案】C
【详解】A.平衡时 的体积分数 随温度升高而增大,则升温平衡左移,
,A正确;
B. 该反应方程式为 ,则按定义,其平衡常数表达式为
,B正确;
C. 由图知,在 时平衡时 ,催化剂通常能加快反应但不影响平衡,
则加入催化剂时 ,C不正确;
D. 达到平衡状态后,充入纯氧不影响平衡常数, ,则再次达到平
衡后, ,D正确;
答案选C。
19
学科网(北京)股份有限公司18.利用 和CO反应生成 的过程中主要涉及的反应如下:
反应Ⅰ kJ⋅mol-1
反应Ⅱ kJ⋅mol-1
[ 的产率 , 的选择性 ]。保持温
度一定,在固定容积的密闭容器中进行上述反应,平衡时 和 的产率及CO和
的转化率随 的变化情况如图所示。下列说法不正确的是
A.当容器内气体总压不变时,反应Ⅱ达到平衡状态75a
B.曲线c表示 的产率随 的变化
C. ,反应达平衡时, 的选择性为50%
D.随着 增大, 的选择性先增大后减小
【答案】B
【详解】A.反应I、Ⅱ可以合并为反应2CO(g)+2H(g)==CH (g)+CO (g),是气体总体
2 4 2
积缩小的反应,当固定密闭容器内总压不变时则反应I、Ⅱ都达到平衡状态,A正确;
B.通过总反应式2CO(g)+2H(g)=CH (g)+CO (g),随着n(H )的增加,超过1时,CH
2 4 2 2 4
的产率n(CO)受CO浓度影响,故CH 的产率曲线会先增大后平缓,应该是a曲线,B
4
错误;
资料收集整理【淘宝店铺:向阳百分百】 第20页,共20页C.通过总反应式2CO(g)+2H(g)=CH (g)+CO (g),当 =0.5时,生成物
2 4 2
n(CH)=n(CO),故CH 的选择性为50%,C正确;
4 4
D.随着 的不断增加,作为反应Ⅱ的生成物浓度不断增加会抑制CO 的生成,
2
故CO 选择性先增大后减小,D正确;
2
故选B。
19.氨催化氧化是硝酸工业的基础。工业上以氨气和氧气为原料,利用“氨催化氧化
法”生产NO,在Pt-Rh合金催化剂作用下,发生主反应Ⅰ和副反应Ⅱ:
Ⅰ.4NH (g) + 5O(g) 4NO(g) + 6H O(g)
3 2 2
Ⅱ.4NH (g) + 3O(g) 2N(g) + 6HO(g)
3 2 2 2
现将1 mol NH 、2 mol O 充入1L恒容密闭容器中,在上述催化剂作用下,反应相同时
3 2
间内,生成物的物质的量随温度变化曲线如图所示:
已知:有效转化率= ×100%
下列说法不正确的是
A.该催化剂在低温时对反应Ⅱ的选择性更好
B.520℃时,NH 的有效转化率约为66.7%
3
C.工业上氨催化氧化生成NO时,最佳温度应控制在840℃左右
D.高于400℃,n(N )随温度升高而下降可能是反应Ⅱ的平衡逆向移动导致
2
【答案】B
【详解】A.由图可知,低温时反应的主要产物为氮气,即主要发生反应Ⅱ,说明该
催化剂在低温时对反应Ⅱ的选择性更好,A正确;
B.由图可知,520℃时,NH 发生反应I生成NO 0.2mol,消耗氨气0.2mol,NH 发生
3 3
反应Ⅱ生成N 0.2mol,消耗氨气0.4mol,则NH 的有效转化率为
2 3
21
学科网(北京)股份有限公司,B错误;
C.由图可知,840℃时,反应相同时间内,NO的物质的量最大,副产物N 的物质的
2
量最小,说明该温度下最有利于NO的生成,因此工业上氨催化氧化生成NO时,最
佳温度应控制在840℃左右,C正确;
D.400℃后n(N )随温度升高而下降,其原因可能是:该反应为放热反应,高于400℃
2
时平衡逆向移动,使得N 的物质的量减少,D正确;
2
故选B。
20.在催化剂作用下, 氧化 可获得 。其主要化学反应为:
反应I.
反应Ⅱ.
压强分别为 、 时,将 和 的混合气体置于密闭容器中反应,不
同温度下体系中乙烷的平衡转化率、乙烯的选择性[ 的选择性
]如图所示。下列说法正确的是
A.反应
B.
C.压强为 ,温度为210℃时,反应达平衡时,体系中
D.一定温度和压强下,可通过选择合适的催化剂提高反应速率和乙烯的选择性
【答案】D
资料收集整理【淘宝店铺:向阳百分百】 第22页,共20页【详解】A.根据盖斯定律,2Ⅰ-Ⅱ得到
,则ΔH=2ΔH-ΔH =2×(177kJ/mol)-
1 2
(+430kJ/mol)=-76kJ/mol,故A错误;
B.反应Ⅰ是个气体体积增大的反应,增大压强,平衡逆向移动,C H 的转化率降低,
2 6
从图中可以看出,温度均为210℃时,当压强为P 时,C H 的转化率为50%;当压强
1 2 6
为P 时,C H 的转化率小于50%,因此P<P,故B错误;
2 2 6 1 2
C.压强为 ,温度为210℃时,乙烷的转化率为50%,乙烯的选择性为80%,参与反
应Ⅰ的乙烷为2mol×50%×80%=0.8mol,反应Ⅰ生成的乙烯、一氧化碳都是0.8mol,参
与反应Ⅱ的乙烷为2mol×50%×20%=0.2mol,反应Ⅱ生成的一氧化碳是0.8mol,则反应
达平衡时 ,故C错误;
D.选择合适催化剂,可以加快化学反应速率,同时还可以提高目标产品的选择性,
减少副反应的发生,因此一定温度和压强下,可通过选择合适的催化剂提高反应速率
和乙烯的选择性,故D正确;
故答案选D。
23
学科网(北京)股份有限公司