文档内容
化学答案
一、选择题(每题3分,共45 分)
1 2 3 4 5 6 7 8 9 10
B A B D C B D B C B
11 12 13 14 15
C A B A C
1. B
A.兽皮的主要成分是蛋白质,A错误;
B.玛瑙的主要成分是二氧化硅,是熔融态二氧化硅快速冷却形成的,B正确;
C.棉花的主要成分是纤维素,属于天然纤维,C错误;
D.在酿酒过程中,淀粉先转化为葡萄糖,葡萄糖再经过发酵生成乙醇,淀粉不能直接转化为乙醇,D错误;
2.A
A.共价键的本质是由于原子相互接近时轨道重叠,原子间通过共用自旋相反的电子使体系能量降低,从而成键
故A正确;
B.胶体和溶液的本质区别是分散质粒子直径大小,B错误;
C.放热反应的实质为形成新化学键释放的能量大于破坏旧化学键吸收的能量,C错误;
D.碳酸氢钠溶解度小于碳酸钠,饱和 Na CO 溶液中通入过量 CO 反应生成碳酸氢钠晶体析出:
2 3 2
2Na++CO 2-+CO +H O=2NaHCO ↓,D错误;
3 2 2 3
故选A。
3. B
A.标况下,22.4LHCl的物质的量是1mol,但HCl为共价化合物,无H+,A错误;
B.铁离子在溶液中水解,所以100mL1mol·L−1FeCl 溶液中所含Fe3+的数目小于0.1N ,B正确;
3 A
C.pH 对应的是氢离子浓度,没有体积无法求算,C错误;
D.反应2SO+O 2SO 是可逆反应,因此密闭容器中,2molSO 和1molO 催化反应后分子总数大于2N,
2 2 3 2 2 A
D错误。答案选B。
4. D
A.FeCl3 是强电解质,在离子方程式中应该拆写,正确的离子方程式为:Cu2Fe3 Cu2+2Fe2,A项错误;
B.Na O 与CO 反应的化学方程式应为:2Na O +2CO =2Na CO +O ,B项错误;
2 2 2 2 2 2 2 3 2
C.Na SO 具有还原性,溴水和亚硫酸根发生氧化还原反应生成H+、Br-和SO2,其中H+会和过量的SO2-反应生
2 3 4 3
成HSO,反应的离子方程式为:Br 3SO2H O2BrSO22HSO-,C项错误;
3 2 3 2 4 3
D.葡萄糖中的醛基能被银氨溶液氧化,发生银镜反应,反应的离子方程式为
CH OH(CHOH) CHO+2 Ag NH + +2OH - Δ CH OH(CHOH) COO-+NH++2Ag+3NH +H O,D项正确;
2 4 3 2 2 4 4 3 2
答案选D。
5. C
该氧化还原反应用双线桥表示为 ,可知实际升价的N原子为2个,所以2个NH 被氧
3
化,同时Cl 全部被还原,观察计量数,Cl 为3个,因而被氧化的NH 与被还原的Cl 的物质的量之比为2:3。
2 2 3 2故答案 选C。
6. B
根据质量守恒可知,X微粒为6He,Y微粒为4He,据此分析解题。
2 2
A.
由分析可知,X微粒为6He,根据质量数等于质子数加中子数可知,该微粒的中子数为4,A错误;
2
B.
由分析可知,X微粒为6He,电子排布式为1s2,则He原子的原子轨道数为1,则核外电子的空间运动状态
2
有1中,B正确;
C.由题干信息可知,13O与15O的半衰期很短,故不适宜用作示踪原子研究化学反应历程,C错误;
8 8
D.自然界中不存在13O 与15O 并不是其化学键不稳定,而是由于13O与15O的半衰期很短,很容易发生核变化,
8 2 8 2 8 8
转化为气体其他原子,O=O的键能与形成该键的核素无关,D错误;
7.D
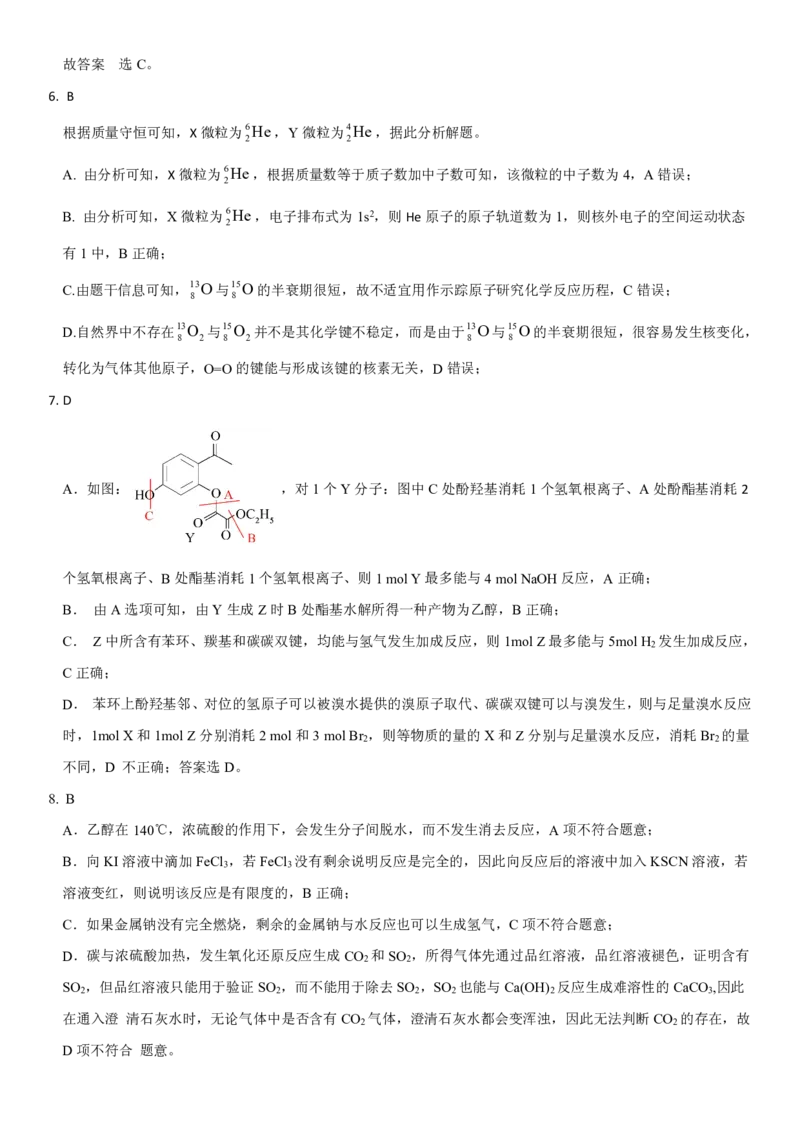
A.如图: ,对1个Y分子:图中C处酚羟基消耗1个氢氧根离子、A处酚酯基消耗2
个氢氧根离子、B处酯基消耗1个氢氧根离子、则1molY最多能与4molNaOH反应,A正确;
B. 由A选项可知,由Y生成Z时B处酯基水解所得一种产物为乙醇,B正确;
C. Z中所含有苯环、羰基和碳碳双键,均能与氢气发生加成反应,则1molZ最多能与5molH 发生加成反应,
2
C正确;
D. 苯环上酚羟基邻、对位的氢原子可以被溴水提供的溴原子取代、碳碳双键可以与溴发生,则与足量溴水反应
时,1molX和1molZ分别消耗2mol和3molBr ,则等物质的量的X和Z分别与足量溴水反应,消耗Br 的量
2 2
不同,D 不正确;答案选D。
8. B
A.乙醇在140℃,浓硫酸的作用下,会发生分子间脱水,而不发生消去反应,A项不符合题意;
B.向KI溶液中滴加FeCl ,若FeCl 没有剩余说明反应是完全的,因此向反应后的溶液中加入KSCN溶液,若
3 3
溶液变红,则说明该反应是有限度的,B正确;
C.如果金属钠没有完全燃烧,剩余的金属钠与水反应也可以生成氢气,C项不符合题意;
D.碳与浓硫酸加热,发生氧化还原反应生成CO 和SO ,所得气体先通过品红溶液,品红溶液褪色,证明含有
2 2
SO ,但品红溶液只能用于验证SO ,而不能用于除去SO ,SO 也能与Ca(OH) 反应生成难溶性的CaCO ,因此
2 2 2 2 2 3
在通入澄 清石灰水时,无论气体中是否含有CO 气体,澄清石灰水都会变浑浊,因此无法判断CO 的存在,故
2 2
D项不符合 题意。9.C
废铜泥灼烧后将金属元素转化为可溶液硫酸的氧化物,酸浸后先加H O 氧化Fe2+,再加NaOH稀溶液,过滤除去
2 2
Fe(OH) ,往滤液中加入Na SO 、NaCl还原后经系列操作得到氯化亚铜产品。
3 2 3
A.根据流程信息,灼烧的目的是使含铜物质尽可能溶解在硫酸溶液中,所以是将CuS、Cu S等转化为CuO,A
2
正确;
B.除杂的目的是使铁元素转化成FeOH 而转化成滤渣,①H O 目的是将Fe2转化成Fe3,②加NaOH稀溶液,
3 2 2
调节溶液的pH,使Fe3转化成FeOH 沉淀,但只加入NaOH稀溶液容易形成FeOH 胶体更难除杂,所以还
3 3
应 加热,B正确;
C.还原反应同时生成H SO ,酸浸又消耗H SO ,所以H SO 可循环使用,但Na SO 没有参与循环,C错误
2 4 2 4 2 4 2 3
D.还原中Cu2+被还原得到氯化亚铜,反应为2Cu2 2ClSO2H O=2CuCl SO2 2H,D正确;
3 2 4
故选C。
10. B
A.从图中分析,反应(I)中氧化剂是H
2
O
2
,其还原产物是A,同时还有·OH,故只有一半的氧原子从-1价降到-2
价,即1mol氧化剂参加反应转移1mole-,A正确;
B.转化(II)的离子方程式:4·OH+H PO-=H PO- +2H O,B错误;
2 2 2 4 2
C.转化(III)表明H PO- 上的H被Fe3+替换,即Fe3+结合PO3-的能力强于H+结合PO3-的能力,C正确;
2 4 4 4
D.H PO-、H PO- 中心原子价电子数对数都是4,均是sp3杂化,D正确;故选B。
2 2 2 4
11.C
结合图中所示结构可知图中两种化合物均为共价化合物,已知X和Z同主族,可得X和Z同为第ⅦA族,Y为
第ⅤA族元素,W为第ⅢA族或第ⅤA族元素,再结合W、X、Y、Z为原子序数依次增大的短周期元素, Y原
子序数为W原子价电子数的3倍推知W、X、Y、Z分别为N、F、P、Cl,据此答题。
A. Z是F,同周期元素,从左到右0族元素电离能最大,A错误;
B.HX是HF,HF内部为极性共价键,属极性分子,B错误;
C.四种元素W(N)、X(F)、Y(P)、Z(Cl)中,W(N)、X(F)有两个电子层,Y(P)、Z(Cl)有三个电
子层,半径大于W(N)和X(F),Y(P)原子序数小于Z(Cl),故Y原子半径在这四种元素中最大;X(F)
原子序数大于W(N),故X原子半径在这四种元素中最小,C正确;
D.原子序数为82的元素为铅元素位于元素周期表ⅣA族,不与N在同一主族,D错误;故选C。
12.A
已知碳的燃烧热为ΔH =akJ·mol-1,则碳燃烧的热化学方程式为:①C(s)+O(g)=CO(g) ΔH1=akJ·mol-1,
1 2 2
②S(s)+2K(s)=K S(s) ΔH =bkJ·mol-1,③2K(s)+N (g)+3O (g)=2KNO (s) ΔH =ckJ·mol-1,
2 2 2 2 3 3根据盖斯定律,可得ΔH=3ΔH +ΔH —ΔH ,即x=3a+b-c,答案选A。
1 2 3
13. B
A.N、Cl是两种不同的元素,因此N-Cl键是极性键;中心N原子价电子对数是4,有1对孤电子对,因此属于
极性分子,即NCl 是由极性键构成的极性分子,A错误;
3
B.N、P、As是第VA的元素,元素的非金属性大于H元素,由于从上到下元素的原子半径逐渐增大,它们与H
形成共价键的极性逐渐减弱,因此极性键之间的排斥力逐渐减小,导致态氢化物NH3 、PH3 、AsH3 的键角逐渐减
小,B正确;
C.在CH
3
Cl分子中C原子形成4个共价键,中心C原子采用sp3杂化;而COCl2 分子中C与O原子之间以共价
双键结合,中心C原子采用sp2杂化,C错误;
D.元素M的基态原子的核外电子排布式为[Kr]4d105s25p5,则M原子的最外层有7个电子,属于第五周期第VIIA
的元素,而不是过渡元素,D错误;故合理选项是B。
14. A
A.收集SO2 气体可以用排饱和NaHSO3 溶液法,A正确;
B.草酸受热易分解,不能用加热法除去草酸中的乙醇,B错误;
C.氨气密度比空气小,不能用向上排空气法收集,C错误;
D.丁装置中氯气不能通过浓硫酸,D错误;故选A。
15.C
A.由图像可知该原电池反应原理为Zn+Cu2+=Zn2++Cu,故Zn电极为负极失电子发生氧化反应,Cu电极为正
极得电子发生还原反应,错误;
B.该装置中为阳离子交换膜只允许阳离子和水分子通过,故两池中c(SO 2-)不变,错误;
4
C.电解过程中溶液中Zn2+由甲池通过阳离子交换膜进入乙池,乙池中Cu2++2e—=Cu,故乙池中为Cu2+~Zn2+,
摩尔质量M(Zn2+)>M(Cu2+)故乙池溶液的总质量增加,正确;
D.该装置中为阳离子交换膜只允许阳离子和水分子通过,电解过程中溶液中Zn2+由甲池通过阳离子交换膜进入
乙池保持溶液中电荷平衡,阴离子并不通过交换膜,错误;本题选C。
二、非选择题(55分)
16. (12每空2分)
(1)加快反应速度
(2)2MoS+2Na2CO3+5O2 2Na2MoO4 +2CO2 +2SO2
(3) Al(OH)3 NaVO3 、NaHCO3
(4)2NH+
4
+6H++4MoO2
4
=(NH4) 2O▪4MoO3▪2H2O+H2O
(5)1:12
【分析】废催化剂在“焙烧”过程中MoS、V O 和Al O 均转化为对应的钠盐,加入水除去固体杂质得到浸出液,
2 5 2 3通入过量二氧化碳生成氢氧化铝沉淀除去铝,得到滤液调节pH,加入氯化铵生成NH VO 沉淀,分离出滤液,加
4 3
入硝 酸铵、硝酸得到(NH
4
)
2
O▪4MnO 2▪2H
2
O;
(1)对于固体来说,粉碎可以增大接触面积,从而加快反应速度,提高反应效率;“焙烧”时需对废催化剂进行
粉碎,目的是加快反应速度;
(2)“焙烧”过程中MoS转化为对应的钠盐,硫元素被氧气氧化为二氧化硫, MoS在焙烧过程中和碳酸钠、氧气
焙烧
反应生成Na MoO 和二氧化碳、二氧化硫,化学方程式为2MoS+2Na CO +5O 2Na MoO +2CO +2SO ;
2 4 2 3 2 2 4 2 2
(3)根据“沉铝”信息可知,“滤渣”的成分为氢氧化铝Al(OH) ;“焙烧”过程中MoS、V O 和Al O 均转化为对应的
3 2 5 2 3
钠盐,沉铝过程中偏铝酸钠和过量二氧化碳生成碳酸氢钠和氢氧化铝沉淀除去了铝,则得到滤液①的主要成分为
Mo、 V的钠盐和生成的碳酸氢钠,故为Na MoO 、NaVO 、NaHCO ;
2 4 3 3
(4)由流程可知,“沉钼”过程中加入硝酸铵和硝酸与MoO2
4
反应生成(NH
4
)
2
O▪4MoO 3▪2H
2
O,离子方程式为
2NH+
4
+6H++4MoO2
4
=(NH
4
)
2
O▪4MoO 3▪2H
2
O+H
2
O;
(5)氢气还原NH O4MoO 2H O得金属钼,钼化合价由+6变为0价,化合价降低发生还原反应为氧化剂;
4 2 3 2
氢气生成水,氢元素化合价由0变为+1,化合价升高发生氧化反应为还原剂;根据电子守恒可知,
NH O4MoO 2H O~24e-~12H ,故氧化剂与还原剂物质的量之比为1:12。
4 2 3 2 2
17.(12分)【答案】
(1) (球形)冷凝管
(2) CoCl 6H O+6SOCl =CoCl +12HCl+6SO
2 2 2 2 2
(3) 防止B中的水蒸气进入A影响实验效果
(4)Ⅲ
(5)
CoC
2
H
5
OH
2
Cl
2
+6H
2
O
Co H
2
O
6
2+ +2Cl +- 2C
2
H
5
OH
(6) A
【分析】把SOCl 滴入三口烧瓶内和CoCl 6H O中的结晶水生成CoCl 、盐酸和二氧化硫,冷凝回流SOCl 反应一
2 2 2 2 2
段时间,将反应混合物隔绝空气减压蒸馏,得到无水CoCl 晶体。
2
(1) 根据装置图,仪器a的名称是球形冷凝管;
(2) 滴加SOCl ,一段时间后容器A中充满白雾,说明SOCl 和吸收CoCl 6H O中的结晶水生成盐酸和二氧化硫,
2 2 2 2
发生反应的化学方程式为CoCl 6H O+6SOCl =CoCl +12HCl+6SO。
2 2 2 2 2
(3) SOCl 常用作吸水剂,遇水剧烈水解生成SO 和HCl,无水CaCl 的作用是防止B中的水蒸气进入A影响实验
2 2 2
效果。(4) 将A中反应混合物隔绝空气减压蒸馏,要用直形冷凝管,适合作为冷凝和接收装置的是Ⅲ。
(5) 滴加蒸馏水溶液由蓝色变为粉红色,说明
CoC
2
H
5
OH
2
Cl
2
加水变为
CoH
2
O
6
2+ ,变色过程中发生反应
的离子方程式为 。
CoC
2
H
5
OH
2
Cl
2
+6H
2
O
Co H
2
O
6
2+ +2Cl +- 2C
2
H
5
OH
(6) A.根据图示可知,该装置中将太阳能转化为电能和化学能,故A错误;B.根据电子流向可知,Cu是正极,
正极上二氧化碳得电子和氢离子反应生成甲烷,电极反应式为:CO +8e-+8H+=CH +2H O,故B正确;C.放电时,
2 4 2
电解质溶液中阳离子向正极移动,所以装置中的H+由左向右移动,故C正确;故选A。
18.(15分,除特殊标注每空2分)
(1) 4d55s1 8:3
(2) > NO+中N原子为sp杂化,键角180°;NO- 中N原子为sp2杂化,键角接近120°
2 2
m 1mol(207+3127+12+14+61)g/mol 620
(3) = = 1021g/cm3;(3分)
V N (a10-7)3 N a3
A A
(4) 3 2
【解析】
(1) Cr原子的价电子排布式为3d54s1,Mo位于Cr同一副族的相邻下一周期,Mo的价电子排布式为4d55s1,基态
Mo3+最高能层N层中电子排布为4s24p64d3,成对电子与单电子的数目比为8:3。
(2)
NO+中N原子为sp杂化,键角180°;NO- 中N原子为sp2杂化,键角接近120°,故NO+键角大于NO- 。
2 2 2 2
1 1
(3)从图(b)可知,一个晶胞中含有Pb2+的数目为1×1=1个,CH NH+的数目为8 =1个,I-的数目为6 =3个,
3 3 8 2
m 1mol(207+3127+12+14+61)g/mol 620
故晶胞的密度为 = = 1021g/cm3;
V N (a10-7)3 N a3
A A
(4) 依据题中对螯合作用的释义,1mol 中Cu与N、O原子形成配位键3mol,跟碳原子
形成一个双键的N共有3个σ键,无孤电子对,是sp2杂化;另一个N原子有3个σ键和一对孤电子对,是sp3杂化,
故该螯合物中N的杂化方式有2种。
19.(16分)
(1) 4 (1分)
(2) (2分)(3) 加成反应 (1分)
(4) C H O (1分) 羰基、酯基(2分)
13 12 3
(5) 酮羰基(1分) 羟基(1分) 还原性 (1分)
(6)1 (1分) a (1分)
(7)H C=CHCH CHO、 、 、 (每个1分)
2 2
【解析】根据所给信息分析同分异构体结构并写出可能的同分异构体;根据有机物结构分析有机物中H原子的化学
环境;根据反应前后有机物结构和分子式推断反应前反应的结构;根据已知条件判断有机反应类型;根据有机
物结构判断有机物可能发生的反应;根据题目所给的合成流程和已知条件选择合适的反应路线制备目标物质。
(1)根据B的结构,有机物B中含有4种不同化学环境的H原子,故在核磁共振氢谱中有4组峰;故答案为:4。
(2)根据有机物C和有机物D的结构,有机物C与有机物X发生酯化反应生成有机物D,则有机物D的结构简
式为
(3) D→E为已知条件的反应,反应类型为加成反应。
(4)根据F的结构简式,有机物F的分子式为C H O ,有机物G中含有的官能团名称是酯基、羰基。
13 12 3
(5)根据G、F的结构简式可知,从G→H中步骤ⅱ实现了由酮羰基到羟基的转化,NaBH 的作用为还原剂
4
(6)根据有机物H的结构,有机物H中含有1个手性碳原子,为左下角与羟基相邻的碳原子;
有机物H中含有羟基,可以与金属Na发生反应;有机物H中含有碳碳双键,可以与酸性高锰酸钾溶液反应;
有机物H中含有酯基,可以被NaOH水解;有机物H中不含与CHCl 反应的基团,故不与CHCl 反应,故选
3 3
择a。
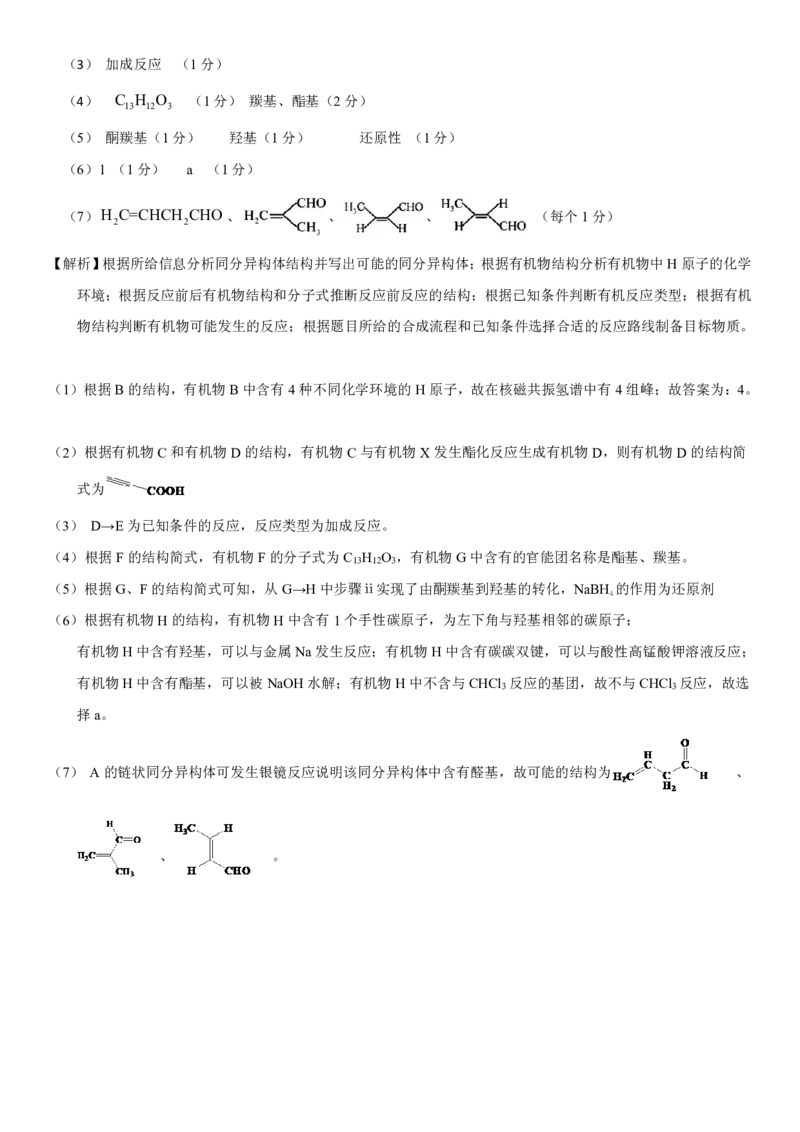
(7) A的链状同分异构体可发生银镜反应说明该同分异构体中含有醛基,故可能的结构为 、
、 。