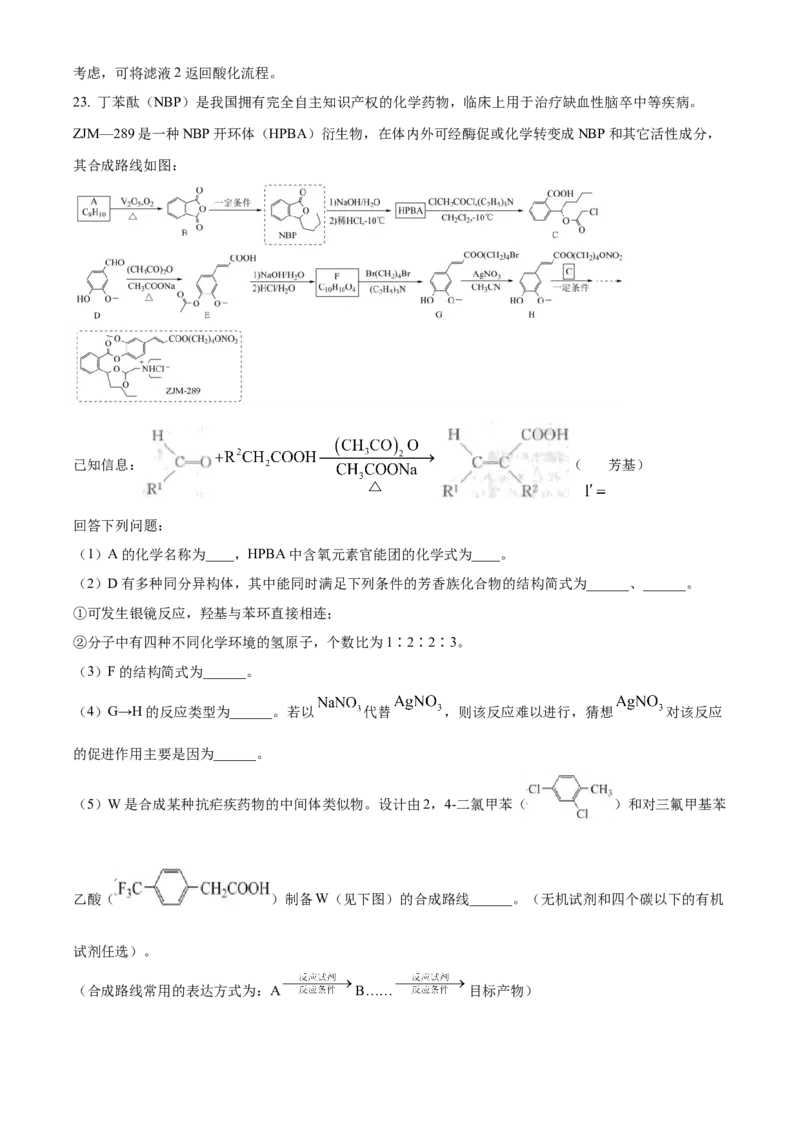
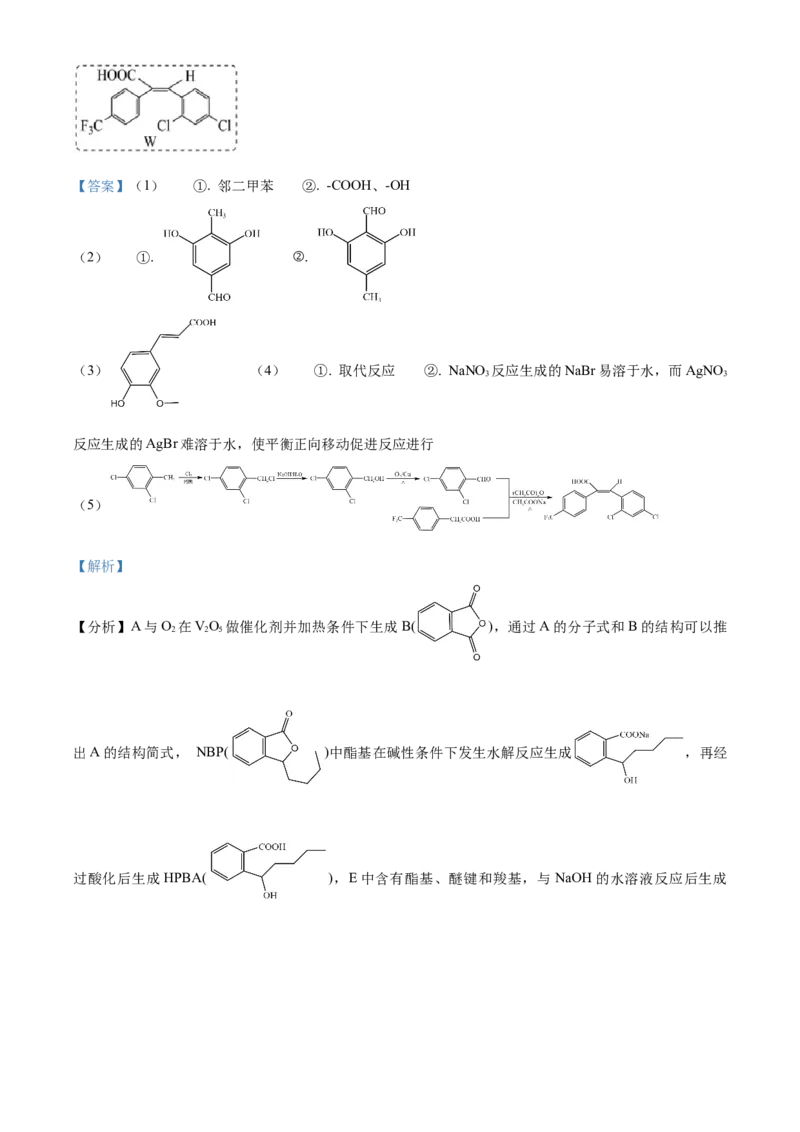
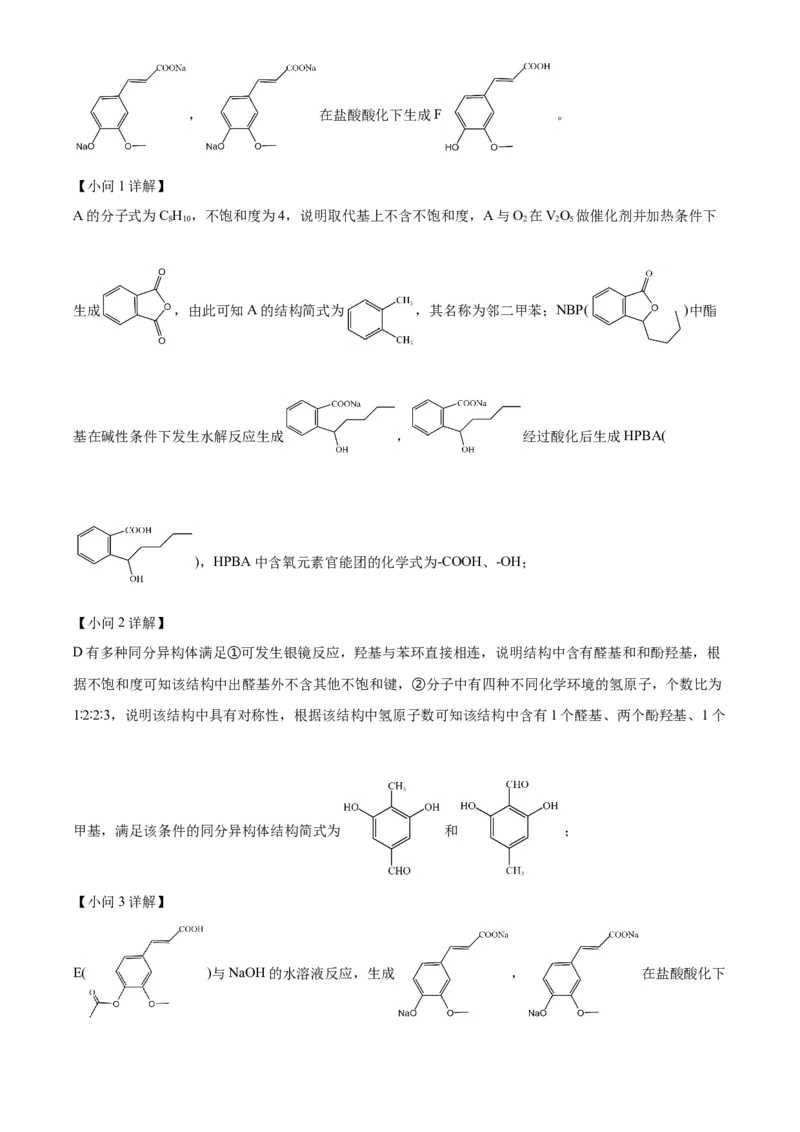
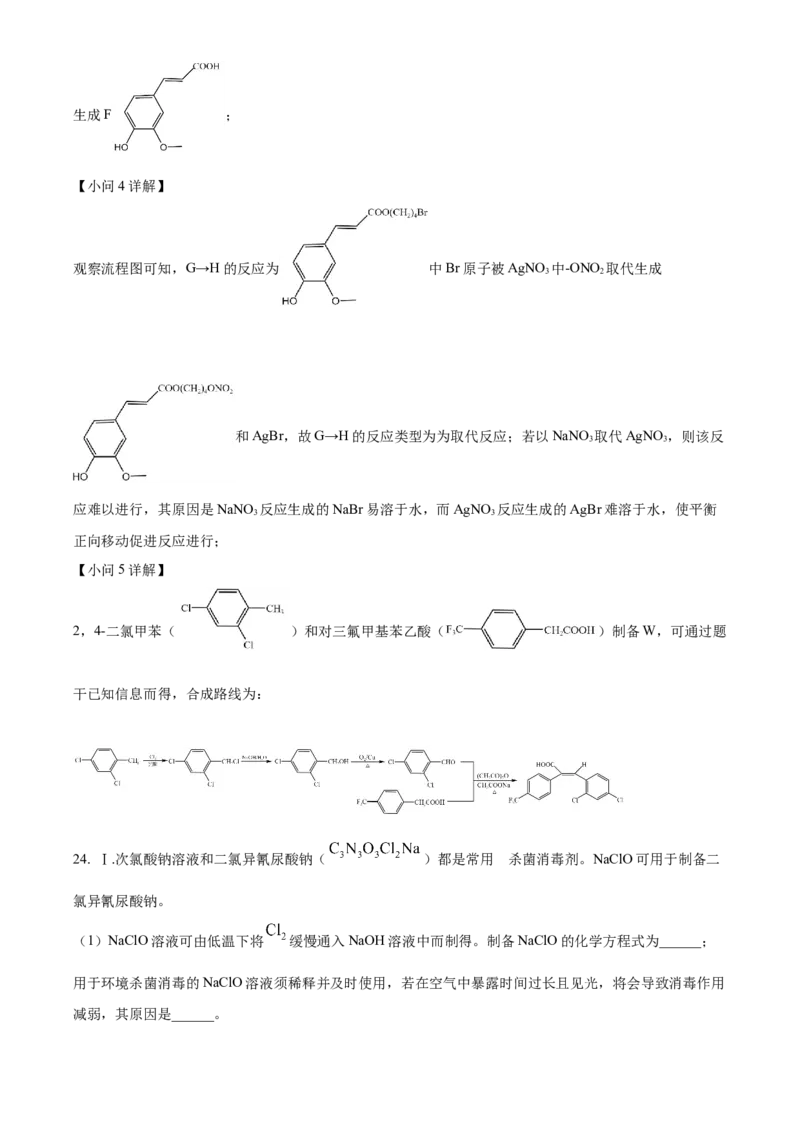
文档内容
2022 学年第一学期高三化学教学质量调研试卷
相对原子质量:H-1 O-16 S-32 P-31 Cl-35.5 C-12 N-14 Na-23
一、选择题(共40分,每小题2分,每小题只有一个正确选项)
1. 生活中处处有化学,下列叙述正确的是
A. HB铅笔芯的成分为二氧化铅 B. 碳酸氢钠可做食品膨松剂
C. 青铜和黄铜是不同结构的单质铜 D. 焰火中红色来源于钠盐灼烧
【答案】B
【解析】
【详解】A.铅笔芯的主要成分为石墨,不含二氧化铅,A错误;
B.碳酸氢钠不稳定,受热易分解产生二氧化碳,能使面团松软,可做食品膨松剂,B正确 ;
C.青铜是在纯铜(紫铜)中加入锡或铅的合金,黄铜为是由铜和锌所组成的合金,两者均属于混合物,不是
铜单质,C错误;
D.钠元素灼烧显黄色,D错误;
故选B。
2. 下列变化需要加入氧化剂才能实现的转化是
A. 浓HSO →SO B. KClO→O C. HS→SO D. →CO
2 4 2 3 2 2 2 2
【答案】C
【解析】
【详解】A.浓HSO →SO ,S元素的价态降低,浓硫酸作氧化剂,需加入还原剂,A不合题意;
2 4 2
B.KClO→O,不需另加氧化剂,因为KClO 分解就可生成O,B不合题意;
3 2 3 2
C.HS→SO ,S元素的化合价升高,HS作还原剂,需加入氧化剂,C符合题意;
2 2 2
D. →CO,没有元素价态的改变,不需加入氧化剂,D不合题意;
2
故选C。
3. 能用于比较硫、氯两种元素非金属性强弱的是
A. 熔点:S > Cl B. 酸性:HClO > H SO
2 4 2 4
C. 相对原子质量:Cl > S D. 氧化性:HClO>HSO
2 3
【答案】B
【解析】
【分析】比较两种元素的非金属性强弱,可根据单质之间的置换反应、与氢气反应的难易程度、氢化物的稳定性以及最高正价氧化物对应水化物酸性强弱,据此分析。
【详解】A.熔点的高低不能作为非金属性的判断依据,故A不符合题意;
B.HClO 和HSO 分别是S和Cl的最高价含氧酸,HClO 的酸性强于HSO 可以说明Cl的非金属性强于
4 2 4 4 2 4
S,故B符合题意;
C.元素的相对原子质量不能作为非金属性的判断依据,故C不符合题意;
D.不能根据含氧酸的氧化性判断元素的非金属性,故D不符合题意。
答案选B。
4. 关于乙烯的说法正确的是
A. 等摩尔乙烷和乙烯中,化学键数相同 B. 所有原子在一直线上
C. 既有极性键又有非极性键 D. 属于极性分子
【答案】C
【解析】
【详解】A.1molC H 有7mol化学键(含1mol碳碳键和6mol碳氢键),1molC H 有5mol化学键(含
2 6 2 4
1mol碳碳双键和4mol碳氢键),则等摩尔乙烷和乙烯中,化学键数不相同,A错误;
B.乙烯中碳原子采用sp2杂化,所有原子共平面但是不共线,B错误;
C.乙烯存在C-H极性共价键、C=C非极性共价键,C正确;
D.乙烯分子中,正电中心和负电中心重合,为非极性分子,D错误;
故选C 。
5. 下列化学用语正确的是
A. 碳原子 核的外电子轨道表示式:
B. 的电子式:
C. 丙烷的比例模型:
D. 原子核内有6个中子的碳原子:
【答案】A
【解析】
【详解】A.碳原子的核外电子排布式为1s22s22p2,轨道表示式为 ,A正确;B. 的电子式为 ,B错误;
C.模型 是丙烷的球棍模型,C错误;
D.碳原子 中含有6个质子和8个中子,D错误;
故答案为:A。
6. 过氧化氢溶液是一种常见的消毒剂,以下对其描述不符合事实的是
A. 外用消毒剂 B. 有漂白作用 C. 需密封保存 D. 有强氧化性,无还原性
【答案】D
【解析】
【详解】A.过氧化氢具有强氧化性,可用作外消毒剂,A项正确;
B.过氧化氢具有强氧化性,可与色素反应,有漂白作用,B项正确;
C.过氧化氢不稳定,易分解,故需密闭保存,C项正确;
D.过氧化氢分解为水和氧气的反应中,过氧化氢即做氧化剂,又作还原剂,故过氧化氢即有强氧化性,
又有还原性,D项错误;
故选D。
7. 在醋酸溶液中,CHCOOH电离达到平衡的标志是
3
A. 溶液显电中性 B. 氢离子浓度恒定不变
C. c(H+) = c(CHCOO¯) D. 溶液中检测不出CHCOOH分子存在
3 3
【答案】B
【解析】
【详解】A.任何电解质溶液中都呈电中性,与弱电解质是否达到电离平衡无关,故A不符合题意;
B.氢离子浓度恒定不变时说明正逆反应速率相等,则该反应达到平衡状态,可作为CHCOOH电离达到
3
平衡的标志,故B符合题意;
C.由于醋酸的电离程度未知,达到平衡时c(H+)与c(CHCOO-)关系不确定,且c(H+)=c(CHCOO-)不符合溶
3 3
液电中性原则,故C不符合题意;
D.CHCOOH为弱电解质,电离为可逆过程,即CHCOOH CHCOO-+H+,溶液中存在CHCOOH分子,
3 3 3 3
故D不符合题意;
答案为B。
8. 能用分液漏斗分离的一组物质是A. AgCl 和NaCl 溶液 B. 苯和水
C. 溴和四氯化碳 D. 乙酸和乙酸乙酯
【答案】B
【解析】
【详解】A.AgCl 和NaCl 溶液选择用过滤操作分离,应选择三角漏斗,不需要分液漏斗,故A错误;
B.苯和水互不相溶,分层,选择分液操作分离,则应选择分液漏斗,故B正确;
C.溴和四氯化碳相互混溶,选择蒸馏操作分离,应选择蒸馏烧瓶、冷凝管等,不需要分液漏斗,故C错
误;
D.乙酸和乙酸乙酯相互混溶,选择蒸馏操作分离,应选择蒸馏烧瓶、冷凝管等,不需要分液漏斗,故D
错误;
为
故答案 B。
9. 下列生产中,水没有参与化学反应的是
A. 氯碱工业 B. 侯氏制碱 C. 湿法炼铜 D. 接触法制硫酸
【答案】C
【解析】
【详解】A.氯碱工业 是电解饱和食盐水,水参与了反应,故A错误。
B.侯氏制碱是在氯化钠的饱和溶液中通入氨气和二氧化碳发生反应生成碳酸氢钠和氯化铵的过程,有水
参与了反应,故B错误。
C.用硫酸将铜矿中的铜转变成可溶性的硫酸铜,再将铁放入硫酸铜溶液中把铜置换出来,没有水参与反
应,故C正确。
D.接触法制硫酸,是利用了三氧化硫和水发生反应,故D错误。
故选C。
10. 加油站有不同型号的汽油,下列说法正确的是
A. 汽油属于纯净物 B. 煤通过干馏可以转化为汽油
C. 石油分馏可以获得汽油 D. 重油的裂解可以提高汽油的产量
【答案】C
【解析】
【详解】A.汽油是主要成分为C ~C 脂肪烃和环烷烃类,以及一定量芳香烃,是混合物,A错误;
5 12
B.煤干馏的产物是煤炭、煤焦油和煤气,B错误;
C.石油分馏可得汽油、柴油等,C正确;
D.裂解是深度裂化,其目的是生成气态烯烃或提高燃油品质,D错误;
故选C。11. FeS 与酸反应时生成HS,HS 与HO 相似,易分解。实验室用过量稀硫酸与FeS 颗粒混合,不可能
2 2 2 2 2 2 2 2
生成的物质是
A. HS B. S C. FeS D. FeSO
2 4
【答案】C
【解析】
【详解】由题意知,FeS 颗粒与硫酸发生反应生成硫酸亚铁和过硫化氢,即FeS+HSO =H S+FeSO ,
2 2 2 4 2 2 4
HS 类似于HO,易分解,HS 发生分解反应生成HS气体和单质S,即HS=H S↑+S↓,则不可能生成
2 2 2 2 2 2 2 2 2 2
的是FeS,C项符合题意。
故选C。
12. 海水提溴常用 达到富集目的,此反应相关物质的叙述正确的是
A. 在常温常压下是红棕色的气体 B. 属于离子化合物
C. 属于非电解质的只有 D. HO分子的空间构型是直线型
2
【答案】C
【解析】
【详解】A. 在常温常压下是红棕色的液体,A错误;
B.HSO 只含共价键属于共价化合物,B错误;
2 4
C.反应中的化合物有SO 、HO、HSO 、HBr,其中只有SO 不能电离,为非电解质,C正确;
2 2 2 4 2
D.HO中心原子价层电子数为4,含有2对孤电子对,所以空间构型为V形,D错误;
2
故答案为:C。
13. 有关水处理的方法错误的是
A. 用可溶性的铝盐、铁盐处理水中悬浮物
B. 用氯气处理水中的Cu2+、Hg2+等重金属离子
C. 用石灰、纯碱等碱性物质处理废水中的酸
D. 用烧碱处理含高浓度 的废水并回收利用氨
【答案】B
【解析】
【详解】A. 铝盐、铁盐能够水解生成氢氧化铝、氢氧化铁胶体,能吸附水中悬浮的杂质,沉降净水,故
可用可溶性的铝盐、铁盐处理水中悬浮物,故A正确;
B. 氯气不能与与Cu2+、Hg2+等重金属离子反应,可用NaS等处理水中的Cu2+、Hg2+等重金属离子,生成
2难溶的CuS,HgS,故B错误;
C. 石灰、纯碱与酸发生反应生成氯化钙、氯化钠,故可用石灰、纯碱等碱性物质处理废水中的酸,故C
正确;
D. 烧碱与高浓度 反应生成氨气,故可用烧碱处理含高浓度 的废水并回收利用氨,故D正确;
故选B。
14. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A. c(H+)/c(OH-)=1×10-14的溶液:Ca2+、Na+、 、
B. 0.1 mol·L-1 KOH溶液: 、Na+、I-、
C. 能使pH试纸显深红色的溶液:Fe3+、Cl-、Ba2+、SCN-
D. 0.1 mol·L-1NaClO溶液:HS-、Na+、Cl-、
【答案】B
【解析】
【详解】A. )=1×10-14的溶液中c(H+)=10-14mol/L,c(OH-)=1mol/L,该溶液显碱性, 不能
在碱性溶液中存在,故A错误;
B.0.1 mol·L-1 KOH溶液: 、Na+、I-、 四种离子之间不发生反应,可以大量共存,故B正确;
C.能使pH试纸显深红色的溶液呈酸性,SCN-和Fe3+形成络合物,不能大量共存,故C错误;
D.0.1 mol·L-1NaClO溶液中,ClO-会和HS-发生氧化还原反应不能大量共存,故D错误;
故选B。
15. 测定CuSO •xH O中水的含量,如果实验值偏低,可能的原因是
4 2
A. 盛晶体的坩埚未完全干燥
B. 加热后白色粉末在空气中冷却
C. 加热后有少量黑色固体产生
D. 加热时有少量晶体溅出
【答案】B
【解析】
【详解】A.坩埚未完全干燥,会使结晶水质量偏大,会使测定结果偏高,A不符合题意;
B.加热后直接在空气中冷却至室温后称量,粉末吸收了空气中的水分,会使测得的结晶水的质量偏低,B
符合题意;C.加热后有少量黑色固体产生,说明生成了CuO,质量变化较大,说明生成的水的质量偏大,导致最终
所测结果偏高,C不符合题意;
D.加热过程中晶体有少量溅失,质量变化较大,说明生成的水的质量偏大,导致结果偏高,D不符合题
意;
故选B。
【点睛】硫酸铜晶体中结晶水含量测定实验过程中,为避免或减少误差,必须注意:①加热硫酸铜晶体用
玻璃棒轻轻搅拌的目的是受热均匀,防止受热不均匀而引起固体飞溅,溅出坩埚;②生成的无水硫酸铜要
在干燥器中冷却,而不能在空气中冷却,是防止无水硫酸铜吸收空气中的水分;③两次第五步的操作,质
量差要小于0.1g,是为了保证实验的准确性和减小误差。
16. 苯并降冰片烯是一种重要的药物合成中间体,结构简式如图。关于该化合物,下列说法正确的是
A. 是苯的同系物
B. 分子中最多8个碳原子共平面
C. 一氯代物有6种(不考虑立体异构)
D. 分子中含有4个碳碳双键
【答案】B
【解析】
【分析】
【详解】A.苯的同系物必须是只含有1个苯环,侧链为烷烃基的同类芳香烃,由结构简式可知,苯并降
冰片烯的侧链不是烷烃基,不属于苯的同系物,故A错误;
B.由结构简式可知,苯并降冰片烯分子中苯环上的6个碳原子和连在苯环上的2个碳原子共平面,共有8
个碳原子,故B正确;
C.由结构简式可知,苯并降冰片烯分子的结构上下对称,分子中含有5类氢原子,则一氯代物有5种,
故C错误;
D.苯环不是单双键交替的结构,由结构简式可知,苯并降冰片烯分子中只含有1个碳碳双键,故D错误;
故选B。
17. 将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在题图所示的情境中,下列有关说法
正确的是A. 阴极的电极反应式为
B. 金属M的活动性比Fe的活动性弱
C. 钢铁设施表面因积累大量电子而被保护
D. 钢铁设施在河水中的腐蚀速率比在海水中的快
【答案】C
【解析】
【分析】该装置为原电池原理的金属防护措施,为牺牲阳极的阴极保护法,金属M作负极,钢铁设备作正
极,据此分析解答。
【详解】A.阴极的钢铁设施实际作原电池的正极,正极金属被保护不失电子,故A错误;
B.阳极金属M实际为原电池装置的负极,电子流出,原电池中负极金属比正极活泼,因此M活动性比Fe
的活动性强,故B错误;
C.金属M失电子,电子经导线流入钢铁设备,从而使钢铁设施表面积累大量电子,自身金属不再失电子
从而被保护,故C正确;
D.海水中的离子浓度大于河水中的离子浓度,离子浓度越大,溶液的导电性越强,因此钢铁设施在海水中
的腐蚀速率比在河水中快,故D错误;
故选:C。
18. 含29.40g HPO 的水溶液滴加到含0.500molCa(OH) 的悬浮液中,反应恰好完全,生成1种难溶盐和
3 4 2
16.2g HO。该难溶盐的化学式可表示为
2
A. B.
C. D.
【答案】B
【解析】
【详解】29.40g HPO 的物质的量为: =0.30mol,n(H O)= =0.9 mol
3 4 2由原子守恒可得生成难溶盐中含 0.5 mol Ca、0.3 mol P、0.1 mol H和1.3 mol O,即难溶盐中N(Ca):
N(P):N(H):N(O)=5:3:1:13,其化学式为Ca (PO )(OH),故答案为:Ca (PO )(OH),故答案为:B。
5 4 3 5 4 3
19. 已知 。一定温度下,在体积恒定的密闭容器中,加入
1mol 与1mol ,下列说法正确的是
A. 充分反应后,放出热量为akJ
B. 若增大Y的浓度,正反应速率增大,逆反应速率减小
C. 当X的物质的量分数不再改变,表明该反应已达平衡
D. 当反应达到平衡状态时,X与W的物质的量浓度之比一定为1:2
【答案】C
【解析】
【详解】A.该反应为可逆反应,不能完全转化,充分反应后,放出热量小于akJ,A错误;
B.若增大Y的浓度,压强增大,正反应速率增大,逆反应速率也增大,B错误;
C.当X的物质的量分数不再改变时,说明X的物质的量不再变化,表明该反应已达平衡,C正确;
D.当反应达到平衡状态时,X与W的物质的量浓度之不一定为1:2,与各物质的初始浓度和转化率有关,
D错误;
故答案为:C。
20. 室温下,反应 的平衡常数 。将 溶液和氨水按一
定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室温时下列指定溶液中微粒
物质的量浓度关系正确的是
A. 0.2mol/L氨水:
B. 溶液( ):
C. 0.2mol/L氨水和 溶液等体积混合:
D. 氨水和 溶液等体积混合:【答案】D
【解析】
【详解】A.0.2mol/L氨水中存在的平衡: 和 ,粒子浓度的大
小为: ,A错误;
B. , 和 发生水解: ,
,因为 , 的水解程度大于 ,所以溶液中粒子浓度的大
小为: ,B错误;
C.0.2mol/L氨水和 溶液等体积混合,根据物料守恒,
,
,C错误;
D. 氨水和 溶液等体积混合,由物料守恒:
,
,根据电荷守恒: ,联
立3个关系式,可得 ,D正确;
故选D。
二、综合题(共60分)
21. 硫及其化合物在生产、生活中有广泛应用。
(1)硫原子最外层有______种不同运动状态的电子,其中能量最高的电子所占电子亚层符号为______。
(2)硫与同主族的氧元素相比,两者各自形成气态氢化物稳定性 ______ (选填“>”、“<”或“=”下同),分别与氢元素形成化学键键能大小关系为H—O______H—S。
(3)正交硫和单斜硫是硫常见的两种单质,它们互为______。已知: (正交)= (单斜)―2.64kJ。
正交硫与单斜硫相比,相对比较稳定的是______。已知通常状况下4g硫粉完全燃烧放出37kJ的热量,写
出该反应的热化学方程式______。
(4)同温同浓度的 、 、 三种溶液, 最大的是______;经测定
溶液中 ,则 溶液呈______(填“酸”或“碱”)性;等物质的量浓
度的下列四种溶液:① ② ③ ④ ,溶液中水的电离程度由大到小排
列顺序为______。
(5)已知 可能会干扰 的检验。写出 和NaCl混合溶液中 的检验方法______。
【答案】(1) ①. 6 ②. 3p
(2) ①. > ②. >
(3) ①. 同素异形体 ②. 正交硫 ③. S +O =SO(g) =-296
2 2
(4) ①. 溶液 ②. 酸 ③. ②>④>③>①
(5)加入Ba(NO ) 溶液至不再产生白色沉淀时,取上层清液,向其中加入 AgNO 溶液,若产生白色沉淀,
3 2 3
则证明混合溶液中含有Cl-
【解析】
【小问1详解】
硫原子最外层有6个电子,每个电子的运动状态都不同,故硫原子最外层有6种不同运动状态的电子;S
的价电子排布式为3s23p4,其中能量最高的电子所占电子亚层符号为3p;
【小问2详解】
非金属性越强,气态氢化物越稳定,非金属性:O>S,故气态氢化物稳定性:HO>HS;O原子半径小于S
2 2
原子半径,且O元素的电负性大于S元素,故H-O键长较短,键能H-O>H-S;
【小问3详解】
正交硫和单斜硫是硫常见的两种单质,两者互为同素异形体;根据已知 (正交)= (单斜)-2.64kJ,可知
(正交)能量低与 (单斜),能量越低越稳定,故正交硫与单斜硫相比,相对比较稳定的是正交硫;通常状况下4g硫粉完全燃烧放出37kJ的热量,则1mol硫粉(32g)放出的热量为37 ×8=296 ,则该反应的
热化学方程式为S +O =SO(g) =-296 ;
2 2
【小问4详解】
同温同浓度的 、 、 三种溶液中, 溶液中NH 促进SO 的水
解,导致SO 浓度变小, 溶液中HSO 只有部分电离出SO ,因此 溶液中
最大; 溶液中HSO 既电离也水解,分别为HSO +H O HSO 、HSO H++SO ,因为
2 2 3
溶液中 ,说明SO 以电离为主,溶液显酸性;等物质的量浓度的下列四种溶液:
① ② ③ ④ ,其中② 溶液中NH 和CO 都促进水的
电离,④ 溶液中HCO 水解为主,促进水的电离,③ 溶液中HSO 以电离为主使溶液显
酸性,抑制水的电离,① 属于强碱,在溶液中全部电离,抑制水电离,因此溶液中水的电离程度
由大到小排列顺序为②>④>③>①;
【小问5详解】
和NaCl混合溶液中检验 ,需要先用Ba2+除去SO ,然后再用AgNO 溶液检验Cl-,故检验
3
方法为:加入Ba(NO ) 溶液至不再产生白色沉淀时,取上层清液,向其中加入AgNO 溶液,若产生白色沉
3 2 3
淀,则证明混合溶液中含有Cl-。
22. 砷(As)是氮的同族元素,且比氮多2个电子层,镓(Ga)与铝同主族,砷化镓是当代国际公认的继
硅之后最成熟的化合物半导体材料。某含砷(As)的有毒工业废水经如图流程转化为粗 。已知:亚
砷酸钙微溶于水,砷酸钙难溶于水。完成下列填空:
(1)砷在元素周期中的位置为第______周期、第______族;砷和热的浓 反应,生成 ,反应
的化学方程式为______;砷化镓(GaAs)和氮化硼(BN)晶体都具有空间网状结构,硬度大,则砷化镓
熔点______氮化硼的熔点(选填“高于”、“低于”或“接近于”)。
(2)“碱浸”的目的是将废水中的 和 转化为盐, 转化为 的离子方程式
为______;加入试剂1的目的是______。
(3)“沉砷”是将 转化为 沉淀,主要反应有(其中 、 都大于0):
① ;② ;
沉砷最佳温度是85℃。用化学平衡原理解释温度高于85℃后,随温度升高沉淀率下降的原因。______。
(4)通过对 溶液进行加热,再过滤可制得粗 。 在不同温度和不同浓度硫酸中的溶
解度(S)曲线如图所示。为提高粗 的沉淀率,则“结晶”过程应控制的最佳条件是______。从绿色
化学和综合利用的角度考虑,滤液2需要处理,其方法是______。
【答案】(1) ①. 四 ②. ⅤA ③. 2As+3H SO (浓) As O+3SO↑+3H O ④. 低于
2 4 2 3 2 2
(2) ①. HAsO +3OH-=AsO +3H O ②. 将AsO 氧化生成AsO
3 4 2
(3)温度升高,反应A平衡逆向移动, 、 下降,反应B平衡逆向移动,Ca (AsO)OH
5 4 3沉淀率下降
(4) ①. 温度约为25℃,HSO 浓度约为7 ②. 返回酸化流程
2 4
【解析】
【分析】流程图中,“碱浸”过程是将废水中的 和 转化为盐;溶液中存在AsO ,通过后
面流程可知需要沉淀的是AsO ,因此加入氧化剂试剂1,将AsO 氧化生成AsO ;“沉砷”时加入石灰
乳,调节为碱性,并提供钙离子,将 转化为 沉淀;“酸化”过程加入硫酸,得到较
纯净的 ;“还原”过程通入SO ,还原 为 ,然后结晶得到粗As O,据此分析。
2 2 3
【小问1详解】
氮是第二周期、第ⅤA族,砷是氮的同族元素,且比氮多2个电子层,因此砷在元素周期中的位置为第四
周期、第ⅤA族;;砷和热的浓 反应,生成 ,反应的化学方程式为2As+3H SO (浓)
2 4
As O+3SO↑+3H O;砷化镓(GaAs)和氮化硼(BN)晶体都具有空间网状结构,说明两者都是原子晶
2 3 2 2
体,原子晶体的熔沸点与键长成反比,原子半径越小,键长越短,键长:B-N