文档内容
自然资源的开发与利用
(一)海水资源
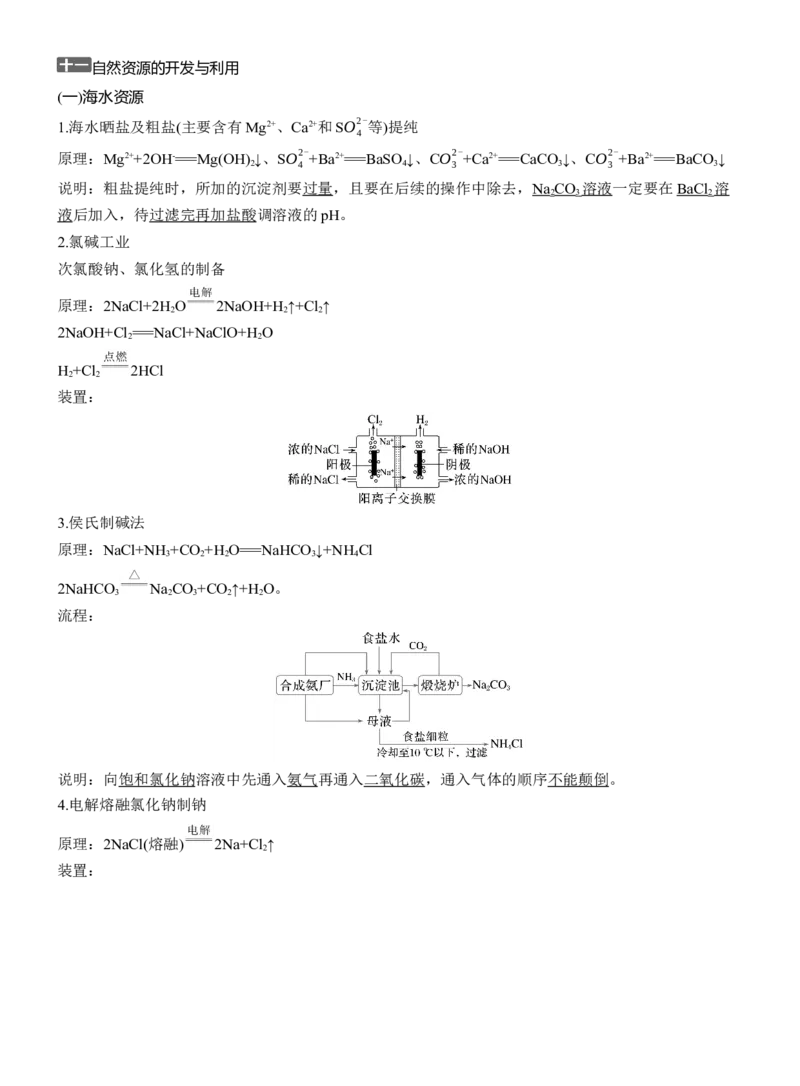
1.海水晒盐及粗盐(主要含有Mg2+、Ca2+和SO2-等)提纯
4
原理:Mg2++2OH-===Mg(OH) ↓、SO2- +Ba2+===BaSO ↓、CO2- +Ca2+===CaCO ↓、CO2- +Ba2+===BaCO ↓
2 4 4 3 3 3 3
说明:粗盐提纯时,所加的沉淀剂要过量,且要在后续的操作中除去,Na CO 溶液一定要在BaCl 溶
2 3 2
液后加入,待过滤完再加盐酸调溶液的pH。
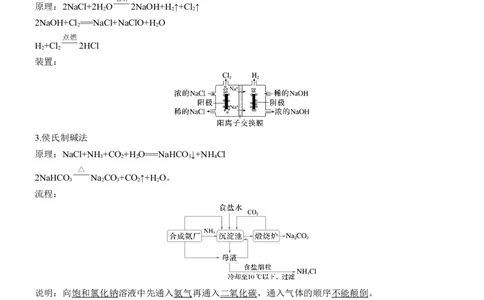
2.氯碱工业
次氯酸钠、氯化氢的制备
原理:2NaCl+2H O 2NaOH+H ↑+Cl ↑
2 2 2
2NaOH+Cl ===NaCl+NaClO+H O
2 2
H +Cl 2HCl
2 2
装置:
3.侯氏制碱法
原理:NaCl+NH +CO +H O===NaHCO ↓+NH Cl
3 2 2 3 4
2NaHCO Na CO +CO ↑+H O。
3 2 3 2 2
流程:
说明:向饱和氯化钠溶液中先通入氨气再通入二氧化碳,通入气体的顺序不能颠倒。
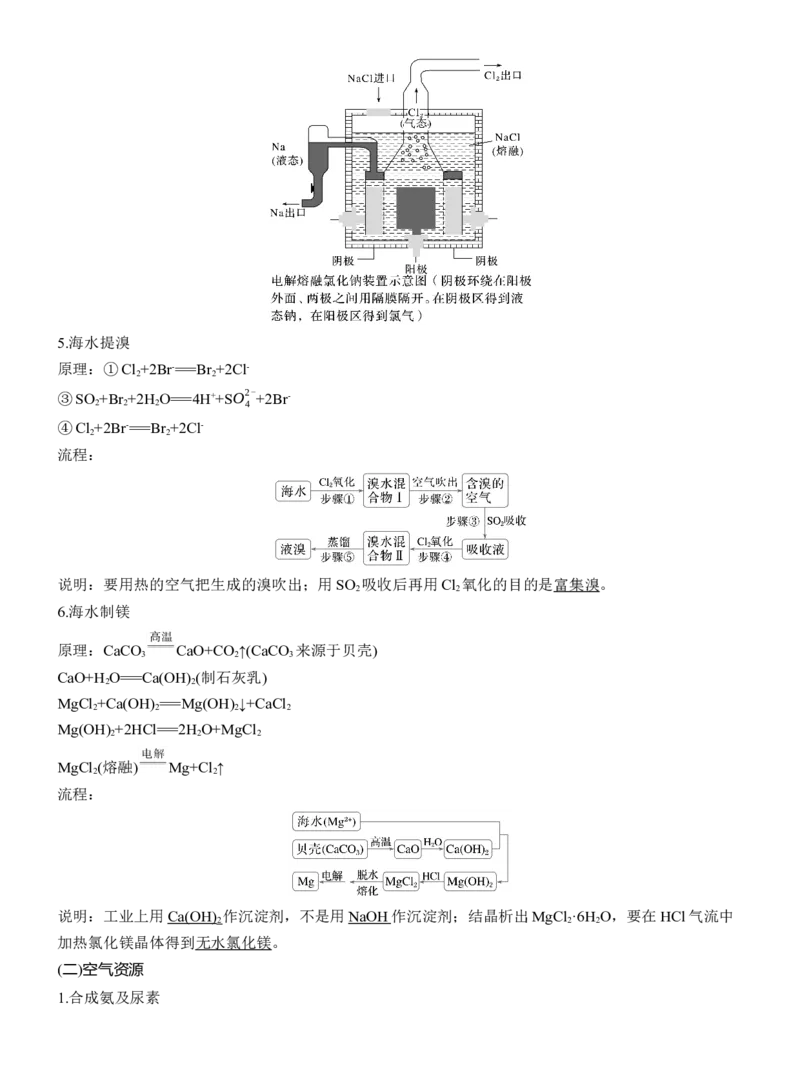
4.电解熔融氯化钠制钠
原理:2NaCl(熔融) 2Na+Cl ↑
2
装置:5.海水提溴
原理:①Cl +2Br-===Br +2Cl-
2 2
③SO +Br +2H O===4H++SO2- +2Br-
2 2 2 4
④Cl +2Br-===Br +2Cl-
2 2
流程:
说明:要用热的空气把生成的溴吹出;用SO 吸收后再用Cl 氧化的目的是富集溴。
2 2
6.海水制镁
原理:CaCO CaO+CO ↑(CaCO 来源于贝壳)
3 2 3
CaO+H O===Ca(OH) (制石灰乳)
2 2
MgCl +Ca(OH) ===Mg(OH) ↓+CaCl
2 2 2 2
Mg(OH) +2HCl===2H O+MgCl
2 2 2
MgCl (熔融) Mg+Cl ↑
2 2
流程:
说明:工业上用Ca(OH) 作沉淀剂,不是用NaOH 作沉淀剂;结晶析出MgCl ·6H O,要在HCl气流中
2 2 2
加热氯化镁晶体得到无水氯化镁。
(二)空气资源
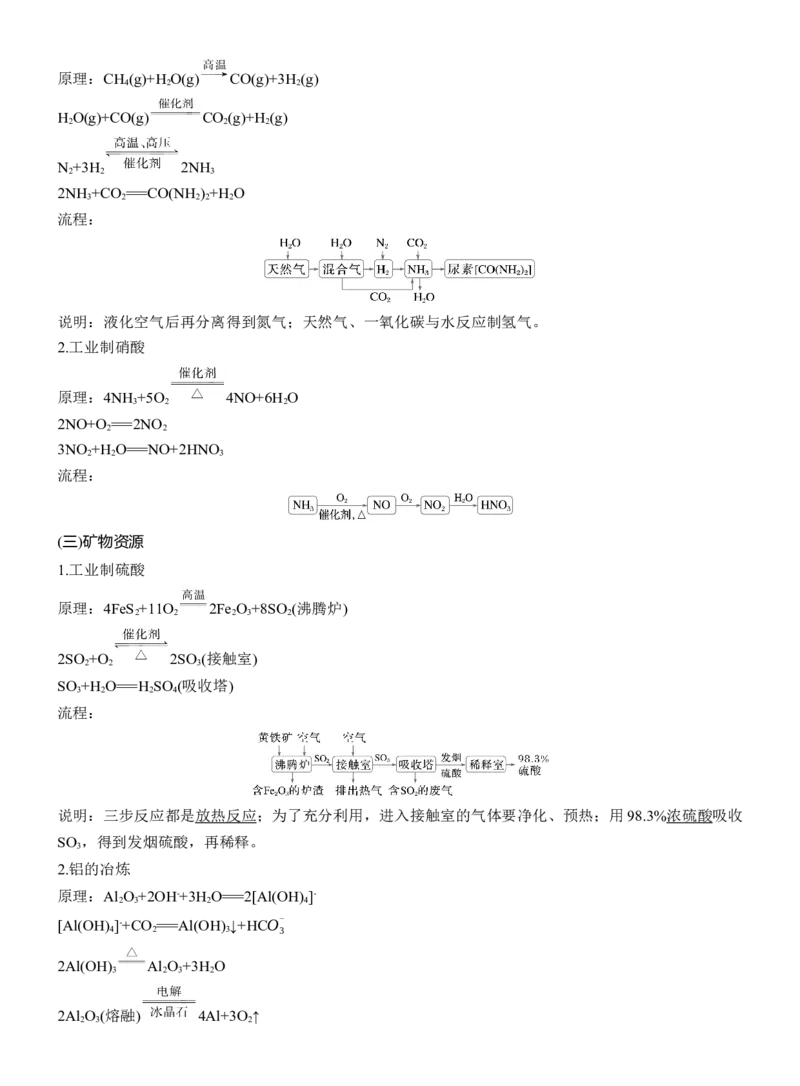
1.合成氨及尿素原理:CH (g)+H O(g) CO(g)+3H (g)
4 2 2
H O(g)+CO(g) CO (g)+H (g)
2 2 2
N +3H 2NH
2 2 3
2NH +CO ===CO(NH ) +H O
3 2 2 2 2
流程:
说明:液化空气后再分离得到氮气;天然气、一氧化碳与水反应制氢气。
2.工业制硝酸
原理:4NH +5O 4NO+6H O
3 2 2
2NO+O ===2NO
2 2
3NO +H O===NO+2HNO
2 2 3
流程:
(三)矿物资源
1.工业制硫酸
原理:4FeS +11O 2Fe O +8SO (沸腾炉)
2 2 2 3 2
2SO +O 2SO (接触室)
2 2 3
SO +H O===H SO (吸收塔)
3 2 2 4
流程:
说明:三步反应都是放热反应;为了充分利用,进入接触室的气体要净化、预热;用98.3%浓硫酸吸收
SO ,得到发烟硫酸,再稀释。
3
2.铝的冶炼
原理:Al O +2OH-+3H O===2[Al(OH) ]-
2 3 2 4
[Al(OH) ]-+CO ===Al(OH) ↓+HCO-
4 2 3 3
2Al(OH) Al O +3H O
3 2 3 2
2Al O (熔融) 4Al+3O ↑
2 3 2流程:
说明:Al O →[Al(OH) ]-→Al(OH) →Al O ,一系列的变化是为了得到纯净的Al O 。
2 3 4 3 2 3 2 3
3.粗硅的提纯
原理:SiO +2C Si+2CO↑
2
粗硅提纯:Si+3HCl SiHCl +H
3 2
SiHCl +H Si+3HCl
3 2
说明:SiO +2C Si+2CO↑,氧化产物是CO。
2
4.硅酸盐工业——玻璃
原理:CaCO +SiO CaSiO +CO ↑
3 2 3 2
Na CO +SiO Na SiO +CO ↑
2 3 2 2 3 2
说明:制玻璃的原料是Na CO 、CaCO 、SiO ,玻璃的主要成分是Na SiO 、CaSiO 、SiO 。
2 3 3 2 2 3 3 2