文档内容
微专题10 “守恒法”在氧化还原反应计算中应
用
1.(2023·浙江·高考真题)关于反应 ,下列说法正确的是
A.生成 ,转移 电子 B. 是还原产物
C. 既是氧化剂又是还原剂 D.若设计成原电池, 为负极产物
2.(2022·全国·高考真题) 为阿伏加德罗常数的值,下列说法正确的是
A.25℃, 下, 氢气中质子的数目为
B. 溶液中, 的数目为
C. 苯甲酸完全燃烧,生成 的数目为
D.电解熔融 ,阴极增重 ,外电路中通过电子的数目为
资料收集整理【淘宝店铺:向阳百分百】 1
学科网(北京)股份有限公司一、 在高中化学计算中通常要遵循三大守恒规律:
1.得失电子守恒 2.质量守恒 3.电荷守恒
二、守恒思想在氧化还原反应计算中的应用
1.对于氧化还原反应的计算,要根据氧化还原反应的实质——反应中氧化剂得到的电子总数与还原剂失
去的电子总数相等,即得失电子守恒。利用守恒的思想,可以抛开繁琐的反应过程,可不写化学方程式,
不追究中间反应过程,只要把物质分为始态和终态,从得电子和失电子两个方面进行整体思维,便可迅速
获得正确结果。
三、考查角度
(1)考查两元素之间得失电子守恒计算
(2)考查多步反应得失电子守恒计算
有的试题涉及的氧化还原反应较多,数量关系较为复杂,若用常规方法求解比较困难,若抓住失电子总数
等于得电子总数这一关系,则解题就变的很简单。解这类试题时,注意不要遗漏某个氧化还原反应,要理
清具体的反应过程,分析在整个反应过程中化合价发生变化的元素得电子数目和失电子数目,即可迅速求
解。
资料收集整理【淘宝店铺:向阳百分百】 2
学科网(北京)股份有限公司1.(2022·河北·高考真题)N 是阿伏加德罗常数的值。下列说法正确的是
A
A.3.9gNa O 与足量水反应,转移电子个数为0.1N
2 2 A
B.1.2gMg在空气中燃烧生成MgO和Mg N ,转移电子个数为0.1N
3 2 A
C.2.7gAl与足量NaOH溶液反应,生成H 的个数为0.1N
2 A
D.6.0gSiO 与足量NaOH溶液反应,所得溶液中SiO 的个数为0.1N
2 A
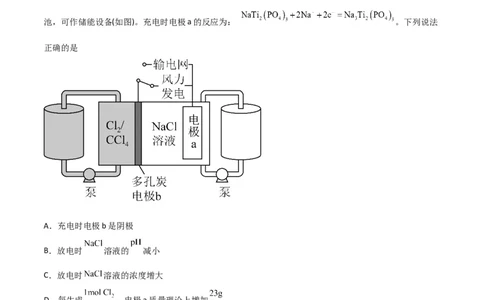
2.(2022·广东·高考真题)科学家基于 易溶于 的性质,发展了一种无需离子交换膜的新型氯流电
池,可作储能设备(如图)。充电时电极a的反应为: 。下列说法
正确的是
A.充电时电极b是阴极
B.放电时 溶液的 减小
C.放电时 溶液的浓度增大
D.每生成 ,电极a质量理论上增加
1.(2022·辽宁·统考高考真题)某储能电池原理如图。下列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】 3
学科网(北京)股份有限公司A.放电时负极反应:
B.放电时 透过多孔活性炭电极向 中迁移
C.放电时每转移 电子,理论上 吸收
D.充电过程中, 溶液浓度增大
2.(2022·福建·统考高考真题)常温常压下,电化学还原制氨气的总反应方程式:
,设 为阿伏加德罗常数的值,下列说法正确的是
A. 水中含有的孤电子对数为
B.每产生 失去的电子数为
C. 氨水中,含有的 分子数少于
D.消耗 (已折算为标况)时,产生的 分子数为
3.(2022·重庆·统考高考真题)工业上用N 和H 合成NH ,N 代表阿伏加德罗常数的值,下列说法正确的
2 2 3 A
是
A.消耗14gN 生成NH 分子数为2 N
2 3 A
B.消耗1molH ,生成N-H键数为2 N
2 A
C.生成标准状况下22.4LNH ,电子转移数为2 N
3 A
D.氧化1molNH 生成NO,需O 分子数为2 N
3 2 A
资料收集整理【淘宝店铺:向阳百分百】 4
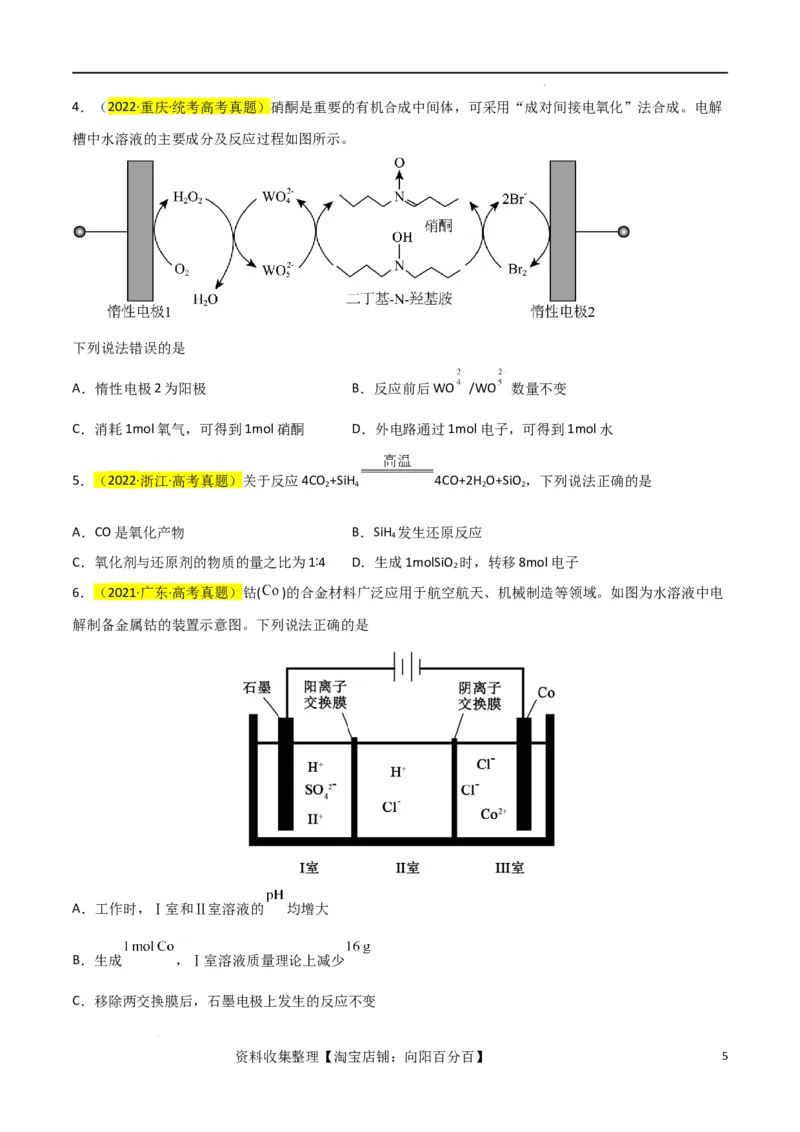
学科网(北京)股份有限公司4.(2022·重庆·统考高考真题)硝酮是重要的有机合成中间体,可采用“成对间接电氧化”法合成。电解
槽中水溶液的主要成分及反应过程如图所示。
下列说法错误的是
A.惰性电极2为阳极 B.反应前后WO /WO 数量不变
C.消耗1mol氧气,可得到1mol硝酮 D.外电路通过1mol电子,可得到1mol水
5.(2022·浙江·高考真题)关于反应4CO +SiH 4CO+2H O+SiO ,下列说法正确的是
2 4 2 2
A.CO是氧化产物 B.SiH 发生还原反应
4
C.氧化剂与还原剂的物质的量之比为1∶4 D.生成1molSiO 时,转移8mol电子
2
6.(2021·广东·高考真题)钴( )的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电
解制备金属钴的装置示意图。下列说法正确的是
A.工作时,Ⅰ室和Ⅱ室溶液的 均增大
B.生成 ,Ⅰ室溶液质量理论上减少
C.移除两交换膜后,石墨电极上发生的反应不变
资料收集整理【淘宝店铺:向阳百分百】 5
学科网(北京)股份有限公司D.电解总反应:
7.(2021·湖南·高考真题) 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反
应为 。下列说法错误的是
A.产生22.4L(标准状况) 时,反应中转移
B.反应中氧化剂和还原剂的物质的量之比为11:6
C.可用石灰乳吸收反应产生的 制备漂白粉
D.可用酸化的淀粉碘化钾溶液检验食盐中 的存在
8.(2021·浙江·高考真题)关于反应8NH +6NO =7N +12H O,下列说法正确的是
3 2 2 2
A.NH 中H元素被氧化
3
B.NO 在反应过程中失去电子
2
C.还原剂与氧化剂的物质的量之比为3:4
D.氧化产物与还原产物的质量之比为4:3
9.(2020·浙江·高考真题)反应 中,氧化产物与还原产物的物
质的量之比是
A.1:2 B.1:1 C.2:1 D.4:1
10.(2021·天津·高考真题)如下所示电解装置中,通电后石墨电极Ⅱ上有O 生成,Fe O 逐渐溶解,下列
2 2 3
判断错误的是
A.a是电源的负极
B.通电一段时间后,向石墨电极Ⅱ附近滴加石蕊溶液,出现红色
C.随着电解的进行,CuCl 溶液浓度变大
2
资料收集整理【淘宝店铺:向阳百分百】 6
学科网(北京)股份有限公司D.当 完全溶解时,至少产生气体336mL (折合成标准状况下)
1.(2022·北京·高考真题)某 多孔材料孔径大小和形状恰好将 “固定”,能高选择性吸附
。废气中的 被吸附后,经处理能全部转化为 。原理示意图如下。
已知:
下列说法不正确的是
A.温度升高时不利于 吸附
B.多孔材料“固定” ,促进 平衡正向移动
C.转化为 的反应是
D.每获得 时,转移电子的数目为
2.(2022·浙江·统考高考真题)关于反应4CO +SiH 4CO+2H O+SiO ,下列说法正确的是
2 4 2 2
A.CO是氧化产物 B.SiH 发生还原反应
4
C.氧化剂与还原剂的物质的量之比为1∶4 D.生成1molSiO 时,转移8mol电子
2
3.(2022·浙江·统考高考真题)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
资料收集整理【淘宝店铺:向阳百分百】 7
学科网(北京)股份有限公司C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
4.(2022·浙江·统考高考真题)关于反应 ,下列说法正确的是
A. 发生还原反应
B. 既是氧化剂又是还原剂
C.氧化产物与还原产物的物质的量之比为2∶1
D. 发生反应,转移 电子
5.(2022·海南·统考高考真题)在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。N 代表阿伏加德罗常数
A
的值,下列说法正确的是
A.反应转移电子为0.1mol B.HCl溶液中 数为3N
A
C. 含有的中子数为1.3N D.反应生成标准状况下气体3.36L
A
6.(2022·湖北·统考高考真题)含磷有机物应用广泛。电解法可实现由白磷直接制备 ,过程
如图所示( 为甲基)。下列说法正确的是
A.生成 ,理论上外电路需要转移 电子
B.阴极上的电极反应为:
C.在电解过程中 向铂电极移动
资料收集整理【淘宝店铺:向阳百分百】 8
学科网(北京)股份有限公司D.电解产生的 中的氢元素来自于
7.(2022·广东·高考真题)我国科学家进行了如图所示的碳循环研究。下列说法正确的是
A.淀粉是多糖,在一定条件下能水解成葡萄糖
B.葡萄糖与果糖互为同分异构体,都属于烃类
C. 中含有 个电子
D. 被还原生成
8.(2021·浙江·高考真题)关于反应K H IO +9HI=2KI+4I +6H O,下列说法正确的是
2 3 6 2 2
A. K H IO 发生氧化反应 B.KI是还原产物
2 3 6
C.生成12.7g I 时,转移0.1mol电子 D.还原剂与氧化剂的物质的量之比为7:1
2
9.(2021·湖北·高考真题)Na Cr O 的酸性水溶液随着H+浓度的增大会转化为CrO 。电解法制备CrO 的原
2 2 7 3 3
理如图所示。下列说法错误的是
A.电解时只允许H+通过离子交换膜
B.生成O 和H 的质量比为8∶1
2 2
C.电解一段时间后阴极区溶液OH-的浓度增大
D.CrO 的生成反应为:Cr O +2H+=2CrO +H O
3 2 3 2
10.(2021·北京·高考真题)用电石(主要成分为CaC ,含CaS和Ca P 等)制取乙炔时,常用CuSO 溶液
2 3 2 4
资料收集整理【淘宝店铺:向阳百分百】 9
学科网(北京)股份有限公司除去乙炔中的杂质。反应为:
①CuSO +H S=CuS↓+H SO
4 2 2 4
②11PH +24CuSO +12H O=3H PO +24H SO +8Cu P↓
3 4 2 3 4 2 4 3
下列分析不正确的是
A.CaS、Ca P 发生水解反应的化学方程式:CaS+2H O=Ca(OH) +H S↑、Ca P +6H O=3Ca(OH) +2PH ↑
3 2 2 2 2 3 2 2 2 3
B.不能依据反应①比较硫酸与氢硫酸的酸性强弱
C.反应②中每24 mol CuSO 氧化11 mol PH
4 3
D.用酸性KMnO 溶液验证乙炔还原性时,H S、PH 有干扰
4 2 3
资料收集整理【淘宝店铺:向阳百分百】 10
学科网(北京)股份有限公司