文档内容
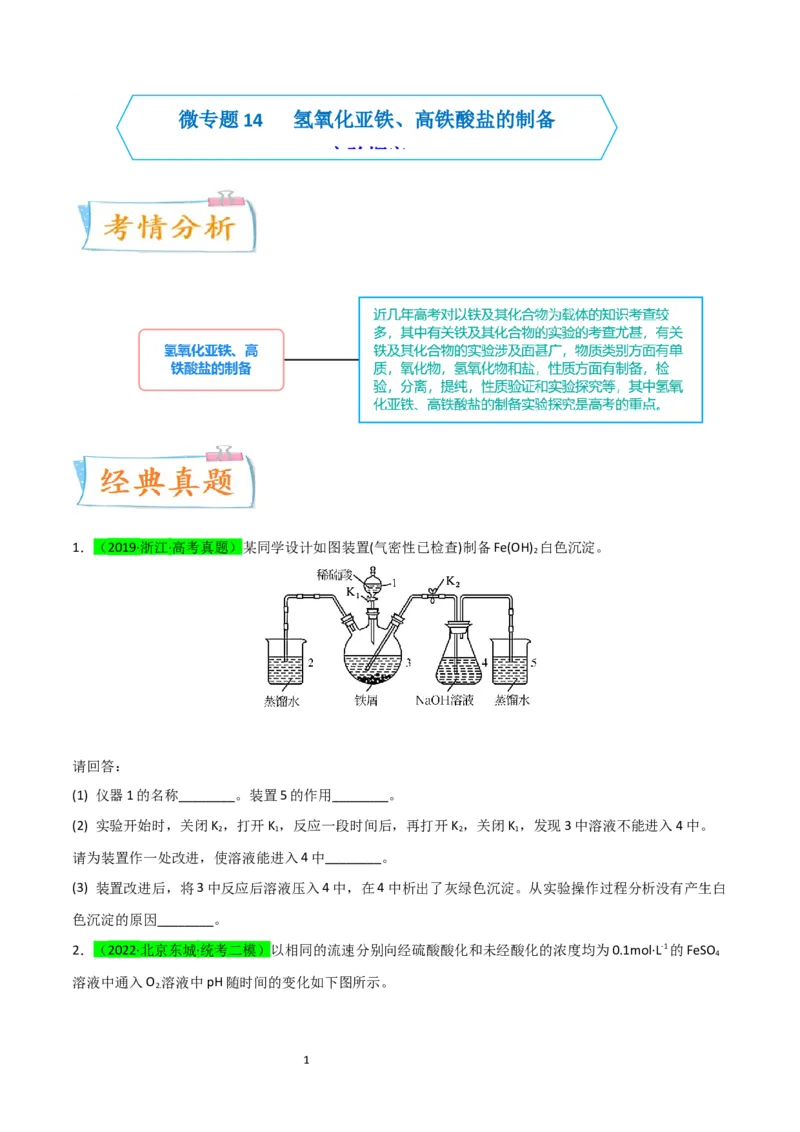
微专题14 氢氧化亚铁、高铁酸盐的制备
实验探究
1.(2019·浙江·高考真题)某同学设计如图装置(气密性已检查)制备Fe(OH) 白色沉淀。
2
请回答:
(1) 仪器1的名称________。装置5的作用________。
(2) 实验开始时,关闭K ,打开K ,反应一段时间后,再打开K ,关闭K ,发现3中溶液不能进入4中。
2 1 2 1
请为装置作一处改进,使溶液能进入4中________。
(3) 装置改进后,将3中反应后溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白
色沉淀的原因________。
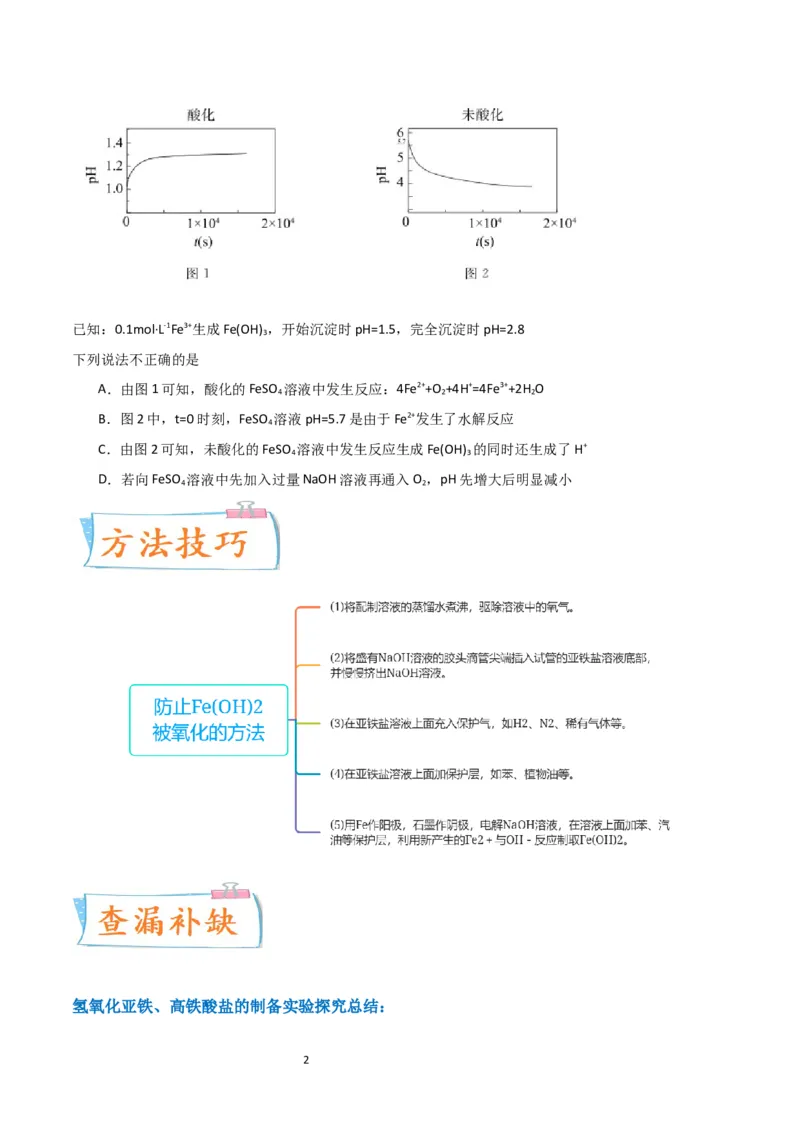
2.(2022·北京东城·统考二模)以相同的流速分别向经硫酸酸化和未经酸化的浓度均为0.1mol·L-1的FeSO
4
溶液中通入O 溶液中pH随时间的变化如下图所示。
2.
1已知:0.1mol·L-1Fe3+生成Fe(OH) ,开始沉淀时pH=1.5,完全沉淀时pH=2.8
3
下列说法不正确的是
A.由图1可知,酸化的FeSO 溶液中发生反应:4Fe2++O +4H+=4Fe3++2H O
4 2 2
B.图2中,t=0时刻,FeSO 溶液pH=5.7是由于Fe2+发生了水解反应
4
C.由图2可知,未酸化的FeSO 溶液中发生反应生成Fe(OH) 的同时还生成了H+
4 3
D.若向FeSO 溶液中先加入过量NaOH溶液再通入O ,pH先增大后明显减小
4 2
氢氧化亚铁、高铁酸盐的制备实验探究总结:
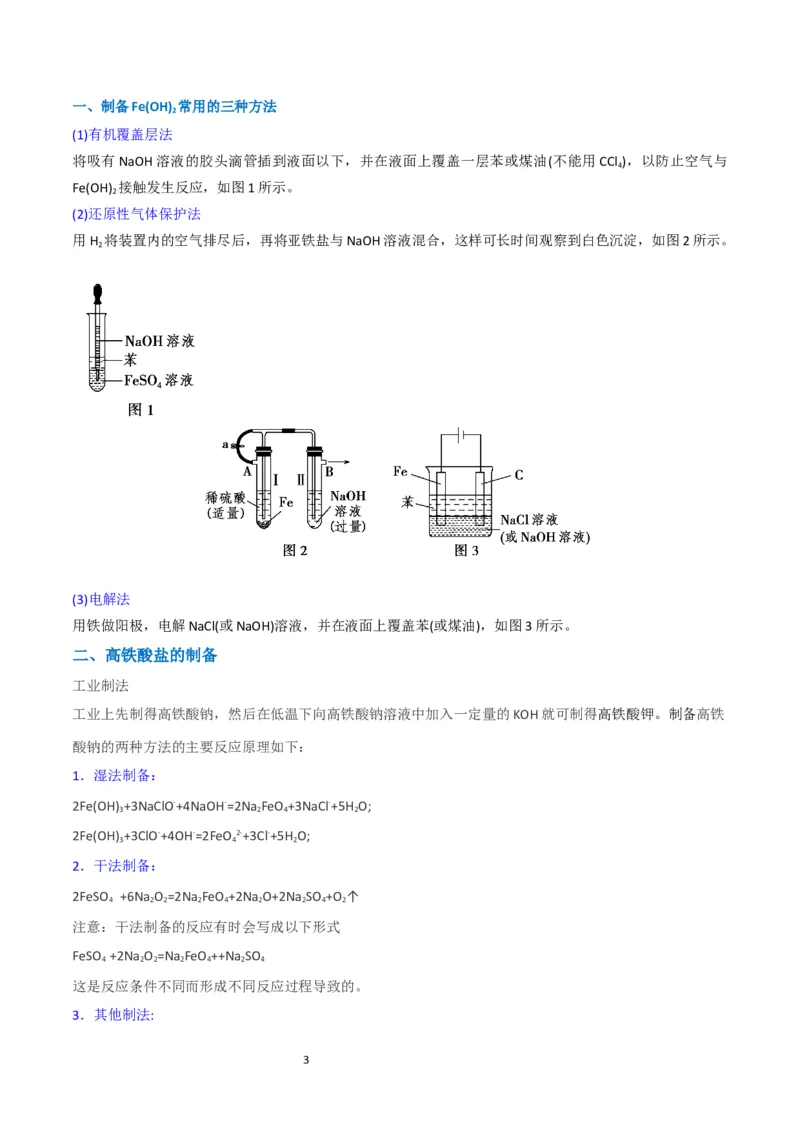
2一、制备Fe(OH) 常用的三种方法
2
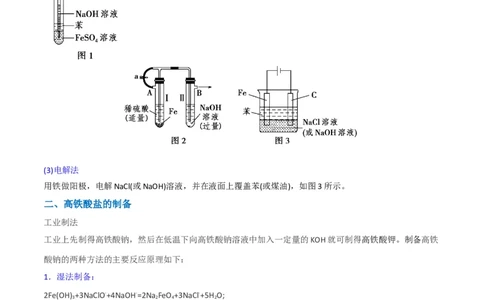
(1)有机覆盖层法
将吸有NaOH溶液的胶头滴管插到液面以下,并在液面上覆盖一层苯或煤油(不能用CCl ),以防止空气与
4
Fe(OH) 接触发生反应,如图1所示。
2
(2)还原性气体保护法
用H 将装置内的空气排尽后,再将亚铁盐与NaOH溶液混合,这样可长时间观察到白色沉淀,如图2所示。
2
(3)电解法
用铁做阳极,电解NaCl(或NaOH)溶液,并在液面上覆盖苯(或煤油),如图3所示。
二、高铁酸盐的制备
工业制法
工业上先制得高铁酸钠,然后在低温下向高铁酸钠溶液中加入一定量的KOH就可制得高铁酸钾。制备高铁
酸钠的两种方法的主要反应原理如下:
1.湿法制备:
2Fe(OH) +3NaClO-+4NaOH-=2Na FeO +3NaCl-+5H O;
3 2 4 2
2Fe(OH) +3ClO-+4OH-=2FeO 2-+3Cl-+5H O;
3 4 2
2.干法制备:
2FeSO +6Na O =2Na FeO +2Na O+2Na SO +O ↑
4 2 2 2 4 2 2 4 2
注意:干法制备的反应有时会写成以下形式
FeSO +2Na O =Na FeO ++Na SO
4 2 2 2 4 2 4
这是反应条件不同而形成不同反应过程导致的。
3.其他制法:
3Fe O +3Na O =2Na FeO +Na O
2 3 2 2 2 4 2
2Fe(NO ) + 16NaOH + 3Cl = 2Na FeO + 6NaCl + 6NaNO + 8H O
3 3 2 2 4 3 2
10NaOH+3Cl +2Fe(OH) ═2Na FeO +6NaCl+8H O;
2 3 2 4 2
电解时阳极发生氧化反应,电极反应方程式为Fe+8OH--6e-═FeO 2-+4H O;
4 2
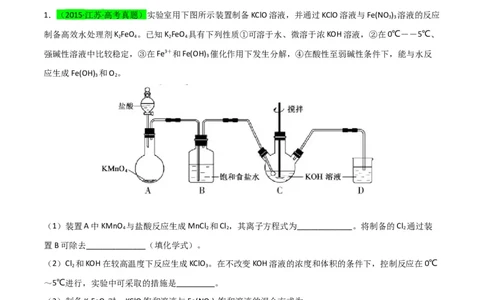
1.(2015·江苏·高考真题)实验室用下图所示装置制备KClO溶液,并通过KClO溶液与Fe(NO ) 溶液的反应
3 3
制备高效水处理剂K FeO 。已知K FeO 具有下列性质①可溶于水、微溶于浓KOH溶液,②在0℃--5℃、
2 4 2 4
强碱性溶液中比较稳定,③在Fe3+和Fe(OH) 催化作用下发生分解,④在酸性至弱碱性条件下,能与水反
3
应生成Fe(OH) 和O 。
3 2
(1)装置A中KMnO 与盐酸反应生成MnCl 和Cl ,其离子方程式为_____________。将制备的Cl 通过装
4 2 2 2
置B可除去______________(填化学式)。
(2)Cl 和KOH在较高温度下反应生成KClO 。在不改变KOH溶液的浓度和体积的条件下,控制反应在0℃
2 3
~5℃进行,实验中可采取的措施是_________。
(3)制备K FeO 时,KClO饱和溶液与Fe(NO ) 饱和溶液的混合方式为_______。
2 4 3 3
(4)提纯K FeO 粗产品[含有Fe(OH) 、KCl等杂质]的实验方案为:将一定量的K FeO 粗产品溶于冷的
2 4 3 2 4
3mol·L-1KOH溶液中,_____(实验中须使用的试剂有:饱和KOH溶液,乙醇;除常用仪器外须使用的仪器
有:砂芯漏斗,真空干燥箱)。
2.(2023·湖北黄冈·黄冈中学校考二模)下列实验中,不能达到实验目的的是
提纯 (含少量HCl、 ) 探究浓度对化学反应速率的影响 制备 除 中的
4A B C D
A.A B.B C.C D.D
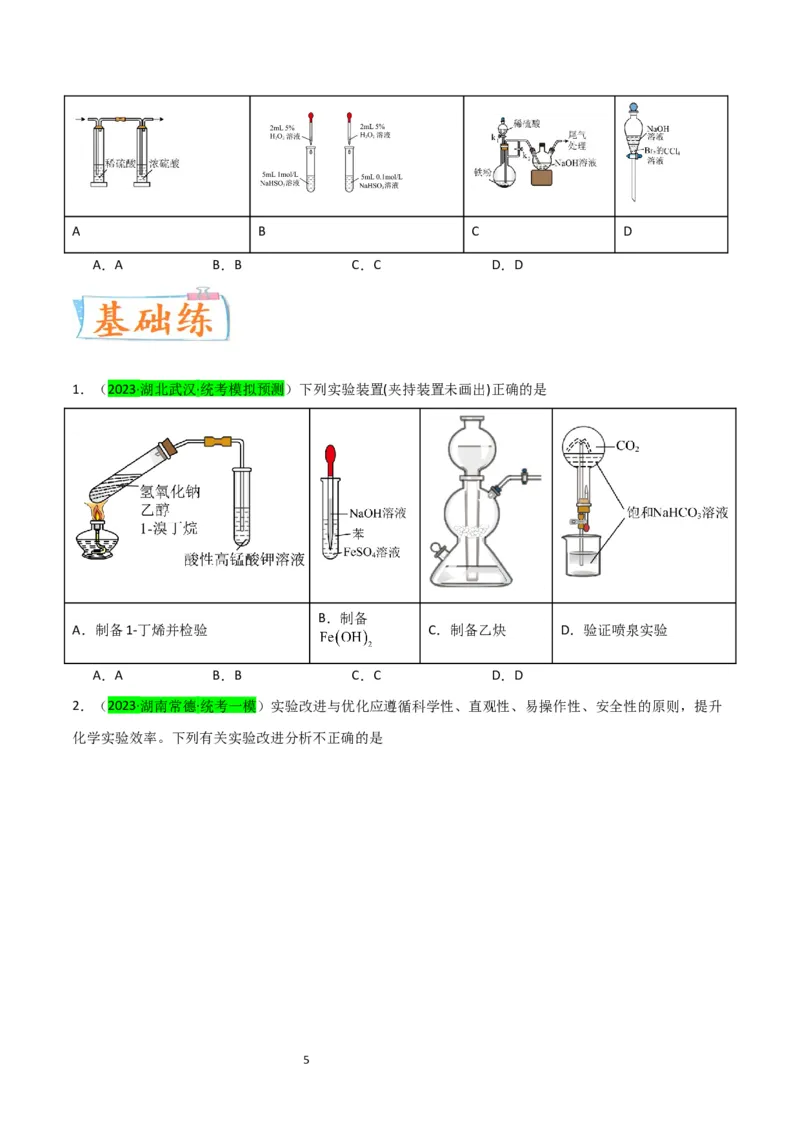
1.(2023·湖北武汉·统考模拟预测)下列实验装置(夹持装置未画出)正确的是
B.制备
A.制备1-丁烯并检验 C.制备乙炔 D.验证喷泉实验
A.A B.B C.C D.D
2.(2023·湖南常德·统考一模)实验改进与优化应遵循科学性、直观性、易操作性、安全性的原则,提升
化学实验效率。下列有关实验改进分析不正确的是
5A.使用恒压滴液漏斗可防止浓氨水污染环境,并使漏斗内液体顺利流下
B.用点燃的木条靠近肥皂泡,听到爆鸣声,可检验产物中有氢气产生
C.该改进装置可用于 性质的探究实验
D.利用此装置可较长时间看到白色絮状沉淀
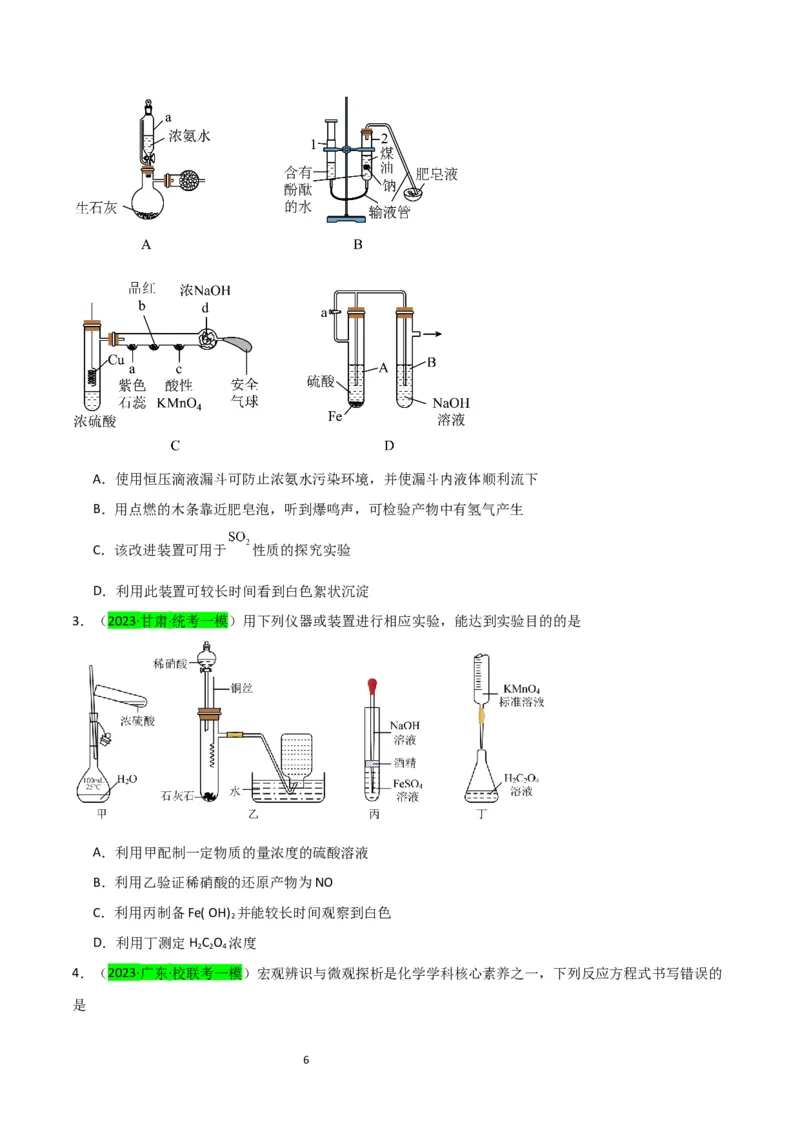
3.(2023·甘肃·统考一模)用下列仪器或装置进行相应实验,能达到实验目的的是
A.利用甲配制一定物质的量浓度的硫酸溶液
B.利用乙验证稀硝酸的还原产物为NO
C.利用丙制备Fe( OH) 并能较长时间观察到白色
2
D.利用丁测定H C O 浓度
2 2 4
4.(2023·广东·校联考一模)宏观辨识与微观探析是化学学科核心素养之一,下列反应方程式书写错误的
是
6A.醋酸除水垢(CaCO ):CaCO +2CH COOH=Ca2++2CH COO-+H O+CO ↑
3 3 3 3 2 2
B.向FeI 溶液中通入少量氯气:2I-+Cl =2Cl-+I
2 2 2
C.硫氰化钾检验溶液中是否存在Fe3+:Fe3++3SCN- =Fe(SCN)
3
D.制备氢氧化亚铁时,白色沉淀会快速变为灰绿色最后变为↓ 红褐色的原因:
4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 3
5.(2023·浙江宁波·镇海中学校考模拟预测)物质的性质决定用途,下列两者对应关系不正确的是
A. 具有强氧化性,可用作消毒剂
B. 固体具有氧化性,可作为黑火药的原料之一
C.SiC中存在共价键,硬度大,可做砂纸和砂轮等磨料
D. 溶液呈蓝色,胆矾可以与石灰乳混合制备波尔多液
6.(2023·山东潍坊·校联考模拟预测)化学与生产、生活、科技密切相关。下列说法错误的是
A.硅胶、生石灰、P O 均可用作食品干燥剂
2 5
B.高铁酸钾可用于水的净化与消毒
C.飞船返回舱表层材料中的玻璃纤维属于无机非金属材料
D.二氧化碳合成淀粉可推进“碳达峰”和“碳中和”
7.(2023·福建·校联考一模)高效净水剂高铁酸钾 的制备流程如图所示,下列离子方程式正确的
是
A.工业制备氯气:
B.反应Ⅱ:
C.反应Ⅲ:
D. 净水原理: (胶体)
78.(2022·黑龙江哈尔滨)高铁酸钾 是一种既能杀菌消毒、又能净水的处理剂。工业制备高铁酸
钾的反应离子方程式为 (未配平),下列有关说法不正确的是
A.高铁酸钾中铁显 价
B.由上述反应可知, 的氧化性强于
C.上述反应中氧化剂和还原剂的物质的量之比为3∶2
D. 处理水时,不仅能消毒杀菌,而且生成的 在一定条件下可形成 胶体能吸附水
中的悬浮杂质
1.(2023·北京顺义·一模)下列方程式与所给事实不相符的是
A.用碳酸钠溶液处理锅炉水垢:
B. 通入水中制氯水:
C.氢氧化亚铁暴露于空气中变色:
D.常温下 氨水的pH约为11:
2.(2023·全国·模拟预测)下列实验装置及试剂的使用正确且能达到实验目的的是
A.实验I :制备
8B.实验II :制备 并观察其颜色
C.实验III:实验室模拟侯氏制碱法实验
D.实验IV:用裂化汽油提纯溴水中的
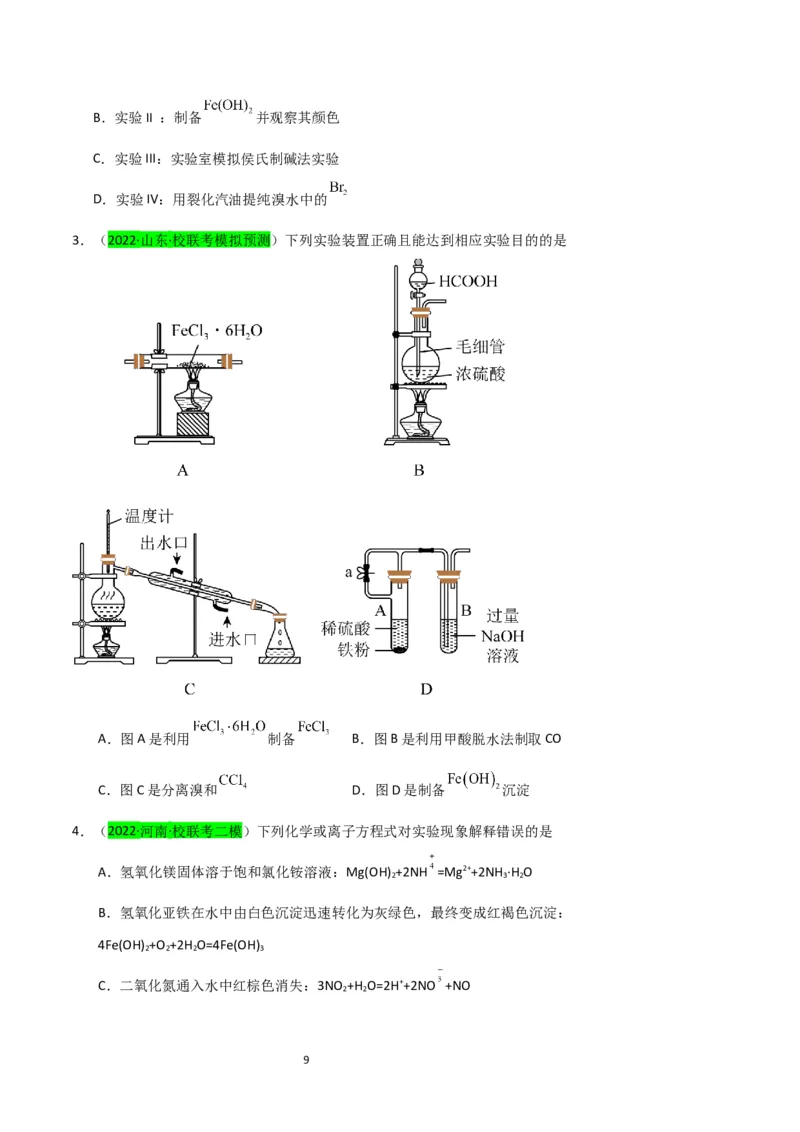
3.(2022·山东·校联考模拟预测)下列实验装置正确且能达到相应实验目的的是
A.图A是利用 制备 B.图B是利用甲酸脱水法制取CO
C.图C是分离溴和 D.图D是制备 沉淀
4.(2022·河南·校联考二模)下列化学或离子方程式对实验现象解释错误的是
A.氢氧化镁固体溶于饱和氯化铵溶液:Mg(OH) +2NH =Mg2++2NH ·H O
2 3 2
B.氢氧化亚铁在水中由白色沉淀迅速转化为灰绿色,最终变成红褐色沉淀:
4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 3
C.二氧化氮通入水中红棕色消失:3NO +H O=2H++2NO +NO
2 2
9D.电解硫酸铜溶液阳极出现无色气泡:CuSO +H O Cu+O ↑+H SO
4 2 2 2 4
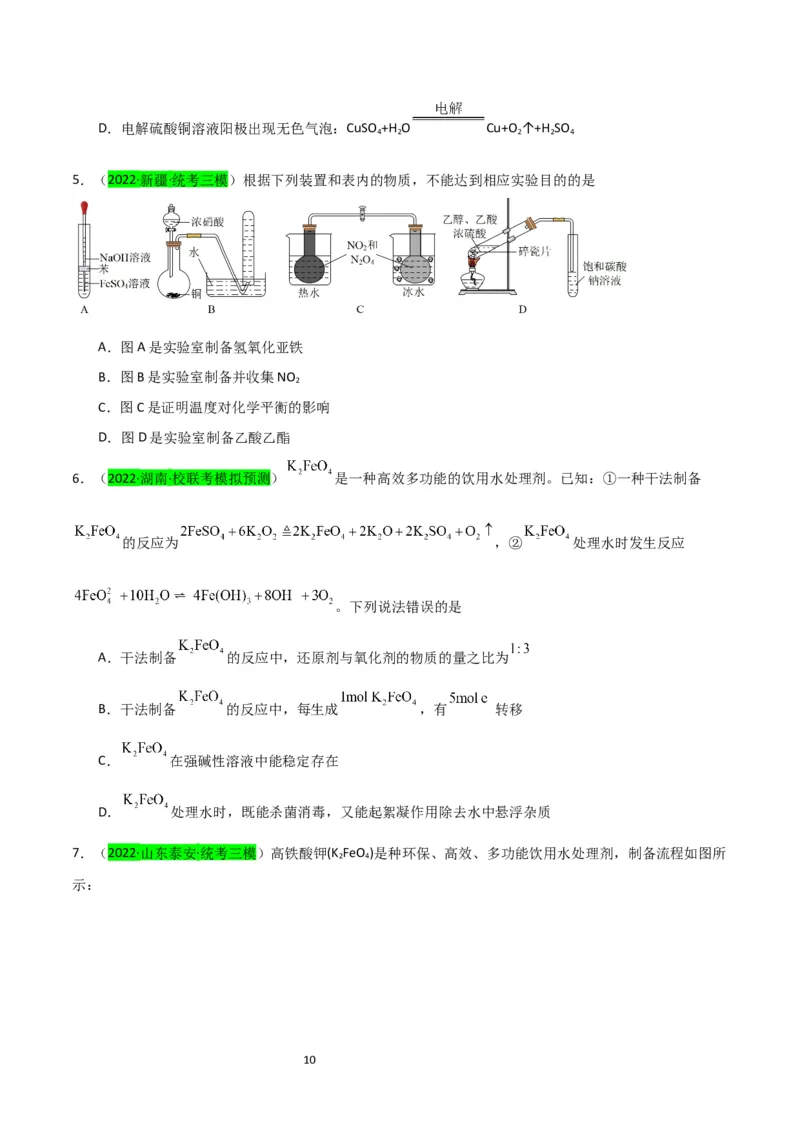
5.(2022·新疆·统考三模)根据下列装置和表内的物质,不能达到相应实验目的的是
A.图A是实验室制备氢氧化亚铁
B.图B是实验室制备并收集NO
2
C.图C是证明温度对化学平衡的影响
D.图D是实验室制备乙酸乙酯
6.(2022·湖南·校联考模拟预测) 是一种高效多功能的饮用水处理剂。已知:①一种干法制备
的反应为 ,② 处理水时发生反应
。下列说法错误的是
A.干法制备 的反应中,还原剂与氧化剂的物质的量之比为
B.干法制备 的反应中,每生成 ,有 转移
C. 在强碱性溶液中能稳定存在
D. 处理水时,既能杀菌消毒,又能起絮凝作用除去水中悬浮杂质
7.(2022·山东泰安·统考三模)高铁酸钾(K FeO )是种环保、高效、多功能饮用水处理剂,制备流程如图所
2 4
示:
10下列叙述错误的是
A.若通过电解法以铁为原料制高铁酸钾,铁棒应做阳极
B.“尾气”可用碱溶液吸收也可用FeCl 等具有还原性的物质溶液吸收
2
C.反应Ⅱ中生成1molNa FeO 时转移的电子数为3N
2 4 A
D.最后一步能制取K FeO 的原因是相同温度下K FeO 的溶解度大于Na FeO
2 4 2 4 2 4
8.(2022·福建漳州·统考二模)高铁酸钾( )具有强氧化性,是一种环保、高效、多功能的饮用水处
理剂,可以用如下流程进行制备。下列说法正确的是
A.“酸溶”前,可用热的 溶液处理铁屑表面的油污
B.“氧化”过程的离子方程式为
C.“制备 ”中氧化剂和还原剂的物质的量之比为2:3
D.“转化”中析出 晶体的原因可能是相同条件下其溶解度大于
9.(2022·北京房山·统考一模)高铁酸钾(K FeO )是一种环保、高效、多功能饮用水处理剂,在水处理过程
2 4
中,高铁酸钾转化为Fe(OH) 胶体,制备高铁酸钾流程如图所示。
3
11下列叙述不正确的是
A.反应I的化学方程式是2Fe+3Cl 2FeCl
2 3
B.用FeCl 溶液吸收反应I中尾气所得产物可再利用
2
C.反应II中氧化剂与还原剂的物质的量之比为2∶3
D.用K FeO 对饮用水杀菌消毒的同时,Fe(OH) 胶体吸附杂质净化水
2 4 3
10.(2022·广东·模拟预测)高铁酸盐是优良的多功能水处理剂。K FeO 为紫色固体,可溶于水,微溶于浓
2 4
KOH溶液,难溶于有机物;在0~5℃、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出O 。某实
2
验小组制备高铁酸钾(K FeO )并测定产品纯度。回答下列问题:
2 4
I.制备K FeO
2 4
装置如图所示,夹持、加热等装置略。
(1)仪器a的名称是 ,装置B中除杂质所用试剂是 ,装置D的作用是 。
(2)A中发生反应的化学方程式为 。
(3)C中反应为放热反应,而反应温度须控制在0~5℃,采用的控温方法为 ,反应中KOH必须过量的
原因是 。
(4)写出C中总反应的离子方程式: 。C中混合物经重结晶、有机物洗涤纯化、真空干燥,得到高铁
酸钾晶体。
II.K FeO 产品纯度的测定
2 4
准确称取1.20g制得的晶体,配成250mL溶液,准确量取25.00mLK FeO 溶液放入锥形瓶,加入足量CrCl
2 4 3
12和NaOH溶液,振荡,再加入稀硫酸酸化后得Fe3+和 ,滴入几滴二苯胺磺酸钠作指示剂,用
0.0500mol/L(NH ) Fe(SO ) 标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗(NH ) Fe(SO ) 标
4 2 4 2 4 2 4 2
准溶液30.00mL。
(5)根据以上数据,样品中K FeO 的质量分数为 。若(NH ) Fe(SO ) 标准溶液部分变质,会使测定结果
2 4 4 2 4 2
(填“偏高”“偏低”或“无影响”)。
13