文档内容
微专题29 非金属及其化合物制备流程与实验探究(Si、N、P、As)
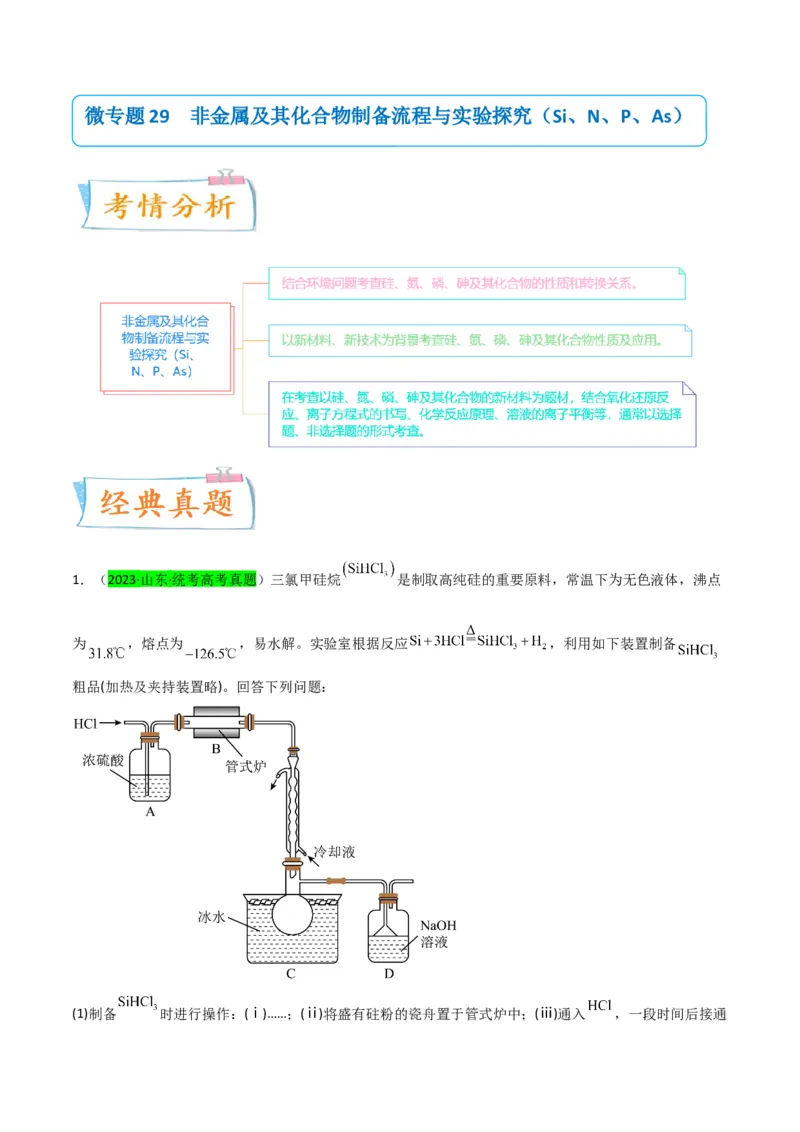
1.(2023·山东·统考高考真题)三氯甲硅烷 是制取高纯硅的重要原料,常温下为无色液体,沸点
为 ,熔点为 ,易水解。实验室根据反应 ,利用如下装置制备
粗品(加热及夹持装置略)。回答下列问题:
(1)制备 时进行操作:(ⅰ)……;(ⅱ)将盛有砫粉的瓷舟置于管式炉中;(ⅲ)通入 ,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为 ;判断制备反应结束的实验现象是 。图示装置存在的两
处缺陷是 。
(2)已知电负性 在浓 溶液中发生反应的化学方程式为 。
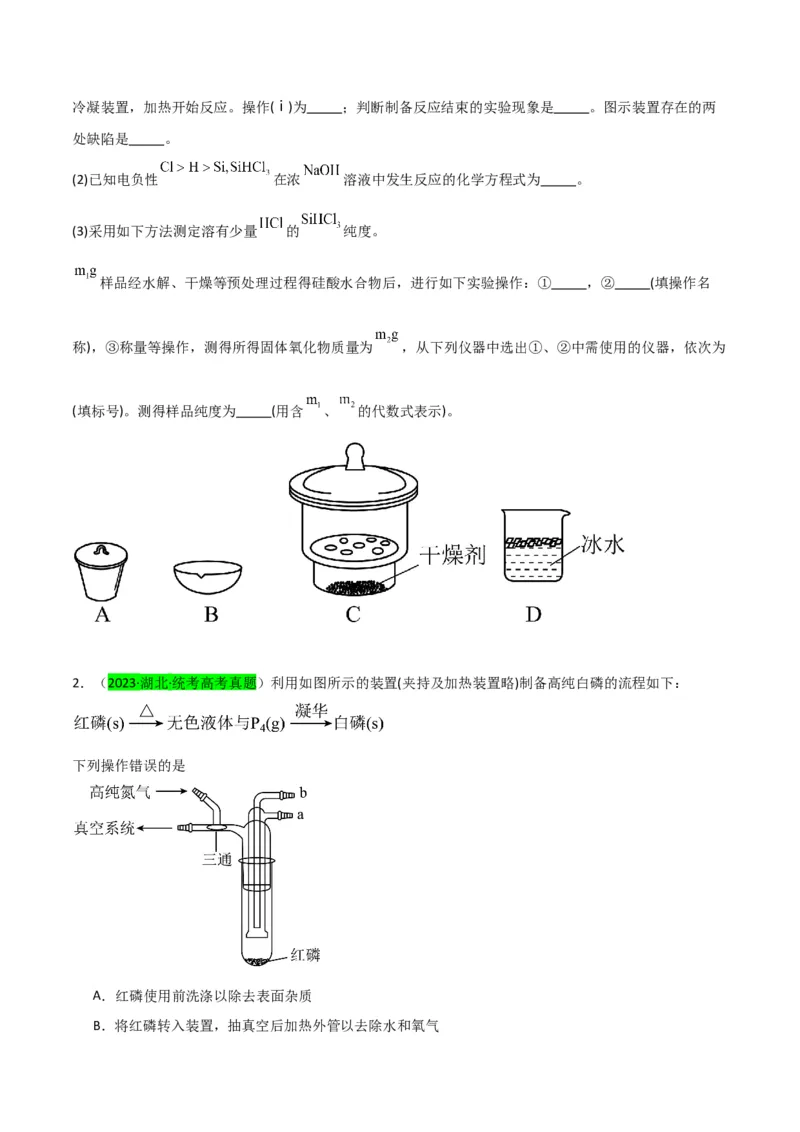
(3)采用如下方法测定溶有少量 的 纯度。
样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:① ,② (填操作名
称),③称量等操作,测得所得固体氧化物质量为 ,从下列仪器中选出①、②中需使用的仪器,依次为
(填标号)。测得样品纯度为 (用含 、 的代数式表示)。
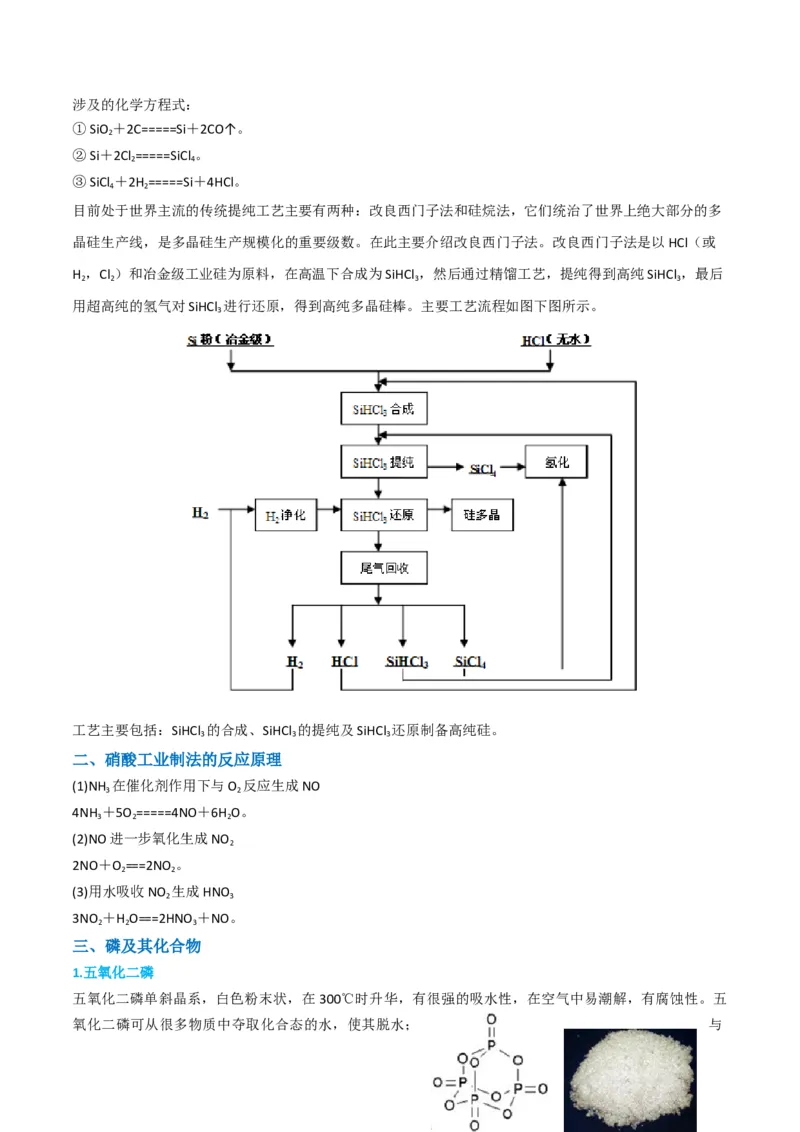
2.(2023·湖北·统考高考真题)利用如图所示的装置(夹持及加热装置略)制备高纯白磷的流程如下:
下列操作错误的是
A.红磷使用前洗涤以除去表面杂质
B.将红磷转入装置,抽真空后加热外管以去除水和氧气C.从a口通入冷凝水,升温使红磷转化
D.冷凝管外壁出现白磷,冷却后在氮气氛围下收集
一、硅及其化合物
1.牢记几种物质的重要用途:
Si——半导体材料、太阳能电池板。
SiO ——光导纤维。
2
H SiO ——硅胶可用作干燥剂。
2 3
Na SiO (水玻璃)——黏合剂、耐火阻燃材料。
2 3
2.熟记7个主要反应:
①Si+2OH-+H O Si +2H ↑;
2 O2- 2
3
②SiO +2OH- Si +H O;
2 O2- 2
3
③SiO +2C Si+2CO↑;
2
④SiO +4HF SiF ↑+2H O;
2 4 2
⑤Si
O2-
+2CO
2
(足量)+2H
2
O H
2
SiO
3
↓+2HC O-;
3 3
⑥Na CO +SiO Na SiO +CO ↑;
2 3 2 2 3 2
⑦CaCO +SiO CaSiO +CO ↑。
3 2 3 2
二、工业生产单质硅过程中应注意的问题
①用焦炭还原SiO ,产物是CO而不是CO 。
2 2
②粗硅中含碳等杂质,与Cl 反应生成的SiCl 中也含CCl 等杂质,经过分馏提纯SiCl 后,再用H 还原,得
2 4 4 4 2
到高纯度硅。
一、硅的工业制法及提纯
――→――→――→涉及的化学方程式:
①SiO +2C=====Si+2CO↑。
2
②Si+2Cl =====SiCl 。
2 4
③SiCl +2H =====Si+4HCl。
4 2
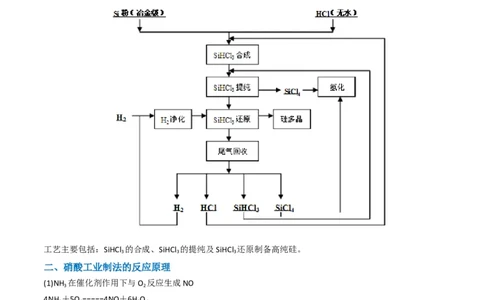
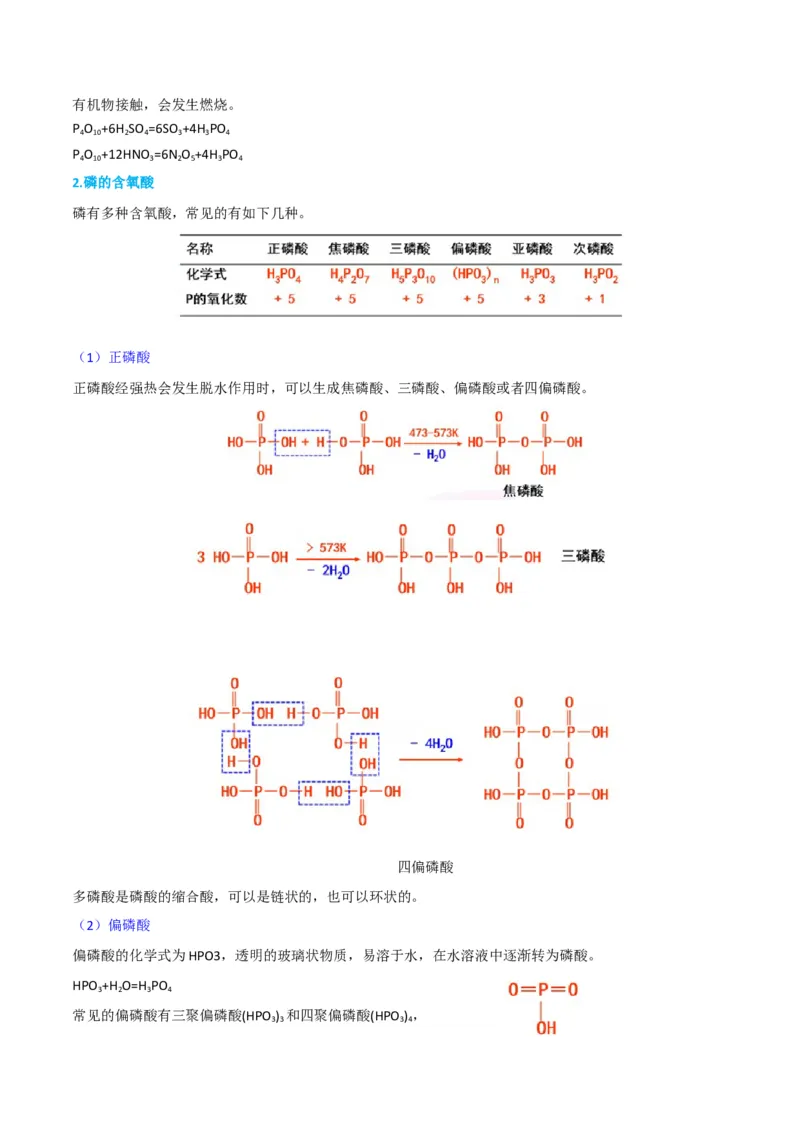
目前处于世界主流的传统提纯工艺主要有两种:改良西门子法和硅烷法,它们统治了世界上绝大部分的多
晶硅生产线,是多晶硅生产规模化的重要级数。在此主要介绍改良西门子法。改良西门子法是以HCl(或
H ,Cl )和冶金级工业硅为原料,在高温下合成为SiHCl ,然后通过精馏工艺,提纯得到高纯SiHCl ,最后
2 2 3 3
用超高纯的氢气对SiHCl 进行还原,得到高纯多晶硅棒。主要工艺流程如图下图所示。
3
工艺主要包括:SiHCl 的合成、SiHCl 的提纯及SiHCl 还原制备高纯硅。
3 3 3
二、硝酸工业制法的反应原理
(1)NH 在催化剂作用下与O 反应生成NO
3 2
4NH +5O =====4NO+6H O。
3 2 2
(2)NO进一步氧化生成NO
2
2NO+O ===2NO 。
2 2
(3)用水吸收NO 生成HNO
2 3
3NO +H O===2HNO +NO。
2 2 3
三、磷及其化合物
1.五氧化二磷
五氧化二磷单斜晶系,白色粉末状,在300℃时升华,有很强的吸水性,在空气中易潮解,有腐蚀性。五
氧化二磷可从很多物质中夺取化合态的水,使其脱水; 与有机物接触,会发生燃烧。
P O +6H SO =6SO +4H PO
4 10 2 4 3 3 4
P O +12HNO =6N O +4H PO
4 10 3 2 5 3 4
2.磷的含氧酸
磷有多种含氧酸,常见的有如下几种。
(1)正磷酸
正磷酸经强热会发生脱水作用时,可以生成焦磷酸、三磷酸、偏磷酸或者四偏磷酸。
四偏磷酸
多磷酸是磷酸的缩合酸,可以是链状的,也可以环状的。
(2)偏磷酸
偏磷酸的化学式为HPO3,透明的玻璃状物质,易溶于水,在水溶液中逐渐转为磷酸。
HPO +H O=H PO
3 2 3 4
常见的偏磷酸有三聚偏磷酸(HPO ) 和四聚偏磷酸(HPO ) ,
3 3 3 4可磷酸高温脱水制得;也可由五氧化二磷与适量冷水制得。
(3)亚磷酸
亚磷酸是无色固体,易溶于水,其浓溶液受强热时会发生歧化反应。
△
4H PO===== 3H PO +PH
3 4 3 4 3
亚磷酸是一个中强二元酸,亚磷酸及其盐在水溶液中都是强还原剂,很容易将Ag+还原为金属银;也能将
热浓硫酸还原为二氧化硫。
(4)次磷酸
在次磷酸钡溶液中加入硫酸,可得到次磷酸。
Ba(H PO ) +H SO =2H PO +BaSO
2 2 2 2 4 3 2 4
次磷酸是一个中强一元酸,分子中的磷原子直接与两个氢原子键合。
H PO H++ ,K=1.0×10-2
3 2 a
次磷酸及其盐都是还原剂。
(5)磷化氢
磷化氢可由金属磷化物与水作用制得;也可由白磷与碱溶液制得。
Ca P +6H O=3Ca(OH) +2PH ↑
3 2 2 2 3
4P+3NaOH+3H O=PH ↑+3NaH PO
2 3 2 2
磷化氢是一种较强的还原剂,能将铜、银、金等金属从其盐中还原出来。
4CuSO +PH +4H O=H PO +2H SO +8Cu
4 3 2 3 4 2 4
6AgNO +PH +3H O=H PO +6HNO +6Ag
3 3 2 3 3 3
四、砷及其化合物
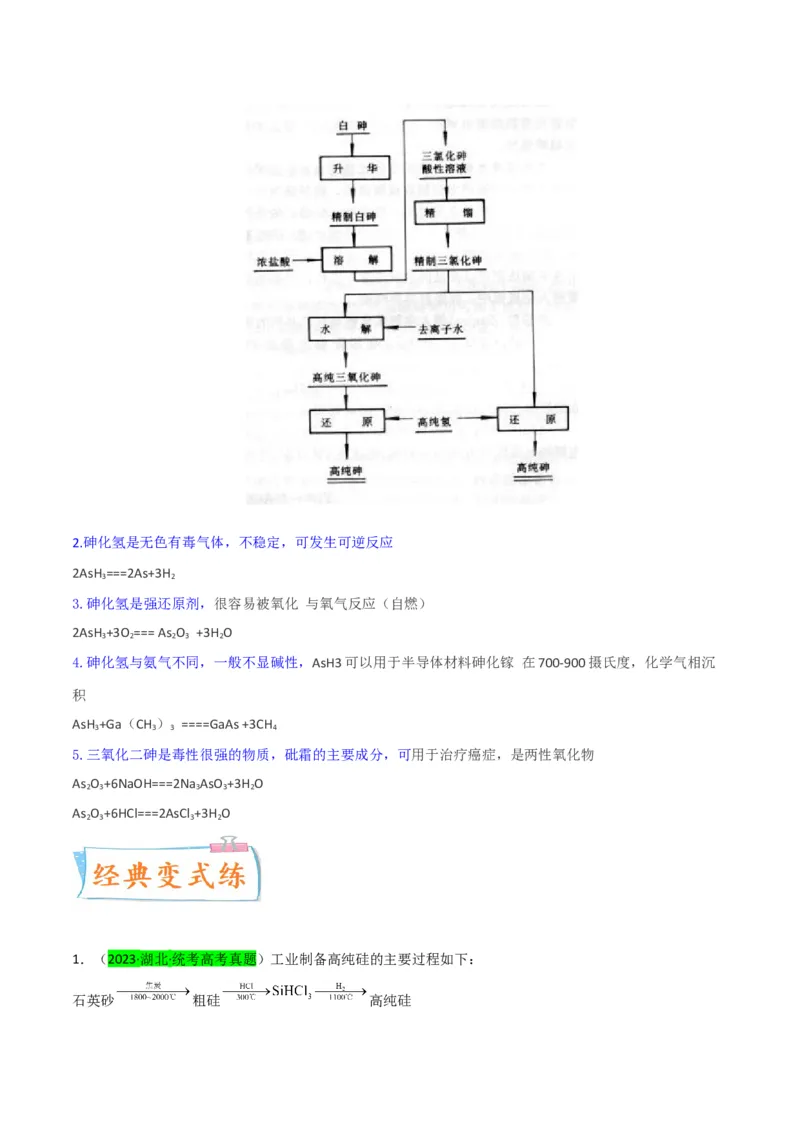
以白砷(三氧化二砷,俗称砒霜)为原料制取高纯砷
1.原料为含三氧化二砷99%以上的粗白砷。生产流程由升华提纯、盐酸溶解、三氯化砷精馏和水解后用高
纯氢还原等过程组成。2.砷化氢是无色有毒气体,不稳定,可发生可逆反应
2AsH ===2As+3H
3 2
3.砷化氢是强还原剂,很容易被氧化 与氧气反应(自燃)
2AsH +3O === As O +3H O
3 2 2 3 2
4.砷化氢与氨气不同,一般不显碱性,AsH3可以用于半导体材料砷化镓 在700-900摄氏度,化学气相沉
积
AsH +Ga(CH ) ====GaAs +3CH
3 3 3 4
5.三氧化二砷是毒性很强的物质,砒霜的主要成分,可用于治疗癌症,是两性氧化物
As O +6NaOH===2Na AsO +3H O
2 3 3 3 2
As O +6HCl===2AsCl +3H O
2 3 3 2
1.(2023·湖北·统考高考真题)工业制备高纯硅的主要过程如下:
石英砂 粗硅 高纯硅下列说法错误的是
A.制备粗硅的反应方程式为
B.1molSi含Si-Si键的数目约为
C.原料气HCl和 应充分去除水和氧气
D.生成 的反应为熵减过程
2.(2022·天津·统考高考真题)燃油汽车行驶中会产生CO、NO等多种污染物。下图为汽车发动机及催化
转化器中发生的部分化学反应。以下判断错误的是
A.甲是空气中体积分数最大的成分 B.乙是引起温室效应的气体之一
C.反应(Ⅰ)在常温下容易发生 D.反应(Ⅱ)中NO是氧化剂
3.(2022·重庆·统考高考真题)工业上用N 和H 合成NH ,N 代表阿伏加德罗常数的值,下列说法正确的
2 2 3 A
是
A.消耗14gN 生成NH 分子数为2 N
2 3 A
B.消耗1molH ,生成N-H键数为2 N
2 A
C.生成标准状况下22.4LNH ,电子转移数为2 N
3 A
D.氧化1molNH 生成NO,需O 分子数为2 N
3 2 A
4.(2023·湖南郴州·统考三模)亚砷酸钠( ),易溶于水,主要用作杀虫剂、防腐剂、分析试剂等。
利用 (分子结构如图)制备亚砷酸钠涉及以下反应: 。下列
说法错误的是
A. 的电子式为B.砷的原子结构示意图为
C. 中所含元素的电负性由大到小的顺序为N>O>H>As
D. 中阳离子的空间结构为正四面体形
1.(2023·全国·统考高考真题)根据实验操作及现象,下列结论中正确的是
选
实验操作及现象 结论
项
常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明显 稀硝酸的氧化性比
A
现象 浓硝酸强
取一定量 样品,溶解后加入 溶液,产生白色沉淀。加入浓
B 此样品中含有
,仍有沉淀
将银和 溶液与铜和 溶液组成原电池。连通后银表面有银白色金 的金属性比
C
属沉积,铜电极附近溶液逐渐变蓝 强
溴与苯发生了加成
D 向溴水中加入苯,振荡后静置,水层颜色变浅
反应
A.A B.B C.C D.D
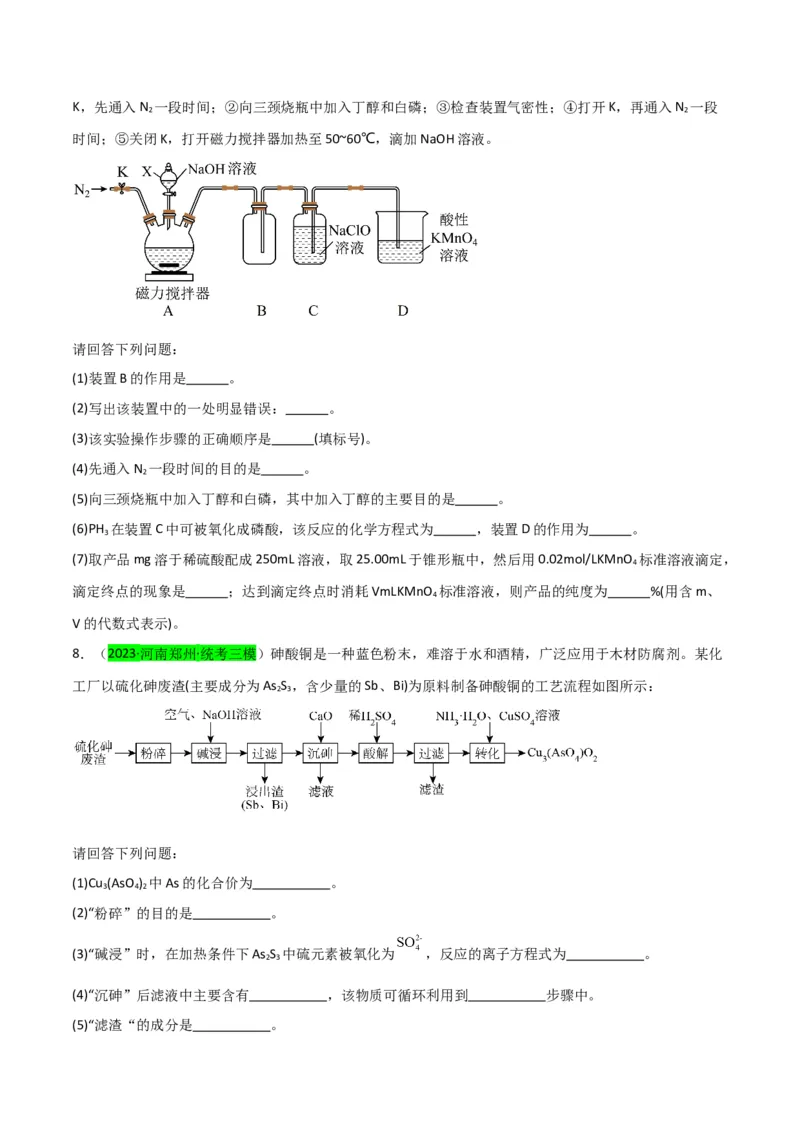
2.(2023·浙江·统考高考真题)下列说法正确的是
A.图①装置可用于制取并收集氨气
B.图②操作可排出盛有 溶液滴定管尖嘴内的气泡C.图③操作俯视刻度线定容会导致所配溶液浓度偏大
D.图④装置盐桥中阳离子向 溶液中迁移
3.(2023·山东·统考高考真题)实验室中使用盐酸、硫酸和硝酸时,对应关系错误的是
A.稀盐酸:配制 溶液
B.稀硫酸:蔗糖和淀粉的水解
C.稀硝酸:清洗附有银镜的试管
D.浓硫酸和浓硝酸的混合溶液:苯的磺化
4.(2023春·河北沧州·高三泊头市第一中学校联考阶段练习)铁盐法是处理含砷废水的主要方法,已知
比 毒性大且不易沉降,砷(V)酸铁、砷(V)酸钙的溶解度很小。以下是硫酸厂酸性含砷(Ⅲ)废水
的处理步骤:
(1)向含砷废水中加入消石灰,调节废水的pH至5~6,过滤后再加入一定量绿矾,得到混合溶液;
(2)向上述混合溶液中加入高浓度双氧水作为氧化剂,搅拌,至溶液由无色透明液变为黄褐色浑浊液;
(3)待步骤(2)完成后,加入碱调节反应后的混合溶液pH至7~9,出现大量褐色沉淀,搅拌充分反应后,静
置、过滤、回收滤渣,检测滤液中砷含量,达标外排。
下列说法正确的是
A.步骤(1)中过滤出的滤渣主要是
B.步骤(2)中双氧水的作用只是将三价砷氧化为五价砷
C.步骤(2)中双氧水可用 代替
D.步骤(3)中,工业上调节反应后的混合溶液pH所用碱最好是
5.(2023·江苏扬州·统考三模)检验微量砷的原理为
。 常温下为无色气体。下列说法正确的是
A.As的基态核外电子排布式为 B. 的空间构型为平面三角形C.固态 属于共价晶体 D. 既含离子键又含共价键
6.(2023春·河北邢台·高三校联考阶段练习)硅的提纯是电子工业一项十分重要的工作,可用粗硅与干燥
的 气体反应制 (其中含有 、 ), 与过量 在 反应制得纯硅。有关
物质的物理常数见下表:
物质
沸点/ 57.7 12.8 33.0
熔点/
回答下列问题:
(1)基态 原子核外电子共有 种运动状态;粗硅与 反应完全后的混合物冷却到标准状况,可通
过 (填写操作名称)提纯得到 。
(2)已知在有 存在的条件下,硅可以和浓硝酸反应生成六氟合硅酸 ,该反应的化学方程式为
。
(3)实验室可以采用如图装置(夹持、尾气处理装置及部分加热装置均略去)用 与过量干燥 反应制取
纯硅。
①仪器a的名称为 ,装置B中的试剂为 。
②将装置C水浴加热,该加热方式的优点是 。
③为保证实验安全,加热装置D前必须完成的操作是:ⅰ.检验装置的气密性;ⅱ. ,该装置中发生
反应的化学方程式为 。
7.(2023·全国·高三专题练习)已知:P (白磷)+3NaOH+3H O NaH PO +PH ↑。PH 有强还原性,是无色、
4 2 2 2 3 3
有毒且能自燃的气体。某同学用如图所示装置制取少量NaH PO ,相关操作步骤(不是正确顺序)为①打开
2 2K,先通入N 一段时间;②向三颈烧瓶中加入丁醇和白磷;③检查装置气密性;④打开K,再通入N 一段
2 2
时间;⑤关闭K,打开磁力搅拌器加热至50~60℃,滴加NaOH溶液。
请回答下列问题:
(1)装置B的作用是 。
(2)写出该装置中的一处明显错误: 。
(3)该实验操作步骤的正确顺序是 (填标号)。
(4)先通入N 一段时间的目的是 。
2
(5)向三颈烧瓶中加入丁醇和白磷,其中加入丁醇的主要目的是 。
(6)PH 在装置C中可被氧化成磷酸,该反应的化学方程式为 ,装置D的作用为 。
3
(7)取产品mg溶于稀硫酸配成250mL溶液,取25.00mL于锥形瓶中,然后用0.02mol/LKMnO 标准溶液滴定,
4
滴定终点的现象是 ;达到滴定终点时消耗VmLKMnO 标准溶液,则产品的纯度为 %(用含m、
4
V的代数式表示)。
8.(2023·河南郑州·统考三模)砷酸铜是一种蓝色粉末,难溶于水和酒精,广泛应用于木材防腐剂。某化
工厂以硫化砷废渣(主要成分为As S ,含少量的Sb、Bi)为原料制备砷酸铜的工艺流程如图所示:
2 3
请回答下列问题:
(1)Cu (AsO ) 中As的化合价为 。
3 4 2
(2)“粉碎”的目的是 。
(3)“碱浸”时,在加热条件下As S 中硫元素被氧化为 ,反应的离子方程式为 。
2 3
(4)“沉砷”后滤液中主要含有 ,该物质可循环利用到 步骤中。
(5)“滤渣“的成分是 。(6)“转化”时发生的化学方程式为 。
(7)该化工厂实验员称取100g硫化砷废渣(As S 质量分数为73.8%),粉碎后通空气并加入NaOH溶液,得到
2 3
1L的悬浊液,测得碱浸后的滤液中Na AsO 的浓度为0.45mol·L-1,该实验员检测砷的浸出率为 。
3 4
1.(2023春·上海宝山·高一上海市吴淞中学校考阶段练习)黄砷( )与白磷( )的结构类似(如图所示),
以下叙述正确的是
A.黄砷的熔点高于白磷 B.黄砷中共价键键能大于白磷
C.两者都是共价化合物 D.两者都含有极性共价键
2.(2023春·湖南常德·高三常德市一中校考阶段练习)雌黄(As S ,其结构如下图所示)是提取砷的主要矿
2 3
物原料,As S 和HNO 有如下反应: 下列说法错误
2 3 3
的是
A.AsO 的空间构型为正四面体形
B.As S 中只含有极性键,且为非极性分子
2 3
C.该分子中所有原子均采用sp3杂化
D.生成0.5mol H AsO ,则反应中转移电子的物质的量为5mol
3 4
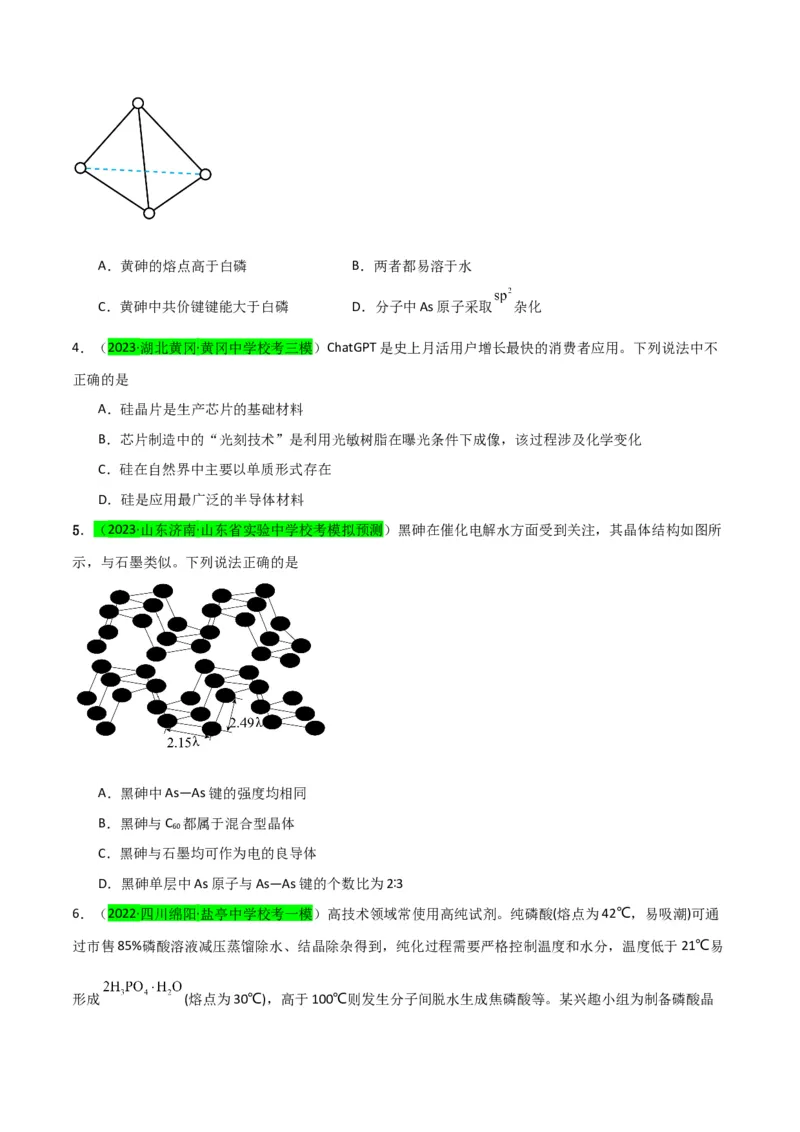
3.(2023春·福建宁德·高二福建省福安市第一中学校联考期中)黄砷 与白磷 的结构类似(如图所
示),以下叙述正确的是A.黄砷的熔点高于白磷 B.两者都易溶于水
C.黄砷中共价键键能大于白磷 D.分子中As原子采取 杂化
4.(2023·湖北黄冈·黄冈中学校考三模)ChatGPT是史上月活用户增长最快的消费者应用。下列说法中不
正确的是
A.硅晶片是生产芯片的基础材料
B.芯片制造中的“光刻技术”是利用光敏树脂在曝光条件下成像,该过程涉及化学变化
C.硅在自然界中主要以单质形式存在
D.硅是应用最广泛的半导体材料
5.(2023·山东济南·山东省实验中学校考模拟预测)黑砷在催化电解水方面受到关注,其晶体结构如图所
示,与石墨类似。下列说法正确的是
A.黑砷中As—As键的强度均相同
B.黑砷与C 都属于混合型晶体
60
C.黑砷与石墨均可作为电的良导体
D.黑砷单层中As原子与As—As键的个数比为2∶3
6.(2022·四川绵阳·盐亭中学校考一模)高技术领域常使用高纯试剂。纯磷酸(熔点为42℃,易吸潮)可通
过市售85%磷酸溶液减压蒸馏除水、结晶除杂得到,纯化过程需要严格控制温度和水分,温度低于21℃易
形成 (熔点为30℃),高于100℃则发生分子间脱水生成焦磷酸等。某兴趣小组为制备磷酸晶体设计的实验装置如下(夹持装置略):
回答下列问题:
(1)空集气瓶的作用 。B的进水口为 (填“a”或“b”)。
(2) 的作用是 。
(3)空气流入毛细管的主要作用是防止 ,还具有搅拌和加速水逸出的作用。
(4)升高温度能提高除水速度,实验选用水浴加热的目的是 。
(5)磷酸易形成过饱和溶液,难以结晶,可向过饱和溶液中加入 促进其结晶。
(6)过滤磷酸晶体时,除了需要干燥的环境外,还需要控制温度为 (填标号)。
A. B. C.
(7)磷酸中少量的水极难除去的原因是 。
7.(2023春·上海宝山·高一上海市吴淞中学校考阶段练习)雄黄(As S )和雌黄(As S )是提取砷的主要矿物
4 4 2 3
原料,二者在自然界中共生。
Ⅰ.雄黄(As S )的制备。
4 4
(1) 和 在盐酸中反应转化为 和 并放出 气体(反应前后硫元素化合价不变)。若
和 恰好完全反应, 和 的物质的量之比为 。
(2)上述反应中的被氧化元素是 ,反应产生的气体可用 吸收,若产生的 气体
(标况下测定),则转移电子数为 。
Ⅱ.雌黄(As S )的性质。
2 3
和 有如下反应:
(3)请用单线桥法标出上述反应的电子转移 。
(4)若生成 ,反应产物 与 (标准状况)混合后用水吸收恰好全部转化成浓 ,需要L(标准状况下)。然后浓 与过量的碳加热进行反应,所产生的 的量 。(填选项)
a.小于 b.等于 c.大于 d.无法确定
(5)已知 为直线型极性分子,该分子中含有 。(填选项)
a.极性共价键 b.非极性共价键 c.离子键 d.金属键