文档内容
【答案】D
(新高考)2021 届高考考前冲刺卷
【解析】A.中子数为8的碳原子的质量数为14,原子符号为 C,故A错误;B.氧离子的核电荷数
化 学(九)
为8,核外电子数为10,离子的结构示意图为 ,故B错误;C.对硝基甲苯中硝基中的氮原子与
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形码粘贴
在答题卡上的指定位置。
苯环上碳原子相连,结构简式为 ,故C错误;D.羟基的结构简式为-OH,电子式为
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,写
在试题卷、草稿纸和答题卡上的非答题区域均无效。
,故D正确;故选D。
3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。写在试题卷、草稿纸和
答题卡上的非答题区域均无效。
3.下列表述正确的是
4.考试结束后,请将本试题卷和答题卡一并上交。
A.键角:HO>NH
2 3
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5
B.用原子轨道描述氯化氢分子中化学键的形成:
一、选择题:每小题2分,共20分。每小题给出的四个选项中,只有一项是符合题目要求的。
C.电负性:N>O>C>H
1.化学与生活紧密相关,下列描述不正确的是
D.冰的密度比水小的性质与氢键无关
A.水泥是由石灰石和黏土为原料烧制而成的
【答案】B
B.佩戴医用口罩预防病毒的原理相当于化学实验中的过滤
【解析】A.HO键角为104.5°,NH 键角为107.3°,A错误;B.氯化氢分子中化学键的形成用原子
2 3
C.火神山医院在建造过程中大量使用HDPE防渗膜,这种塑料是一种新型的无机材料
D.碳纳米管比表面积大,可用作新型储氢材料 轨道描述如图所示 ,B正确;C.电负性应O> N,C错误;D.冰
【答案】C
的密度比水小的性质与氢键有关,冰和水密度不同主要是由于水分子间存在氢键,在水液态时,一个
【解析】A.水泥是由石灰石和黏土为原料烧制而成的,A项正确;B.佩戴口罩预防病毒,目的是允
水分子与四个水分子相连,而水凝固为冰时,氢键会拉伸水分子使水分子之间距离增大,体积也就增
许空气透过,但不允许灰尘、病毒等透过,其原理相当于化学实验中的过滤操作,B项正确;C.HDPE
大了,故冰密度比水小与氢键有关,D错误;故选B。
防渗膜是一种有机高分子材料,C项错误;D.碳纳米管是由碳原子组成的六角形蜂巢状平面薄膜卷
4.有机物与社会生活的各个方面密不可分,下列说法错误的是
曲而成,所以比表面积大,可用作新型储氢材料,D项正确;答案选C。
A.直馏汽油和裂化汽油的主要成分都是烃类
2.下列化学用语表示正确的是
B.乙酸乙酯的碱性水解属于皂化反应
A.中子数为8的碳原子: C C.棉花、蚕丝都属于天然纤维但主要成分不同
D.葡萄糖和果糖均不能发生水解反应
B.O2−的结构示意图: 【答案】B
【解析】A.直馏汽油和裂化汽油的主要成分都是烃类,其中直馏汽油的主要成分是饱和烃,裂化汽
油既含有饱和烃又含有不饱和烃,A正确;B.油脂(高级脂肪酸甘油三酯)的碱性水解又叫皂化反应,
C.对硝基甲苯的结构简式是
其他酯类水解不属于皂化反应,B错误;C.棉花、蚕丝都属于天然纤维,棉花主要成分是纤维素,蚕丝
主要成分是蛋白质,C正确;D.葡萄糖和果糖都是单糖,均不能发生水解反应,D正确;故选答案B。
D.羟基的电子式是
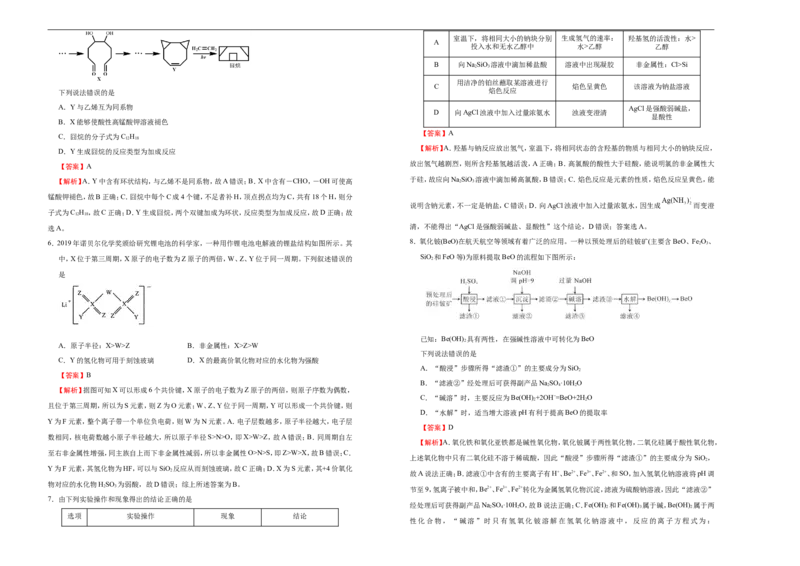
5.中国科学家合成囧烷的路线局部如图:
封密不订装只卷此
号位座
号场考
号证考准
名姓
级班室温下,将相同大小的钠块分别 生成氢气的速率: 羟基氢的活泼性:水>
A
投入水和无水乙醇中 水>乙醇 乙醇
B 向NaSiO 溶液中滴加稀盐酸 溶液中出现凝胶 非金属性:Cl>Si
2 3
用洁净的铂丝蘸取某溶液进行
C 焰色呈黄色 该溶液为钠盐溶液
焰色反应
下列说法错误的是
A.Y与乙烯互为同系物 AgCl是强酸弱碱盐,
D 向AgCl浊液中加入过量浓氨水 浊液变澄清
显酸性
B.X能够使酸性高锰酸钾溶液褪色
【答案】A
C.囧烷的分子式为C H
12 18
【解析】A.羟基与钠反应放出氢气,室温下,将相同状态的含羟基的物质与相同大小的钠块反应,
D.Y生成囧烷的反应类型为加成反应
放出氢气越剧烈,则所含羟基氢越活泼,A正确;B.高氯酸的酸性大于硅酸,能说明氯的非金属性大
【答案】A
【解析】A.Y中含有环状结构,与乙烯不是同系物,故A错误;B.X中含有-CHO,-OH可使高 于硅,故应向Na 2 SiO 3 溶液中滴加稀高氯酸,B错误;C.焰色反应是元素的性质,焰色反应呈黄色,能
锰酸钾褪色,故B正确;C.囧烷中每个C成4个键,不足者补H,顶点拐点均为C,共有18个H,则分
说明含钠元素,不一定是钠盐,C错误;D.向AgCl浊液中加入过量浓氨水,因生成 而变澄
子式为C H ,故C正确;D.Y生成囧烷,两个双键加成为环状,反应类型为加成反应,故D正确;故
12 18
选A。 清,不能得出“AgCl是强酸弱碱盐、显酸性”这个结论,D错误;答案选A。
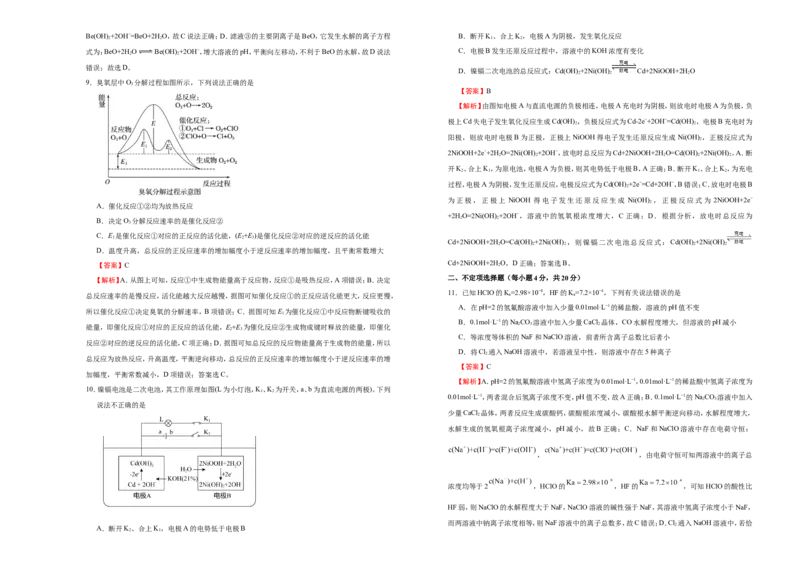
6.2019年诺贝尔化学奖颁给研究锂电池的科学家,一种用作锂电池电解液的锂盐结构如图所示。其 8.氧化铍(BeO)在航天航空等领域有着广泛的应用。一种以预处理后的硅铍矿(主要含BeO、Fe 2 O 3 、
中,X位于第三周期,X原子的电子数为Z原子的两倍,W、Z、Y位于同一周期。下列叙述错误的 SiO 2 和FeO等)为原料提取BeO的流程如下图所示:
是
已知:Be(OH) 具有两性,在强碱性溶液中可转化为BeO
2
A.原子半径:X>W>Z B.非金属性:X>Z>W
下列说法错误的是
C.Y的氢化物可用于刻蚀玻璃 D.X的最高价氧化物对应的水化物为强酸
A.“酸浸”步骤所得“滤渣①”的主要成分为SiO
2
【答案】B
B.“滤液②”经处理后可获得副产品NaSO ·10H O
2 4 2
【解析】据图可知X可以形成6个共价键,X原子的电子数为Z原子的两倍,则原子序数为偶数,
C.“碱溶”时,主要反应为Be(OH) +2OH−=BeO+2H O
2 2
且位于第三周期,所以为S元素,则Z为O元素;W、Z、Y位于同一周期,Y可以形成一个共价键,则
D.“水解”时,适当增大溶液pH有利于提高BeO的提取率
Y为F元素,整个离子带一个单位负电荷,则W为N元素。A.电子层数越多,原子半径越大,电子层
【答案】D
数相同,核电荷数越小原子半径越大,所以原子半径S>N>O,即X>W>Z,故A错误;B.同周期自左
【解析】A.氧化铁和氧化亚铁都是碱性氧化物,氧化铍属于两性氧化物,二氧化硅属于酸性氧化物,
至右非金属性增强,同主族自上而下非金属性减弱,所以非金属性O>N>S,即Z>W>X,故B错误;C.
上述氧化物中只有二氧化硅不溶于稀硫酸,因此“酸浸”步骤所得“滤渣①”的主要成分为 SiO,
2
Y为F元素,其氢化物为HF,可以与SiO 反应从而刻蚀玻璃,故C正确;D.X为S元素,其+4价氧化
2 故A说法正确;B.滤液①中含有的主要离子有H+、Be2+、Fe3+、Fe2+、和SO,加入氢氧化钠溶液将pH调
物对应的水化物HSO 为弱酸,故D错误;综上所述答案为B。
2 3 节至9,氢离子被中和,Be2+、Fe3+、Fe2+转化为金属氢氧化物沉淀,滤液为硫酸钠溶液,因此“滤液②”
7.由下列实验操作和现象得出的结论正确的是
经处理后可获得副产品NaSO ·10H O,故B说法正确;C.Fe(OH) 和Fe(OH) 属于碱,Be(OH) 属于两
2 4 2 2 3 2
选项 实验操作 现象 结论
性化合物,“碱溶”时只有氢氧化铍溶解在氢氧化钠溶液中,反应的离子方程式为:Be(OH) +2OH−=BeO+2H O,故C说法正确;D.滤液③的主要阴离子是BeO,它发生水解的离子方程 B.断开K、合上K,电极A为阴极,发生氧化反应
2 2 1 2
式为:BeO+2H O Be(OH) +2OH−,增大溶液的pH,平衡向左移动,不利于BeO的水解,故D说法 C.电极B发生还原反应过程中,溶液中的KOH浓度有变化
2 2
错误;故选D。
D.镍镉二次电池的总反应式:Cd(OH) +2Ni(OH) Cd+2NiOOH+2H O
2 2 2
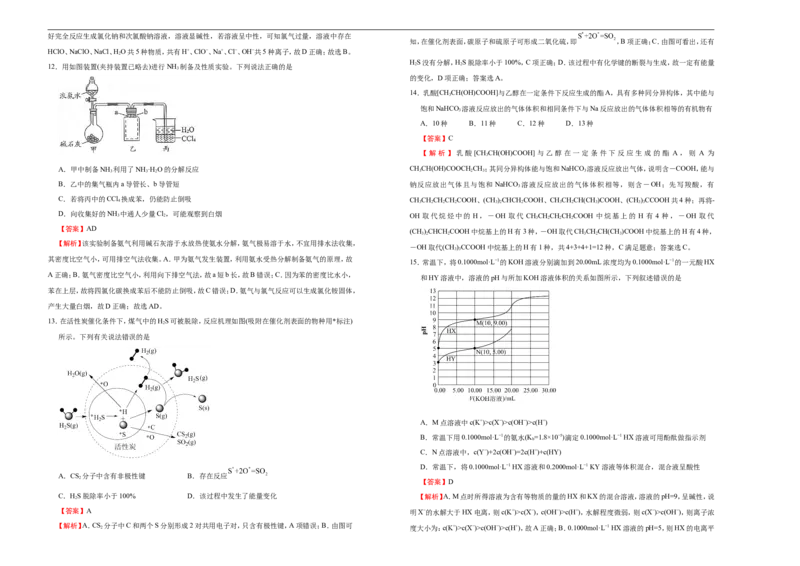
9.臭氧层中O 分解过程如图所示,下列说法正确的是
3
【答案】B
【解析】由图知电极A与直流电源的负极相连,电极A充电时为阴极,则放电时电极A为负极,负
极上Cd失电子发生氧化反应生成Cd(OH) ,负极反应式为Cd-2e−+2OH−=Cd(OH) ,电极B充电时为
2 2
阳极,则放电时电极B为正极,正极上NiOOH得电子发生还原反应生成Ni(OH) ,正极反应式为
2
2NiOOH+2e−+2H O=2Ni(OH) +2OH−,放电时总反应为Cd+2NiOOH+2H O=Cd(OH) +2Ni(OH) 。A.断
2 2 2 2 2
开K、合上K,为原电池,电极A为负极,则其电势低于电极B,A正确;B.断开K、合上K,为充电
2 1 1 2
过程,电极A为阴极,发生还原反应,电极反应式为Cd(OH) +2e−=Cd+2OH−,B错误;C.放电时电极B
2
为正极,正极上 NiOOH 得电子发生还原反应生成 Ni(OH) ,正极反应式为 2NiOOH+2e−
2
A.催化反应①②均为放热反应
+2H O=2Ni(OH) +2OH−,溶液中的氢氧根浓度增大,C正确;D.根据分析,放电时总反应为
2 2
B.决定O 分解反应速率的是催化反应②
3
C.E 是催化反应①对应的正反应的活化能,(E+E)是催化反应②对应的逆反应的活化能
1 2 3
Cd+2NiOOH+2H O=Cd(OH) +2Ni(OH) ,则镍镉二次电池总反应式:Cd(OH) +2Ni(OH)
2 2 2 2 2
D.温度升高,总反应的正反应速率的增加幅度小于逆反应速率的增加幅度,且平衡常数增大
Cd+2NiOOH+2H O,D正确;答案选B。
【答案】C 2
【解析】A.从图上可知,反应①中生成物能量高于反应物,反应①是吸热反应,A项错误;B.决定
二、不定项选择题(每小题4分,共20分)
11.已知HClO的K=2.98×10−8,HF的K=7.2×10−4,下列有关说法错误的是
总反应速率的是慢反应,活化能越大反应越慢,据图可知催化反应①的正反应活化能更大,反应更慢, a a
A.在pH=2的氢氟酸溶液中加入少量0.01mol·L−1的稀盐酸,溶液的pH值不变
所以催化反应①决定臭氧的分解速率,B项错误;C.据图可知E 为催化反应①中反应物断键吸收的
1
B.0.1mol·L−1的NaCO 溶液中加入少量CaCl 晶体,CO水解程度增大,但溶液的pH减小
2 3 2
能量,即催化反应①对应的正反应的活化能,E+E 为催化反应②生成物成键时释放的能量,即催化
2 3
C.等浓度等体积的NaF和NaClO溶液,前者所含离子总数比后者小
反应②对应的逆反应的活化能,C项正确;D.据图可知总反应的反应物能量高于生成物的能量,所以
D.将Cl 通入NaOH溶液中,若溶液呈中性,则溶液中存在5种离子
2
总反应为放热反应,升高温度,平衡逆向移动,总反应的正反应速率的增加幅度小于逆反应速率的增
【答案】C
加幅度,平衡常数减小,D项错误;答案选C。
【解析】A.pH=2的氢氟酸溶液中氢离子浓度为0.01mol·L−1,0.01mol·L−1的稀盐酸中氢离子浓度为
10.镍镉电池是二次电池,其工作原理如图(L为小灯泡,K、K 为开关,a、b为直流电源的两极)。下列
1 2
0.01mol·L−1,两者混合后氢离子浓度不变,pH值不变,故A正确;B.0.1mol·L−1的NaCO 溶液中加入
2 3
说法不正确的是
少量CaCl 晶体,两者反应生成碳酸钙,碳酸根浓度减小,碳酸根水解平衡逆向移动,水解程度增大,
2
水解生成的氢氧根离子浓度减小,pH减小,故B正确;C.NaF和NaClO溶液中存在电荷守恒:
, ,由电荷守恒可知两溶液中的离子总
浓度均等于2 ,HClO的 ,HF的 ,可知HClO的酸性比
HF弱,则NaClO的水解程度大于NaF,NaClO溶液的碱性强于NaF,其溶液中氢离子浓度小于NaF,
而两溶液中钠离子浓度相等,则NaF溶液中的离子总数多,故C错误;D.Cl 通入NaOH溶液中,若恰
2
A.断开K、合上K,电极A的电势低于电极B
2 1好完全反应生成氯化钠和次氯酸钠溶液,溶液显碱性,若溶液呈中性,可知氯气过量,溶液中存在
知,在催化剂表面,碳原子和硫原子可形成二氧化硫,即 ,B项正确;C.由图可看出,还有
HClO、NaClO、NaCl、HO共5种物质,共有H+、ClO−、Na+、Cl−、OH−共5种离子,故D正确;故选B。
2
HS没有分解,HS脱除率小于100%,C项正确;D.该过程中有化学键的断裂与生成,故一定有能量
12.用如图装置(夹持装置已略去)进行NH 制备及性质实验。下列说法正确的是 2 2
3
的变化,D项正确;答案选A。
14.乳酸[CHCH(OH)COOH]与乙醇在一定条件下反应生成的酯A,具有多种同分异构体,其中能与
3
饱和NaHCO 溶液反应放出的气体体积和相同条件下与Na反应放出的气体体积相等的有机物有
3
A.10种 B.11种 C.12种 D.13种
【答案】C
【解析】乳酸[CHCH(OH)COOH]与乙醇在一定条件下反应生成的酯 A,则 A 为
3
A.甲中制备NH 利用了NH ·H O的分解反应 CHCH(OH)COOCH CH;其同分异构体能与饱和NaHCO 溶液反应放出气体,说明含-COOH,能与
3 3 2 3 2 3 3
B.乙中的集气瓶内a导管长、b导管短 钠反应放出气体且与饱和 NaHCO 溶液反应放出的气体体积相等,则含-OH;先写羧酸,有
3
C.若将丙中的CCl 4 换成苯,仍能防止倒吸 CH 3 CH 2 CH 2 CH 2 COOH、(CH 3 ) 2 CHCH 2 COOH、CH 3 CH 2 CH(CH 3 )COOH、(CH 3 ) 3 CCOOH共4种;再将-
D.向收集好的NH 中通人少量Cl,可能观察到白烟
3 2 OH 取代烷烃中的 H,-OH 取代 CHCHCHCHCOOH 中烷基上的 H 有 4 种,-OH 取代
3 2 2 2
【答案】AD
(CH)CHCH COOH中烷基上的H有3种,-OH取代CHCHCH(CH )COOH中烷基上的H有4种,
3 2 2 3 2 3
【解析】该实验制备氨气利用碱石灰溶于水放热使氨水分解,氨气极易溶于水,不宜用排水法收集,
-OH取代(CH)CCOOH中烷基上的H有1种,共4+3+4+1=12种,C满足题意;答案选C。
3 3
其密度比空气小,可用排空气法收集。A.甲为氨气发生装置,利用氨水受热分解制备氨气的原理,故
15.常温下,将0.1000mol·L−1的KOH溶液分别滴加到20.00mL浓度均为0.1000mol·L−1的一元酸HX
A正确;B.氨气密度比空气小,利用向下排空气法,故a短b长,故B错误;C.因为苯的密度比水小,
和HY溶液中,溶液的pH与所加KOH溶液体积的关系如图所示,下列叙述错误的是
苯在上层,故将四氯化碳换成苯后不能防止倒吸,故C错误;D.氨气与氯气反应可以生成氯化铵固体,
产生大量白烟,故D正确;故选AD。
13.在活性炭催化条件下,煤气中的HS可被脱除,反应机理如图(吸附在催化剂表面的物种用*标注)
2
所示。下列有关说法错误的是
A.M点溶液中c(K+)>c(X−)>c(OH−)>c(H+)
B.常温下用0.1000mol·L−1的氨水(K =1.8×10−5)滴定0.1000mol·L−1 HX溶液可用酚酞做指示剂
b
C.N点溶液中,c(Y−)+2c(OH−)=2c(H+)+c(HY)
D.常温下,将0.1000mol·L−1 HX溶液和0.2000mol·L−1 KY溶液等体积混合,混合液呈酸性
A.CS 分子中含有非极性键 B.存在反应
2
【答案】D
C.HS脱除率小于100% D.该过程中发生了能量变化 【解析】A.M点时所得溶液为含有等物质的量的HX和KX的混合溶液,溶液的pH=9,呈碱性,说
2
【答案】A 明X−的水解大于HX电离,则c(K+)>c(X−),c(OH−)>c(H+),水解程度微弱,则c(X−)>c(OH−),则离子浓
【解析】A.CS 2 分子中C和两个S分别形成2对共用电子对,只含有极性键,A项错误;B.由图可 度大小为:c(K+)>c(X−)>c(OH−)>c(H+),故A正确;B.0.1000mol·L−1 HX溶液的pH=5,则HX的电离平加入HgO固体,加热三颈瓶至25℃,搅拌45min,氯气几乎完全反应。过滤三颈瓶内的混合物。
衡常数为 c(H+),溶液呈碱性,故D错误;故选D。 【答案】(1)A→C→B→D→B→E
(2)2MnO+16H++10Cl−=2Mn2++5Cl↑+8HO
2 2
三、非选择题(共60分。)
(3)除去Cl 中的氯化氢气体 Cl+HO=HCl+HClO或ClO+HO=2HClO等
2 2 2 2 2
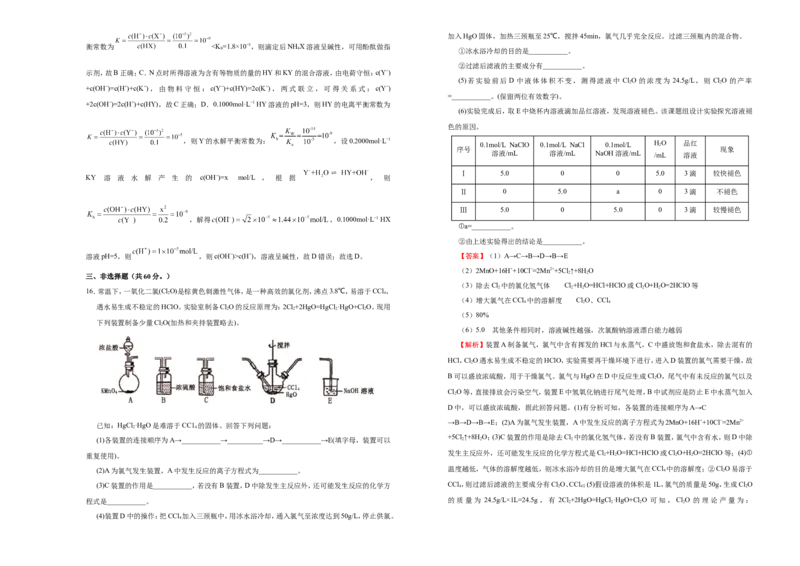
16.常温下,一氧化二氯(Cl O)是棕黄色刺激性气体,是一种高效的氯化剂,沸点3.8℃,易溶于CCl ,
2 4
(4)增大氯气在CCl 中的溶解度 ClO、CCl
4 2 4
遇水易生成不稳定的HClO。实验室制备ClO的反应原理为:2Cl+2HgO=HgCl ·HgO+Cl O。现用
2 2 2 2
(5)80%
下列装置制备少量ClO(加热和夹持装置略去)。
2
(6)5.0 其他条件相同时,溶液碱性越强,次氯酸钠溶液漂白能力越弱
【解析】装置A制备氯气,氯气中含有挥发的HCl与水蒸气,C中盛放饱和食盐水,除去混有的
HCl,ClO遇水易生成不稳定的HClO,实验需要再干燥环境下进行,进入D装置的氯气需要干燥,故
2
B可以盛放浓硫酸,用于干燥氯气。氯气与HgO在D中反应生成ClO,尾气中有未反应的氯气以及
2
ClO等,直接排放会污染空气,装置E中氢氧化钠进行尾气处理,B中试剂应是防止E中水蒸气加入
2
D中,可以盛放浓硫酸,据此回答问题。(1)有分析可知,各装置的连接顺序为A→C
→B→D→B→E;(2)A为氯气发生装置,A中发生反应的离子方程式为2MnO+16H++10Cl−=2Mn2+
已知:HgCl ·HgO是难溶于CC1 的固体。回答下列问题:
2 4
+5Cl↑+8HO;(3)C装置的作用是除去Cl 中的氯化氢气体,若没有B装置,氯气中含有水,则D中除
(1)各装置的连接顺序为A→___________→__________→D→___________→E(填字母,装置可以 2 2 2
发生主反应外,还可能发生反应的化学方程式是Cl+HO=HCl+HClO或ClO+HO=2HClO等;(4)①
重复使用)。 2 2 2 2
温度越低,气体的溶解度越低,则冰水浴冷却的目的是增大氯气在CCl 中的溶解度;②ClO易溶于
(2)A为氯气发生装置,A中发生反应的离子方程式为___________。 4 2
(3)C装置的作用是___________,若没有B装置,D中除发生主反应外,还可能发生反应的化学方 CCl 4 ,则过滤后滤液的主要成分有Cl 2 O、CCl 4 ;(5)假设溶液的体积是1L,氯气的质量是50g,生成Cl 2 O
程式是___________。 的质量为 24.5g/L×1L=24.5g,有 2Cl 2 +2HgO=HgCl 2 ·HgO+Cl 2 O 可知,Cl 2 O 的理论产量为:
(4)装置D中的操作:把CCl 加入三颈瓶中,用冰水浴冷却,通入氯气至浓度达到50g/L,停止供氯。
4Ni-CeO 320℃
2
=30.6g,则ClO的产率= =80%;(6)①探究浓度对溶液褪色的影
2 (3)CO+8H++8e−=CH +2HO 2×104mol
2 4 2
【解析】(1)已知①CH(g)+HO(g)=3H (g)+CO(g) ΔH=206kJ·mol−1;
4 2 2
响,保持溶液的体积不变,则a=5.0ml;②通过分析实验,可以得出其他条件相同时,溶液碱性越强,次
②CO(g)+HO(g)=H (g)+CO(g) ΔH=-41kJ·mol−1;
2 2 2
氯酸钠溶液漂白能力越弱。
根据盖斯定律-(①+②)可得CO(g)+4H(g)=CH (g)+2HO(g)的ΔH=-(206 kJ·mol−1-41kJ·mol−1)=-165
2 2 4 2
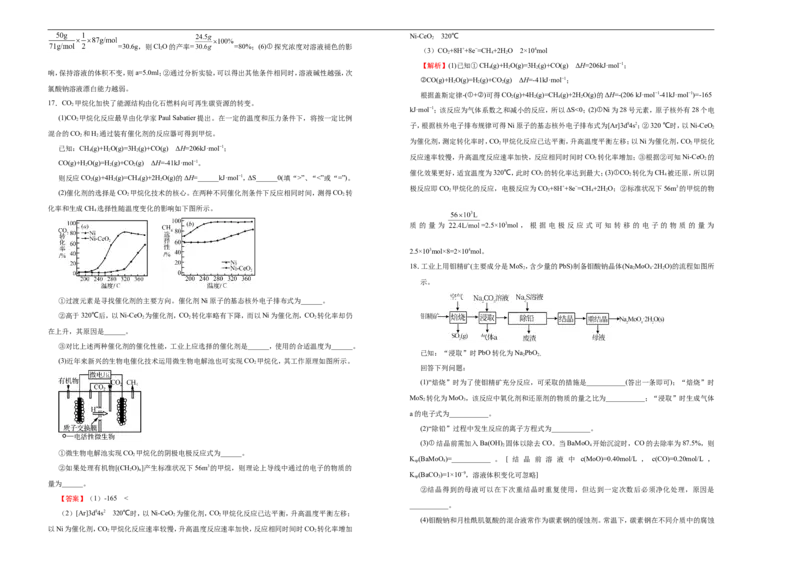
17.CO 甲烷化加快了能源结构由化石燃料向可再生碳资源的转变。
2
kJ·mol−1;该反应为气体系数之和减小的反应,所以ΔS<0;(2)①Ni为28号元素,原子核外有28个电
(1)CO 甲烷化反应最早由化学家Paul Sabatier提出。在一定的温度和压力条件下,将按一定比例
2
子,根据核外电子排布规律可得Ni原子的基态核外电子排布式为[Ar]3d84s2;②320 ℃时,以Ni-CeO
2
混合的CO 和H 通过装有催化剂的反应器可得到甲烷。
2 2
为催化剂,测定转化率时,CO 甲烷化反应已达平衡,升高温度平衡左移;以Ni为催化剂,CO 甲烷化
2 2
已知:CH(g)+HO(g)=3H (g)+CO(g) ΔH=206kJ·mol−1;
4 2 2
反应速率较慢,升高温度反应速率加快,反应相同时间时CO 转化率增加;③根据②可知Ni-CeO 的
2 2
CO(g)+HO(g)=H (g)+CO(g) ΔH=-41kJ·mol−1。
2 2 2
催化效果更好,适宜温度为320℃,此时CO 的转化率达到最大;(3)①CO 转化为CH 被还原,所以阴
则反应CO(g)+4H(g)=CH (g)+2HO(g)的ΔH=______kJ·mol−1,ΔS______0(填“>”、“<”或“=”)。 2 2 4
2 2 4 2
极反应即CO 甲烷化的反应,电极反应为CO+8H++8e−=CH +2HO;②标准状况下56m3的甲烷的物
(2)催化剂的选择是CO 甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO 转 2 2 4 2
2 2
化率和生成CH 选择性随温度变化的影响如下图所示。
4
质 的 量 为 =2.5×103mol , 根 据 电 极 反 应 式 可 知 转 移 的 电 子 的 物 质 的 量 为
2.5×103mol×8=2×104mol。
18.工业上用钼精矿(主要成分是MoS ,含少量的PbS)制备钼酸钠晶体(Na MoO ·2H O)的流程如图所
2 2 4 2
示。
①过渡元素是寻找催化剂的主要方向。催化剂Ni原子的基态核外电子排布式为______。
②高于320℃后,以Ni-CeO 为催化剂,CO 转化率略有下降,而以Ni为催化剂,CO 转化率却仍
2 2 2
在上升,其原因是______。
③对比上述两种催化剂的催化性能,工业上应选择的催化剂是______,使用的合适温度为______。
已知:“浸取”时PbO转化为NaPbO
2 2。
(3)近年来新兴的生物电催化技术运用微生物电解池也可实现CO 甲烷化,其工作原理如图所示。
2
回答下列问题:
(1)“焙烧”时为了使钼精矿充分反应,可采取的措施是___________(答出一条即可);“焙烧”时
MoS 转化为MoO ,该反应中氧化剂和还原剂的物质的量之比为___________;“浸取”时生成气体
2 3
a的电子式为___________。
(2)“除铅”过程中发生反应的离子方程式为___________。
(3)①结晶前需加入Ba(OH) 固体以除去CO。当BaMoO 开始沉淀时,CO的去除率为87.5%,则
2 4
①微生物电解池实现CO 甲烷化的阴极电极反应式为______。
2
K (BaMoO )=___________ 。 [ 结 晶 前 溶 液 中 c(MoO)=0.40mol/L , c(CO)=0.20mol/L ,
sp 4
②如果处理有机物[(CH O) ]产生标准状况下56m3的甲烷,则理论上导线中通过的电子的物质的
2 n
K (BaCO)=1×10−9,溶液体积变化可忽略]
sp 3
量为______。
②结晶得到的母液可以在下次重结晶时重复使用,但达到一定次数后必须净化处理,原因是
【答案】(1)-165 <
___________。
(2)[Ar]3d84s2 320℃时,以Ni-CeO 为催化剂,CO 甲烷化反应已达平衡,升高温度平衡左移;
2 2
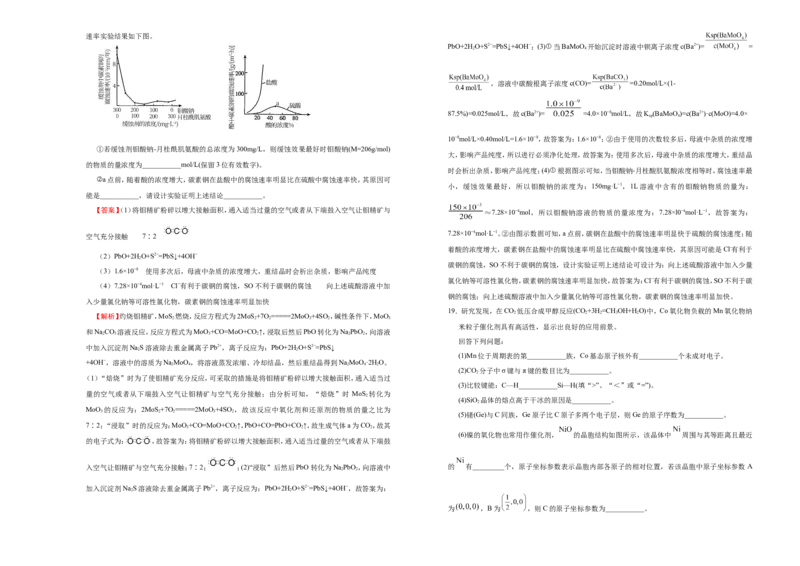
(4)钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在不同介质中的腐蚀
以Ni为催化剂,CO 甲烷化反应速率较慢,升高温度反应速率加快,反应相同时间时CO 转化率增加
2 2速率实验结果如下图。
PbO+2H O+S2−=PbS↓+4OH−;(3)①当BaMoO 开始沉淀时溶液中钡离子浓度c(Ba2+)= =
2 4
,溶液中碳酸根离子浓度c(CO)= =0.20mol/L×(1-
87.5%)=0.025mol/L,故c(Ba2+)= =4.0×10−8mol/L,故K (BaMoO )=c(Ba2+)·c(MoO)=4.0×
sp 4
10−8mol/L×0.40mol/L=1.6×10−8,故答案为:1.6×10−8;②由于使用的次数较多后,母液中杂质的浓度增
①若缓蚀剂钼酸钠-月桂酰肌氨酸的总浓度为300mg/L,则缓蚀效果最好时钼酸钠(M=206g/mol)
大,影响产品纯度,所以进行必须净化处理,故答案为:使用多次后,母液中杂质的浓度增大,重结晶
的物质的量浓度为___________mol/L(保留3位有效数字)。
时会析出杂质,影响产品纯度;(4)①根据图示可知,当钼酸钠-月桂酸肌氨酸浓度相等时,腐蚀速率最
②a点前,随着酸的浓度增大,碳素钢在盐酸中的腐蚀速率明显比在硫酸中腐蚀速率快,其原因可
小,缓蚀效果最好,所以钼酸钠的浓度为:150mg·L−1,1L溶液中含有的钼酸钠物质的量为:
能是___________,请设计实验证明上述结论___________。
【答案】(1)将钼精矿粉碎以增大接触面积,通入适当过量的空气或者从下端鼓入空气让钼精矿与 ≈7.28×10−4mol,所以钼酸钠溶液的物质的量浓度为:7.28×l0−4mol·L−1,故答案为:
7.28×10−4mol·L−1。②由图示数据可知,a点前,碳钢在盐酸中的腐蚀速率明显快于硫酸的腐蚀速度;随
空气充分接触 7∶2
着酸的浓度增大,碳素钢在盐酸中的腐蚀速率明显比在硫酸中腐蚀速率快,其原因可能是Cl-有利于
(2)PbO+2H O+S2−=PbS↓+4OH−
2
碳钢的腐蚀,SO不利于碳钢的腐蚀,设计实验证明上述结论可设计为:向上述硫酸溶液中加入少量
(3)1.6×10−8 使用多次后,母液中杂质的浓度增大,重结晶时会析出杂质,影响产品纯度
氯化钠等可溶性氯化物,碳素钢的腐蚀速率明显加快,故答案为:Cl−有利于碳钢的腐蚀,SO不利于碳
(4)7.28×10−4mol·L−1 Cl−有利于碳钢的腐蚀,SO不利于碳钢的腐蚀 向上述硫酸溶液中加
钢的腐蚀;向上述硫酸溶液中加入少量氯化钠等可溶性氯化物,碳素钢的腐蚀速率明显加快。
入少量氯化钠等可溶性氯化物,碳素钢的腐蚀速率明显加快
19.研究发现,在CO 低压合成甲醇反应(CO+3H =CH OH+H O)中,Co氧化物负载的Mn氧化物纳
2 2 2 3 2
【解析】灼烧钼精矿,MoS 燃烧,反应方程式为2MoS +7O =====2MoO +4SO,碱性条件下,MoO
2 2 2 3 2 3
米粒子催化剂具有高活性,显示出良好的应用前景。
和NaCO 溶液反应,反应方程式为MoO +CO=MoO+CO↑,浸取后然后PbO转化为NaPbO ,向溶液
2 3 3 2 2 2
回答下列问题:
中加入沉淀剂NaS溶液除去重金属离子Pb2+,离子反应为:PbO+2H O+S2−=PbS↓
2 2
(1)Mn位于周期表的第___________族,Co基态原子核外有___________个未成对电子。
+4OH−,溶液中的溶质为NaMoO ,将溶液蒸发浓缩、冷却结晶,然后重结晶得到NaMoO ·2HO。
2 4 2 4 2
(2)CO 分子中σ键与π键的数目比为___________。
2
(1)“焙烧”时为了使钼精矿充分反应,可采取的措施是将钼精矿粉碎以增大接触面积,通入适当过
(3)比较键能:C—H___________Si—H(填“>”、“<”或“=”)。
量的空气或者从下端鼓入空气让钼精矿与空气充分接触;由分析可知,“焙烧”时 MoS 转化为
2
(4)SiO 晶体的熔点高于干冰的原因是___________。
2
MoO 的反应为:2MoS +7O =====2MoO +4SO ,故该反应中氧化剂和还原剂的物质的量之比为
3 2 2 3 2
(5)锗(Ge)与C同族,Ge原子比C原子多两个电子层,则Ge的原子序数为___________。
7∶2;“浸取”时的反应为:MoO +CO=MoO+CO↑,PbO+CO=PbO+CO ↑,故生成气体a为CO,故其
3 2 2 2
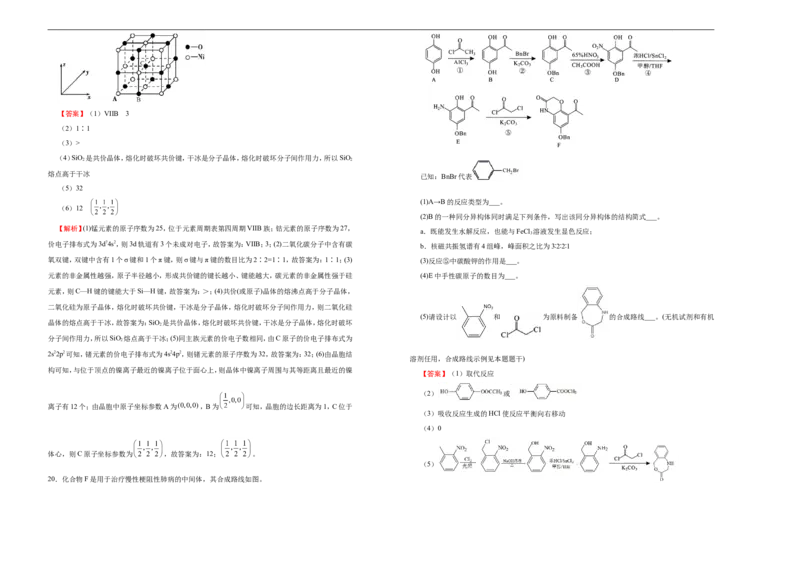
(6)镍的氧化物也常用作催化剂, 的晶胞结构如图所示,该晶体中 周围与其等距离且最近
的电子式为: ,故答案为:将钼精矿粉碎以增大接触面积,通入适当过量的空气或者从下端鼓
入空气让钼精矿与空气充分接触;7∶2; ;(2)“浸取”后然后PbO转化为NaPbO ,向溶液中 的 有_________个,原子坐标参数表示晶胞内部各原子的相对位置,若该晶胞中原子坐标参数 A
2 2
加入沉淀剂NaS溶液除去重金属离子Pb2+,离子反应为:PbO+2H O+S2−=PbS↓+4OH−,故答案为:
2 2
为 ,B为 ,则C的原子坐标参数为___________。【答案】(1)VIIB 3
(2)1∶1
(3)>
(4)SiO 是共价晶体,熔化时破坏共价键,干冰是分子晶体,熔化时破坏分子间作用力,所以SiO
2 2
熔点高于干冰
已知:BnBr代表
(5)32
(1)A→B的反应类型为___。
(6)12
(2)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式___。
【解析】(1)锰元素的原子序数为25,位于元素周期表第四周期VIIB族;钴元素的原子序数为27,
a.既能发生水解反应,也能与FeCl 溶液发生显色反应;
3
价电子排布式为3d74s2,则3d轨道有3个未成对电子,故答案为:VIIB;3;(2)二氧化碳分子中含有碳
b.核磁共振氢谱有4组峰,峰面积之比为3∶2∶2∶1
氧双键,双键中含有1个σ键和1个π键,则σ键与π键的数目比为2∶2=1∶1,故答案为:1∶1;(3) (3)反应⑤中碳酸钾的作用是___。
元素的非金属性越强,原子半径越小,形成共价键的键长越小、键能越大,碳元素的非金属性强于硅 (4)E中手性碳原子的数目为___。
元素,则C—H键的键能大于Si—H键,故答案为:>;(4)共价(或原子)晶体的熔沸点高于分子晶体,
二氧化硅为原子晶体,熔化时破坏共价键,干冰是分子晶体,熔化时破坏分子间作用力,则二氧化硅
(5)请设计以 和 为原料制备 的合成路线___。(无机试剂和有机
晶体的熔点高于干冰,故答案为:SiO 是共价晶体,熔化时破坏共价键,干冰是分子晶体,熔化时破坏
2
分子间作用力,所以SiO 熔点高于干冰;(5)同主族元素的价电子数相同,由C原子的价电子排布式为
2
2s22p2可知,锗元素的价电子排布式为4s24p2,则锗元素的原子序数为32,故答案为:32;(6)由晶胞结
溶剂任用,合成路线示例见本题题干)
构可知,与位于顶点的镍离子最近的镍离子位于面心上,则晶体中镍离子周围与其等距离且最近的镍
【答案】(1)取代反应
(2) 或
离子有12个;由晶胞中原子坐标参数A为 ,B为 可知,晶胞的边长距离为1,C位于
(3)吸收反应生成的HCl使反应平衡向右移动
(4)0
体心,则C原子坐标参数为 ,故答案为:12; 。
(5)
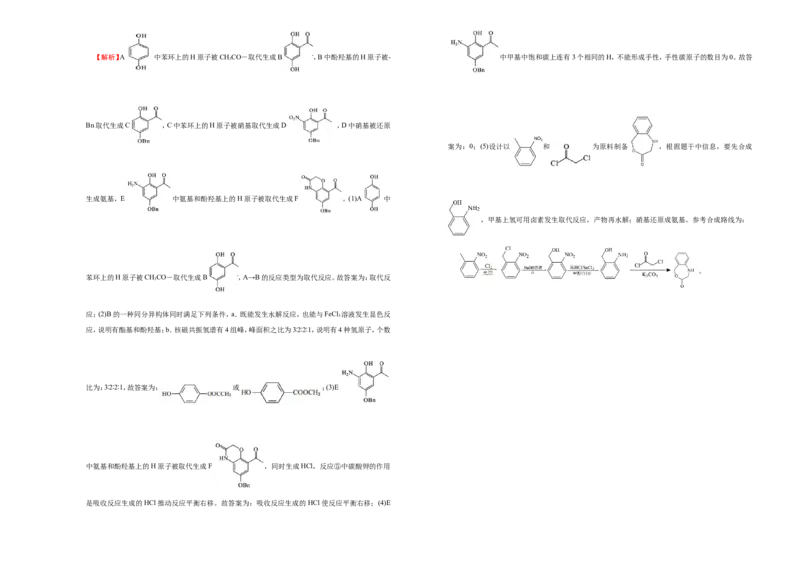
20.化合物F是用于治疗慢性梗阻性肺病的中间体,其合成路线如图。【解析】A 中苯环上的H原子被CHCO-取代生成B ,B中酚羟基的H原子被- 中甲基中饱和碳上连有3个相同的H,不能形成手性,手性碳原子的数目为0。故答
3
Bn取代生成C ,C中苯环上的H原子被硝基取代生成D ,D中硝基被还原
案为:0;(5)设计以 和 为原料制备 ,根据题干中信息,要先合成
生成氨基,E 中氨基和酚羟基上的H原子被取代生成F 。(1)A 中
,甲基上氢可用卤素发生取代反应,产物再水解;硝基还原成氨基。参考合成路线为:
。
苯环上的H原子被CHCO-取代生成B ,A→B的反应类型为取代反应。故答案为:取代反
3
应;(2)B的一种同分异构体同时满足下列条件,a.既能发生水解反应,也能与FeCl 溶液发生显色反
3
应,说明有酯基和酚羟基;b.核磁共振氢谱有4组峰,峰面积之比为3∶2∶2∶1,说明有4种氢原子,个数
比为:3∶2∶2∶1,故答案为: 或 ;(3)E
中氨基和酚羟基上的H原子被取代生成F ,同时生成HCl,反应⑤中碳酸钾的作用
是吸收反应生成的HCl推动反应平衡右移。故答案为:吸收反应生成的HCl使反应平衡右移;(4)E