文档内容
汕头市金山中学 2023 届高三第一学期第二次月考
化 学
可能用到的相对原子质量:H-1 C-12 Al-27 P-31
一、选择题:本题共10小题,每小题4分,共40分。每小题只有一个选项符合题意。
1.下列现象或做法与化学反应速率无关的是( )
A.“冰墩墩”制作材料生产过程中添加抗老化助剂 B.水果箱中放置乙烯利
C.馒头制作过程中在35℃用酵母发酵 D.新冠病毒可能通过气溶胶加速传
播
2.在指定条件下,下列有关汽车尾气无害化处理或资源化利用的物质转化能一步实现的是(
)
−
3.次磷酸根(H PO2 )的球棍模型如图所示,下列说法错误的是( )
2
A.P的原子结构示意图为
B.次磷酸根的电子式为
C.次磷酸根的结构式为 D.次磷酸分子式为HPO
3 2
4.我国科技工作者发现菜“小分子胶水”(结构如图)能助力自噬细胞“吞没”致病蛋白。
下列说法正确的是( )
A.该分子中所有碳原子一定共平面
B.该分子能与蛋白质分子形成氢键
C.1mol该物质最多能与3mol NaOH反应
D.该物质能发生取代、加成和消去反应
5.下列实验对应的离子方程式不正确的是( )
−
A.将碳酸氢钙溶液与过量的澄清石灰水混合:HCO3 +Ca2+ +OH- =CaCO ↓+H O
3 2
B.将少量NO 通入NaOH液:2NO +2OH- =NO- +NO- +H O
2 2 3 2 2
2−
C.将少量SO 通入NaClO溶液:SO +H O+2ClO- =SO3 +2HClO
2 2 2+
D.向氨水中滴入少量硝酸银溶液:Ag++2NH·HO=Ag(NH)2 +2H O
3 2 3 2
6.己知X、Y、Z、W、M为原子序数依次递增韵短周期元素,其中X、Y、Z元素同周期,
Y与W元素同主族,它们可以形成一种重要化合物甲.其结构如图所示。下列说法正确
的是( )
A.原子半径:M>W>Z B.第一电离能:Y>Z>X
C.氢化物的沸点:Z>Y>X D.甲中W的杂化方式为sp2
7.超临界状态下的CO 流体溶解性与有机溶剂相似,可提取中药材的有效成分,工艺流程如
2
下。
下列说法中错误的是( )
A.浸泡时加入乙醇有利于中草药有效成分的浸出
B.高温条件下更有利于超临界CO 流体萃取
2
C.升温、减压的目的是实现CO 与产品分离
2
D.超临界CO 流体萃取中药材具有无溶剂残留、绿色环保等优点
2
8.中国自古有“信口雌黄”“雄黄入药”之说。雌黄As S
2 3
和雄黄As S 都是自然界中常见的砷化物,早期都曾用作
4 4
绘画颜料,因都有抗病毒疗效也用来入药。砷元素有
+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关
系如图所示。下列说法错误的是
A.反应I中,As S 和SnCl 的物质的量之比为1:1时可
2 3 2
恰
好完全反应
B.反应II中,物质a可能是S、SO
2
C.反应I、II、Ⅳ是氧化还原反应;反应III是非氧化还原反应
D.反应I可用NaOH溶液吸收HS,向吸收后的溶液中加入足量稀硫酸可为反应Ⅳ提供
2
HS
2
9.设计如图装置回收金属钴。保持细菌所在环境pH
稳定,借助其降解乙酸盐生成CO ,将废旧锂离子
2
电池的正极材料LiCoO (s)转化为CO2+,工作时保
2
持厌氧环境,并定时将乙室溶液转移至甲室。己知
电极材料均为石墨材质,右侧装置为原电池。下列
说法正确的是( )
A.装置工作时,甲室溶液pH逐渐增大
B.装置工作一段时间后,乙室不用补充盐酸
C.乙室电极反应式为LiCoO +2H O+e- Li+ +Co2+ +4OH-
2 2
D.若甲室Co2+减少200mg,乙室Co2+增加300mg,则此时己进行过溶液转移
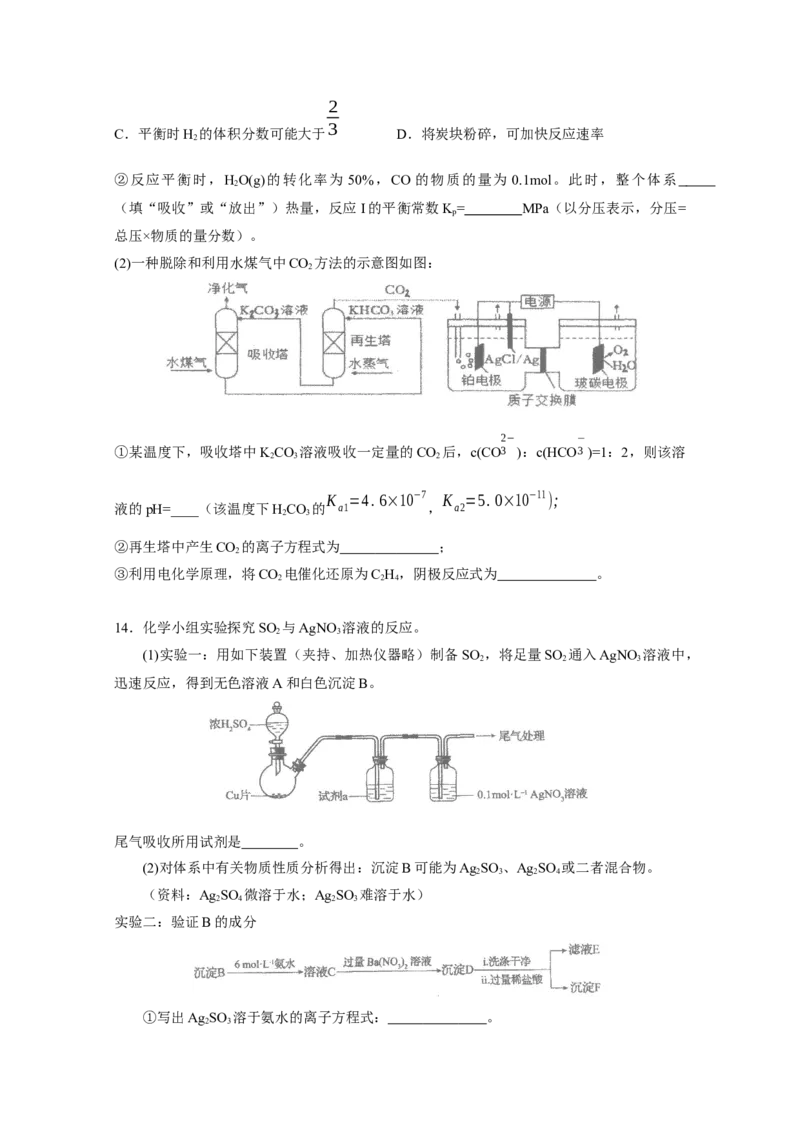
10.工业上以SrSO (s)为原料生产 SrCO (s),对其工艺条件进行研究。现有含 SrCO (s)的
4 3 3
0.1mol·L-1、1.0mol·L-1 Na CO 溶液,和含SrSO (s)的0.1mol·L-1、1.0mol·L-1 Na SO 溶液。
2 3 4 2 4
在一定pH范围内,四种溶液中1g[c(Sr2+)/mol·L-1]随pH的变化关系如图所示。下列说法
错误的是( )
2− 2−
A.反应SrSO (s)+CO3 SrCO (s)+SO4 的平衡常数
4 3
K (SrSO )
sp 4
K=
K (SrCO )
sp 3
B.a= -6.5
C.曲线④代表含SrCO (s)的1.0mol·L-1 Na CO 溶液的变化曲线
3 2 3
D.对含SrSO (s)且NaSO 和NaCO 初始浓度均为1.0mol·L-1的混合溶液,pH>7.7时才
4 2 4 2 3
发生沉淀转化
二、简答题(共有5小题,每题12分,共60分)
11.铝、磷、硫及其化合物在生产生活及科研中应用广泛。
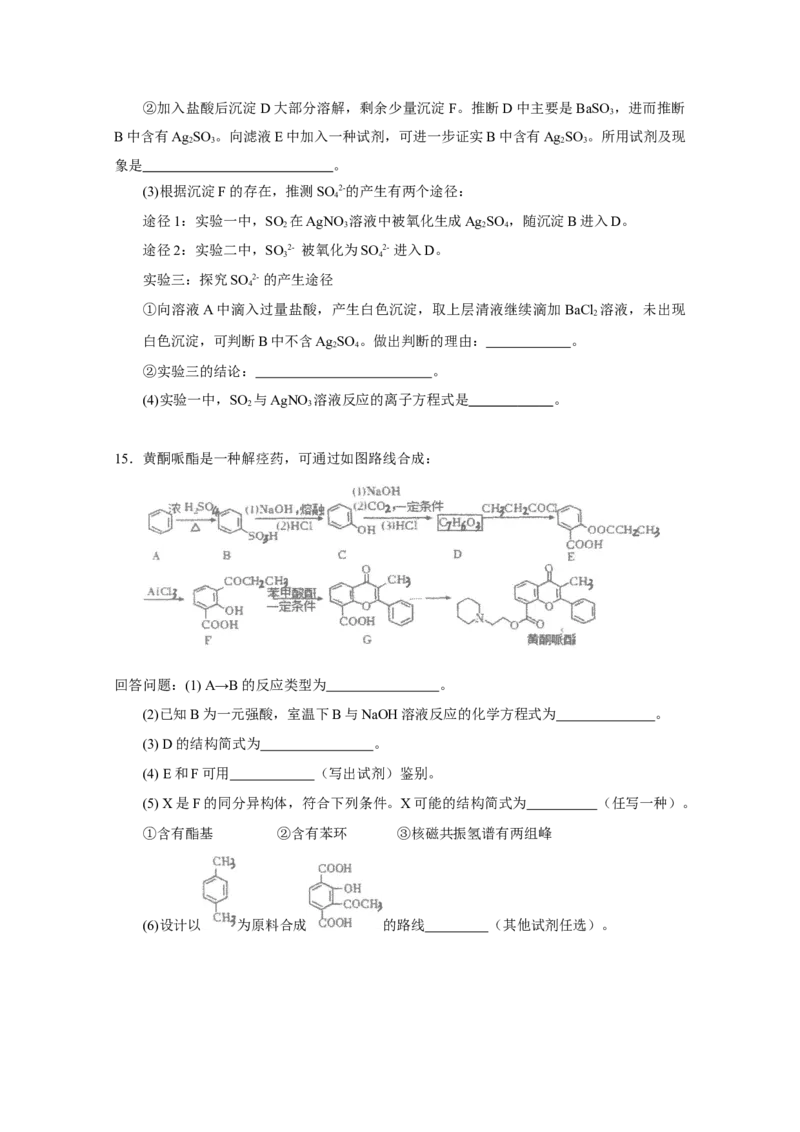
(1) P S 可用于制造火柴,其分子结构如图1所示。
4 3
①PS 分子中硫原子的杂化类型为 。
4 3
1个PS 分子中孤电子对的数目为 。
4 3
[Mo(CO) (P S )]
②P S 分子可以形成配合物 5 4 3 ,该
4 3
配合物中Mo的配位数为 。
(2)磷化铝熔点为2000℃,磷化铝晶胞结构如图2所示。
①磷化铝晶体中磷与铝微粒间的作用力为 。
②已知相邻的P原子和Al原子的核间距是d nm,B原子的分数坐标为 ,磷化铝晶
胞的密度为 g·cm-3。
12.钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为TiO ,含少量
2V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
已知“降温收尘”后,粗TiCl 中含有的几种物质的沸点:
4
物质 TiCl VOCl SiCl AlCl
4 3 4 3
沸点/℃ 136 127 57 180
回答下列问题:
(1) TiO 与C. Cl ,在600℃的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
2 2
物质 TiCl CO CO Cl
4 2 2
分压MPa 4.59×10-2 1.84×10-2 3.70×10-2 5.98×10-9
①该温度下,TiO 与C.Cl 反应的总化学方程式为 ;
2 2
②随着温度升高,尾气中CO的含量升高,原因是 。
(2)“除钒”过程中的化学方程式为 ;
(3)“除硅、铝”过程中,分离TiCl 中含Si、Al杂质的方法是 。
4
(4)“除钒”和“除硅、铝”的顺序不能交换,理由是 。
(5)下列金属冶炼方法与本工艺流程中加入Mg冶炼Ti的方法相似的是 。
A.高炉炼铁 B.电解熔融氯化钠制钠 C.铝热反应制锰 D.氧化汞分解制汞
13.2021年我国制氢量位居世界第一,煤的气化是一种重要的制氢途经。回答下列问题:
(1)在一定温度下,向体积固定的密闭容器中加入足量的 C(s)和1mol HO(g),起始压强为
2
0.2MPa时,发生下列反应生成水煤气:
I.C(s)+HO(g) CO(g)+H(g) △H= +131.4kJ·mol-1
2 2 1
II.CO(g)+HO(g) CO(g)+H(g) △H= -41.1kJ·mol-1
2 2 2 2
①下列说法正确的是 ;
A.平衡时向容器中充入惰性气体,反应I的平衡逆向移动
B.混合气体的密度保持不变时,说明反应体系已达到平衡2
3
C.平衡时H 的体积分数可能大于 D.将炭块粉碎,可加快反应速率
2
②反应平衡时,HO(g)的转化率为 50%,CO 的物质的量为 0.1mol。此时,整个体系
2
(填“吸收”或“放出”)热量,反应I的平衡常数K= MPa(以分压表示,分压=
p
总压×物质的量分数)。
(2)一种脱除和利用水煤气中CO 方法的示意图如图:
2
2− −
①某温度下,吸收塔中KCO 溶液吸收一定量的CO 后,c(CO3 ):c(HCO3 )=1:2,则该溶
2 3 2
K =4.6×10−7 K =5.0×10−11 );
液的pH=____(该温度下HCO 的 a1 , a2
2 3
②再生塔中产生CO 的离子方程式为 ;
2
③利用电化学原理,将CO 电催化还原为C H,阴极反应式为 。
2 2 4
14.化学小组实验探究SO 与AgNO 溶液的反应。
2 3
(1)实验一:用如下装置(夹持、加热仪器略)制备SO ,将足量SO 通入AgNO 溶液中,
2 2 3
迅速反应,得到无色溶液A和白色沉淀B。
尾气吸收所用试剂是 。
(2)对体系中有关物质性质分析得出:沉淀B可能为Ag SO 、Ag SO 或二者混合物。
2 3 2 4
(资料:Ag SO 微溶于水;Ag SO 难溶于水)
2 4 2 3
实验二:验证B的成分
①写出Ag SO 溶于氨水的离子方程式: 。
2 3②加入盐酸后沉淀D大部分溶解,剩余少量沉淀F。推断D中主要是BaSO ,进而推断
3
B中含有Ag SO 。向滤液E中加入一种试剂,可进一步证实B中含有Ag SO 。所用试剂及现
2 3 2 3
象是 。
(3)根据沉淀F的存在,推测SO 2-的产生有两个途径:
4
途径1:实验一中,SO 在AgNO 溶液中被氧化生成Ag SO ,随沉淀B进入D。
2 3 2 4
途径2:实验二中,SO 2- 被氧化为SO 2- 进入D。
3 4
实验三:探究SO 2- 的产生途径
4
①向溶液A中滴入过量盐酸,产生白色沉淀,取上层清液继续滴加BaCl 溶液,未出现
2
白色沉淀,可判断B中不含Ag SO 。做出判断的理由: 。
2 4
②实验三的结论: 。
(4)实验一中,SO 与AgNO 溶液反应的离子方程式是 。
2 3
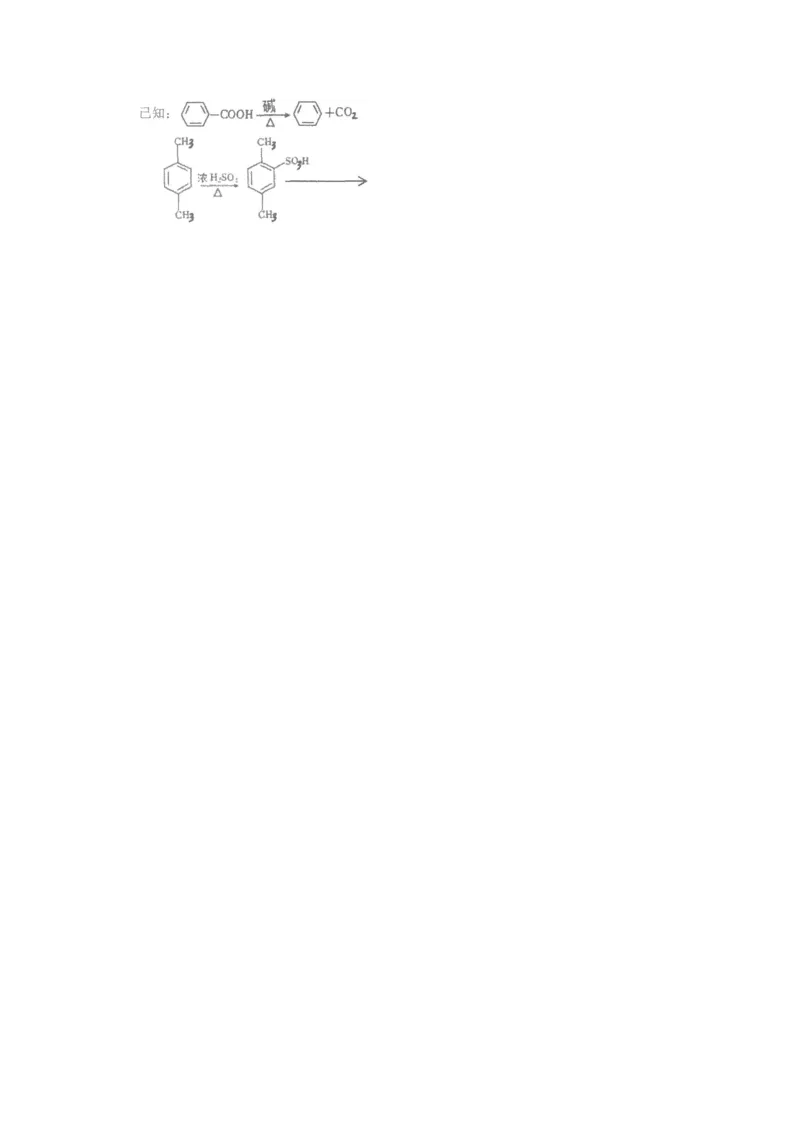
15.黄酮哌酯是一种解痉药,可通过如图路线合成:
回答问题:(1) A→B的反应类型为 。
(2)已知B为一元强酸,室温下B与NaOH溶液反应的化学方程式为 。
(3) D的结构简式为 。
(4) E和F可用 (写出试剂)鉴别。
(5) X是F的同分异构体,符合下列条件。X可能的结构简式为 (任写一种)。
①含有酯基 ②含有苯环 ③核磁共振氢谱有两组峰
(6)设计以 为原料合成 的路线 (其他试剂任选)。化学参考答案
一、单项选择题(共有10小题,每题4分,共40分)
题号 1 2 3 4 5 6 7 8 9 10
答案 D B B B C B B C D D
二、简答题(共有5小题,每题12分,共60分)
sp3
11.(12分,每空2分) (1) 10 6 (2)极性共价键(或共价键)
87√3
8d3N ×10−21
(1/4,1/4,3/4) A
12.(12分,每空2分)(1) 5TiO +6C+10Cl 5TiCl +2CO+4CO
2 2 4 2
随着温度升高,CO 与C发生反应 C+CO 2CO
2 2
(2) 3VOCl +Al=3VOCl +AlCl
3 2 3
(3)蒸馏 (4)若先“除硅、铝”再“除钒”,“除钒”时需要加入Al,又引入Al杂质;
(5) AC
13.(12分,每空2分)(1)①BD; ②吸收; 0.02MPa;
(2)①10;②2HCO CO2- +CO +H O ,③2CO+12H+ +12e- =C H+4H O
3 3 2 2 2 2 4 2
14.(12分,每空2分)(1) NaOH溶液
2−
(2)①Ag SO +4NH·HO=2Ag(NH)++SO3 +4H O
2 3 3 2 3 2 2
②H O 溶液,产生白色沉淀
2 2
(3)①Ag SO 溶解度大于BaSO,没有BaSO 沉淀时,必定没有Ag SO
2 4 4 4 2 4
2− 2−
②途径1不产生SO4 ,途径2产生SO4
(4) 2Ag+ +SO+H O=Ag SO ↓+2H+ (2分)
2 2 2 3
15.(12分)(1)取代反应或磺化反应;(1分)
(2) ;(2分)(3) ;(2分)