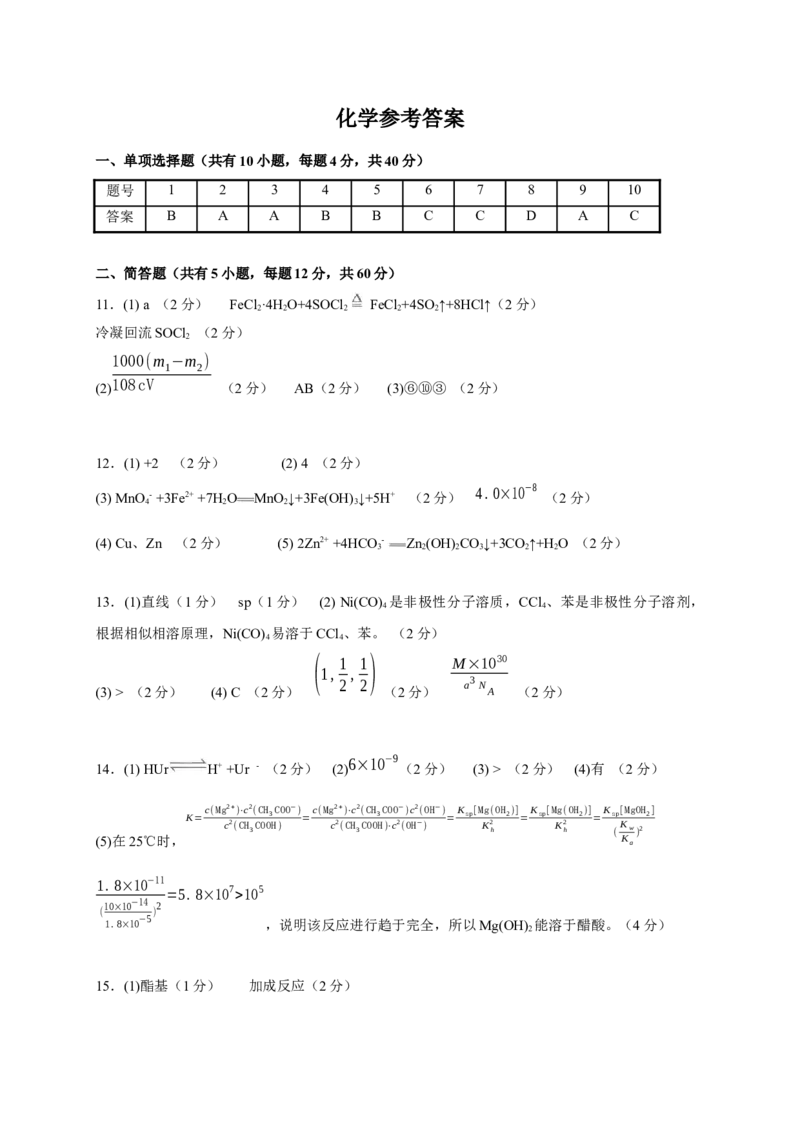文档内容
汕头市金山中学 2023 届高三第一学期摸底考试
化 学
可能用到原子量:H-1 C-12 O-16 Ba-137
一、单项选择题(共有10小题,每题4分,共40分)
1.关于化工生产的叙述中,符合生产实际的是( )
A.石油化工中,采用于馏的方法把石油分成不同沸点范围的产品
B.硫酸工业中,利用热交换器预热反应物,降低能耗提高生产效率
C.纯碱工业中,采用侯氏制碱法时向饱和食盐水中依次通入CO 和NH ,提高原料的利用率
2 3
D.合成氨工业中,采用高压条件,增大合成氨反应的平衡常数,增大原料转化率
2.下列离子方程式中正确的是( )
−
A.NO 在大气中形成酸雨:4NO +O +2H O=4H++4NO3
2 2 2 2
B.实验室制Fe(OH) 胶体:Fe3++3OH- Fe(OH) (胶体)
3 3
− 2−
C.NaAlO 溶液中通入过量CO:2AlO2 +CO +3H O=2Al(OH) ↓+CO3
2 2 2 2 3
−
D.过量Fe溶于稀硝酸:Fe+4H- +NO3 =Fe3++NO↑+2HO
2
3.设N 为阿伏伽德罗常数的值,下列叙述错误的是( )
A
+
A.1L 0.1mol·L-1 (NH )SO 溶液中NH4离子的数目为0.2N
4 2 4 A
B.Zn与浓硫酸反应,产生22.4L气体(标准状况)时,转移的电子数一定为2N
A
C.16.9g过氧化钡(BaO)固体中阴、阳离子总数为0.2N
2 A
D.42.0g 乙烯和丙烯的混合气体中含有的碳原子数为3N
A
4.下列实验目的对应的方案设计、现象和结论都正确的是( )
实验目的 方案设计 现象和结论
探究金属钠在氧气中 若无气体生成,则固体粉
取少量固体粉末,加入2~3mL蒸馏
A 燃烧所得固体粉末的 末为 NaO;若有气体生
水 2
成分 成,则固体粉末为NaO
2 2
B 比较 AgCl 和 AgI 的 向等体积饱和AgCl溶液和饱和AgI 得到沉淀n(AgCl)>n(AgI),溶
K 相对大小 则K (AgCl)>K (AgI)
sp 液中分别滴加等量的浓AgNO 溶液 sp sp
3
比较Cl、Br 、I 的 向KBr、KI混合溶液中依次加入少量 溶液分层,下层呈紫红
2 2 2
C 色 , 证 明 氧 化 性 :
氧化性 氯水和CCl ,振荡,静置 Cl>Br >I
4 2 2 2
用pH计测定pH:
比较HCO 与
2 3 pH①>②,证明HCO 酸性
D ①NaHCO 溶液 2 3
3 弱于CHCOOH
CHCOOH的酸性 3
3
②CH COONa溶液
3
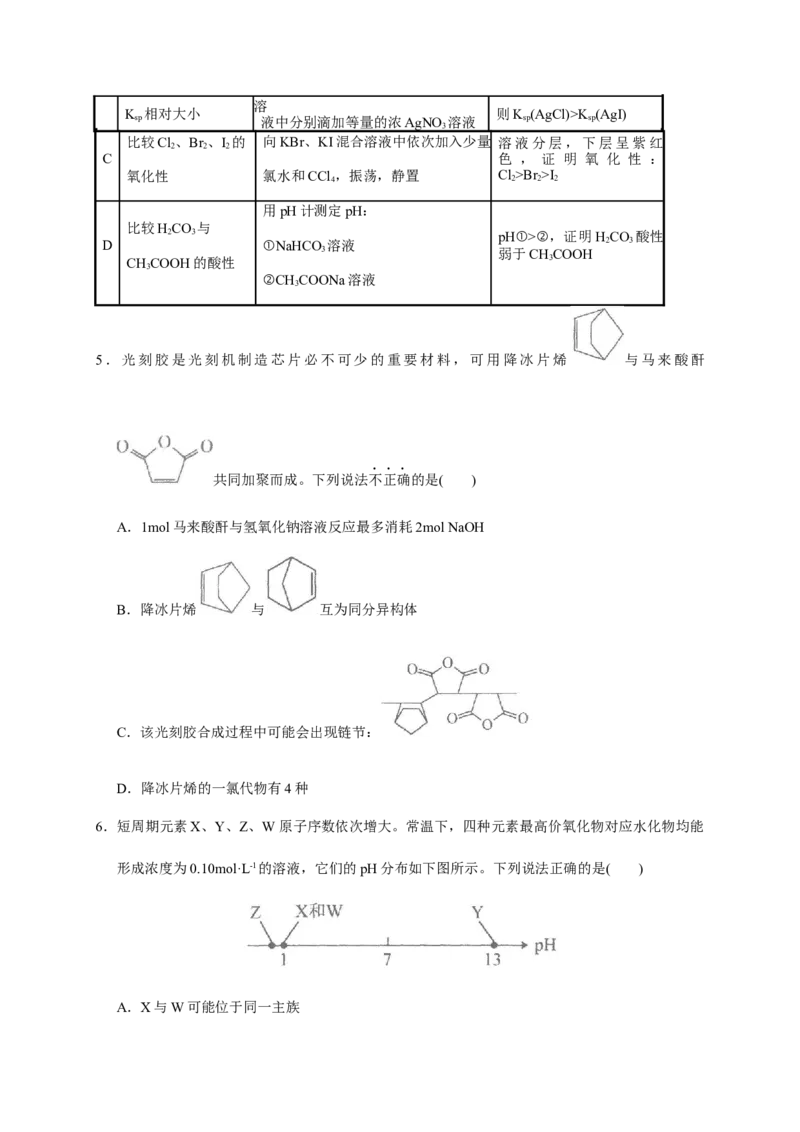
5.光刻胶是光刻机制造芯片必不可少的重要材料,可用降冰片烯 与马来酸酐
共同加聚而成。下列说法不正确的是( )
A.1mol马来酸酐与氢氧化钠溶液反应最多消耗2mol NaOH
B.降冰片烯 与 互为同分异构体
C.该光刻胶合成过程中可能会出现链节:
D.降冰片烯的一氯代物有4种
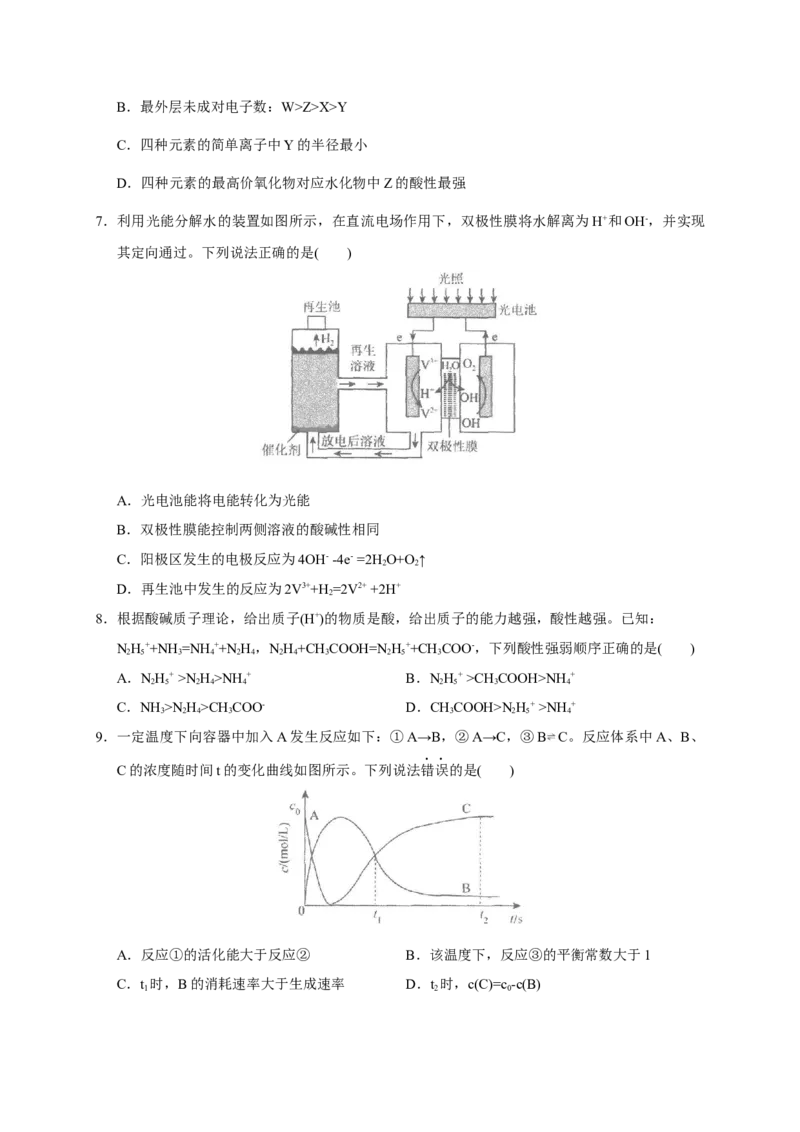
6.短周期元素X、Y、Z、W原子序数依次增大。常温下,四种元素最高价氧化物对应水化物均能
形成浓度为0.10mol·L-1的溶液,它们的pH分布如下图所示。下列说法正确的是( )
A.X与W可能位于同一主族B.最外层未成对电子数:W>Z>X>Y
C.四种元素的简单离子中Y的半径最小
D.四种元素的最高价氧化物对应水化物中Z的酸性最强
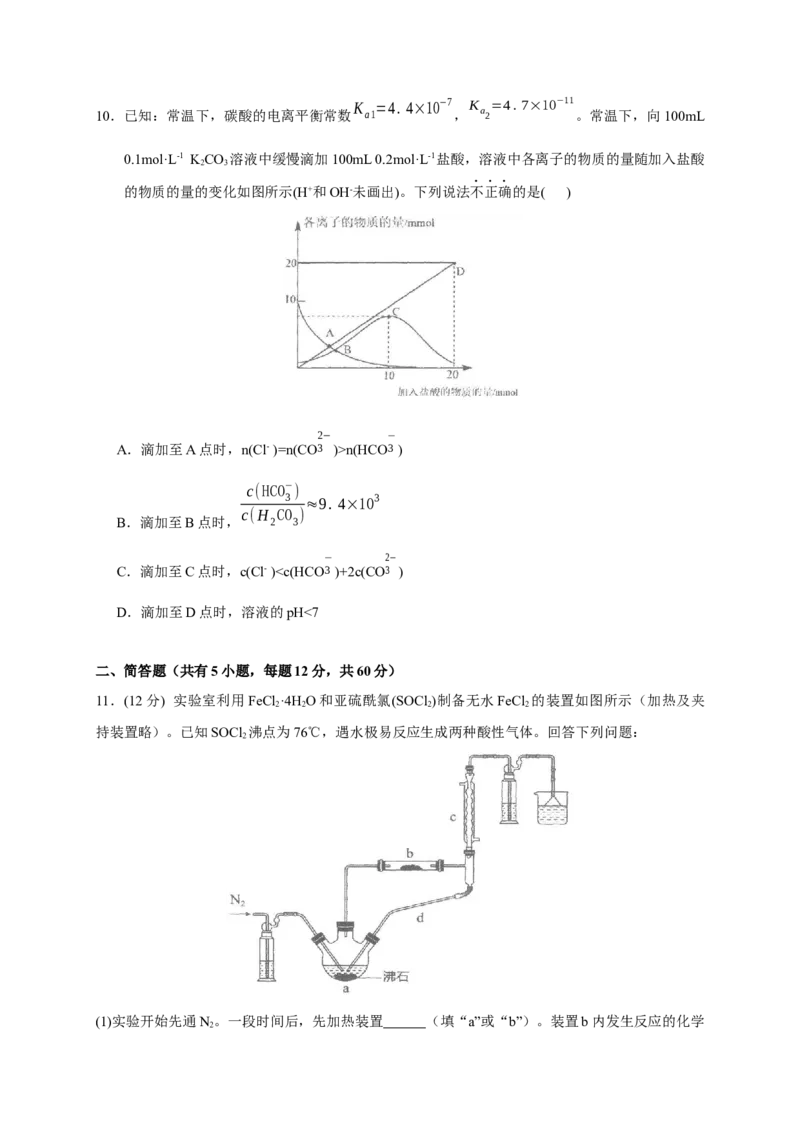
7.利用光能分解水的装置如图所示,在直流电场作用下,双极性膜将水解离为H+和OH-,并实现
其定向通过。下列说法正确的是( )
A.光电池能将电能转化为光能
B.双极性膜能控制两侧溶液的酸碱性相同
C.阳极区发生的电极反应为4OH- -4e- =2H O+O↑
2 2
D.再生池中发生的反应为2V3++H =2V2+ +2H+
2
8.根据酸碱质子理论,给出质子(H+)的物质是酸,给出质子的能力越强,酸性越强。已知:
NH++NH=NH++N H,NH+CH COOH=N H++CH COO-,下列酸性强弱顺序正确的是( )
2 5 3 4 2 4 2 4 3 2 5 3
A.NH+ >N H>NH+ B.NH+ >CH COOH>NH +
2 5 2 4 4 2 5 3 4
C.NH >N H>CH COO- D.CHCOOH>N H+ >NH+
3 2 4 3 3 2 5 4
9.一定温度下向容器中加入A发生反应如下:①A→B,②A→C,③B C。反应体系中A、B、
C的浓度随时间t的变化曲线如图所示。下列说法错误的是( )
A.反应①的活化能大于反应② B.该温度下,反应③的平衡常数大于1
C.t 时,B的消耗速率大于生成速率 D.t 时,c(C)=c -c(B)
1 2 0K =4.4×10−7 K =4.7×10−11
10.已知:常温下,碳酸的电离平衡常数 a1 , a 2 。常温下,向100mL
0.1mol·L-1 KCO 溶液中缓慢滴加100mL 0.2mol·L-1盐酸,溶液中各离子的物质的量随加入盐酸
2 3
的物质的量的变化如图所示(H+和OH-未画出)。下列说法不正确的是( )
2− −
A.滴加至A点时,n(Cl- )=n(CO3 )>n(HCO3 )
c(HCO−)
3 ≈9.4×103
c(H CO )
B.滴加至B点时, 2 3
− 2−
C.滴加至C点时,c(Cl- )”、“<”或“=”)。
1 1 1 1 2 2
(4)①(CHNH )PbI 的晶胞结构如图所示:
3 3 3
(1 1 1)
, ,
2 2 2
其中B代表Pb2+。则 代表I-,原子分数坐标A为(0,0,0),B为 ,则C的原子分
数坐标为 。
②已知(CHNH )PbI 的摩尔质量为 Mg·mol-1,N 为阿伏加德罗常数的值,则该晶体的密度为
3 3 3 A
g·cm-3。
14.(12分)人体内尿酸(HUr)含量偏高,关节滑液中产生尿酸钠晶体(NaUr)会引发痛风,NaUr(s)
Na+(aq)+Ur- (aq) △H>0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
已知:①37℃时,K(HUr)=
4×10−6
,K =
2.4×10−14
,K (NaUr)=
6.4×10−5
a w sp
②37℃时,模拟关节滑液pH=7.4,c(Ur- )=
4.6×10−4
mol·L-1
(1)尿酸电离方程式为 。
(2) K 为盐的水解常数,37℃时,K(Ur- )= 。
h h
(3) 37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液中 c(Na+) c(Ur -)
(填“>”、“<”或“=”)。
(4) 37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+)=0.2mol·L-1时, (填“有”或“无”)
NaUr晶体析出。
(5)为探究Mg(OH) 在酸中的溶解性,利用以下相关数据计算出反应:Mg(OH) (s)+2CHCOOH(aq)
2 2 3
Mg2+(aq)+2CH COO- (aq)+2H O(l)在25℃时的平衡常数K,并据此推断Mg(OH) 能否溶解于醋酸?
3 2 2
(要求有列式推导并代入数据进行运算的过程,根据计算结果进行判断。已知 25℃时:K
w
=1.0×10−14
,K(CHCOOH)=
1.8×10−5
,K (Mg(OH) ]=
1.8×10−11
,1.83≈5.8)
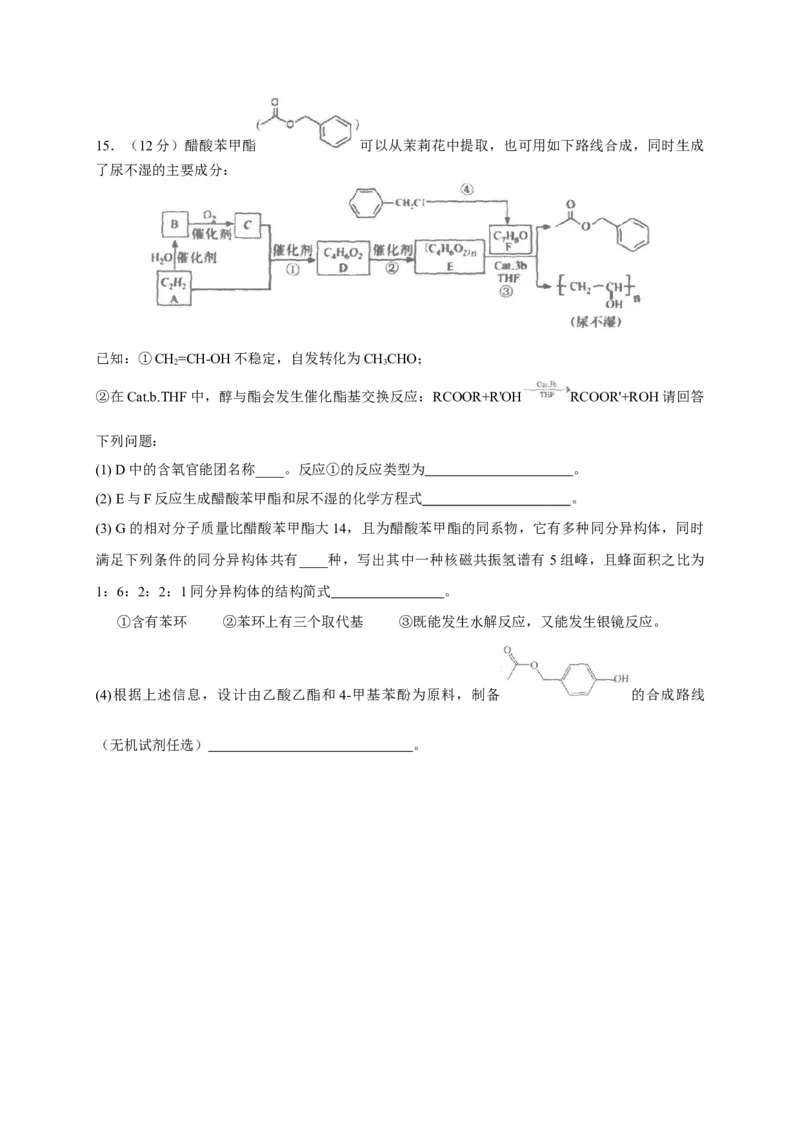
a 3 sp 215.(12分)醋酸苯甲酯 可以从茉莉花中提取,也可用如下路线合成,同时生成
了尿不湿的主要成分:
已知:①CH=CH-OH不稳定,自发转化为CHCHO;
2 3
②在Cat.b.THF中,醇与酯会发生催化酯基交换反应:RCOOR+R'OH RCOOR'+ROH请回答
下列问题:
(1) D中的含氧官能团名称____。反应①的反应类型为 。
(2) E与F反应生成醋酸苯甲酯和尿不湿的化学方程式 。
(3) G的相对分子质量比醋酸苯甲酯大14,且为醋酸苯甲酯的同系物,它有多种同分异构体,同时
满足下列条件的同分异构体共有____种,写出其中一种核磁共振氢谱有5组峰,且蜂面积之比为
1:6:2:2:1同分异构体的结构简式 。
①含有苯环 ②苯环上有三个取代基 ③既能发生水解反应,又能发生银镜反应。
(4)根据上述信息,设计由乙酸乙酯和4-甲基苯酚为原料,制备 的合成路线
(无机试剂任选) 。化学参考答案
一、单项选择题(共有10小题,每题4分,共40分)
题号 1 2 3 4 5 6 7 8 9 10
答案 B A A B B C C D A C
二、简答题(共有5小题,每题12分,共60分)
11.(1) a (2分) FeCl ·4HO+4SOCl FeCl +4SO↑+8HCl↑(2分)
2 2 2 2 2
冷凝回流SOCl (2分)
2
1000(m −m )
1 2
108cV
(2) (2分) AB(2分) (3)⑥⑩③ (2分)
12.(1) +2 (2分) (2) 4 (2分)
(3) MnO- +3Fe2+ +7H O MnO ↓+3Fe(OH) ↓+5H+ (2分)
4.0×10−8
(2分)
4 2 2 3
(4) Cu、Zn (2分) (5) 2Zn2+ +4HCO- Zn(OH) CO↓+3CO ↑+H O (2分)
3 2 2 3 2 2
13.(1)直线(1分) sp(1分) (2) Ni(CO) 是非极性分子溶质,CCl 、苯是非极性分子溶剂,
4 4
根据相似相溶原理,Ni(CO) 易溶于CCl 、苯。 (2分)
4 4
( 1 1) M×1030
1, ,
2 2 a 3 N
(3) > (2分) (4) C (2分) (2分) A (2分)
14.(1) HUr H+ +Ur - (2分) (2)
6×10−9
(2分) (3) > (2分) (4)有 (2分)
K=
c(Mg2+)⋅c2(CH
3
COO−)
=
c(Mg2+)⋅c2(CH
3
COO−)c2(OH−)
=
K sp[Mg(OH
2
)]
=
K sp[Mg(OH
2
)]
=
K sp[MgOH
2
]
c2(CH
3
COOH) c2(CH
3
COOH)⋅c2(OH−) K2
h
K2
h (
K
w)2
(5)在25℃时, K
a
1.8×10−11
=5.8×107 >105
10×10−14
2
( )
1.8×10−5 ,说明该反应进行趋于完全,所以Mg(OH) 能溶于醋酸。(4分)
2
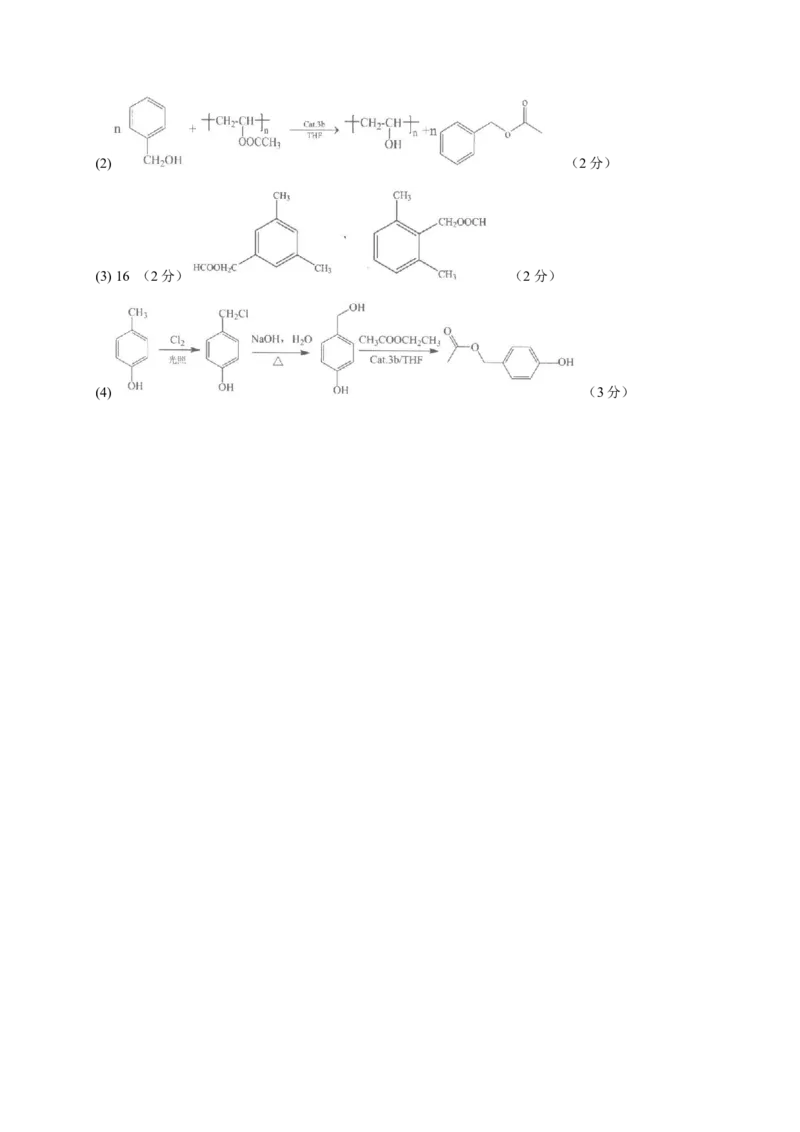
15.(1)酯基(1分) 加成反应(2分)(2) (2分)
(3) 16 (2分) (2分)
(4) (3分)下载最新免费模拟卷,到公众号:一枚试卷君