文档内容
2018 年浙江省金华市、丽水市中考化学试题
一、选择题
1. 如图是微信热传的“苯宝宝表情包”,苯(化学式C H)、六氯苯(化学式C Cl)都是重要的化
6 6 6 6
工原料,下列有关说法正确的是( )
A. 苯分子由碳、氢两种元素组成
B. 苯中氢元素的质量分数小于10%
C. 六氯苯中碳氯两种元素的质量比为1:1
D. 六氯苯由6个碳原子和6个氯原子构成
【答案】D
【解析】A、苯由碳、氢两种元素组成,错误;B、苯中氢元素的质量分数=
×100%=7.7%<10%,正确;C、六氯苯中碳氯两种元素的质量比为(12×6):(35.5×6)=24:
71,错误;D、一个六氯苯分子由6个碳原子和6个氯原子构成,错误。故选B。
2. “丹砂烧之成水银”中的“丹砂”指的是硫化汞。该反应的微观示意图如下,有关说法正确的
是( )
A. “●”代表非金属单质汞 B. 此反应遵循质量守恒定律
C. 反应前后原子的种类发生改变 D. 反应前后各元素的化合价都不变
【答案】B
【解析】根据微观示意图可知,此反应的化学方程式为HgS+O =Hg+SO;A、单质汞属于金属,
2 2
故A错误;B、任何化学反应都遵循质量守恒定律,故B正确;C、反应前后原子的种类、数目、
质量都不改变,故C错误;D、根据化学方程式HgS+O =Hg+SO,三种元素的化合价都发生
2 2
了改变,故D错误。故选B。
3. 20℃时,在各盛有100克水的烧杯中,分别加入10克甲、乙、丙三种纯净物(不含结晶水,不
与水反应),充分溶解后,结果如图。下列说法正确的是( )A. 所得溶液可能都是饱和溶液
B. 20℃时,乙溶液的溶质质量最小
C. 溶液溶质的质量分数:甲>丙>乙
D. 升高温度,溶液溶质的质量分数一定变大
【答案】A
4. 用所给实验器材(规格和数量不限),就能顺利完成相应实验的是( )
选项 相应实验 实验器材(省略夹持装置)
A 硫酸铜晶体的制备和生长 烧杯、玻璃棒、蒸发皿、量筒
B 分离氯化钾和二氧化锰的混合物 烧杯、玻璃棒、胶头滴管、滤纸
C 用固体氯化钠配制5%的溶液 烧杯、玻璃棒、胶头滴管、量筒
D 用pH试纸测定溶液的酸碱性强弱 烧杯、玻璃棒、pH试纸、标准比色卡
A. A B. B C. C D. D
【答案】D
【解析】A、硫酸铜溶液的浓缩结晶,应加热蒸发水分,所需实验器材有酒精灯、蒸发皿、玻璃
棒、铁架台、坩埚钳等,题目提供的实验器材无法完成该实验,故A错误;B、氯化钾易溶于水,
二氧化锰难溶于水,可采取加水溶解、过滤、洗涤、干燥的方法得到二氧化锰,然后对滤液蒸发结晶得到氯化钾,所需实验器材有烧杯、玻璃棒、漏斗、滤纸、铁架台、酒精灯、蒸发皿等,
题目提供的实验器材无法完成该实验,故B错误;C、用固体氯化钠配制5%的溶液,首先计
算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,在这些
操作中需要的实验器材:托盘天平、药匙、量筒、胶头滴管、烧杯和玻璃棒,题目提供的实验器
材无法完成该实验,故C错误;D、测定溶液的酸碱性可使用pH试纸,所需实验器材有烧杯、
玻璃棒、pH试纸、标准比色卡,题目提供的实验器材可以完成该实验,故D正确。故选D。
二、非选择题
5. 中国是全球第一个实现在海域“可燃冰”试开采中获得连续稳定产气的国家。“可燃冰”是甲
烷和水在低温、高压条件下形成的水合物(CH·nH O)。
4 2
(1)在常温常压下,“可燃冰”会发生反应:CH·nH O=CH+nH O,该反应属于______(填基本反
4 2 4 2
应类型);
(2)甲烷可制成合成气(CO、H),再制成甲醇(CHOH),代替日益供应紧张的燃油。由合成气制
2 3
甲醇的反应方程式为:CO+2H CHOH,由甲烷制成合成气有两种方法:
2 3
①CH+H O CO+3H ②2CH+O 2CO+4H
4 2 2 4 2 2
从原料配比角度比较方法①和②,更适宜用于合成甲醇的方法是__________(填序号)。
【答案】 (1). 分解反应 (2). ②
【解析】(1)根据“CH·nH O=CH+nH O”可知,该反应属于分解反应;(2) 由合成气制甲醇的反
4 2 4 2
应方程式可知需要一氧化碳和氢气的分子个数比为1:2;对比两个方案,只有方案②中一氧
化碳和氢气的分子个数比为1:2。
6. A、B、C、D是初中科学常见的四种物质,其中A、B属于相同物质类别的化合物,C、D物质
类别不同,它们之间的转化和反应关系如图。图中“→”表示某一种物质经一步反应可转化为
另一种物质,“—”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去,
请回答:
(1)若C是二氧化碳,B是氢氧化钙,则B→A的化学方程式是________________;
(2)若C是锌,A和B都属于酸,写出D可能的化学式____________(物质类别不同的两种即
可)。
【答案】 (1). NaCO+Ca(OH) =CaCO ↓+2NaOH (2). NaCO、CuO、NaOH(或其它碳酸盐、
2 3 2 3 2 3金属氧化物、碱的化学式)三种中的任意两种
【解析】A、B、C、D是初中化学常见的四种物质,其中A、B属于相同类别的化合物,C、D属
于不同类别的纯净物,B会转化为A,C、D会与A、B反应,所以:(1)若C是二氧化碳,B为氢
氧化钙,D为酸或可溶性的铜盐或铁盐等,B→A的反应是氢氧化钙和碳酸钠反应生成碳酸
钙沉淀和氢氧化钠,化学方程式是:Ca(OH) +Na CO=CaCO ↓+2NaOH;(2)若C是锌,A和B
2 2 3 3
都属于酸,A为盐酸,B为硫酸,则D为碳酸盐或碱或金属氧化物。
7. 有一包白色固体可能含有碳酸钠、硫酸钠、硝酸钡、氢氧化钠中的一种或几种。某科学兴趣
小组为探究其成分做了以下实验:
①取少量固体于烧杯中,加足量的水溶解,烧杯内有固体残留并得到无色溶液甲;
②取少量无色溶液甲于试管中,滴加酚酞溶液,溶液不变色;
③继续向①的烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸质量的变化
如图所示。
(1)仅通过①可以得出的结论是:原白色固体中一定有______________;
(2)无色溶液甲中一定不存在的物质是_________(填字母)。
A.碳酸钠 B.硫酸钠 C.硝酸钡 D.氢氧化钠
【答案】 (1). Ba(NO ) (2). ABD
3 2
【解析】(1)加足量的水溶解,烧杯内有固体残留并得到无色溶液甲,说明了上述物质间发生反
应生成了沉淀,由于碳酸钠、硫酸钠都能与硝酸钡反应生成沉淀,由此可知,一定存在硝酸钡;
(2)②取少量无色溶液甲于试管中,滴加酚酞溶液,溶液不变色,说明溶液甲一定不含碳酸钠
和氢氧化钠,③继续向①的烧杯中滴加稀硝酸并不断搅拌,沉淀部分溶解,沉淀应为碳酸钡
和硫酸钡的混合物,若甲溶液中含有硫酸钠,加入稀硝酸,碳酸钡沉淀会转化为硫酸钡沉淀,
固体质量会增大,根据图示可知,甲溶液中一定没有硫酸钠。
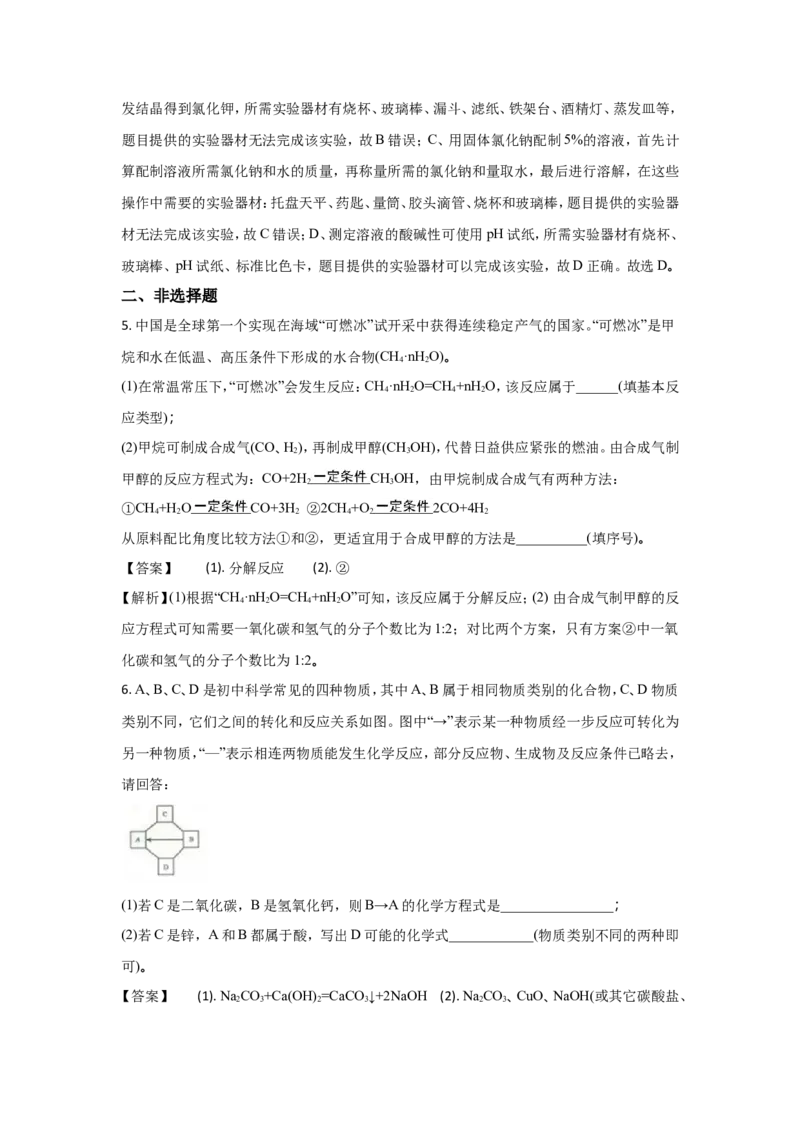
8. 某混合气体由CO、CO、SO 三种气体组成,某兴趣小组对此进行了相关实验:
2 2
【查阅资料】①SO 能使品红溶液褪色;②SO 易与高锰酸钾溶液反应而被吸收,并能使其褪
2 2
色;③SO 能使氢氧化钡溶液和澄清石灰水变浑浊;④CO和CO 均不能使品红溶液褪色,也
2 2
不与高锰酸钾溶液反应。
【实验研究】为验证这三种气体,同学们设计并进行如下实验:【事实与结论】通过实验验证了以上三种气体都存在
(1)装置A的作用是__________________;
(2)能证明气体中含有CO 的现象是______________________;
2
【反思与评价】
(3)若装置按C→D→A→B→E的顺序连接,则无法验证的气体是____________________;
(4)有同学提出上述原装置中省略D装置也能达到实验目的,你认为该同学的设计有无道理
并说明理由_____________________。
【答案】 (1). 检验并吸收二氧化硫,排除对二氧化碳的验证产生干扰 (2). B中品红不
褪色,C中溶液变浑浊 (3). CO、SO (4). 有道理,CO 气体对CO气体的实验没有干扰
2 2 2
【解析】(1) SO 易与高锰酸钾溶液反应而被吸收,并能使其褪色,SO 能使氢氧化钡溶液和澄
2 2
清石灰水变浑浊,装置A的作用是:检验并吸收二氧化硫,排除对二氧化碳的验证产生干扰;
(2)证明含有CO 的现象是B中品红溶液不褪色,C中溶液变浑浊;(3)若装置按
2
C→D→A→B→E的顺序连接,因为二氧化硫也能使石灰水变浑浊,因此二氧化碳和二氧化
硫都无法验证;(4) CO 气体对CO气体的实验没有干扰,故原装置中可以省略D装置。
2
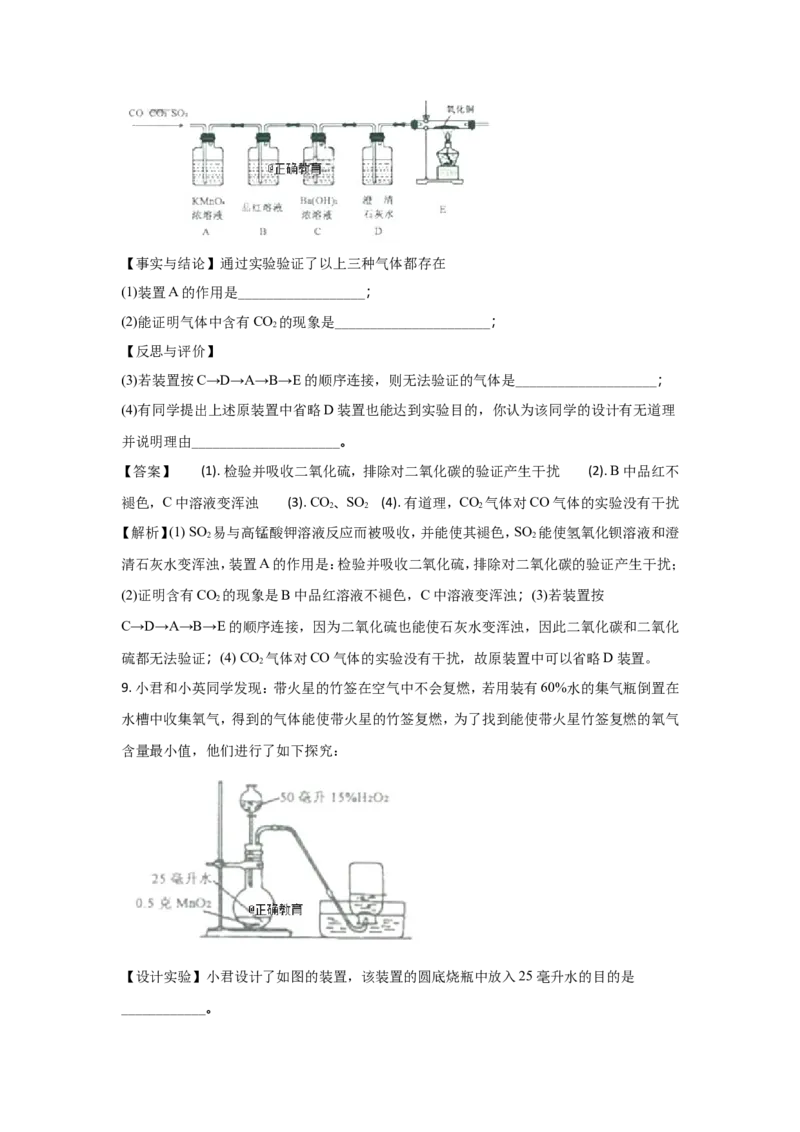
9. 小君和小英同学发现:带火星的竹签在空气中不会复燃,若用装有60%水的集气瓶倒置在
水槽中收集氧气,得到的气体能使带火星的竹签复燃,为了找到能使带火星竹签复燃的氧气
含量最小值,他们进行了如下探究:
【设计实验】小君设计了如图的装置,该装置的圆底烧瓶中放入25毫升水的目的是
____________。【实验研究】第一组实验:取3只集气瓶,编号为①②③,分别装入15%30%和45%的水,盖上
盖玻片倒置在水槽中。当气泡___________________放出后,导管口伸入集气瓶把其中的水
全部排出,将相同的3支带火星竹签分别插入①~③号瓶中,记录实验现象。
获得第一组实验现象后,小君又做了第二组实验,并记录实验现象,两组实验数据和现象见
下表:
实验分组 第一组 第二组
实验序号 ① ② ③ ④ ⑤ ⑥
集气瓶装水的体积分数/% 15 30 45 34 38 42
带火星竹签状况 亮 很亮 复燃 很亮 复燃 复燃
得出上述两组实验现象后,小英认为还不能确定能使带火星竹签复燃的氧气含量最小值,需
继续进行实验。则实验序号⑦的集气瓶装水的体积分数应该是_________%。
【实验结论】再经过数次实验并计算后得出:能使带火星竹签复燃的氧气含量最小值为
48.7%。
【继续探究】小君认为采用该方法收集的氧气中含有一定量的水蒸气,请你提出实验改进的
措施______________________。
【答案】 (1). 稀释过氧化氢溶液,减缓过氧化氢的分解速度 (2). 连续、均匀 (3). 36
(4). 收集氧气前增加气体的干燥装置,再用排油法收集氧气
【解析】【设计实验】据图可知,分液漏斗中是15%的过氧化氢溶液,浓度过大,会导致反应速
率太快,故圆底烧瓶中放入25毫升水的目的是稀释过氧化氢溶液,减缓过氧化氢的分解速
度;【实验研究】当导管口出现连续均匀的气泡时才开始收集;由第二组数据以及带火星竹签
的燃烧情况,可选择在34-38间的36作为第⑦;【继续探究】因为氧气不溶于油,浓硫酸等能
吸收水,故改进的措施:收集氧气前增加气体的干燥装置,再用排油法收集氧气。
10. 碳酸氢钠片是一种常用药,能用于治疗胃酸过多,这是因为人体的胃液中含有盐酸。已知:
NaHCO +HCl=NaCl+H O+CO↑,为测定药片中碳酸氢钠的含量,小科进行了如下实验:
3 2 2(1)小科认为,要测定药片中碳酸氢钠的含量,实验中需要采集两个数据:一是测出碳酸氢钠
片样品的质量;二是根据碳酸氢钠与盐酸的反应原理,通过实验测出反应生成的_______质
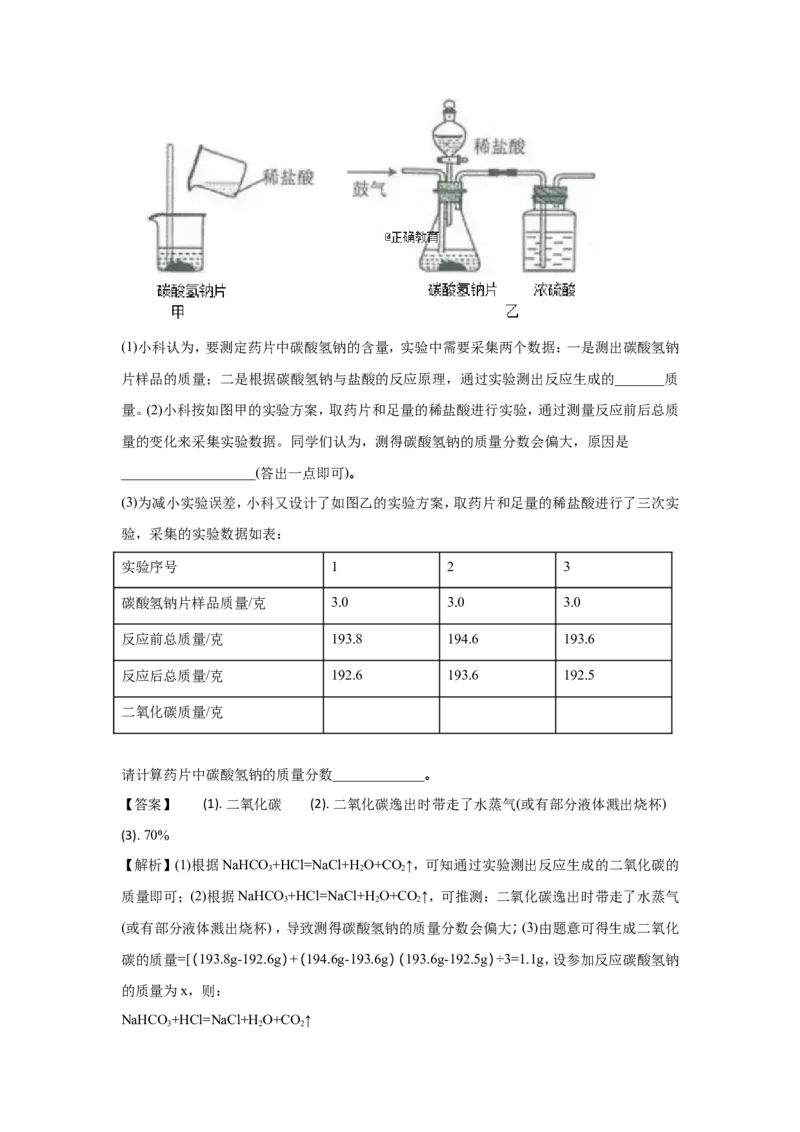
量。(2)小科按如图甲的实验方案,取药片和足量的稀盐酸进行实验,通过测量反应前后总质
量的变化来采集实验数据。同学们认为,测得碳酸氢钠的质量分数会偏大,原因是
___________________(答出一点即可)。
(3)为减小实验误差,小科又设计了如图乙的实验方案,取药片和足量的稀盐酸进行了三次实
验,采集的实验数据如表:
实验序号 1 2 3
碳酸氢钠片样品质量/克 3.0 3.0 3.0
反应前总质量/克 193.8 194.6 193.6
反应后总质量/克 192.6 193.6 192.5
二氧化碳质量/克
请计算药片中碳酸氢钠的质量分数_____________。
【答案】 (1). 二氧化碳 (2). 二氧化碳逸出时带走了水蒸气(或有部分液体溅出烧杯)
(3). 70%
【解析】(1)根据NaHCO +HCl=NaCl+H O+CO↑,可知通过实验测出反应生成的二氧化碳的
3 2 2
质量即可;(2)根据NaHCO +HCl=NaCl+H O+CO↑,可推测:二氧化碳逸出时带走了水蒸气
3 2 2
(或有部分液体溅出烧杯) ,导致测得碳酸氢钠的质量分数会偏大;(3)由题意可得生成二氧化
碳的质量=([ 193.8g-192.6g)+(194.6g-193.6g)(193.6g-192.5g)÷3=1.1g,设参加反应碳酸氢钠
的质量为x,则:
NaHCO +HCl=NaCl+H O+CO↑
3 2 284 44
x 1.1g
x=2.1g,
药片中碳酸氢钠的质量分数= 100%=70%。
11. 某拓展性学习小组在学校科学实验创新比赛中,做了一个有趣的实验,装置如图。
实验设计三颈烧瓶中充满二氧化碳气体,A颈、B颈分别连接充满氢氧化钠溶液和盐酸的注
射器,C颈插有两端开口的玻璃导管(伸入瓶内的一端连有小气球),装置气密性良好。
实验操作:先通过A颈往瓶内注入氢氧化钠溶液,观察到小气球的形状发生了变化;过一段
时间后再通过B颈往瓶中注入盐酸,发现小气球的形状又发生了改变。
请描述小气球形状的变化情况,并对此作出合理的解释。_________________________
【答案】小气球形状的变化情况:气球“先膨胀,后变瘪”(或“先变大,后变小”)