文档内容
第四章 物质结构 元素周期律
单元检测
一、选择题(本题包括16小题,每小题3分,共48分,每小题只有一个选项符合题意。)
1.(2022·辽宁大连·高一期末)下列说法不正确的是
A.道尔顿提出了原子学说,为近代化学的发展奠定了坚实的基础。
B.门捷列夫将元素按原子序数由小到大的顺序依次排列,制出了第一张元素周期表
C.我国化学家侯德榜发明了侯氏制碱法,为我国的化学工业发展和技术创新做出了重要贡献
D.我国科学家居呦呦因在研制青蒿素等抗疟药物方面的卓越贡献,被授予诺贝尔生理学或医学奖
2.(2022·浙江·高一期中)元素的原子结构决定其性质和在周期表中的位置。下列说法正确的是
A.元素原子的最外层电子数等于元素的最高化合价
B.元素核外电子排布时,先排满K层,再排L层,先排满M层,再排N层
C.P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强
D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
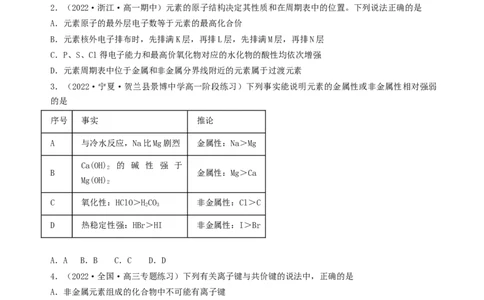
3.(2022·宁夏·贺兰县景博中学高一阶段练习)下列事实能说明元素的金属性或非金属性相对强弱
的是
序号 事实 推论
A 与冷水反应,Na比Mg剧烈 金属性:Na>Mg
Ca(OH) 的 碱 性 强 于
2
B 金属性:Mg>Ca
Mg(OH)
2
C 氧化性:HClO>HCO 非金属性:Cl>C
2 3
D 热稳定性强:HBr>HI 非金属性:I>Br
A.A B.B C.C D.D
4.(2022·全国·高三专题练习)下列有关离子键与共价键的说法中,正确的是
A.非金属元素组成的化合物中不可能有离子键
B.共价键通过原子之间得失电子形成
C.单质中一定没有离子键,一定有共价键
D.共价化合物中一定没有离子键
5.(2022·甘肃·武威十八中高一期中)下列各组微粒中微粒半径由大到小的是
A.N、P、Si、Al B.O2-、 F-、 Na+、 Mg2+
C.Al3+ 、 Mg2+、 K+ 、 Li+ D.F 、Cl、 Br、 I
6.(2022·云南省富源县第一中学高一期中)现有五种短周期主族元素a、b、c、d、e,它们最高(或
最低)化合价与原子半径的关系如图。下列有关说法错误的是
学科网(北京)股份有限公司A.a、e是同主族元素
B.最简单氢化物的稳定性:d>c
C.简单离子半径:d>c>b>e
D.d的一种氧化物能使溴水褪色
7.(2022·全国·高一课时练习)已知短周期主族元素X、Y、Z、W的原子序数依次增大,Y在周期表
中的周期数等于其族的序数,其在周期表的相对位置如下图所示。
X
Y Z W
下列说法正确的是A.W元素的原子半径,在同周期主族元素中是最小的
B.X元素原子的最高价为+6价
C.Z的原子序数是X的3倍
D.Y的氢氧化物化学式为Y(OH)
2
8.(2022·江苏·常州市平陵高级中学高三期中)氯化亚砜( )又称亚硫酰氯,常用作有机合成工
业中的氯化剂,遇水立即水解。下列说法正确的是
A.半径大小:
B.酸性:
C.热稳定性:
D. 水解生成 和HCl
9.(2022·河北·石家庄二中高二阶段练习)Q、X、Y、Z是原子序数依次增大的短周期主族元素,其
最外层电子数之和为19。Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电
子数的2倍。下列说法正确的是
A.非金属性:X>Q B.Y为铝
C.简单氢化物的沸点:Z>Q D.最高价含氧酸的酸性:Z>Y
10.(2022·上海市进才中学高一期中)下列说法正确的是
A.两种微粒的质子数和电子数都相等,不可能是一种分子和一种离子
B.质子数相同的微粒一定属于同一种元素
学科网(北京)股份有限公司C.一种元素只有一种质量数
D.由于同位素的质子数相同,所以性质相同
11.(2022·湖南常德·模拟预测)短周期主族元素X、Y、Z、W、M的原子序数依次递增。相邻元素
Y、Z位于同一周期且均具有多种常见气态氧化物。X分别与Y、Z可形成10个电子的分子。W的单质在空
气中燃烧发出耀眼白光。M原子最外层电子数是其K层电子数的3倍。下列有关说法正确的是
A.简单氢化物的稳定性:
B.W的最高价氧化物的水化物为强碱
C.X、Y、Z形成的化合物中可能含有极性键和非极性键
D.M在空气中燃烧的主要产物为
12.(2022·全国·高一课时练习)如图为某国外学术期刊上刊登的八角形元素周期表,八角形的每个顶角
对应一种元素,下列说法错误的是
A.图中虚线八角形所标元素属于我们现行元素周期表的第四周期
B.图中虚线箭头所经过的元素按箭头,原子的电子层数增多
C.图中①代表的元素单质在常温下能稳定存在,不发生化学反应
D.此八角形元素周期表中所表示的所有元素中没有副族元素
13.(广东省韶关市等4地深圳实验学校高中部等5校2022-2023学年高三上学期11月期中考试化学试
题)某化合物的结构如图所示,其中X、Y、Z、Q、W为原子序数依次增大的五种短周期元素,Q核外最外
层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小的,下列叙述正确的是
A.WX溶于水后溶液呈中性 B.氧化物沸点;Y>Z
C.Z的氧化物对应的水化物是一元强酸 D.X、Y、Z、W均能和Q形成两种或两种以上化合物
14.(2022·河南·南阳市第六完全学校高级中学高一阶段练习)下列各表为周期表的一部分(表中数
字为原子序数),其中正确的是
学科网(北京)股份有限公司A. B.
C. D.
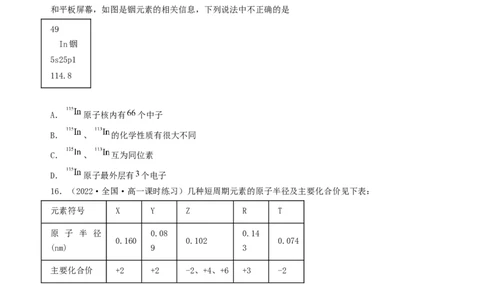
15.(2022·四川·广安育才学校高一阶段练习)稀有金属铟由于其良好的性能常用于生产液晶显示器
和平板屏幕,如图是铟元素的相关信息,下列说法中不正确的是
49
In铟
5s25p1
114.8
A. 原子核内有 个中子
B. 、 的化学性质有很大不同
C. 、 互为同位素
D. 原子最外层有 个电子
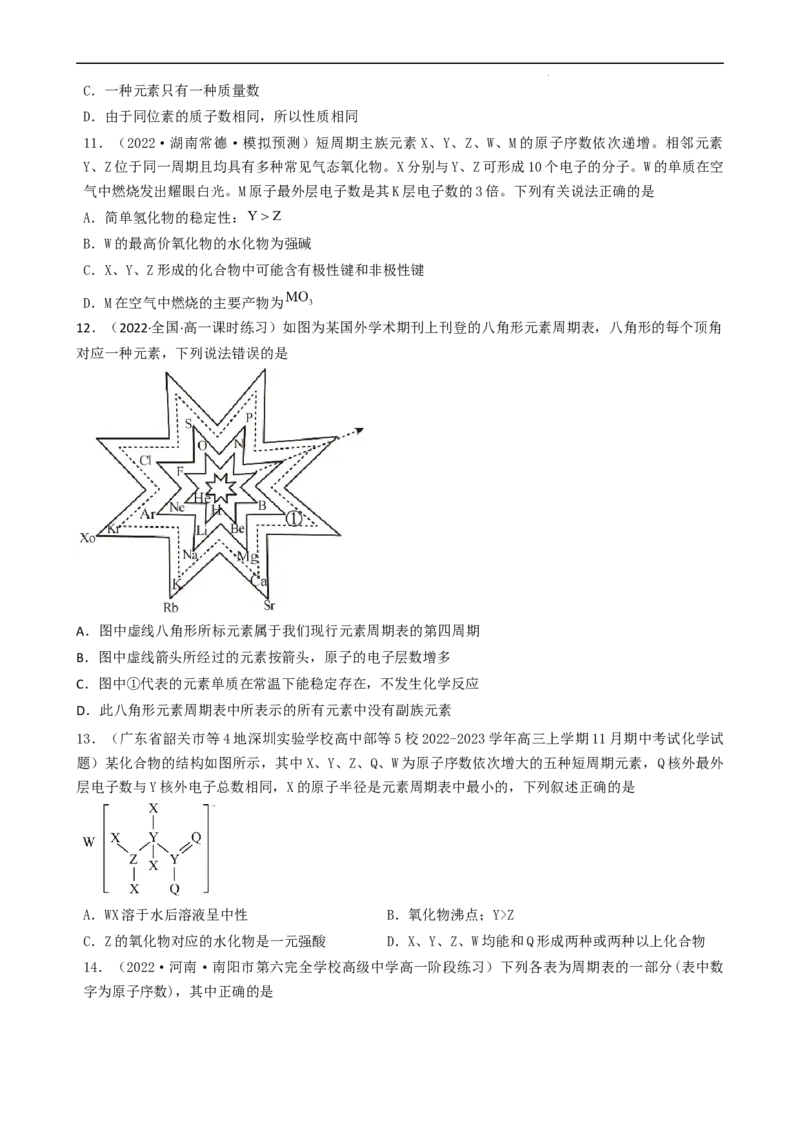
16.(2022·全国·高一课时练习)几种短周期元素的原子半径及主要化合价见下表:
元素符号 X Y Z R T
原 子 半 径 0.08 0.14
0.160 0.102 0.074
(nm) 9 3
主要化合价 +2 +2 -2、+4、+6 +3 -2
根据表中信息,判断以下说法正确的是A.单质与稀硫酸反应的剧烈程度:R>Y>X
B.离子半径:X2+>R3+>T2-
C.最高价氧化物水化物的碱性:R>X
D.相同条件下,简单气态氢化物的稳定性:T>Z
二、非选择题(本题包括4小题,共52分)
17.(2022·全国·高一课时练习)以下是四种粒子的结构示意图:
A. B. C. D.
学科网(北京)股份有限公司(1)上述粒子中氧化性最强的元素是_______(填序号),将它的单质通入 KI 溶液的化学方程式为
_______。
(2)D的单质与NaOH溶液发生反应的离子方程式为_______。
(3)电子层结构与C相同,化学性质最稳定的元素原子的核电荷数是_______,用原子结构与元素性质的
关系说明它化学性质稳定的原因_______。
(4)A的一种同位素可用于考古断代,这种同位素的符号是_______,这种用途取决于它的_______性。
18.(2022·陕西·延安市第一中学高一期中)现有部分短周期元素的性质或原子结构如表:
元素编号 元素的性质或原子结构
T M层上有6个电子
X 最外层电子数是次外层电子数的2倍
Y 常温下单质为双原子分子,其氢化物的水溶液呈碱性
Z 元素的最高正化合价是+7价
(1)元素X的一种核素可用于测定文物年代,这种核素的符号是_______。
(2)元素Y与氢元素形成一种离子YH ,写出某溶液中含该微粒的检验方法:_______。
(3)元素Z与元素T相比,原子得电子能力较强的是_______(用元素符号表示),下列表述中能证明这一
事实的是_______(填序号)。
①常温下Z的单质和T的单质状态不同 ;
②Z的氢化物比T的氢化物稳定
③一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物对应的水化物
中化学性质明显不同于其他三种的是_______(填化学式),理由是_______。
19.(2022·黑龙江·穆棱市第二中学高一期末)元素X、Y、Z、M、R均为短周期主族元素,且原子序
数依次增大。已知:Y为地壳中含量最多的元素;M原子的最外层电子数与次外层电子数之比为 3:4;
R-、Z+、X+的离子半径逐渐减小;化合物XR常温下为气体。请回答下列问题:
(1)M元素周期表中的位置为____;Z+的结构示意图为____。
(2)写出X、Y、R按原子个数之比1:1:1形成的化合物的电子式:____。
(3)X与Y可分别形成10电子分子和18电子分子,写出18电子分子转化成10电子分子的化学方程式:
____。
(4)R的非金属性强于M的,下列能证明这一事实的是____(填字母)。
A.常温下的R单质熔沸点比M单质的高
B.R的简单氢化物比M的更稳定
C.一定条件下,R和M的单质都能与NaOH溶液反应
D.最高价氧化物对应水化物的酸性强弱:R>M
20.(2021·河北·沧州市一中高一开学考试)为了庆祝元素周期表诞生150周年,联合国将2019年定
学科网(北京)股份有限公司为“国际化学元素周期表年”。元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学
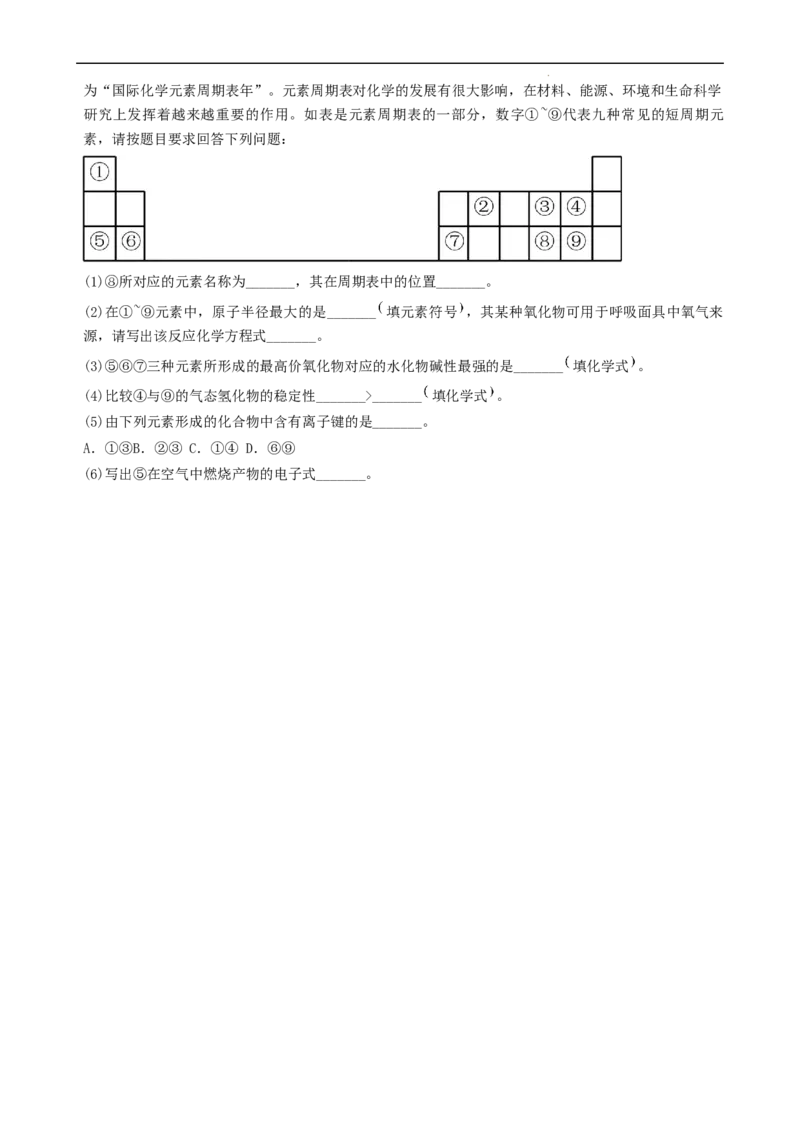
研究上发挥着越来越重要的作用。如表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元
素,请按题目要求回答下列问题:
(1)⑧所对应的元素名称为_______,其在周期表中的位置_______。
(2)在①~⑨元素中,原子半径最大的是_______ 填元素符号 ,其某种氧化物可用于呼吸面具中氧气来
源,请写出该反应化学方程式_______。
(3)⑤⑥⑦三种元素所形成的最高价氧化物对应的水化物碱性最强的是_______ 填化学式 。
(4)比较④与⑨的气态氢化物的稳定性_______>_______ 填化学式 。
(5)由下列元素形成的化合物中含有离子键的是_______。
A.①③B.②③ C.①④ D.⑥⑨
(6)写出⑤在空气中燃烧产物的电子式_______。
学科网(北京)股份有限公司学科网(北京)股份有限公司