文档内容
第7讲 盐 化学肥料
命题点1 常见的盐的性质和用途
1.(2017·扬州)下列物质属于盐的是()
A.Fe B.CuO
C.NaCO D.HSO
2 3 2 4
2.(2017·长沙)下列盐的用途中,错误的是()
A.用含亚硝酸钠的工业盐制香肠
B.用碳酸钙做补钙剂
C.用氯化钠配制生理盐水
D.用碳酸氢钠做焙制糕点的发酵粉
3.(2017·广东)下图为××泡打粉的标签示意图,下列说法错误的是()
A.碳酸氢钠俗称小苏打
B.泡打粉可以随意放置
C.加入泡打粉制作的蛋糕更松软
D.面粉是有机物,碳酸盐是无机物
命题点2 复分解反应及其应用
4.(2017·株洲)我国制碱工业的先驱——侯德榜先生,1921年留美回国后,潜心研究制碱技术,发明了将制碱与
制氨结合起来的联合制碱法(又称侯氏制碱法),为纯碱和氮肥工业技术的发展做出了杰出贡献。下列物质中能与纯碱
发生反应的是()
A.NaOH B.NaHCO C.HSO D.KSO
3 2 4 2 4
5.(2017·菏泽)下列物质在水溶液中能大量共存的是()
A.NaCl NaCO HSO
2 3 2 4
B.CuSO KNO NaSO
4 3 2 4
C.BaCl NaOH NaCO
2 2 3
D.HCl NaSO NaOH
2 4
6.(2017·天水)下列各组物质加入水中充分搅拌后,同组反应物恰好完全反应,过滤后,在滤纸上留下两种不溶物
质的是()
A.Ca(NO )、BaCl 、AgNO
3 2 2 3
B.MgCl 、KOH、NaCl
2
C.KCO、CuSO 、KCl
2 3 4
D.CuSO 、Ba(OH) 、Cu(NO )
4 2 3 2
命题点3 化学肥料
7.(2017·扬州)下列物质可用作氮肥的是()
A.KSO B.Ca (PO ) C.NH HCO D.NaCl
2 4 3 4 2 4 3
8.(2017·临沂)农作物种植过程中可以施用下列化肥,其中属于复合肥的是()
A.NH NO B.KNO C.Ca(HPO ) D.CO(NH )
4 3 3 2 4 2 2 2
9.(2017·河北)下列对化肥的认识不正确的是()
A.KNO 是一种复合肥
3
B.施用氮肥,能促进植物茎叶生长
C.铵态氮肥不能与碱性肥料混合使用D.化肥能提高粮食产量,施用越多越好
命题点4 粗盐中难溶性杂质的去除
10.(2017·绍兴)以粗盐(含杂质NaSO 、MgCl 、CaCl 、泥沙)为原料制备精盐。
2 4 2 2
(1)加水溶解后,用如图装置除去粗盐中的泥沙,玻璃棒的作用是______。
(2)为除去NaSO 、MgCl 、CaCl ,并得到中性的食盐溶液,下列所加试剂和操作:①加过量的NaCO 溶液,②过
2 4 2 2 2 3
滤,③加过量的NaOH溶液,④加适量的稀HCl,⑤加过量的BaCl 溶液,能达到目的的顺序是________。
2
A.⑤③②①④ B.③⑤①④②
C.③⑤①②④
(3)用pH试纸检验溶液是否呈中性的操作是_________________________________________________________。
重难点1 盐的化学性质
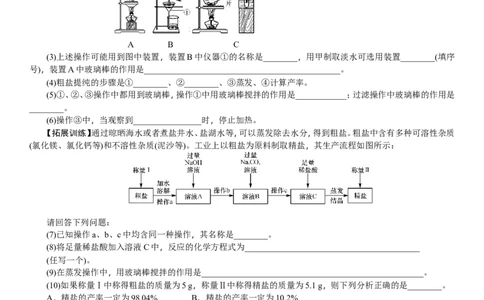
如图是可以与碳酸钾反应的一些物质(—表示可以相互反应),回答下列问题。
(1)向KCO 溶液中滴加无色酚酞溶液,溶液为________(填“红色”或“无色”)。
2 3
(2)写出盐酸与KCO 溶液发生反应的化学方程式________________________________。
2 3
(3)写出KCO 溶液与Ca(OH) 溶液发生反应的化学方程式__________________________________,如果将
2 3 2
KCO 换成CaCO 该反应________(填“可以”或“不可以”)发生。
2 3 3
(4)K CO 溶液与CaCl 溶液发生反应的现象为_______________________________________________________。
2 3 2
(5)金属盐溶液还有一条特殊的性质是可以与活泼金属发生置换反应,写出铁与硫酸铜溶液发生反应的化学方程
式:____________________,反应后溶液的质量________(填“增加”或“减小”)。
重难点2 复分解反应及其应用
现有甲、乙、丙、丁四种无色溶液,它们分别是稀HCl、稀HSO 、BaCl 溶液、NaCO 溶液中的一种,已知
2 4 2 2 3
甲+乙→无明显现象,乙+丙→白色沉淀,丙+丁→白色沉淀,甲+丁→无色气体;BaCO 、BaSO 难溶于水。试回答:
3 4
(1)丁物质中的溶质是________(填化学式)。
(2)写出乙和丙反应的化学方程式___________________________________________________。
(3)写出甲和丁反应的化学方程式___________________________________________________,该反应属于
________________(填基本反应类型)。
(2017·苏州)下列各组离子在水溶液中能大量共存的是()
A.Cu2+、Na+、NO、OH- B.H+、K+、CO、Cl-
C.Mg2+、NH、OH-、SO D.Na+、Ca2+、NO、Cl-
(2016·兰州)下列物质之间的转化,经过一步反应不能实现的是()
A.CuCl →KCl B.KNO→KSO C.Fe(OH) →Fe (SO ) D.BaCl →BaCO
2 3 2 4 3 2 4 3 2 3
(2017·广州)下列除杂所选用试剂与操作方法均正确的是()
选项 物质(括号内为杂质) 除杂试剂 实验操作
A CaO(CaCO) 水 溶解、过滤
3B H(CO) 灼热CuO 洗气
2
C NaCl(Na SO ) 过量BaCl 溶液 过滤
2 4 2
D NaCl(Na CO) 足量稀盐酸 蒸发结晶
2 3
实验突破 粗盐中难溶性杂质的去除
(2016·重庆B卷)工业上用海水获取粗盐以及实验室用粗盐制得精盐都包含许多化学实验知识,分析以下过
程后填写下列空白:
(1)操作Ⅰ的名称是________。
(2)海水晒盐与下列操作中________的原理相同。
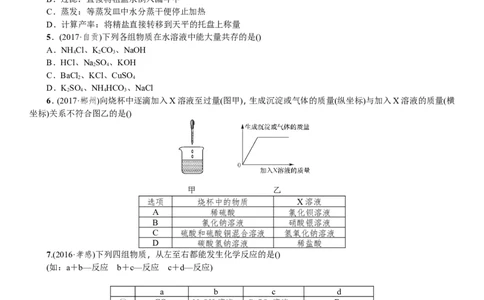
A B C
(3)上述操作可能用到图中装置,装置B中仪器①的名称是________,用甲制取淡水可选用装置________(填序
号),装置A中玻璃棒的作用是______________________________________________。
(4)粗盐提纯的步骤是①________、②________、③蒸发、④计算产率。
(5)①、②、③操作中都用到玻璃棒,操作①中用玻璃棒搅拌的作用是____________;过滤操作中玻璃棒的作用是
________。
(6)操作③中,当观察到________________时,停止加热。
【拓展训练】通过晾晒海水或者煮盐井水、盐湖水等,可以蒸发除去水分,得到粗盐。粗盐中含有多种可溶性杂质
(氯化镁、氯化钙等)和不溶性杂质(泥沙等)。工业上以粗盐为原料制取精盐,其生产流程如图所示:
请回答下列问题:
(7)已知操作a、b、c中均含同一种操作,其名称是________。
(8)将足量稀盐酸加入溶液C中,反应的化学方程式为_________________________________________
(任写一个)。
(9)在蒸发操作中,用玻璃棒搅拌的作用是____________________________________________________。
(10)如果称量Ⅰ中称得粗盐的质量为5 g,称量Ⅱ中称得精盐的质量为5.1 g,则下列分析正确的是________。
A.精盐的产率一定为98.04% B.精盐的产率一定为10.2%
C.蒸发操作中可能有水分没有蒸干 D.溶解操作中可能有粗盐没有溶解
E.除杂过程中有NaCl生成
1.(2017·襄阳)硝酸钾(KNO)是一种能使农作物增产的常用化肥。它属于()
3
A.复合肥 B.氮肥
C.磷肥 D.钾肥
2.(2017·青岛)物质的性质与用途密切相关。下列做法不合理的是()
A.工业上用稀盐酸除铁锈B.农业上用熟石灰改良酸性土壤
C.碳酸钠用于玻璃、造纸、洗涤剂的生产
D.水壶中的水垢(主要成分是碳酸钙和氢氧化镁)用水清洗
3.(2017·重庆B卷)氯化铵(NH Cl)是“侯氏制碱法”的一种副产品。已知氯化铵的水溶液显酸性,下列关于氯化
4
铵的说法正确的是()
A.氯化铵属于酸
B.氯化铵是一种复合肥
C.氯化铵与熟石灰混合使用可提高肥效
D.氯化铵溶液与硝酸银溶液混合会产生白色沉淀
4.(2017·邵阳)在“粗盐中难溶性杂质的去除”实验中,操作步骤为:溶解、过滤、蒸发、计算产率。下列各步骤中
的一些做法正确的是()
A.溶解:用玻璃棒搅拌以加速溶解
B.过滤:直接将粗盐水倒入漏斗中
C.蒸发:等蒸发皿中水分蒸干便停止加热
D.计算产率:将精盐直接转移到天平的托盘上称量
5.(2017·自贡)下列各组物质在水溶液中能大量共存的是()
A.NH Cl、KCO、NaOH
4 2 3
B.HCl、NaSO 、KOH
2 4
C.BaCl 、KCl、CuSO
2 4
D.KSO 、NH HCO 、NaCl
2 4 4 3
6.(2017·郴州)向烧杯中逐滴加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横
坐标)关系不符合图乙的是()
甲 乙
选项 烧杯中的物质 X溶液
A 稀硫酸 氯化钡溶液
B 氯化钠溶液 硝酸银溶液
C 硫酸和硫酸铜混合溶液 氢氧化钠溶液
D 碳酸氢钠溶液 稀盐酸
7.(2016·孝感)下列四组物质,从左至右都能发生化学反应的是()
(如:a+b—反应 b+c—反应 c+d—反应)
a b c d
① CO NaOH溶液 CuSO 溶液 Fe
2 4
② 稀盐酸 NaCO 溶液 CaCl 溶液 CO
2 3 2 2
③ AgNO 溶液 BaCl 溶液 稀硫酸 Fe O
3 2 2 3
④ Zn 稀盐酸 NH NO 溶液 Ca(OH) 溶液
4 3 2
A.①②③ B.①③④
C.①③ D.①②③④
8.(2017·广州)向KCO 溶液中滴入Ba(OH) 溶液至恰好完全反应。
2 3 2
(1)可以观察到的实验现象是______________________________________________________。
(2)如图表示该反应前后溶液中存在的主要离子,写出每种图形代表的离子。(填离子符号)________ ________ ________
(3)下列物质能与KCO 溶液反应产生类似上述实验现象的是________。
2 3
A.Ca(OH) B.HCl C.BaCl D.(NH )SO
2 2 4 2 4
9.(2017·上海)提纯含少量泥沙的粗盐样品,实验过程和氯化钠的溶解度数据如下:
温度(℃) 溶解度(g/100 g水)
20 36.0
40 36.6
60 37.3
(1)20 ℃时氯化钠的溶解度是__________g/100 g水。
(2)该实验是利用泥沙难溶于水而氯化钠________的性质进行提纯,操作Ⅲ的名称是________。
(3)关于蒸发叙述正确的是________(填编号)。
A.蒸发是通过加热的方法将水汽化除去
B.所需仪器为酒精灯、蒸发皿、温度计
C.搅拌可以防止蒸发过程中食盐飞溅
D.加热过程中用试管夹夹住蒸发皿移动,使其均匀受热
(4) 溶 解 时 , 加 入 水 的 合 适 的 量 约 为 ________mL( 填 “ 15”“30” 或 “ 60”) , 理 由 是
_______________________________________________________________________。
10.(2016·资阳)下图中各组物质(或溶液)反应均可生成盐(中心圈)。
(1)分析图中信息,填写相应的文字,完善该图。
①________;②________________。
(2)列举相应的化学方程式说明①②:
①________________________________________________________________________;
②________________________________________________________________________。
11.(2017·丽水)BaCl 是一种重金属盐,其水溶液具有很强的毒性。若误服了BaCl 溶液可立即服用MgSO 溶液
2 2 4
解毒。为测定某BaCl 溶液的溶质质量分数,现取100克BaCl 溶液,不断加入MgSO 溶液,反应过程中溶液总质量与
2 2 4
加入MgSO 溶液的质量关系如图所示,请回答:
4(1)P点时溶液中的溶质名称是________;
(2)反应生成沉淀的最大质量为________克;
(3)求原BaCl 溶液的溶质质量分数。
2
12.(2017·青岛)为除去粗盐中含有的氯化镁、硫酸钠、氯化钙等杂质,应加入过量的氢氧化钠、氯化钡、碳酸钠等
物质,将杂质转化为沉淀。过滤去除沉淀后,再向滤液中加入适量的盐酸得到精盐水。实验操作过程如下图所示:
下列说法错误的是()
A.实验操作步骤也可以是①③④②⑤⑥
B.操作⑥中,加入盐酸的目的是除去过量的氢氧化钠和碳酸钠,将滤液的pH调为7
C.在实验操作过程中,氯化钡和碳酸钠溶液的添加顺序可以颠倒
D.操作⑤得到的沉淀中共有四种物质
13.(2017·泰安)下列各组变化中,每个转化在一定条件下均能一步实现的是()
①) ② ③) ④
A.①④ B.①②④ C.①③④ D.①②③④
14.(2017·菏泽)下列初中化学常见的几种物质相互转化关系图,其中B为黑色固体,N为蓝色沉淀,其中部分生
成物和反应条件已略去。
请回答:
(1)D的化学式为________。
(2)B→A的化学方程式为________________________________________________________________________。
(3)C和F反应的化学方程式为________________________________,其基本反应类型为________________。
15.(2017·金华)有一包白色固体样品,可能含碳酸钠、硫酸钠、氯化钠、氢氧化钠中的一种或几种。小科同学为探
究其成分做了以下实验:
Ⅰ.取少量固体样品于烧杯中,先加足量水溶解,再加入足量的BaCl 溶液,有白色沉淀产生;
2
Ⅱ.继续向烧杯中滴加稀盐酸并不断搅拌,烧杯内固体质量随加入稀盐酸质量的变化如图所示。请回答下列问题:
(1)AB段观察到的现象是________________________________________________________________________。
(2)C点时,溶液中一定含有的溶质是____________________。
16.(2017·菏泽)实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如下图),化学小组的同学经过询问老
师后只知道是NaCl、NaOH、NaCO、NaHCO 中的一种溶液,为确认原瓶中是何种溶质并判断其是否变质,化学小组
2 3 3
的同学进行了如下的探究活动:
【进行猜想】
猜想Ⅰ:原溶液的溶质是NaCl;
猜想Ⅱ:原溶液的溶质是NaOH;
猜想Ⅲ:原溶液的溶质是NaCO;
2 3
猜想Ⅳ:原溶液的溶质是NaHCO 。
3
【查阅资料】
常温下,有关物质的相关信息如下表:
物质 NaCl NaOH NaCO NaHCO
2 3 3
常温下的溶解度/g 36 109 21.5 9.6
常温下稀溶液的pH 7 13 11 9
从物质的相关信息可知,原溶液的溶质一定不是NaHCO ,因为_________________________________________。
3
【进行实验】
(1)取少量样品,测得溶液的pH大于7,则原溶液的溶质肯定不是________。
(2)同学们另取样品又进行了如下实验,实验过程如下:
①生成白色沉淀A的化学方程式________________________________。
②通过实验可以判断样品无色溶液中含有的溶质有________________。
【获得结论】
实验完成后,最终得到的结论:原瓶中的溶质是________,且已变质。
参考答案
第7讲 盐 化学肥料
中考真题展
1.C 2.A 3.B 4.C 5.B 6.D 7.C 8.B 9.D 10.(1)引流 (2)C(3)用洁净的玻璃棒蘸取少量溶液,滴在pH
试纸上,显示的颜色与标准比色卡对照
导学提分训练
例1 (1)红色 (2)K CO +2HCl===2KCl+HO+CO↑ (3)K CO +Ca(OH) ===CaCO ↓+2KOH 不可以
2 3 2 2 2 3 2 3
(4)有白色沉淀生成 (5)Fe+CuSO ===FeSO +Cu 减小 例2 (1)Na CO (2)H SO +BaCl ===2HCl+BaSO↓
4 4 2 3 2 4 2 4
(3)2HCl+NaCO===2NaCl+HO+CO↑ 复分解反应 例3 D 例4 B 例5 D 例6 (1)溶解 (2)A (3)
2 3 2 2漏斗 C 搅拌,防止液滴受热不均匀,造成液滴飞溅 (4)溶解 过滤 (5)加速溶解 引流 (6)出现较多固体 (7)
过滤 (8)NaOH+HCl===NaCl+HO (9)使液体受热均匀,防止局部过热造成液滴飞溅 (10)CE
2
课后提分训练
1.A 2.D 3.D 4.A 5.D 6.C 7.C 8.(1)有白色沉淀生成 (2)K+ CO OH- (3)AC 9.(1)36.0 (2)易溶
于水 过滤 (3)AC (4)30 20 ℃时,氯化钠的溶解度为36 g/100 g水,实验中称取的粗盐质量为10 g,加入约30
mL水既可使粗盐中的氯化钠充分溶解,又不会因加水过多而影响后续蒸发操作的效率。 10.(1)①酸(金属) ②碱;
非金属氧化物 (2)①HCl+AgNO===AgCl↓+HNO ②2NaOH+CO===Na CO+HO 11.(1)氯化镁 (2)23.3
3 3 2 2 3 2
(3)设原BaCl 溶液的溶质质量分数为x。
2
BaCl +MgSO ===BaSO ↓+MgCl
2 4 4 2
208 233
100 g×x 23.3 g
= x=20.8%
答:原BaCl 溶液的溶质质量分数为20.8%。
2
12.C 13.A 14.(1)CaO (2)CuO+CO=====Cu+CO (3)2NaOH+CuSO ===Cu(OH) ↓+NaSO 复分解反
2 4 2 2 4
应 15.(1)固体部分溶解并有气泡产生 (2)NaCl、BaCl 、HCl 16【. 查阅资料】常温下,碳酸氢钠的溶解度是9.6 g,不
2
可能得溶质质量分数为 10%的溶液 【进行实验】(1)氯化钠 (2)①CaCl +NaCO===CaCO ↓+2NaCl
2 2 3 3
②NaCO、NaOH 【获得结论】NaOH
2 3