文档内容
广州市执信中学 2023 届高三年级第二次月考
化 学
本试卷分选择题和非选择题两部分,共8页,满分为100分。考试用时75分钟。
注意事项:
1.答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名和学号填写在答题卡和
答卷密封线内相应的位置上,用2B铅笔将自己的学号填涂在答题卡上。
2.选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;如需改
动,用橡皮擦干净后,再选涂其他答案;不能答在试卷上。
3.非选择题必须用黑色字迹的钢笔或签字笔在答卷纸上作答,答案必须写在答卷纸各
题目指定区域内的相应位置上,超出指定区域的答案无效;如需改动,先划掉原来的答案,
然后再写上新的答案;不准使用铅笔和涂改液。不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁和平整。
可能用到的相对原子质量H l C 12 N 14 O 16 Ti 48
第一部分 选择题(共44分)
一、选择题:本题共16个小题,共44分。第1-10小题,每小题2分;第11-16小题,每小
题4分。在每小题给出的四个选项中,只有一个选项符合题目要求的。
1.2022年北京冬奥会火炬“飞扬”以耐高温碳纤维材料为外壳,铝合金为点火段材料,氢
气为燃料,辅以可调节火焰颜色的“配方”。下列说法正确的是( )
A.碳纤维属于天然高分子材料 B.氢气作燃料对环境友好无污染
C.铝合金密度小、硬度小、耐腐蚀 D.含钾元素的“配方”可使火焰呈黄色
2.第130届广交会助力乡村振兴,参展的商品有竹制品、丝绸、药酒、蜂蜜等。下列说法不
正确的是( )
A.竹子富含纤维素 B.蚕丝是蛋白质纤维
C.酿酒过程淀粉直接转化乙醇 D.蜂蜜中的葡萄糖和果糖都属于单糖
3.下列说法正确的是( )
A.同一原子中,在离核较远的区域运动的电子能量较高
B.原子核外电子排布,先排满K层再排L层、先排满M层再排N层
C.同一周期中,随着核电荷数的增加,元素的原子半径逐渐增大
D.同一周期中,ⅡA与ⅢA族元素原子的核电荷数都相差1
4.下列有关砷元素及其化合物的说法正确的是( )
A.基态As的电子排布式为[Ar]4s24p3 B.灰砷、黑砷和黄砷是砷的同素异形体
C.AsH 在同族简单氢化物中沸点最高 D.第一电离能:I(Ge)H PO B.电负.性:SH O D.熔点:金刚石>硅
2 2
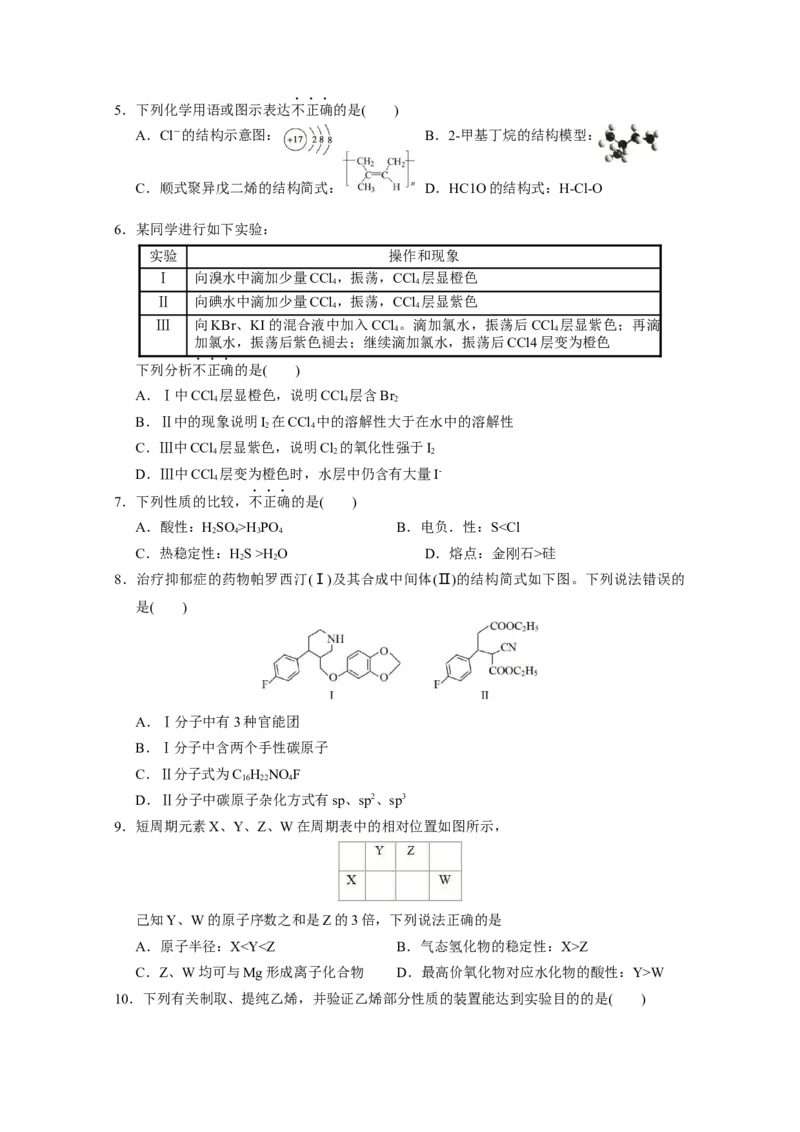
8.治疗抑郁症的药物帕罗西汀(Ⅰ)及其合成中间体(Ⅱ)的结构简式如下图。下列说法错误的
是( )
A.Ⅰ分子中有3种官能团
B.Ⅰ分子中含两个手性碳原子
C.Ⅱ分子式为C H NOF
16 22 4
D.Ⅱ分子中碳原子杂化方式有sp、sp2、sp3
9.短周期元素X、Y、Z、W在周期表中的相对位置如图所示,
己知Y、W的原子序数之和是Z的3倍,下列说法正确的是
A.原子半径:XZ
C.Z、W均可与Mg形成离子化合物 D.最高价氧化物对应水化物的酸性:Y>W
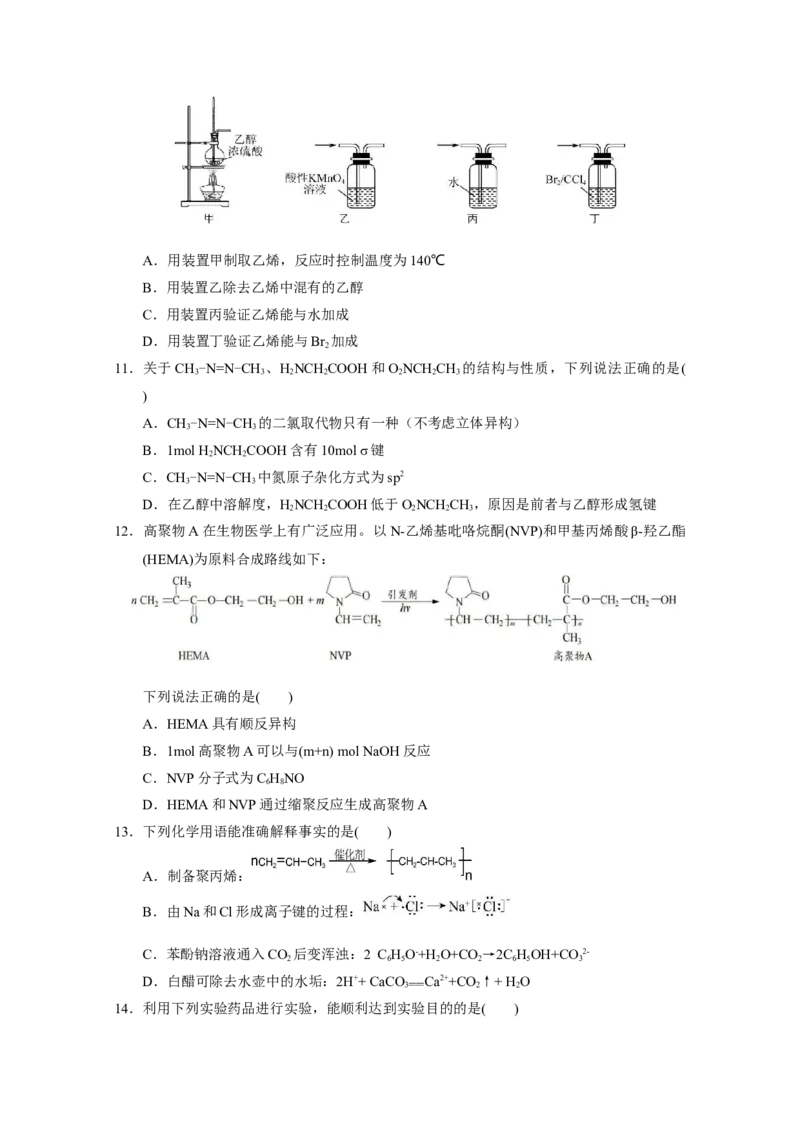
10.下列有关制取、提纯乙烯,并验证乙烯部分性质的装置能达到实验目的的是( )A.用装置甲制取乙烯,反应时控制温度为140℃
B.用装置乙除去乙烯中混有的乙醇
C.用装置丙验证乙烯能与水加成
D.用装置丁验证乙烯能与Br 加成
2
11.关于CH-N=N-CH 、HNCH COOH和ONCH CH 的结构与性质,下列说法正确的是(
3 3 2 2 2 2 3
)
A.CH-N=N-CH 的二氯取代物只有一种(不考虑立体异构)
3 3
B.1mol HNCH COOH含有10mol σ键
2 2
C.CH-N=N-CH 中氮原子杂化方式为sp2
3 3
D.在乙醇中溶解度,HNCH COOH低于ONCH CH,原因是前者与乙醇形成氢键
2 2 2 2 3
12.高聚物A在生物医学上有广泛应用。以N-乙烯基吡咯烷酮(NVP)和甲基丙烯酸β-羟乙酯
(HEMA)为原料合成路线如下:
下列说法正确的是( )
A.HEMA具有顺反异构
B.1mol高聚物A可以与(m+n) mol NaOH反应
C.NVP分子式为C HNO
6 8
D.HEMA和NVP通过缩聚反应生成高聚物A
13.下列化学用语能准确解释事实的是( )
A.制备聚丙烯:
B.由Na和Cl形成离子键的过程:
C.苯酚钠溶液通入CO 后变浑浊:2 C HO-+H O+CO→2C HOH+CO2-
2 6 5 2 2 6 5 3
D.白醋可除去水壶中的水垢:2H++ CaCO Ca2++CO↑+ H O
3 2 2
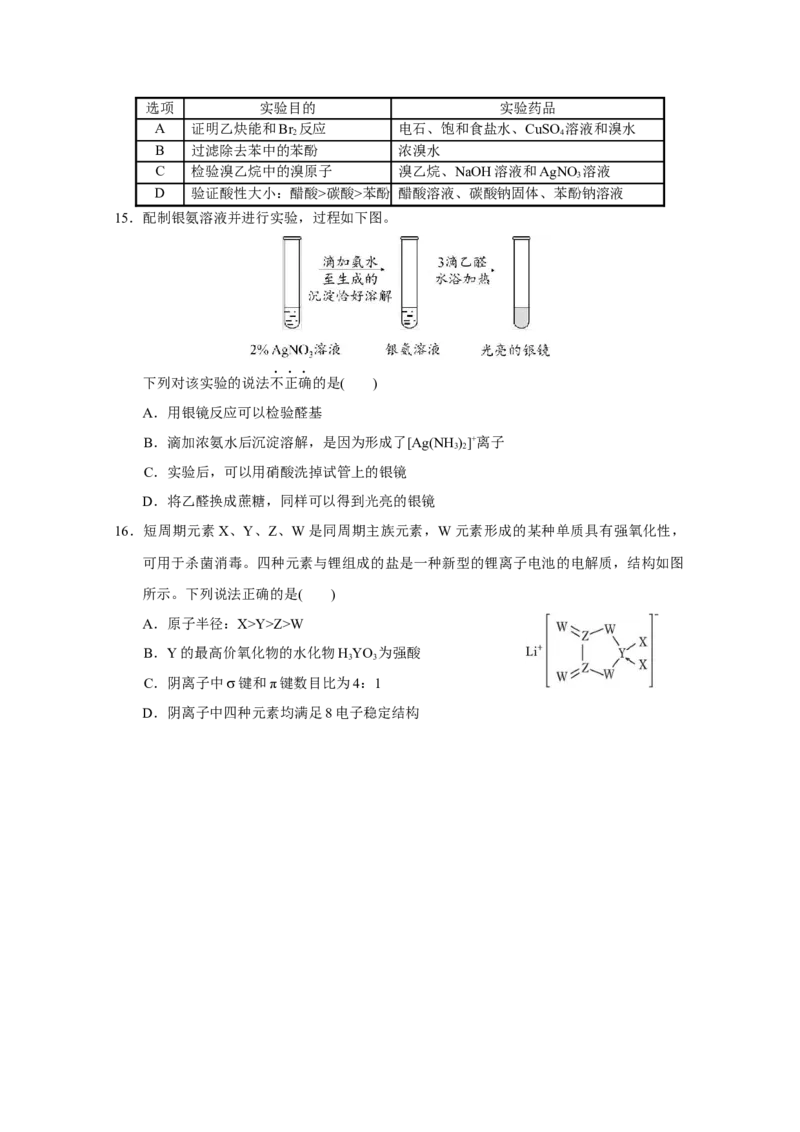
14.利用下列实验药品进行实验,能顺利达到实验目的的是( )选项 实验目的 实验药品
A 证明乙炔能和Br 反应 电石、饱和食盐水、CuSO 溶液和溴水
2 4
B 过滤除去苯中的苯酚 浓溴水
C 检验溴乙烷中的溴原子 溴乙烷、NaOH溶液和AgNO 溶液
3
D 验证酸性大小:醋酸>碳酸>苯酚 醋酸溶液、碳酸钠固体、苯酚钠溶液
15.配制银氨溶液并进行实验,过程如下图。
下列对该实验的说法不正确的是( )
A.用银镜反应可以检验醛基
B.滴加浓氨水后沉淀溶解,是因为形成了[Ag(NH)]+离子
3 2
C.实验后,可以用硝酸洗掉试管上的银镜
D.将乙醛换成蔗糖,同样可以得到光亮的银镜
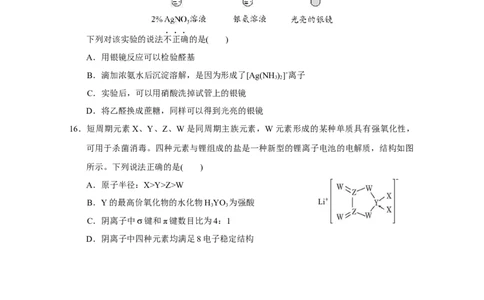
16.短周期元素X、Y、Z、W是同周期主族元素,W元素形成的某种单质具有强氧化性,
可用于杀菌消毒。四种元素与锂组成的盐是一种新型的锂离子电池的电解质,结构如图
所示。下列说法正确的是( )
A.原子半径:X>Y>Z>W
B.Y的最高价氧化物的水化物HYO 为强酸
3 3
C.阴离子中σ键和π键数目比为4:1
D.阴离子中四种元素均满足8电子稳定结构第二部分 非选择题(共56分)
17 (14分)醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:
可能用到的有关数据如下:
相对分子质量 密度/(g·cm-3) 沸点/℃ 溶解性
环己醇 100 0.9618 161 微溶于水
环己烯 82 0.8102 83 难溶于水
合成反应:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸。b中通入冷却水
后,开始缓慢加热a,控制馏出物的温度不超过90℃。
分离提纯:
反应粗产物倒入分液漏斗中,先用水洗,再分别用少量5%碳酸钠溶液和水洗涤,分离后加
入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯8.2g。
回答下列问题:
(1)环己醇沸点大于环己烯的主要原因是 ,其在水中溶解度大于环己烯的原因
是 。
(2)装置b的名称是 ,进水口是 (填“①”或“②”)。
(3)本实验中最容易产生的有机副产物的结构简式为 。
(4)分液漏斗在使用前须清洗干净并 ;在本实验分离过程中,产物应该从分液漏斗的
(填“上口倒出”或“下口放出”)。
(5)分离提纯过程中每次洗涤后的操作是 ,加入无水氯化钙的目的是 。
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有 (填正确答案标号)。
A.圆底烧瓶 B.温度计 C.吸滤瓶 D.球形冷凝管 E.接收器
(7)本实验所得到的环己烯产率是 (填正确答案标号)。
A.41% B.50% C.61% D.70%
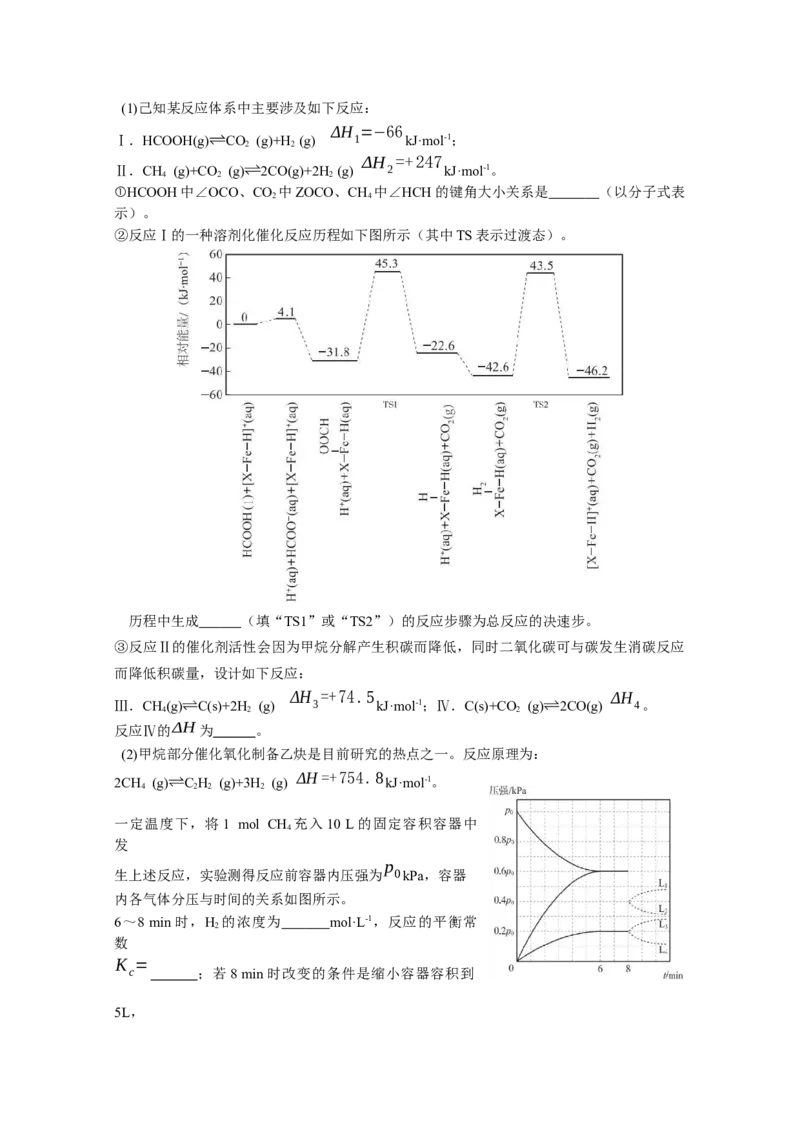
18(12分)随着我国碳达峰、碳中和目标的确定,含碳化合物的综合利用备受关注。(1)己知某反应体系中主要涉及如下反应:
ΔH =−66
Ⅰ.HCOOH(g) CO (g)+H (g) 1 kJ·mol-1;
2 2
ΔH =+247
Ⅱ.CH (g)+CO (g) 2CO(g)+2H (g) 2 kJ·mol-1。
4 2 2
①HCOOH中∠OCO、CO 中ZOCO、CH 中∠HCH的键角大小关系是 (以分子式表
2 4
示)。
②反应Ⅰ的一种溶剂化催化反应历程如下图所示(其中TS表示过渡态)。
历程中生成 (填“TS1”或“TS2”)的反应步骤为总反应的决速步。
③反应Ⅱ的催化剂活性会因为甲烷分解产生积碳而降低,同时二氧化碳可与碳发生消碳反应
而降低积碳量,设计如下反应:
ΔH =+74.5 ΔH
Ⅲ.CH(g) C(s)+2H (g) 3 kJ·mol-1;Ⅳ.C(s)+CO (g) 2CO(g) 4。
4 2 2
反应Ⅳ的ΔH为 。
(2)甲烷部分催化氧化制备乙炔是目前研究的热点之一。反应原理为:
ΔH=+754.8
2CH (g) C H (g)+3H (g) kJ·mol-1。
4 2 2 2
一定温度下,将1 mol CH 充入10 L的固定容积容器中
4
发
p
生上述反应,实验测得反应前容器内压强为 0kPa,容器
内各气体分压与时间的关系如图所示。
6~8 min时,H 的浓度为 mol·L-1,反应的平衡常
2
数
K =
c ;若8 min时改变的条件是缩小容器容积到
5L,其中C H 分压与时间关系可用图中曲线 (填“L”“L”“L”或“L”)表示。
2 2 1 2 3 4
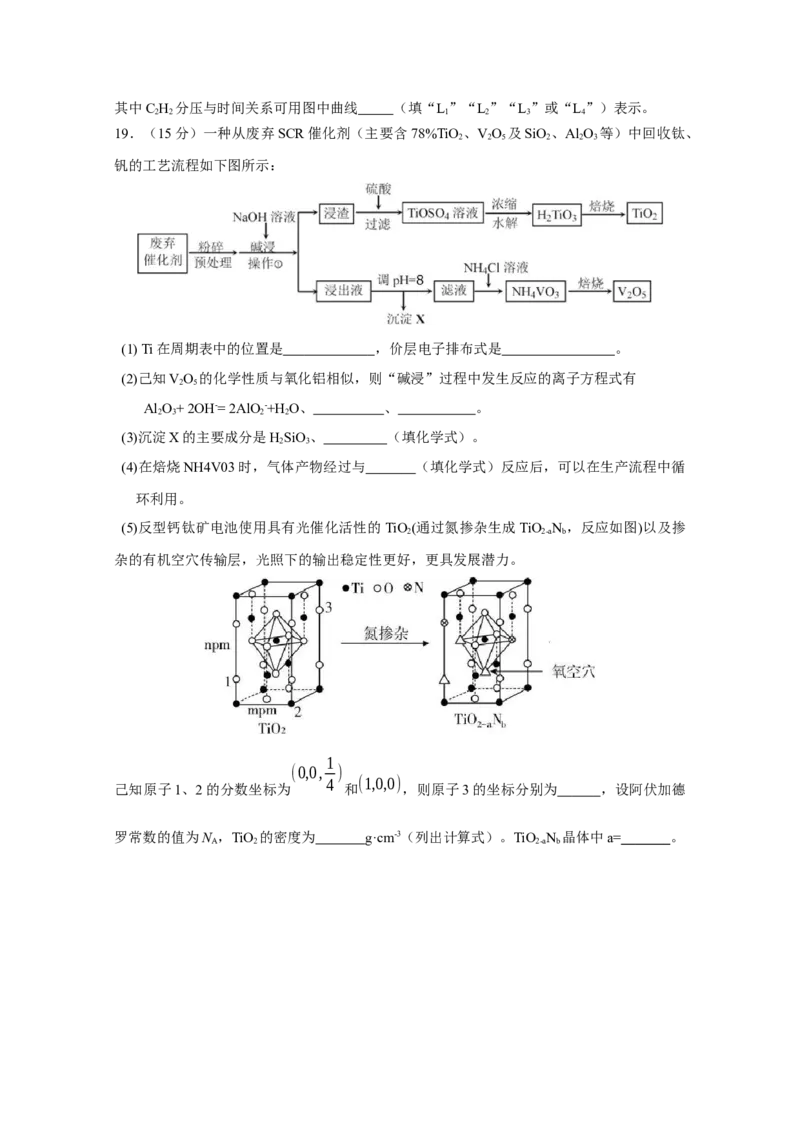
19.(15分)一种从废弃SCR催化剂(主要含78%TiO 、VO 及SiO 、Al O 等)中回收钛、
2 2 5 2 2 3
钒的工艺流程如下图所示:
(1) Ti在周期表中的位置是 ,价层电子排布式是 。
(2)己知VO 的化学性质与氧化铝相似,则“碱浸”过程中发生反应的离子方程式有
2 5
Al O+ 2OH-= 2AlO-+H O、 、 。
2 3 2 2
(3)沉淀X的主要成分是HSiO、 (填化学式)。
2 3
(4)在焙烧NH4V03时,气体产物经过与 (填化学式)反应后,可以在生产流程中循
环利用。
(5)反型钙钛矿电池使用具有光催化活性的TiO(通过氮掺杂生成TiO N ,反应如图)以及掺
2 2-a b
杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
1
(0,0, )
4 (1,0,0)
己知原子1、2的分数坐标为 和 ,则原子3的坐标分别为 ,设阿伏加德
罗常数的值为N ,TiO 的密度为 g·cm-3(列出计算式)。TiO N 晶体中a= 。
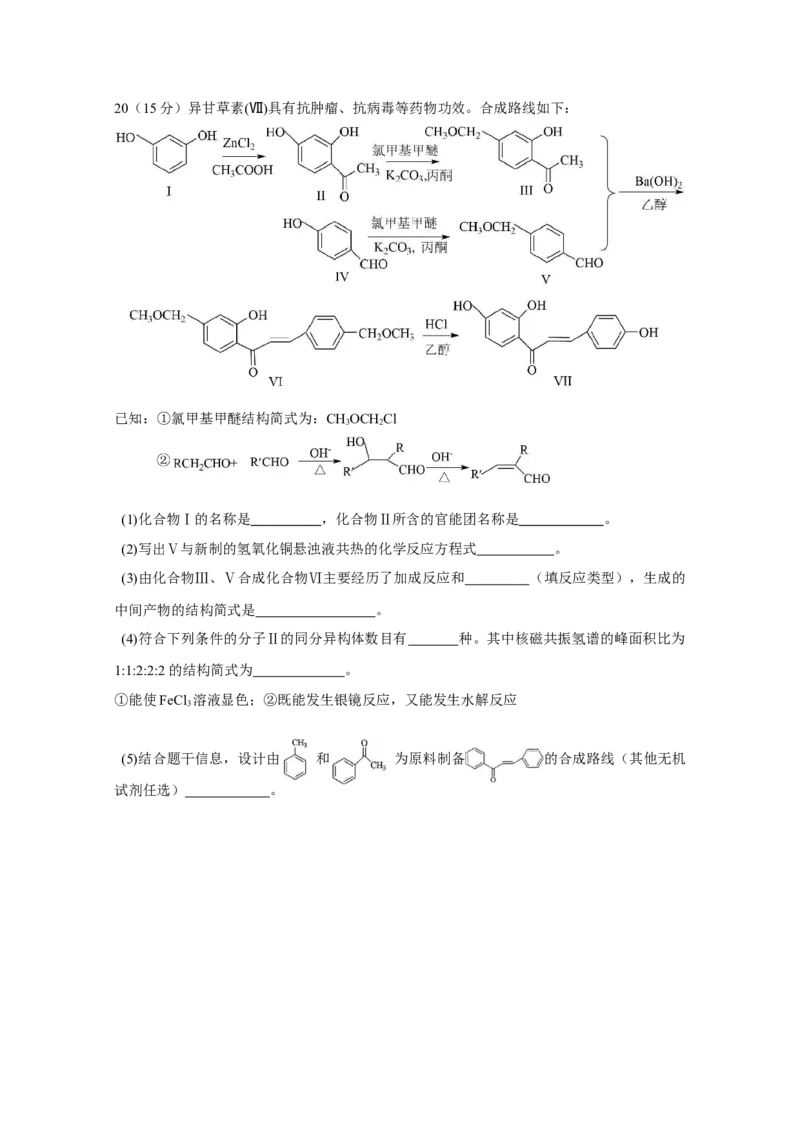
A 2 2-a b20(15分)异甘草素(Ⅶ)具有抗肿瘤、抗病毒等药物功效。合成路线如下:
已知:①氯甲基甲醚结构简式为:CHOCH Cl
3 2
(1)化合物Ⅰ的名称是 ,化合物Ⅱ所含的官能团名称是 。
(2)写出Ⅴ与新制的氢氧化铜悬浊液共热的化学反应方程式 。
(3)由化合物Ⅲ、Ⅴ合成化合物Ⅵ主要经历了加成反应和 (填反应类型),生成的
中间产物的结构简式是 。
(4)符合下列条件的分子Ⅱ的同分异构体数目有 种。其中核磁共振氢谱的峰面积比为
1:1:2:2:2的结构简式为 。
①能使FeCl 溶液显色;②既能发生银镜反应,又能发生水解反应
3
(5)结合题干信息,设计由 和 为原料制备 的合成路线(其他无机
试剂任选) 。化学参考答案
1 2 3 4 5 6 7 8
B C A B D D C C
9 10 11 12 13 14 15 16
C D C B B A D D
17.(14分)(1)环己醇能形成分子间氢键(1分) 环己醇能与水分子形成氢键(1分)
(2)直形冷凝管(1分) ② (1分)
(3) (2分)
(4)检漏(1分);上口倒出(1分)
(5)分液(1分) 干燥(或除水除醇)(1分)
(6) CD(2分)
(7) B (2分)
18.(12分) (1)①CO>HCOOH>CH (2分) ②TS2 (2分) ③+172.5kJ/mol (2
2 4
分)
(2) 0.06 (2分)
1.2×10−3
(mol/L)2 (2分) L(2分)
2
3d24s2
19.(15分) (1)第四周期IVB族(2分) (1分)
−
(2) V O+2OH- 2VO3 +H O (2分) SiO+2OH- = SiO2- +H O (2分)
2 5 2 2 3 2
(3) Al(OH) (1分)
3
(4) HCl (1分)
3 3
4×(48+16×2)
5
(1,1, ) (0, 0, )
4 4 N m2n×10−30 8
(5) 或 (2分) ③. A (2分) (2分)
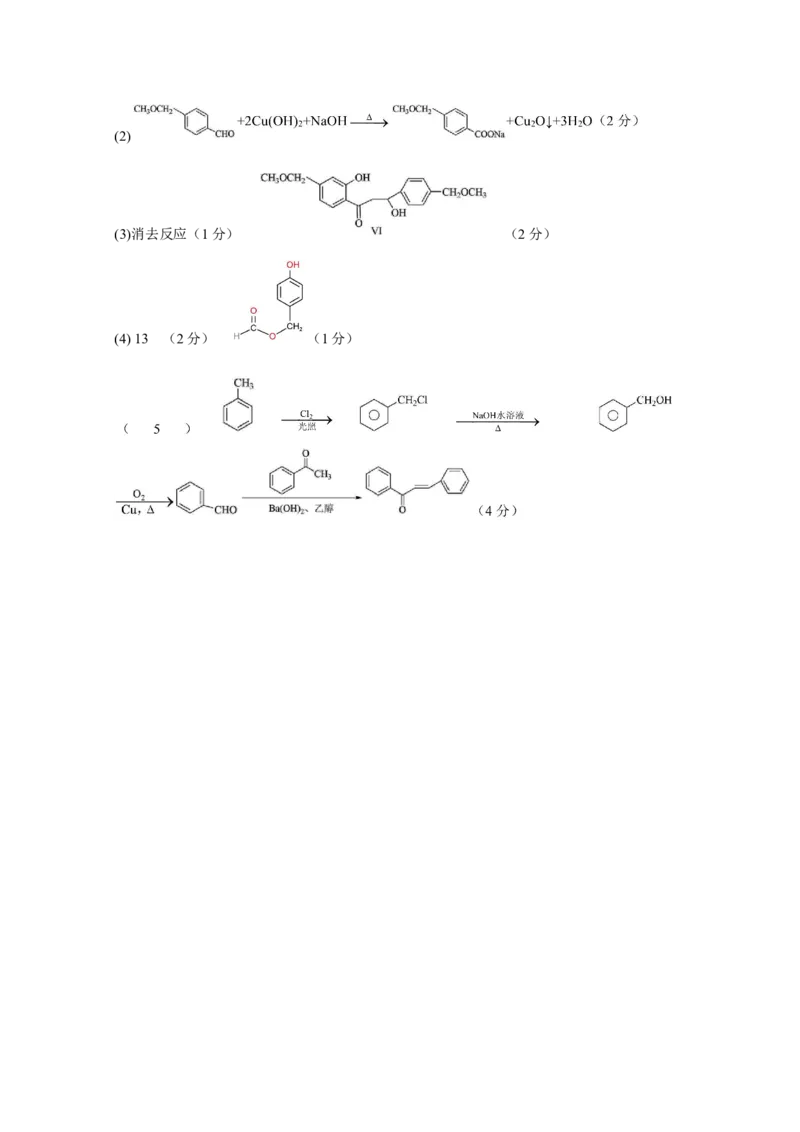
20.(15分)(1)①.间苯二酚或1,3-苯二酚(1分) ②.羟基和酮羰基(2分)(2)
(3)消去反应(1分) (2分)
(4) 13 (2分) (1分)