文档内容
广东省实验中学 2023 届高三级第一次阶段考试
化 学
本试卷分选择题和非选择题两部分,共8页,满分100分,考试用时75分钟。
注意事项:
1.答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名、考号填写在答题卷上。
2.选择题每小题选出答案后,用2B铅笔把答题卷上对应题目的答案标号涂黑;如需改动,
用橡皮擦干净后,再选涂其它答案;不能答在试卷上。
3.非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卷各题目指定区域内
的相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和
涂改液.不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁,考试结束后,将答题卷收回。
第一部分 选择题(共44分)
一、单选题(每题2分,共20分)
1.下列说法正确的是( )
A.电解质溶液导电的过程发生了化学变化
B.原子核外电子发生跃迁属于化学变化
C.石油分馏利用了石油中各组分化学性质的差异
D.“碳中和”是指利用中和反应吸收CO
2
2.化学与生活、科学、技术、社会、环境密切相关。下列说法正确的是( )
A.高温结构陶瓷、醋酸纤维、光导纤维都属于新型无机非金属材料
B.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁
C.明矾净水的原理是水解生成的氢氧化铝能凝聚水中的悬浮物、吸附色素并杀菌消毒
D.用飞机播撒AgI是实现人工增雨的方法之一
3.下列反应的离子方程式书写正确的是
−
A.金属铝溶于氢氧化钠溶液:Al+2OH- =AlO2 +H ↑
2
B.用惰性电极电解饱和MgCl 溶液:2Cl- +2H O Cl↑+H ↑+2OH-
2 2 2 2
−
C.向饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液:Ca2+ +HCO3 +OH- =CaCO ↓+H O
3 2D.向硫酸铁酸性溶液中通入足量硫化氢:2Fe3+ +S2- =2Fe2+ +S↓
4.陈述I和陈述II均正确,且具有因果关系的是
选项 陈述I 陈述II
A 钠金属性比钾强 可用Na和熔融KCl在高温下反应制备K
B 过氧化钠用于制造呼吸面具 过氧化钠与人呼出的HO、CO 都能发生反应生成O
2 2 2
C Al O 的熔点高 可用氧化铝坩埚熔化NaOH固体
2 3
D 浓硫酸具有吸水性 用浓硫酸干燥HS
2
5.下列各组物质充分反应后,只能得到一种气体(不考虑水蒸气)的是( )
A.木炭和浓硫酸共热 B.足量的铜跟一定量的浓硝酸反应
C.Na与稀硫酸反应 D.汽油在汽车发动机中燃烧后排出的气体
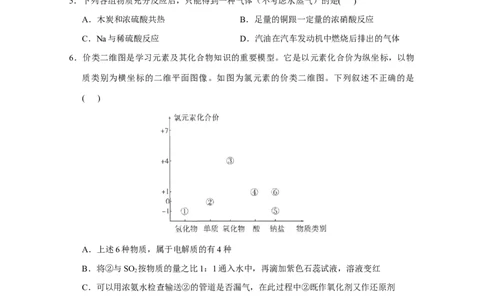
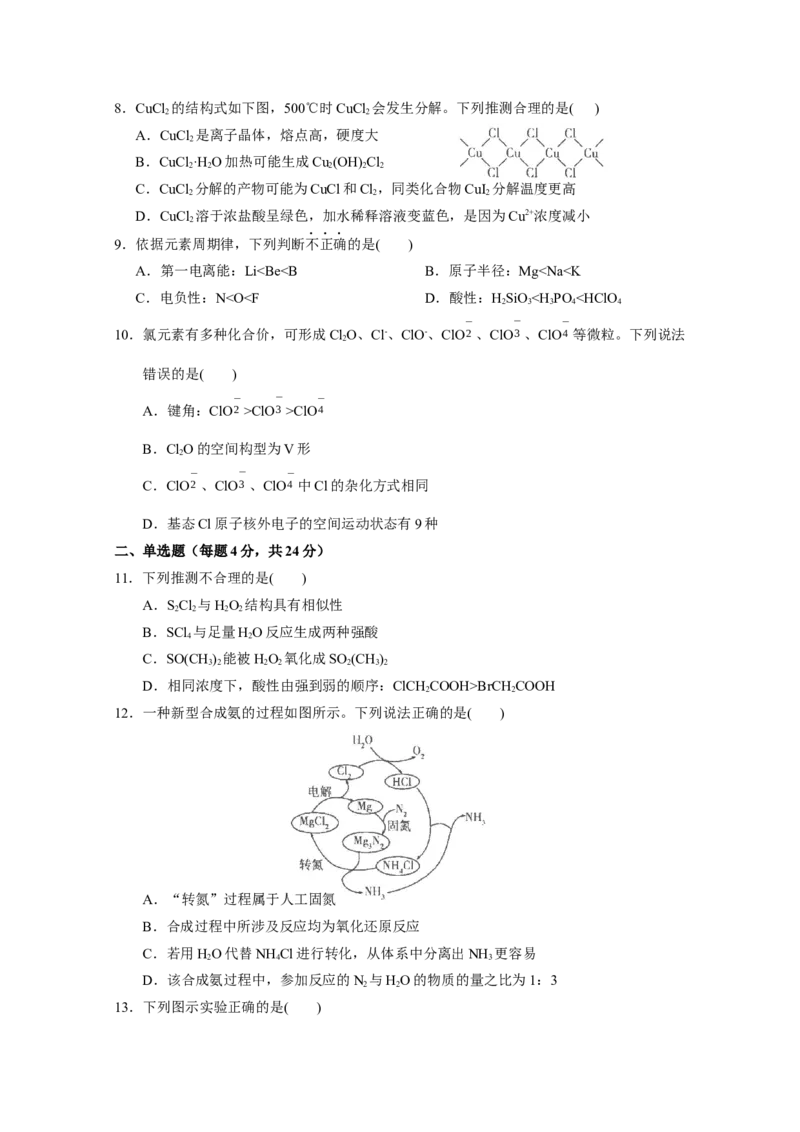
6.价类二维图是学习元素及其化合物知识的重要模型。它是以元素化合价为纵坐标,以物
质类别为横坐标的二维平面图像。如图为氯元素的价类二维图。下列叙述不正确的是
( )
A.上述6种物质,属于电解质的有4种
B.将②与SO 按物质的量之比1:1通入水中,再滴加紫色石蕊试液,溶液变红
2
C.可以用浓氨水检查输送②的管道是否漏气,在此过程中②既作氧化剂又作还原剂
D.用HC O 、NaClO 和HSO 三种物质制取③时,还会生成CO 等。生成1mol CO 转
2 2 4 3 2 4 2 2
移电子的物质的量为1mol
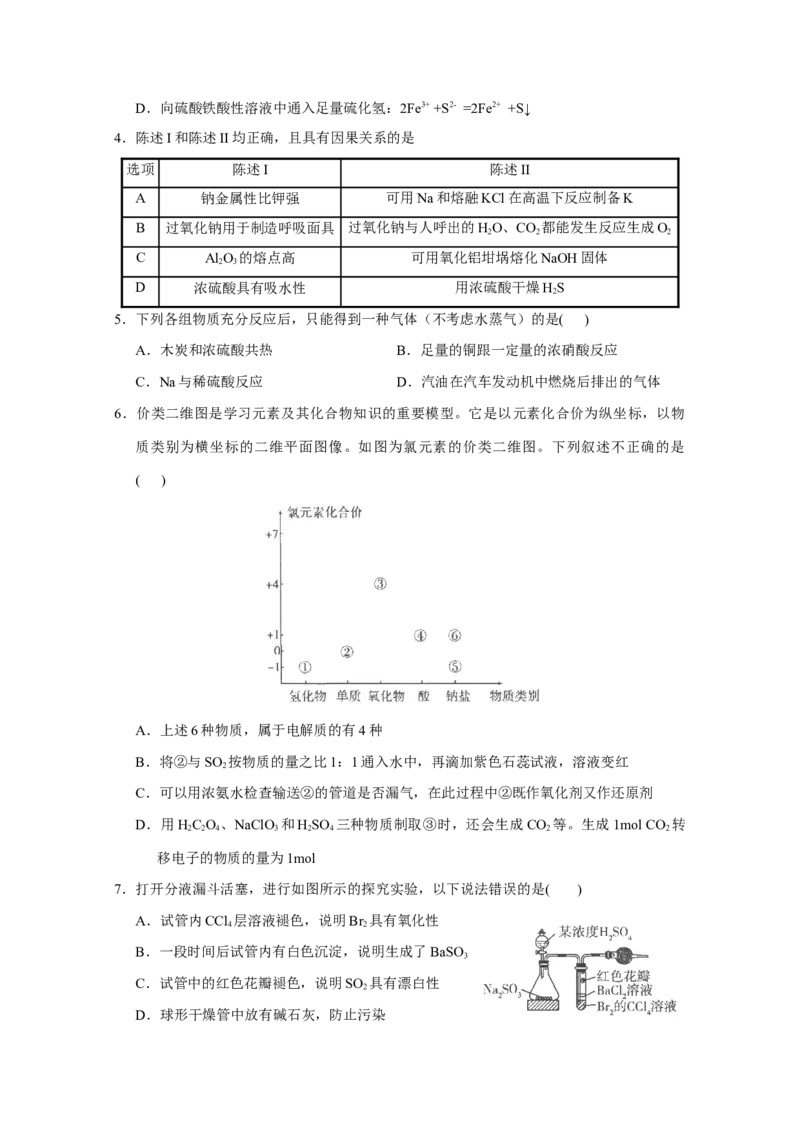
7.打开分液漏斗活塞,进行如图所示的探究实验,以下说法错误的是( )
A.试管内CCl 层溶液褪色,说明Br 具有氧化性
4 2
B.一段时间后试管内有白色沉淀,说明生成了BaSO
3
C.试管中的红色花瓣褪色,说明SO 具有漂白性
2
D.球形干燥管中放有碱石灰,防止污染8.CuCl 的结构式如下图,500℃时CuCl 会发生分解。下列推测合理的是( )
2 2
A.CuCl 是离子晶体,熔点高,硬度大
2
B.CuCl ·HO加热可能生成Cu (OH) Cl
2 2 2 2 2
C.CuCl 分解的产物可能为CuCl和Cl,同类化合物CuI 分解温度更高
2 2 2
D.CuCl 溶于浓盐酸呈绿色,加水稀释溶液变蓝色,是因为Cu2+浓度减小
2
9.依据元素周期律,下列判断不正确的是( )
A.第一电离能:LiClO3 >ClO4
B.ClO的空间构型为V形
2
− − −
C.ClO2 、ClO3 、ClO4 中Cl的杂化方式相同
D.基态Cl原子核外电子的空间运动状态有9种
二、单选题(每题4分,共24分)
11.下列推测不合理的是( )
A.SCl 与HO 结构具有相似性
2 2 2 2
B.SCl 与足量HO反应生成两种强酸
4 2
C.SO(CH ) 能被HO 氧化成SO (CH)
3 2 2 2 2 3 2
D.相同浓度下,酸性由强到弱的顺序:ClCH COOH>BrCH COOH
2 2
12.一种新型合成氨的过程如图所示。下列说法正确的是( )
A.“转氮”过程属于人工固氮
B.合成过程中所涉及反应均为氧化还原反应
C.若用HO代替NH Cl进行转化,从体系中分离出NH 更容易
2 4 3
D.该合成氨过程中,参加反应的N 与HO的物质的量之比为1:3
2 2
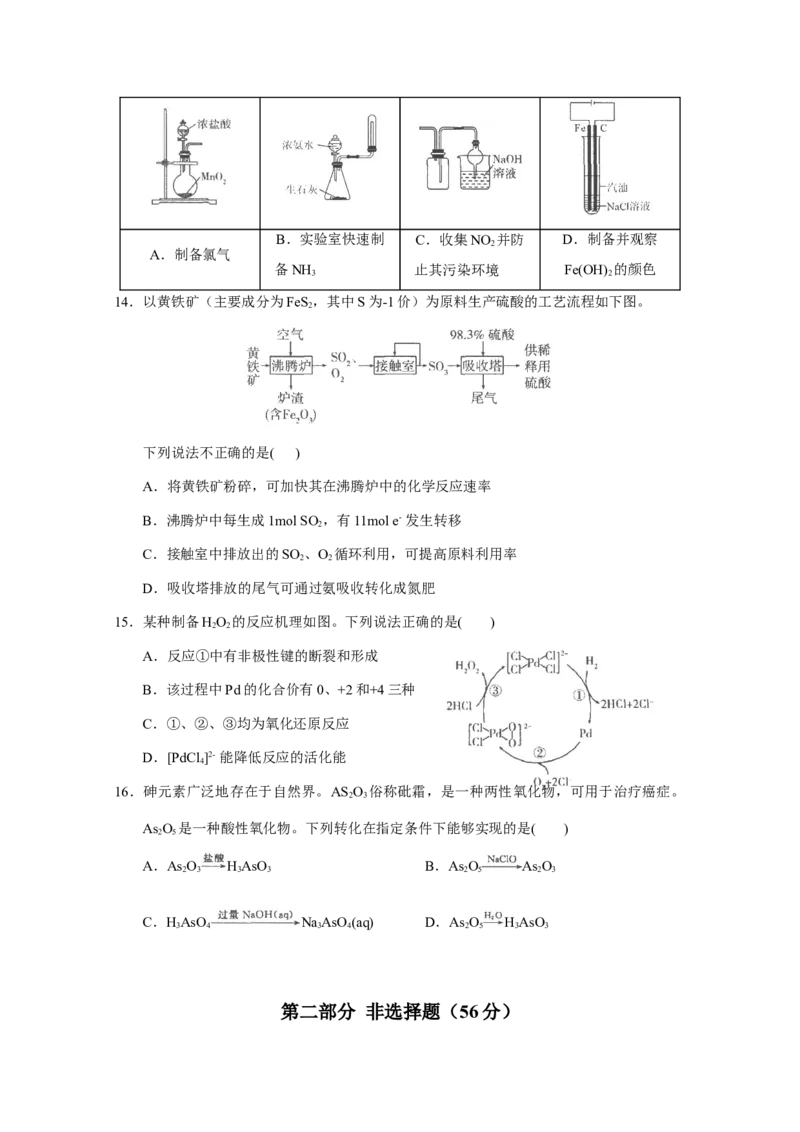
13.下列图示实验正确的是( )B.实验室快速制 C.收集NO 并防 D.制备并观察
2
A.制备氯气
备NH 止其污染环境 Fe(OH) 的颜色
3 2
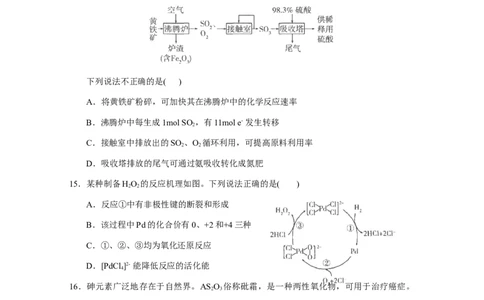
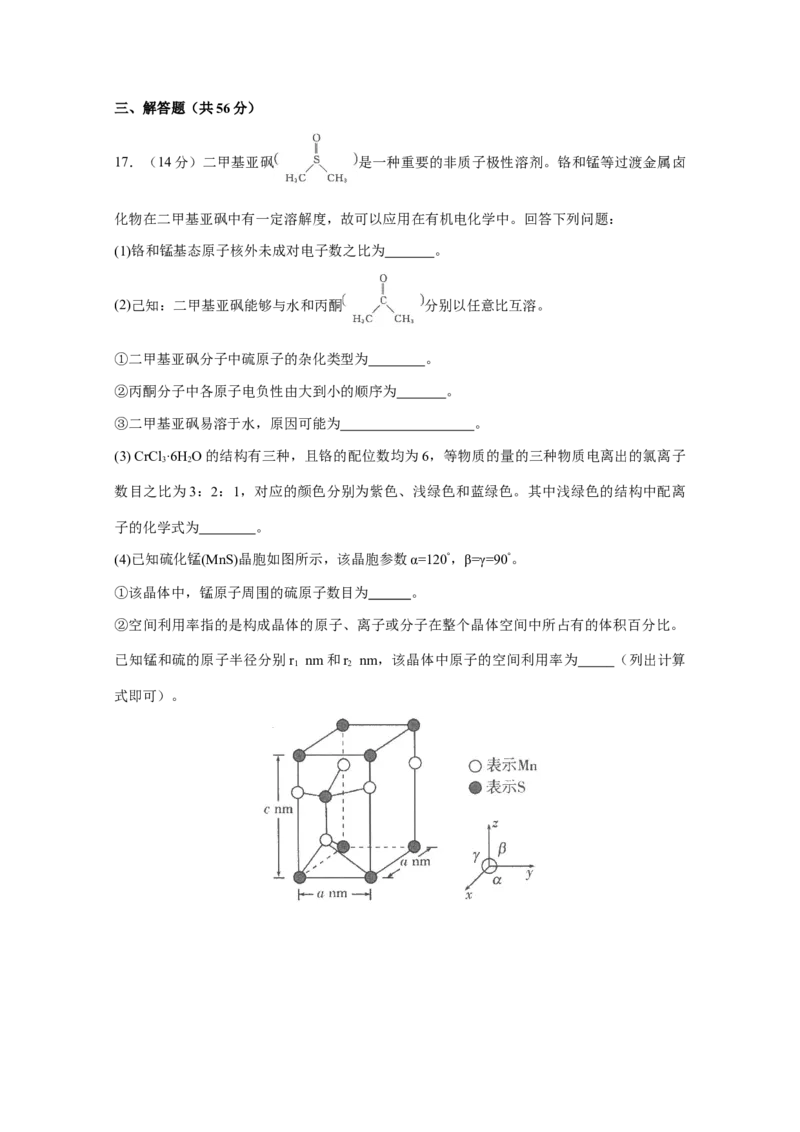
14.以黄铁矿(主要成分为FeS,其中S为-1价)为原料生产硫酸的工艺流程如下图。
2
下列说法不正确的是( )
A.将黄铁矿粉碎,可加快其在沸腾炉中的化学反应速率
B.沸腾炉中每生成1mol SO ,有11mol e- 发生转移
2
C.接触室中排放出的SO 、O 循环利用,可提高原料利用率
2 2
D.吸收塔排放的尾气可通过氨吸收转化成氮肥
15.某种制备HO 的反应机理如图。下列说法正确的是( )
2 2
A.反应①中有非极性键的断裂和形成
B.该过程中Pd的化合价有0、+2和+4三种
C.①、②、③均为氧化还原反应
D.[PdCl ]2- 能降低反应的活化能
4
16.砷元素广泛地存在于自然界。AS O 俗称砒霜,是一种两性氧化物,可用于治疗癌症。
2 3
As O 是一种酸性氧化物。下列转化在指定条件下能够实现的是( )
2 5
A.As O HAsO B.As O As O
2 3 3 3 2 5 2 3
C.HAsO NaAsO (aq) D.As O HAsO
3 4 3 4 2 5 3 3
第二部分 非选择题(56分)三、解答题(共56分)
17.(14分)二甲基亚砜 是一种重要的非质子极性溶剂。铬和锰等过渡金属卤
化物在二甲基亚砜中有一定溶解度,故可以应用在有机电化学中。回答下列问题:
(1)铬和锰基态原子核外未成对电子数之比为 。
(2)己知:二甲基亚砜能够与水和丙酮 分别以任意比互溶。
①二甲基亚砜分子中硫原子的杂化类型为 。
②丙酮分子中各原子电负性由大到小的顺序为 。
③二甲基亚砜易溶于水,原因可能为 。
(3) CrCl ·6HO的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子
3 2
数目之比为3:2:1,对应的颜色分别为紫色、浅绿色和蓝绿色。其中浅绿色的结构中配离
子的化学式为 。
(4)已知硫化锰(MnS)晶胞如图所示,该晶胞参数α=120°,β=γ=90°。
①该晶体中,锰原子周围的硫原子数目为 。
②空间利用率指的是构成晶体的原子、离子或分子在整个晶体空间中所占有的体积百分比。
已知锰和硫的原子半径分别r nm和r nm,该晶体中原子的空间利用率为 (列出计算
1 2
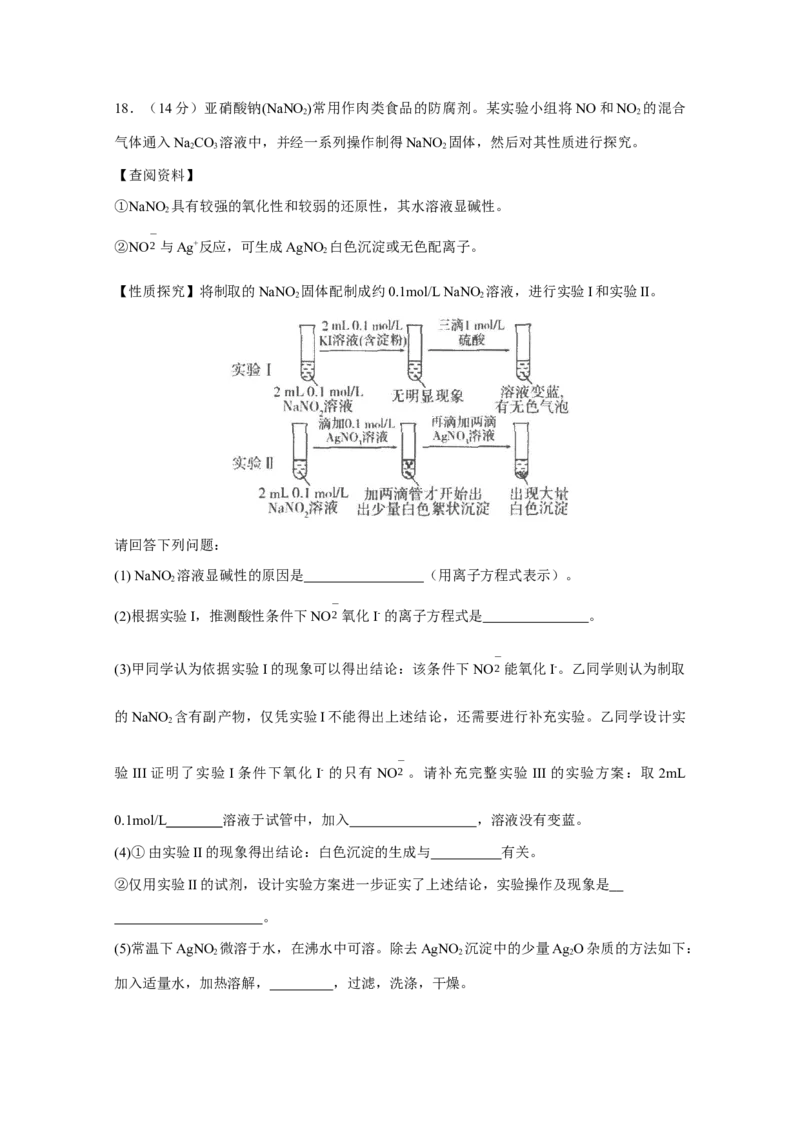
式即可)。18.(14分)亚硝酸钠(NaNO )常用作肉类食品的防腐剂。某实验小组将NO和NO 的混合
2 2
气体通入NaCO 溶液中,并经一系列操作制得NaNO 固体,然后对其性质进行探究。
2 3 2
【查阅资料】
①NaNO 具有较强的氧化性和较弱的还原性,其水溶液显碱性。
2
−
②NO2 与Ag+反应,可生成AgNO 白色沉淀或无色配离子。
2
【性质探究】将制取的NaNO 固体配制成约0.1mol/L NaNO 溶液,进行实验I和实验II。
2 2
请回答下列问题:
(1) NaNO 溶液显碱性的原因是 (用离子方程式表示)。
2
−
(2)根据实验I,推测酸性条件下NO2 氧化I- 的离子方程式是 。
−
(3)甲同学认为依据实验I的现象可以得出结论:该条件下NO2 能氧化I-。乙同学则认为制取
的NaNO 含有副产物,仅凭实验I不能得出上述结论,还需要进行补充实验。乙同学设计实
2
−
验III证明了实验 I条件下氧化 I- 的只有NO2 。请补充完整实验 III的实验方案:取 2mL
0.1mol/L 溶液于试管中,加入 ,溶液没有变蓝。
(4)①由实验II的现象得出结论:白色沉淀的生成与 有关。
②仅用实验II的试剂,设计实验方案进一步证实了上述结论,实验操作及现象是
。
(5)常温下AgNO 微溶于水,在沸水中可溶。除去AgNO 沉淀中的少量Ag O杂质的方法如下:
2 2 2
加入适量水,加热溶解, ,过滤,洗涤,干燥。19.(14分)实验室以CuSO ·5HO为原料制备[Cu(NH )]SO ·HO并进行定量分析。
4 2 3 4 4 2
已知:CuSO +4NH·HO [Cu(NH )]SO +4H O
4 3 2 3 4 4 2
+
[Cu(NH )]2+ +4H+ Cu2+ +4NH4
3 4
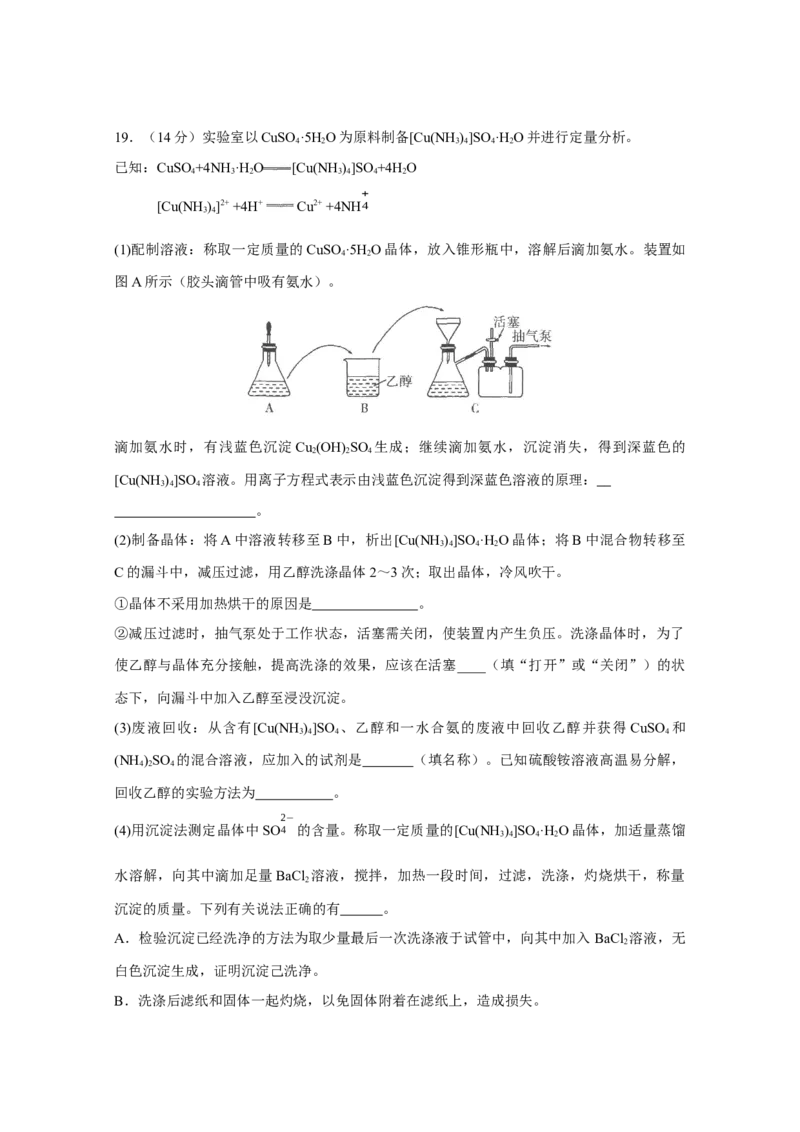
(1)配制溶液:称取一定质量的CuSO ·5HO晶体,放入锥形瓶中,溶解后滴加氨水。装置如
4 2
图A所示(胶头滴管中吸有氨水)。
滴加氨水时,有浅蓝色沉淀Cu (OH) SO 生成;继续滴加氨水,沉淀消失,得到深蓝色的
2 2 4
[Cu(NH )]SO 溶液。用离子方程式表示由浅蓝色沉淀得到深蓝色溶液的原理:
3 4 4
。
(2)制备晶体:将A中溶液转移至B中,析出[Cu(NH )]SO ·HO晶体;将B中混合物转移至
3 4 4 2
C的漏斗中,减压过滤,用乙醇洗涤晶体2~3次;取出晶体,冷风吹干。
①晶体不采用加热烘干的原因是 。
②减压过滤时,抽气泵处于工作状态,活塞需关闭,使装置内产生负压。洗涤晶体时,为了
使乙醇与晶体充分接触,提高洗涤的效果,应该在活塞____(填“打开”或“关闭”)的状
态下,向漏斗中加入乙醇至浸没沉淀。
(3)废液回收:从含有[Cu(NH )]SO 、乙醇和一水合氨的废液中回收乙醇并获得 CuSO 和
3 4 4 4
(NH )SO 的混合溶液,应加入的试剂是 (填名称)。已知硫酸铵溶液高温易分解,
4 2 4
回收乙醇的实验方法为 。
2−
(4)用沉淀法测定晶体中SO4 的含量。称取一定质量的[Cu(NH )]SO ·HO晶体,加适量蒸馏
3 4 4 2
水溶解,向其中滴加足量BaCl 溶液,搅拌,加热一段时间,过滤,洗涤,灼烧烘干,称量
2
沉淀的质量。下列有关说法正确的有 。
A.检验沉淀已经洗净的方法为取少量最后一次洗涤液于试管中,向其中加入 BaCl 溶液,无
2
白色沉淀生成,证明沉淀己洗净。
B.洗涤后滤纸和固体一起灼烧,以免固体附着在滤纸上,造成损失。C.加热一段时间有助与减少硫酸钡沉淀吸附杂质。
(5)探究小组用滴定法测定原料中CuSO ·5HO(相对分子质量为250)的含量。取a g试样配
4 2
成100mL溶液,每次取20.00mL,消除干扰离子后,用c mol·L-1 EDTA(HY2-)标准溶液滴
2
定至终点,平均消耗b mL EDTA溶液。
滴定反应如下:Cu2+ +H Y2- CuY2- +2H+。
2
写出计算CuSO ·5HO质量分数的表达式:ω= 。
4 2
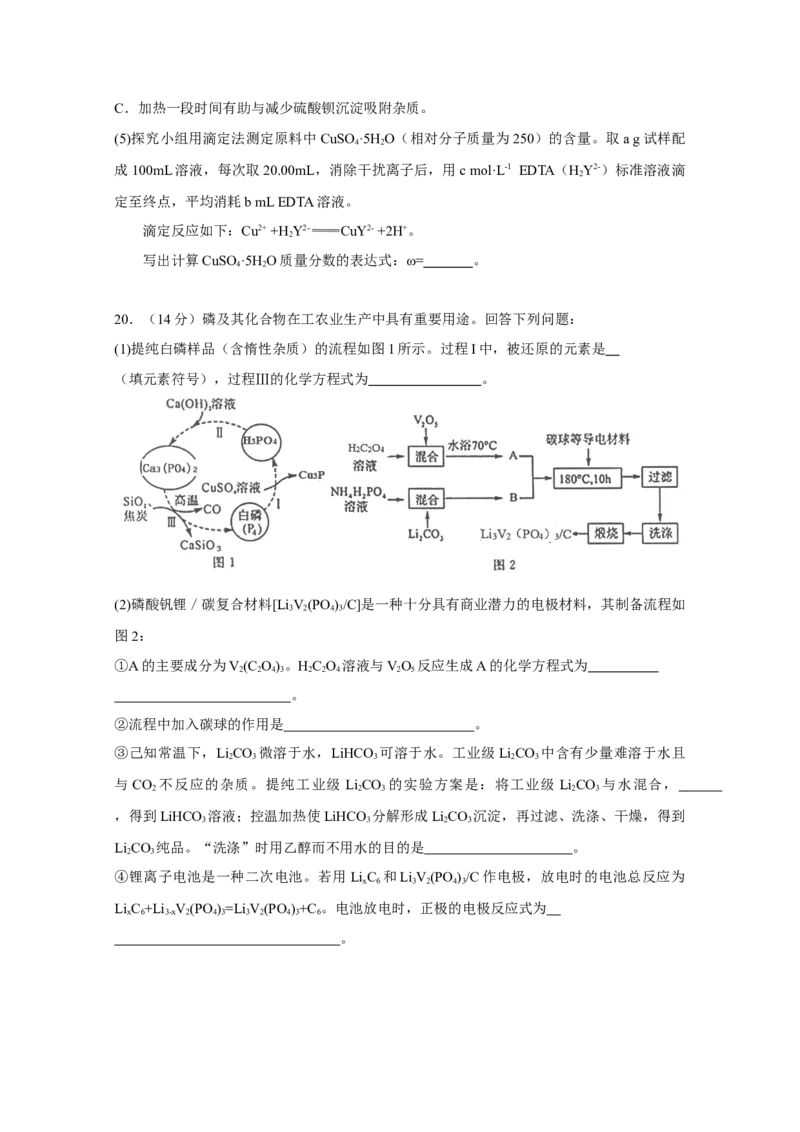
20.(14分)磷及其化合物在工农业生产中具有重要用途。回答下列问题:
(1)提纯白磷样品(含惰性杂质)的流程如图1所示。过程I中,被还原的元素是
(填元素符号),过程Ⅲ的化学方程式为 。
(2)磷酸钒锂/碳复合材料[Li V(PO )/C]是一种十分具有商业潜力的电极材料,其制备流程如
3 2 4 3
图2:
①A的主要成分为V(C O)。HC O 溶液与VO 反应生成A的化学方程式为
2 2 4 3 2 2 4 2 5
。
②流程中加入碳球的作用是 。
③己知常温下,LiCO 微溶于水,LiHCO 可溶于水。工业级LiCO 中含有少量难溶于水且
2 3 3 2 3
与CO 不反应的杂质。提纯工业级 LiCO 的实验方案是:将工业级 LiCO 与水混合,
2 2 3 2 3
,得到LiHCO 溶液;控温加热使LiHCO 分解形成LiCO 沉淀,再过滤、洗涤、干燥,得到
3 3 2 3
LiCO 纯品。“洗涤”时用乙醇而不用水的目的是 。
2 3
④锂离子电池是一种二次电池。若用LiC 和LiV(PO )/C作电极,放电时的电池总反应为
x 6 3 2 4 3
LiC +Li V(PO )=Li V(PO )+C 。电池放电时,正极的电极反应式为
x 6 3-x 2 4 3 3 2 4 3 6
。化学参考答案
1-5 ADCBC 6-10 CBBAA 11-16 BDDBDC
17.(1) 6:5
sp3
(2)① ②O>C>H ③二甲基亚砜可以与水分子形成分子间氢键
(3) [Cr(HO) Cl]2+
2 5
16π(r3 +r3
)
1 2 ×100%
(4)①4 ②
3√3a2c
−
18.(1) NO2 +H O HNO+OH-
2 2
−
(2) 2NO2 +2I- +4H+ 2NO↑+I +2H O
2 2
(3) NaNO ; 2mL 0.1mol/L KI溶液(含淀粉),再滴加三滴1mol/L硫酸
3
(4)①AgNO 溶液和NaNO 溶液的相对用量
3 2
②向AgNO 溶液中逐滴滴加NaNO 溶液,先有白色沉淀生成,后沉淀逐渐溶解
3 2
(5)趁热过滤冷却结晶
2−
19.(1) Cu (OH) SO +8NH·HO 2[Cu(NH )]2+ +SO4 +2OH- +8H O
2 2 4 3 2 3 4 2
(2)①晶体受热易脱水脱氨(晶体受热易分解) ②打开
(3)(稀)硫酸; 减压蒸馏
(4) BC
c mol⋅L−1 ×b×10−3L×250g⋅mol−1 ×5
×100%
ag
(5) (单位可以统一约去)
20.(1) Cu、P ;2Ca (PO )+6SiO +10C 6CaSiO +10CO↑+P 。
3 4 2 2 3 4
(2)①VO+5H C O V(C O)+4CO ↑+5H O;
2 5 2 2 4 2 2 4 3 2 2
②增强复合材料的导电性
③通入足量CO 气体后过滤; 减少产品损耗
2
④Li V(PO )+xLi+ +xe- =Li V(PO )
3-x 2 4 3 3 2 4 3