文档内容
第四章 化学反应与电能
知识清单
考点1 原电池
1.定义:将化学 能转化成 电 能的装置
2.本质: 氧化还原 反应
3.工作原理:以铜-锌原电池为例
电极反应:负极: Zn—2 e — =Z n 2 + ;正极: C u 2 + +2 e — = Cu
总反应: Zn+C u 2 + =Z n 2 + +C u
注:( 1)盐桥的作用:成分: 含琼胶的 KC l 饱和溶液
作用: ① 构成通路,代替两溶液直接接触
② 平衡电荷
优点:隔离氧化剂和还原剂,不同区域实现电子定向移动,产生持续、稳定的电
流
(2)电子只能在 两极和外电路中 中流动
(3)溶液中是由 电解质溶液中的阴阳离子 定向移动形成闭合回路的
4.构成条件: 两极一液一连线,氧化还原是条件
(1)一看反应:看是否有能自发进行的氧化还原反应发生(一般是活泼性强的金属与电解质溶
液反应)。
(2)二看两电极:一般是活泼性不同的两电极。
(3)三看是否形成闭合回路,形成闭合回路需三个条件:①电解质溶液;②两电极直接或间接接
触;③两电极插入电解质溶液。
5.正负极的判断方法:
(1)电极反应:负极— 氧化 反应,正极— 还原 反应(2)电子或电流的流向:电子:负极 →正极 ;电流: 正极 → 负极
(3)离子流向:阳离子→ 正 极,阴离子→ 负 极;
6.电极反应式的书写
(1)注意电解质溶液环境:电极产物在电解质溶液中应稳定存在
在碱性介质中,不能存在: H + 、 CO 、金属阳离子
2
在酸性介质中,不能存在: OH -
(2)两极反应式叠加得总反应式 ,总反应式减去正极反应式,可得负极反应式
(3)规律:一般来说,金属M作负极的原电池
负极:酸性或中性介质中: M—ne - =M n+
碱性介质中: M—n e - +nOH - =M(OH )
n
正极:酸性介质中: 2H + +2 e - =H ↑
2
金属阳离子NX+与金属反应的介质中: N X + +x e - =N
阳离子不与金属反应的介质中: O +4e - +2H O=4OH -
2 2
7.常见原电池电极反应式、总反应式的书写
①Fe|稀HCl|C
正极:2H++2e-=H ↑
2
负极:Fe—2e—= Fe2+
总反应:Fe+2H+=H ↑+Fe2+
2
②Mg︱稀硫酸︱Cu
正极:2H++2e-=H ↑ 负极:Mg—2e—= Mg2+
2
总反应:Mg+2H+=H ↑+ Mg2+
2
③Zn|AgNO 溶液|Pt
3
正极:Ag++e—= Ag 负极:Zn—2e—=Zn2+
总反应:Zn+2Ag+= 2Ag+ Zn2+
④Cu︱FeCl 溶液︱Pt
3
正极:Fe3++e—= Fe2+ 负极:Cu—2e—= Cu2+
总反应:Cu+ 2Fe3+= 2Fe2++ Cu2+
⑤Mg︱NaOH溶液︱Cu
正极:O +4e-+2H O=4OH- 负极:Mg—2e—+2OH—= Mg(OH)
2 2 2
总反应:2Mg+ O +2H O=2Mg(OH)
2 2 2⑥Fe︱KCl溶液︱Cu
正极:O +4e-+2H O=4OH— 负极:Fe—2e—= Fe2+
2 2
总反应:2Fe+ O +2H O=2Fe(OH)
2 2 2
⑦Al|NaOH溶液|Mg
正极:2e—+2H O= H ↑+ 2OH― 负极:Al —3e—+4OH—=AlO —+2H O
2 2 2 2
总反应:2Al+2OH―+2H O=2AlO —+3H ↑
2 2 2
⑧Cu|浓HNO |Fe
3
正极:2H++NO —+e—= H O+NO ↑ 负极: Cu —2e—=Cu2+
3 2 2
总反应:Cu+4H++2NO —=Cu2++2H O+2NO ↑
3 2 2
考点2 化学电源
1.分类: 一次电池 、 二次电池 、 燃料
2.判断电池优劣的主要标准: 比能量 、 比功率 、 电池可储存时间的长短
3.常见的一次电池
(1)普通锌锰干电池
电极材料及电极反应:负极材料:锌筒;负极反应: Zn-2 e - =Z n 2 +
正极材料:石墨;正极反应:2NH + +2MnO +2e -
4 2
=2NH ↑+Mn O +H O
3 2 3 2
总反应: Zn+2MnO +2NH Cl=ZnCl +2NH ↑+Mn O +H O
2 4 2 3 2 3 2
(2)碱性锌锰电池
电极材料及电极反应:负极材料: 锌筒 ;负极反应: Zn-2 e - +2OH - =Zn(OH )
2
正极材料:MnO ;正极反应:2MnO +2e - +2H O=2MnO(OH)
2 2 2
+2OH -
总反应: Zn+2MnO +2H O=2MnO(OH)+Zn(OH)
2 2 2
4.二次电池(可充电电池)
举例:铅酸蓄电池
①电极材料:负极材料: Pb 正极材料:PbO 电解质: H SO
2 2 4
②电极反应式:负极: Pb-2 e - +SO 2 - =PbSO
4 4
正极: PbO +4H + +2e - +SO 2 - =PbSO +2H O
2 4 4 2
总反应: Pb+PbO +2H SO =2PbSO +2H O
2 2 4 4 2③接线方式:充电时,待充电电池的负极要接电源的负 极,待充电电池的正极要接电源的
正 极
注:放电: 化学 能转化为电 能;
充电:电 能转化为 化学 能
5.燃料电池
(1)特点:燃料电池中,燃料(还原性气体等)作 负 极,发生氧化反应,氧化剂(通常为
氧气或空气)作 正 极发生还原反应
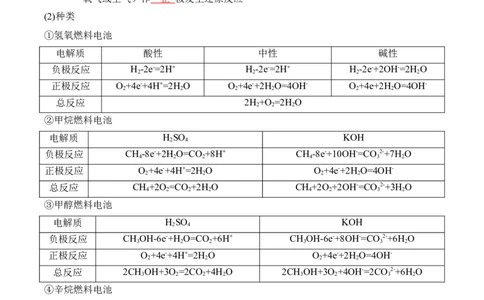
(2)种类
①氢氧燃料电池
电解质 酸性 中性 碱性
负极反应 H -2e-=2H+ H -2e-=2H+ H -2e-+2OH-=2H O
2 2 2 2
正极反应 O +4e-+4H+=2H O O +4e-+2H O=4OH- O +4e+2H O=4OH-
2 2 2 2 2 2
总反应 2H +O =2H O
2 2 2
②甲烷燃料电池
电解质 H SO KOH
2 4
负极反应 CH -8e-+2H O=CO +8H+ CH -8e-+10OH-=CO 2-+7H O
4 2 2 4 3 2
正极反应 O +4e-+4H+=2H O O +4e-+2H O=4OH-
2 2 2 2
总反应 CH +2O =CO +2H O CH +2O +2OH-=CO 2-+3H O
4 2 2 2 4 2 3 2
③甲醇燃料电池
电解质 H SO KOH
2 4
负极反应 CH OH-6e-+H O=CO +6H+ CH OH-6e-+8OH-=CO 2-+6H O
3 2 2 3 3 2
正极反应 O +4e-+4H+=2H O O +4e-+2H O=4OH-
2 2 2 2
总反应 2CH OH+3O =2CO +4H O 2CH OH+3O +4OH-=2CO 2-+6H O
3 2 2 2 3 2 3 2
④辛烷燃料电池
电解质 H SO KOH
2 4
负极反应 C H -50e—+16H O=8CO +50H+ C H -50e—+66OH—=8CO 2-+42H O
8 18 2 2 8 18 3 2
正极反应 O +4e-+4H+=2H O O +4e-+2H O=4OH-
2 2 2 2
总反应 2C H +25O =16CO +18H O 2C H +25O +32OH—=16CO 2-+34H O
8 18 2 2 2 8 18 2 3 2
⑤乙醇燃料电池
电解质 H SO KOH
2 4
负极反应 C H O-12e—+3H O=2CO +12H+ C H O-12e—+16OH—=2CO 2-+11H O
2 6 2 2 2 6 3 2
正极反应 O +4e-+4H+=2H O O +4e-+2H O=4OH-
2 2 2 2总反应 C H O+3O =2CO +3H O C H O+3O +4OH—=2CO 2-+5H O
2 6 2 2 2 2 6 2 3 2
⑥熔融盐电池
例如:用Li CO 和Na CO 的熔融盐混合物作电解质的燃料电池,CO为燃料,空气与CO 的
2 3 2 3 2
混合气为助燃气,制得在 650℃下工作的燃料电池,在工作过程中,电解质熔融盐的组
成、浓度不变
电极反应式:负极:2CO+2CO 2 - -4e - =4CO 正极:O +2CO +4e - =2CO 2 - 总反应:
3 2 2 2 3
2CO+O =2CO
2 2
6、燃料电池中常见正极反应式的书写
(1)在酸性溶液中: O +4e - +4H + =2H O
2 2
(2)在碱性或中性溶液中: O +4e - +2H O=4OH -
2 2
(3)在熔融碳酸盐中: O +2CO +4e - =2CO 2-
2 2 3
(4)在可传导O2-的晶体电解质中(例如:掺杂(Y O )氧化钇的(ZrO )氧化锆晶体):O +4e -
2 3 2 2
=2O 2 -
考点3 电解池
1.电解池的定义:将电 能转变为 化学能的装置,也称电解槽
2.构成条件: 两极一液一电源,氧化还原是条件
①阴极连接电源的 负 极,吸引 阳 离子,发生 还原 反应
②阳极连接电源的 阳极,吸引 阴 离子,发生 氧化 反应
注:阳极分为两种:(1)活性电极:电极自身放电即电极自身发生氧化反应,常见的活性电
极金属为:
Fe 、 Cu 、 Ag
(2)惰性电极:电极自身不反应,由电解质中的阴离子发生氧化反应。
常见的惰性电极为: P t 、 C
3、电子和离子的移动方向4.电极的放电顺序
①常见阳极的放电顺序: 活性电极 > S 2 - > I - > B r - > C l - > OH - > 含氧酸根 > F -
②常见阳离子放电顺序:金属活动性顺序的 倒 序
Ag + > Hg 2+ > Fe 3+ > Cu 2+ > H + ( 酸 ) > Pb 2+ > Fe 2+ > Zn 2+ > H + (水)
> Al 3+ Mg 2+ > Na + > Ca 2+ > K +
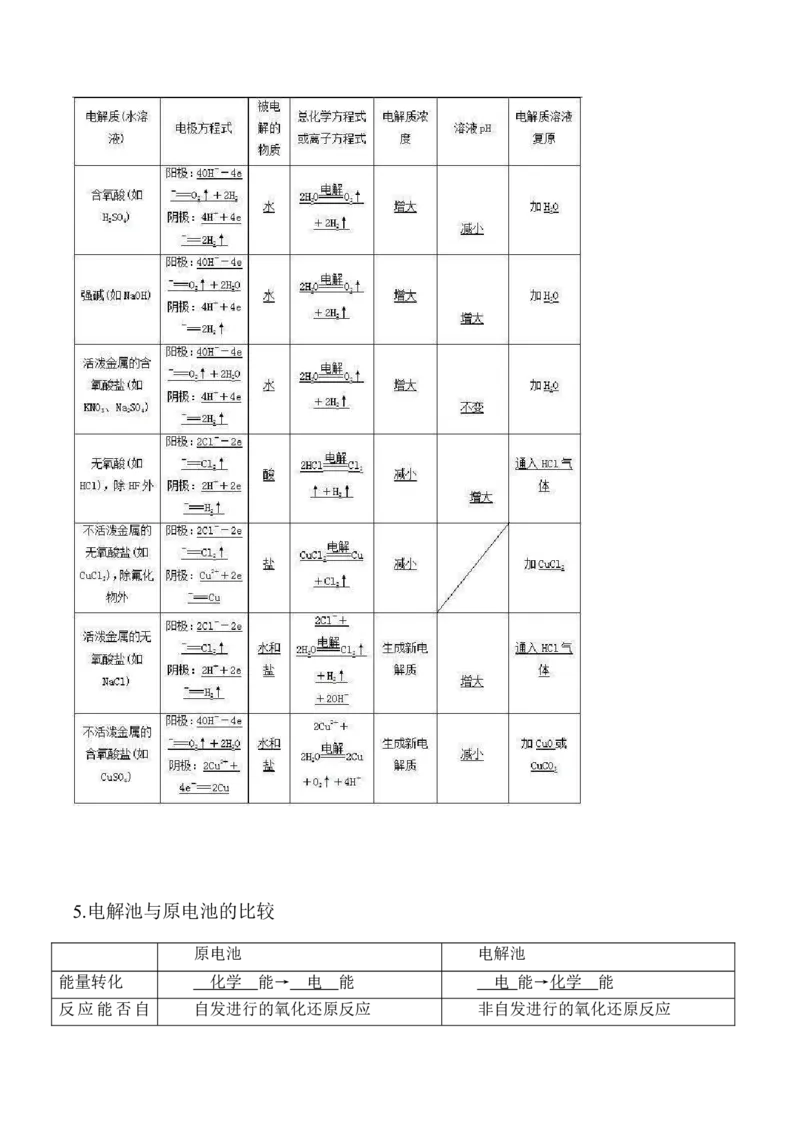
4.常考的电解池反应式:
①惰性电极的情况下,电解NaOH溶液:
阴极: 2H O+2e - =H ↑+2OH -
2 2
阳极: 2H O — 4e - =4H + +O ↑
2 2
总反应: 2H O 2H ↑+O ↑
2 2 2
②惰性电极的情况下,电解KOH溶液:
阴极:2H O+2e - =H ↑+2OH -
2 2
阳极:2H O — 4e - =4H + +O ↑
2 2
电解
总反应: 2H
2
O 2H
2
↑+O
2
↑
③惰性电极的情况下,电解H SO 溶液:
2 4
阴极: 2H O+2e - =H ↑+2OH -
2 2
阳极: 2H O — 4e - =4H + +O ↑
2 2
电解
总反应: 2H
2
O 2H
2
↑+O
2
↑
④惰性电极的情况下,电解HNO 溶液:
3
阴极: 2H O+2e - =H ↑+2OH -
2 2
阳极: 2H O — 4e - =4H + +O ↑
2 2电解
总反应: 2H
2
O 2H
2
↑+O
2
↑
⑤惰性电极的情况下,电解KNO 溶液:
3
阴极: 2H O+2e - =H ↑+2OH -
2 2
阳极: 2H O — 4e - =4H + +O ↑
2 2
电解
总反应: 2H
2
O 2H
2
↑+O
2
↑
⑥惰性电极的情况下,电解Na SO 溶液:
2 4
阴极: 2H O+2e - =H ↑+2OH -
2 2
阳极: 2H O — 4e - =4H + +O ↑
2 2
电解
总反应: 2H
2
O 2H
2
↑+O
2
↑
⑦惰性电极的情况下,电解HCl溶液:
阴极: 2H + +2 e - =H ↑
2
阳极: 2C l —— 2 e — =C l ↑
2
电解
总反应: 2H + +2C l — H
2
↑+ Cl
2
↑
⑧惰性电极的情况下,电解CuCl 溶液:
2
阴极: C u 2 + +2 e — = Cu
阳极: 2C l —— 2 e — =C l ↑
2
电解
总反应: C u 2 + +2C l — Cu+ Cl
2
↑
⑨惰性电极的情况下,电解NaCl溶液:
阴极: 2H O+2e - =H ↑+2OH -
2 2
阳极: 2C l —— 2 e — =C l ↑
2
电解
总反应: 2H
2
O+2Cl — Cl
2
↑+H
2
↑+2OH -
⑩惰性电极的情况下,电解MgCl 溶液:
2
阴极: M g 2 + +2H O+2e - =H ↑+ Mg(OH)
2 2 2
阳极: 2C l —— 2 e — =C l ↑
2
电解
总反应: M g 2 + +2H
2
O+ 2Cl — H
2
↑+ Mg(OH)
2
+ Cl
2
↑
(11)惰性电极的情况下,电解CuSO 溶液:
4阴极: C u 2 + +2 e — = Cu
阳极: 2H O — 4e - =4H + +O ↑
2 2
电解
总反应: 2C u 2 + +2H
2
O 2Cu+4H + +O
2
↑
(12)惰性电极的情况下,电解AgNO 溶液:
3
阴极: A g + + e — = Ag
阳极: 2H O — 4e - =4H + +O ↑
2 2
电解
总反应: 4Ag + +2H
2
O 4Ag +4H + +O
2
↑
电解不同溶液的情况对比5.电解池与原电池的比较
原电池 电解池
能量转化 化学 能→ 电 能 电 能→化学 能
反应能否自 自发进行的氧化还原反应 非自发进行的氧化还原反应发进行
构成装置 两极、电解质、导线 两极、电解质、电源
电极名称 负 极 正 极 阴 极(与负 阳 极(与正
极相连) 极相连)
电极反应 失电子—氧化反应 得电子—还原反 得电子—还原反应 失电子—氧化反应
应
电子流向 负极→外电路→正极 负极→阴极,阳极→正极
电流流向 正极→外电路→负极 正极→阳极,阴极→负极
离子流向 阳离子→ 正 极,阴离子→负 阳离子→阴极,阴离子→阳 极
极
6、电解原理的应用
(1)氯碱工业—— 电解饱和食盐水制烧碱和氯气
①原理: 阴极:2H O+2e - =H ↑+2OH -
2 2
阳极: 2C l - —2 e - =C l ↑
2
电解
总反应: 2C l ― +2H
2
O 2OH ― +Cl
2
↑+H
2
↑
②现象及检验:
阴极:有 无色、无味气泡 产生,滴加酚酞——变 红
阳极:有黄绿色、刺激性气味 的气体产生,使湿润的淀粉KI试纸变 蓝
③阳离子交换膜的作用
(1)将电解池隔成 阳极室和阴极室 ,只允许 阳离子 通过,而阻止阴离子和气体 通过
(2)既能防止阴极产生的H 和阳极产生的 C l 而引起爆炸,又能避免Cl 和NaOH 作用生
2 2 2
成 NaClO 而影响烧碱的质量
(2)电镀
①电镀池的构成:
阴极:待镀金属 ——镀件
阳极:镀层金属 (通常是一些在空气或溶液里不易起变化的金属(如Cr、Ni、Ag和合金
(如黄铜))
电解质溶液:含有 镀层金属阳离子的电解质溶液——电镀液
②实例:铁上镀铜③特点:一多一少一不变
阳极溶解,阴极沉积,电镀液的浓度不变。
(3)电解精炼铜
阳极反应: Cu—2 e - =C u 2 + ( Zn—2 e - =Z n 2 + 、 Fe—2 e - =F e 2 + 、 Ni—2 e - =N i 2 + )
阳极泥成分: A u 、 Ag
阴极反应: C u 2 + +2 e - =Cu
(4)电冶金
①特点: 电解 是最强有力的氧化还原手段
②常见金属的冶炼方法:
热还原法(常见还原剂:C、CO、H 、
电解法(熔融态) 2 热分解法 物理方法
Al)
K、Ca、Na、Mg、Al Zn、Fe、Sn、Pb、Cu Hg、Ag Pt、Au
考点4 金属的腐蚀
1.金属腐蚀的本质
金属原子 失去电子变为 金属阳离子,金属发生 氧化反应。
2.金属腐蚀的类型
(1)化学腐蚀
①定义: 金属与其表面接触的一些物质(如 O 、 C l 、 SO 等)直接反应而引起的腐蚀
2 2 2
②特点: 无 电流产生,化学腐蚀的速度随温度升高而 加快 。
(2)电化学腐蚀
①定义:不纯的金属与电解质溶液接触时会发生原电池反应,比较活泼的金属发生氧化反应
而被腐蚀,
这种腐蚀叫做电化学腐蚀。
②特点: 有微弱 电流产生
注:化学腐蚀与电化学腐蚀的联系:化学腐蚀和电化学腐蚀往往同时 发生,但 电化学 腐
蚀更普遍,
电化学腐蚀 危害更大,腐蚀速率更 快3、钢铁的电化学腐蚀
(1)原电池的组成:负极:铁 正极: 碳 电解质:潮湿空气
(2)种类:根据钢铁表面水膜的酸性强弱分为 析氢 腐蚀和吸氧 腐蚀
①析氢腐蚀: 在酸性环境中,由于在腐蚀过程中不断有 H 放出,所以叫做析氢腐蚀。
2
水膜酸性较强: 负极: Fe—2 e - =F e 2 +
正极: 2H + +2 e - =H ↑
2
总反应: Fe+2H + =F e 2 + +H ↑
2
②吸氧腐蚀:钢铁表面吸附的水膜酸性很弱或呈中性,但溶有一定量的氧气,此时就会发生
吸氧腐蚀
水膜中溶有O ,呈弱酸性、中性或碱性: 负极: Fe—2 e - =F e 2 +
2
正极: O +4e - +2H O=4OH -
2 2
总反应: 2F e +O +2H O=2 Fe( OH )
2 2 2
4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 3
2Fe(OH) =Fe O ·xH O(铁锈)+(3-x)H O
3 2 3 2 2
注:I、只有 位于金属活动性顺序中氢前 的金属才可能发生析氢腐蚀
II、 氢前和氢后的金属 可发生吸氧腐蚀
4、金属的防护(1)电化学保护法
①牺牲阳极法—— 原电池 原理:
原理:正极: 被保护金属 负极: 活泼金属
注:Fe2+的检验:Fe2++K [Fe(CN) ]→KFe[Fe(CN) ]↓
3 6 6
黄 色 特征蓝 色
②外加电流法—— 电解池 原理:
原理:阴极: 被保护
(2)金属腐蚀快慢的规律
①构成原电池两极的活动性不同的两种金属,活动性差别越大,腐蚀越快 ;
②对于同一金属而言,纯度越高,腐蚀速率越慢
③对于同一种电解质来说,电解质溶液浓度越大,腐蚀速率越快
④同一种金属在相同浓度不同介质中,腐蚀由快到慢的顺序为:强电解质溶液 > 弱电解质溶
液 > 非电解质溶液
⑤在同一电解质中:电解池原理引起的腐蚀 > 原电池原理引起的腐蚀 > 化学腐蚀 > 有防护
措施的腐蚀
⑥有无保护措施的腐蚀快慢顺序:无保护措施的金属腐蚀 > 有一定保护措施的金属腐蚀 >
牺牲阳极法引起的腐蚀 > 有外加电流法引起的金属腐蚀