文档内容
树德中学高 2024 级高一上学期 10 月阶段性测试化学试题
考试时间:75分钟 总分:100分
可能用到的相对原子量:H1 C12 O16 Cl35.5 Na23 K39 Ca40 Fe56
选择题(每道题只有一个正确选项,每小题三分)
1. 中国传统文化对人类文明贡献巨大,《本草纲目》中有如下记载:“(火药)乃焰消(KNO)、硫黄、杉
3
木炭所合,以为烽燧铳机诸药者”,其中利用KNO 的性质是
3
A. 自燃性 B. 稳定性 C. 还原性 D. 氧化性
2. 盐是一类常见的物质,下列物质通过一步反应可直接形成盐的是
①金属单质 ②碱性氧化物 ③碱 ④非金属单质 ⑤酸性氧化物 ⑥酸
A. ①②③⑥ B. ①④⑤⑥ C. ②③⑤⑥ D. 全部
3. 能够在人体血管中通行的药物分子运输车-“纳米药物分子运输车”在中国科学院上海硅酸盐研究所研
制成功,该“运输车”可提高肿瘤的治疗效果,其结构如图所示。下列有关说法正确的是
A. 该“运输车”分散于水中所得的分散系属于胶体
B. 该“运输车”的外壳含有碳元素
C. 该“运输车”中的四氧化三铁为碱性氧化物
D. 二氧化硅属于属于酸性氧化物,是电解质
4. 下列离子方程式中,只能表示一个化学反应的是
①
②
③
④
A. ② B. ③ C. ④ D. 没有
第1页/共8页
学科网(北京)股份有限公司的
5. 如图是含氮化合物及单质 “类别-价态”二维图,结合二维图及氧化还原反应原理的基本规律,下列
相关分析或预测错误的是
A. 和 在一定条件下均能反应,可用氨气处理氮氧化物
B. 和 通入水的化学方程式:
C. 硝酸用于清洗粘有银的试管,因为银可以置换出稀硝酸中的
D. 可能被 氧化生成氮气
6. 下列叙述正确的是
A. B的阳离子的氧化性比A的阳离子强,说明A元素的金属性一定比B元素的强
B. 发生氧化还原反应时A原子失去的电子比B原子多,证明A的金属性一定比B的强
C. 已知氧化性: ,则 可以发生
D. 暖贴中的铁粉遇空气放热,该应用中涉及到氧化还原反应
7. 某研究性学习小组欲分析某矿石的主要成分,粉碎后将其溶于过量稀盐酸中充分反应,过滤后用所得滤
液进行如下实验,下列说法正确的是
A. 取少量滤液,向其中滴加过量 溶液,产生白色沉淀,说明矿石中含有
B. 取少量滤液,向其中滴加少量 溶液,无白色沉淀,说明矿石中一定不含
C. 取少量滤液,向其中加入硝酸酸化的硝酸银溶液,产生白色沉淀,说明矿石中一定含有
.
D 取少量滤液,向其中滴加适量 溶液,产生白色沉淀,说明矿石中一定含有
8. 下列相关条件下的离子方程式书写正确的是
第2页/共8页
学科网(北京)股份有限公司A. 向氢氧化钠溶液中通入足量二氧化硫:
B. 与 混合:
C. 向 溶液中加入足量的 溶液:
D. 碳酸氢钠溶液中滴加少量澄清石灰水:
9. 下列相关说法正确的是
化学反应方程式 相关说法
A 双线桥:
B 每生成1个 ,转移2个电子
C 氧化性:
将混合气体通入装饱和 溶液的洗气
D 除去 中的 气体
瓶
A. A B. B C. C D. D
10. 将一定量的氯气通入热的 浓溶液中,恰好完全反应,溶液中形成 和 的
共存体系。下列判断错误的是
A. 参加反应的氯气与 个数比为
B. 生成物中 和 的个数比可能为
C. 若有一个氯气参加反应,转移的电子数目1到 之间
D. 反应后的溶液中, 与 个数比可能为
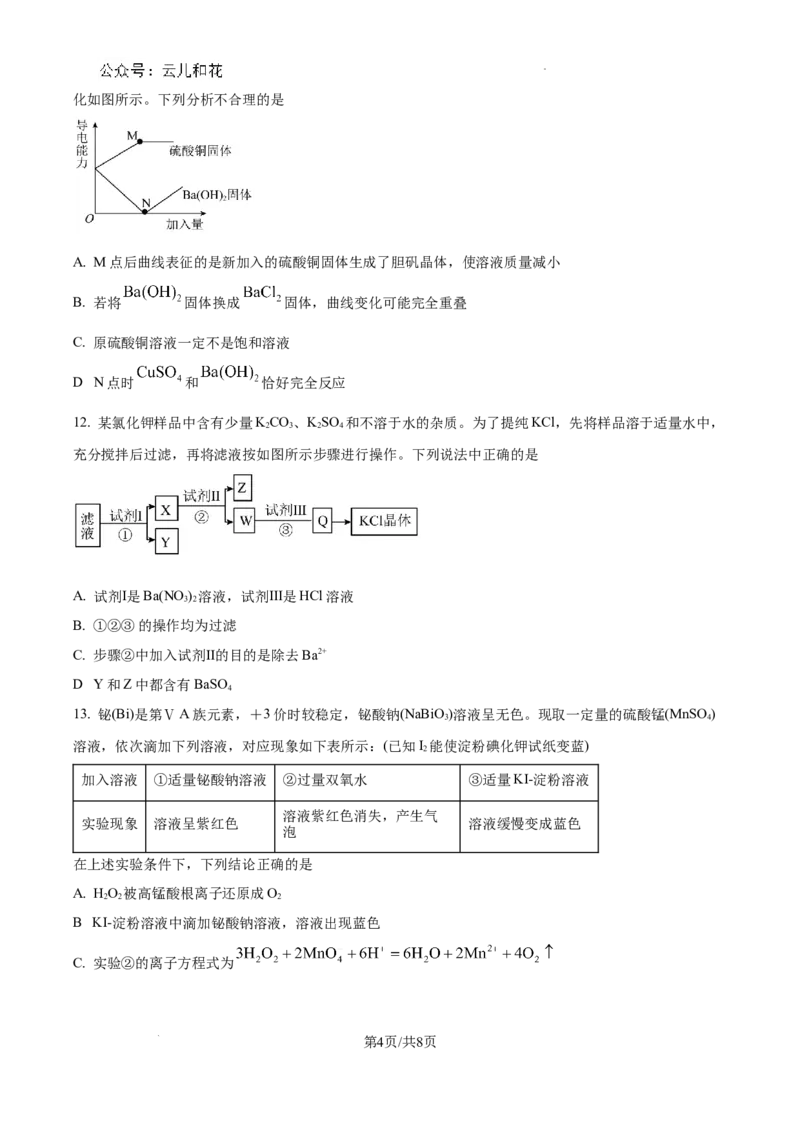
11. 常温下,向某硫酸铜溶液中分别加入硫酸铜固体和 固体,随着二者的加入,溶液的导电性变
第3页/共8页
学科网(北京)股份有限公司化如图所示。下列分析不合理的是
A. M点后曲线表征的是新加入的硫酸铜固体生成了胆矾晶体,使溶液质量减小
B. 若将 固体换成 固体,曲线变化可能完全重叠
C. 原硫酸铜溶液一定不是饱和溶液
.
D N点时 和 恰好完全反应
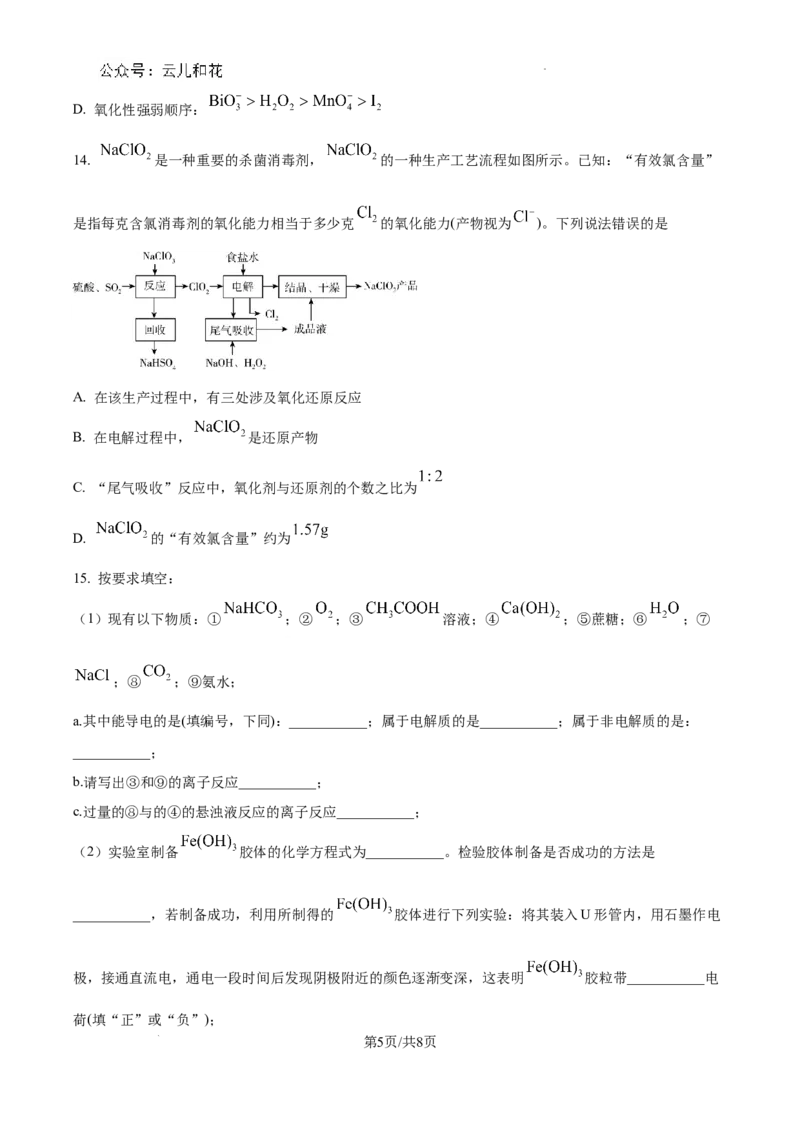
12. 某氯化钾样品中含有少量KCO、KSO 和不溶于水的杂质。为了提纯KCl,先将样品溶于适量水中,
2 3 2 4
充分搅拌后过滤,再将滤液按如图所示步骤进行操作。下列说法中正确的是
A. 试剂Ⅰ是Ba(NO ) 溶液,试剂Ⅲ是HCl溶液
3 2
B. ①②③的操作均为过滤
C. 步骤②中加入试剂Ⅱ的目的是除去Ba2+
.
D Y和Z中都含有BaSO
4
13. 铋(Bi)是第ⅤA族元素,+3价时较稳定,铋酸钠(NaBiO)溶液呈无色。现取一定量的硫酸锰(MnSO )
3 4
溶液,依次滴加下列溶液,对应现象如下表所示:(已知I 能使淀粉碘化钾试纸变蓝)
2
加入溶液 ①适量铋酸钠溶液 ②过量双氧水 ③适量KI-淀粉溶液
溶液紫红色消失,产生气
实验现象 溶液呈紫红色 溶液缓慢变成蓝色
泡
在上述实验条件下,下列结论正确的是
A. HO 被高锰酸根离子还原成O
2 2 2
.
B KI-淀粉溶液中滴加铋酸钠溶液,溶液出现蓝色
C. 实验②的离子方程式为
第4页/共8页
学科网(北京)股份有限公司D. 氧化性强弱顺序:
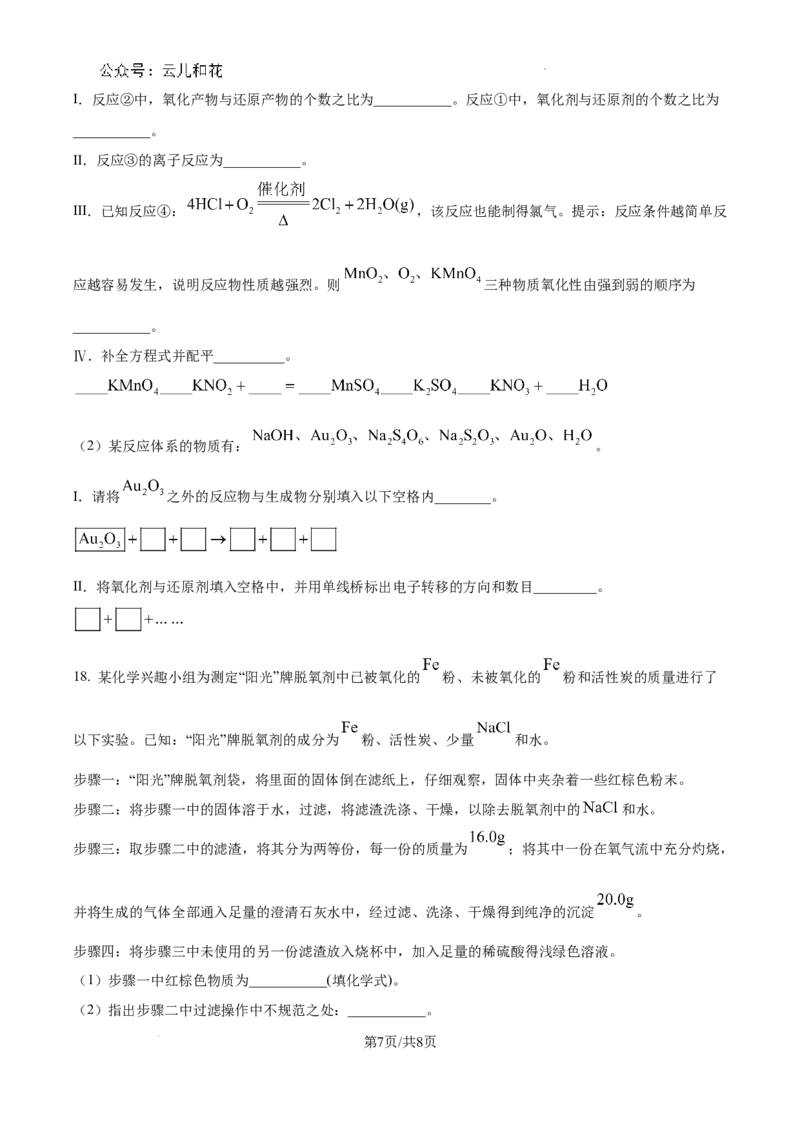
14. 是一种重要的杀菌消毒剂, 的一种生产工艺流程如图所示。已知:“有效氯含量”
是指每克含氯消毒剂的氧化能力相当于多少克 的氧化能力(产物视为 )。下列说法错误的是
A. 在该生产过程中,有三处涉及氧化还原反应
B. 在电解过程中, 是还原产物
C. “尾气吸收”反应中,氧化剂与还原剂的个数之比为
D. 的“有效氯含量”约为
15. 按要求填空:
(1)现有以下物质:① ;② ;③ 溶液;④ ;⑤蔗糖;⑥ ;⑦
;⑧ ;⑨氨水;
a.其中能导电的是(填编号,下同):___________;属于电解质的是___________;属于非电解质的是:
___________;
b.请写出③和⑨的离子反应___________;
c.过量的⑧与的④的悬浊液反应的离子反应___________;
(2)实验室制备 胶体的化学方程式为___________。检验胶体制备是否成功的方法是
___________,若制备成功,利用所制得的 胶体进行下列实验:将其装入U形管内,用石墨作电
极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明 胶粒带___________电
荷(填“正”或“负”);
第5页/共8页
学科网(北京)股份有限公司(3)在反应 中,若有10分子 参加反应,被水还原的溴
元素个数为___________;
(4) 与一定浓度的 反应,生成 和 ,当生成的
和 个数之比为 时,实际参加反应的 与 的个数之比为___________。
16. 已知: ,某溶液X中可能含有下列离子中的若干种:
,且所含离子的个数均相等。为了确定该溶液的组
成,某同学取上述溶液X,进行如下实验:
(1)白色沉淀1的成分是___________(写化学式)。
(2)溶液中一定存在的阳离子是___________(写离子符号,下同)。
(3)溶液中一定不存在的阴离子是___________。
(4)①写出加入足量 溶液产生白色沉淀的离子方程式___________。
②写出生成气体2的离子方程式___________。
17. 氧化还原反应在物质制备方面应用广泛。
(1)下面三个方法都可以用来制氯气:
①
②
③
根据以上三个反应,回答下列有关问题。
第6页/共8页
学科网(北京)股份有限公司I.反应②中,氧化产物与还原产物的个数之比为___________。反应①中,氧化剂与还原剂的个数之比为
___________。
Ⅱ.反应③的离子反应为___________。
Ⅲ.已知反应④: ,该反应也能制得氯气。提示:反应条件越简单反
应越容易发生,说明反应物性质越强烈。则 三种物质氧化性由强到弱的顺序为
___________。
Ⅳ.补全方程式并配平__________。
(2)某反应体系的物质有: 。
I.请将 之外的反应物与生成物分别填入以下空格内________。
Ⅱ.将氧化剂与还原剂填入空格中,并用单线桥标出电子转移的方向和数目_________。
18. 某化学兴趣小组为测定“阳光”牌脱氧剂中已被氧化的 粉、未被氧化的 粉和活性炭的质量进行了
以下实验。已知:“阳光”牌脱氧剂的成分为 粉、活性炭、少量 和水。
步骤一:“阳光”牌脱氧剂袋,将里面的固体倒在滤纸上,仔细观察,固体中夹杂着一些红棕色粉末。
步骤二:将步骤一中的固体溶于水,过滤,将滤渣洗涤、干燥,以除去脱氧剂中的 和水。
步骤三:取步骤二中的滤渣,将其分为两等份,每一份的质量为 ;将其中一份在氧气流中充分灼烧,
并将生成的气体全部通入足量的澄清石灰水中,经过滤、洗涤、干燥得到纯净的沉淀 。
步骤四:将步骤三中未使用的另一份滤渣放入烧杯中,加入足量的稀硫酸得浅绿色溶液。
(1)步骤一中红棕色物质为___________(填化学式)。
(2)指出步骤二中过滤操作中不规范之处:___________。
第7页/共8页
学科网(北京)股份有限公司(3)由步骤三可知, 滤渣中活性炭的质量为___________g。
(4)步骤四中发生的离子反应方程式为___________。
第8页/共8页
学科网(北京)股份有限公司