文档内容
泰安市肥城第二学期初三期中考试
化学试卷
时间:50分钟 满分:50分
一、选择题(共16分)
1.下列材料属于合金的是 ( )
A.纯硅 B.青铜器 C.青花瓷器 D.汉白玉雕塑
2.溶液析出晶体后,其剩余溶液是 ( )
A.饱和溶液 B.不饱和溶液 C.只有溶剂 D.稀溶液
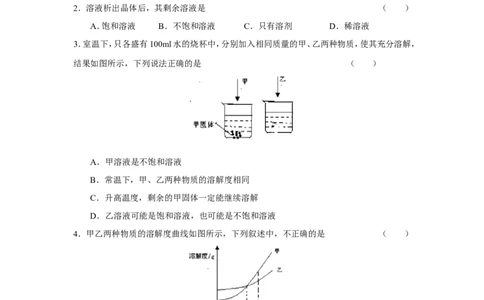
3.室温下,只各盛有100ml水的烧杯中,分别加入相同质量的甲、乙两种物质,使其充分溶解,
结果如图所示,下列说法正确的是 ( )
A.甲溶液是不饱和溶液
B.常温下,甲、乙两种物质的溶解度相同
C.升高温度,剩余的甲固体一定能继续溶解
D.乙溶液可能是饱和溶液,也可能是不饱和溶液
4.甲乙两种物质的溶解度曲线如图所示,下列叙述中,不正确的是 ( )
A.甲、乙两种物质的溶解度都随温度升高而增大
B.t℃时,甲物质的溶解度等于乙物质的溶解度
1
C.t℃时,甲物质的溶解度大于乙物质的溶解度
2
D.t℃时,甲、乙饱和溶液中溶质的质量分数相等
2
5.对于大多数固体溶质的不饱和溶液,要使之变为饱和溶液,可采取的方法有:①降低温度;②升高温度;③加入该温度下相同溶质的饱和溶液;④加入该固体物质,其中正确的方法有
( )
A.①②③ B.②③④ C.②④ D.①④
6.碳酸氢钠是生活中常见的盐,下列说法中,错误的是 ( )
A.发酵粉中含有碳酸氢钠,能使焙制出的糕点疏松多孔
B.干粉灭火器中含有碳酸氢钠,可用来扑灭油、气燃烧引起的火灾
C.碳酸氢钠和柠檬酸、水等混合可制成汽水
D.碳酸氢钠不能用来治疗胃酸过多
7.种试剂鉴别盐酸、氯化钠和氢氧化钠三种溶液,应选用的试剂是 ( )
A.稀硫酸 B.碳酸钠溶液 C.氯化钡溶液 D.氢氧化钾溶液
8.一些重金属盐的离子如:Ag+、Cu2+、Ba2+、Pb2+等能使蛋白质丧失生理功能,使生物体中毒,
人体胃液中含有盐酸,误服含有下列物质的药剂不会引起人体中毒的是 ( )
A.CuCO B.CuSO C.BaCO D.BaSO
3 4 3 4
9.溶质能大量共存于水溶液中的是 ( )
A.HNO Ca(OH) NaCl B.KNO CuCl NaSO
3 2 3 2 4
C.NaOH MgSO BaCl D.HCl NaCO Ca(NO )
4 2 2 3 3 2
10.物间的转化,不能一步实现的是 ( )
A.MgSO MgCl B.NaCO NaOH
4 2 2 3
C.CaCO Ca(OH) D.Fe(OH) FeCl
3 2 3 3
11.有X、Y、Z三种金属,将X、Y、Z分别浸入稀硫酸中,Z溶解,X、Y不溶解,将X浸入Y的
化合物的溶液中,在X的表面有Y析出,则X、Y、Z三种金属的活动性由强到弱的顺序为
( )
A.Z>Y>X B.Y>Z>X C.Z>X>Y D.Y>X>Z
12.白蚁会蛀蚀木头,它分泌的蚁酸是一种酸,还能腐蚀很多建筑材料,下列建筑材料最不易受
到白蚁分泌物腐蚀的是 ( )
A.铜塑像 B.钢筋 C.大理石 D.铝合金
13.下列关于铁制品及铁制品的说法中不正确的是 ( )
A.铁制品生锈后可以隔绝里面的铁与空气的进一步接触
B.铁制品生锈是缓慢氧化过程
C.车、船表面涂上一层油漆可以防止铁生锈
D.生铁报废的铁制品可以回收重新提炼14.食品包装袋内常有一小包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸剂”,
下列物质可以作“双吸剂”的是 ( )
A.木炭粉 B.铁粉 C.铜粉 D.氯化钠
15.化学在生活中无处不在,生活中的下列做法,你认为合理的是 ( )
A.家居装饰好后应立即入住
B.霉变的大米蒸熟后可放心食用
C.火腿肠中含有防腐剂亚硝酸钠,所以火腿肠都不能食用
D.硫酸铜有毒,但可用少量的硫酸铜消毒游泳池
16.草木灰是农村广泛使用的农家钾肥,它的水溶液呈碱性,下列化肥中能与它混合施用的
是 ( )
A.KSO B.NH Cl C.NH NO D.(NH )SO 二、
2 4 4 4 3 4 2 4
填空题(共27分)
17.以下是几种常见化肥的主要成分:
①NH HCO ②KCO ③(NH )HPO ④KCl
4 3 2 3 4 2 4
(1)属于复合肥的是 (填序号)
(2)NH HCO 受热易分解为氨气、水和二氧化碳,其反应的化学方程式为:
4 3
18.青少年正处在生长发育期,应注意营养均衡,膳食合理。
(1)有些青少年不爱吃蔬菜、水果,影响生长发育,这主要是由于摄入 (填序号)不足
而引起的。
①维生素 ②油脂 ③蛋白质
(2)“XX糕点”主要营养成分如下表所示。请根据该表回答。
XX糕点
营养素 每100g含有
蛋白质 4.8g
油脂 20g
糖类 40g
β-胡萝卜素(维生素类) 1.8mg
碳酸钙 400mg
①所含营养素中属于无机盐的是 ,没有列出的一类营养素是 。
②正常情况下,人每日摄入的油脂不超过60g,由此计算,每日食用该糕点最多不应超过
g.
③糖类是人体所需 的主要来源。19.佛山是有色金属之乡,其中铝合金材料的产量约占全国的一半,合金材料属于
(填“混合物”或“化合物”),铝是活泼金属,生活中的铝锅却有较强的抗腐蚀性,原因是
(用化学方程式表示)。如果将表面有
氧化膜的铝片投入稀硫酸中。片刻之后才有气泡产生,请用化学方程式表示这一过程:
, 。
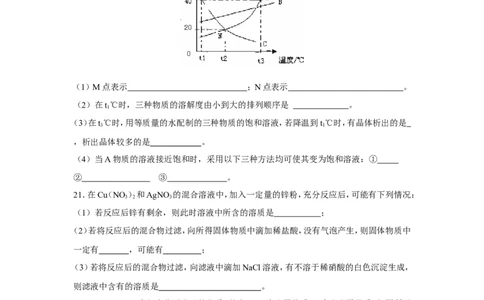
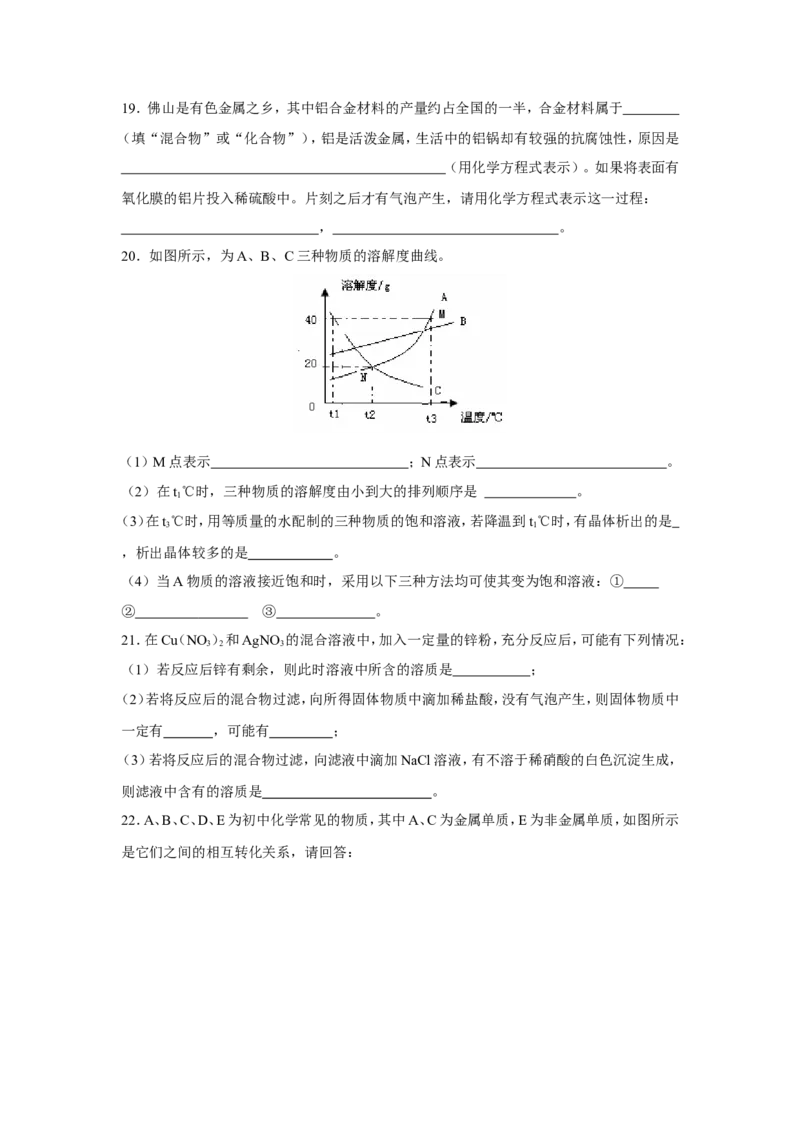
20.如图所示,为A、B、C三种物质的溶解度曲线。
(1)M点表示 ;N点表示 。
(2)在t℃时,三种物质的溶解度由小到大的排列顺序是 。
1
(3)在t℃时,用等质量的水配制的三种物质的饱和溶液,若降温到t℃时,有晶体析出的是
3 1
,析出晶体较多的是 。
(4)当A物质的溶液接近饱和时,采用以下三种方法均可使其变为饱和溶液:①
② ③ 。
21.在Cu(NO )和AgNO 的混合溶液中,加入一定量的锌粉,充分反应后,可能有下列情况:
3 2 3
(1)若反应后锌有剩余,则此时溶液中所含的溶质是 ;
(2)若将反应后的混合物过滤,向所得固体物质中滴加稀盐酸,没有气泡产生,则固体物质中
一定有 ,可能有 ;
(3)若将反应后的混合物过滤,向滤液中滴加NaCl溶液,有不溶于稀硝酸的白色沉淀生成,
则滤液中含有的溶质是 。
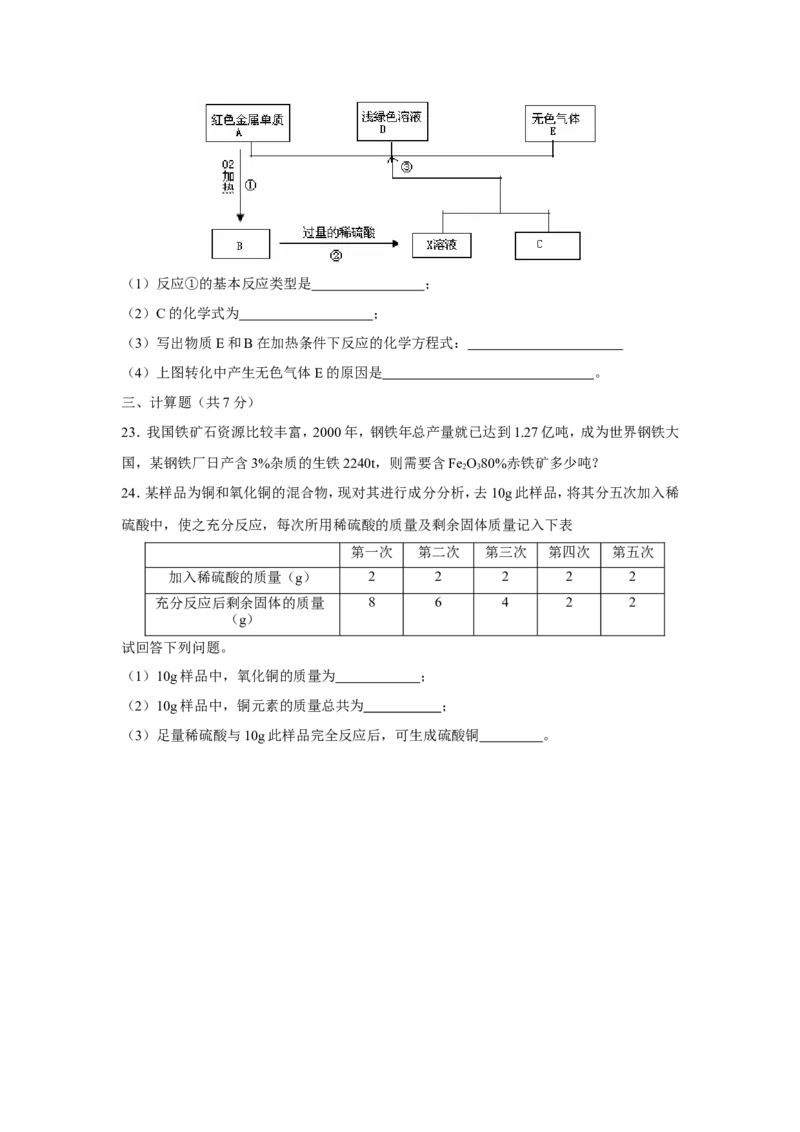
22.A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,如图所示
是它们之间的相互转化关系,请回答:(1)反应①的基本反应类型是 ;
(2)C的化学式为 ;
(3)写出物质E和B在加热条件下反应的化学方程式:
(4)上图转化中产生无色气体E的原因是 。
三、计算题(共7分)
23.我国铁矿石资源比较丰富,2000年,钢铁年总产量就已达到1.27亿吨,成为世界钢铁大
国,某钢铁厂日产含3%杂质的生铁2240t,则需要含Fe O80%赤铁矿多少吨?
2 3
24.某样品为铜和氧化铜的混合物,现对其进行成分分析,去10g此样品,将其分五次加入稀
硫酸中,使之充分反应,每次所用稀硫酸的质量及剩余固体质量记入下表
第一次 第二次 第三次 第四次 第五次
加入稀硫酸的质量(g) 2 2 2 2 2
充分反应后剩余固体的质量 8 6 4 2 2
(g)
试回答下列问题。
(1)10g样品中,氧化铜的质量为 ;
(2)10g样品中,铜元素的质量总共为 ;
(3)足量稀硫酸与10g此样品完全反应后,可生成硫酸铜 。化学试卷参考答案
一、 选择题
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16
B A D A D D B D B C C D A B D A
二、 填空题
17.(1)③ (2)NH HCO
4 3
18.(1)① (2)① 碳酸钙 水 ② 300 ③ 能量
19.混合物 4Al+3O ==2AlO Al O+3H SO ==Al(SO )+3HO
2 2 3 2 3 2 4 2 4 3 2
== Al (SO )
2 4 3
20.(1)t℃时,A物质的溶解度为40g
3
t℃时,A、C两物质的溶解度相同都为20g
2
(2)A B C (3) AB A
(4)①增加溶质 ②蒸发溶剂 ③降低温度
21.(1)Zn(NO ) (2)Ag Cu (3)Zn(NO ) Cu(NO ) AgNO
3 2 3 2 3 2 3
22.(1)化合反应 (2)Fe (3) Cu+HO (4)略
2
23.3880t
24.(1) 8g (2) 8.4g (3) 16g