文档内容
第四章 物质结构 元素周期律
单元复习检测
1.(2020·全国高一课时练习)已知某元素的原子核外最外层电子数=最内层电子数=
电子层数,则该元素是( )
A.氦 B.锂 C.铍 D.镁
2.(2020·全国高一课时练习)下列对于第二周期主族元素的叙述正确的是( )
A.从左到右,原子得电子能力逐渐减弱 B.从左到右,元素的非金属性逐渐增强
C.从左到右,元素的最高正价依次升高 D.从左到右,原子半径依次增大
3.(2020·全国高一课时练习)人们发现金星大气层有一种称为羰基硫(COS)的分子,
其结构与 类似,羰基硫是一种与生命密切相关的物质,下列推测不正确的是
( )
A.COS是含有极性键的共价化合物 B.COS为直线形分子
C.COS的电子式为: D.COS中所有原子都满足8电子稳定结
构
4.(2020·全国高一课时练习)下列微粒中半径最小的是( )
A.Na B.F— C.Al3+ D.Cl—
5.(2020·全国高一课时练习)高铁动车车厢禁止吸烟。高铁装有的离子式烟雾传感
器具有稳定性好、灵敏度高的特点,其主体是一个放有镅( Am)放射源的电离室。
下列关于 Am的说法中,不正确的是( )
A.质子数为95 B.质量数为241
C.核外电子数为146 D.中子数为146
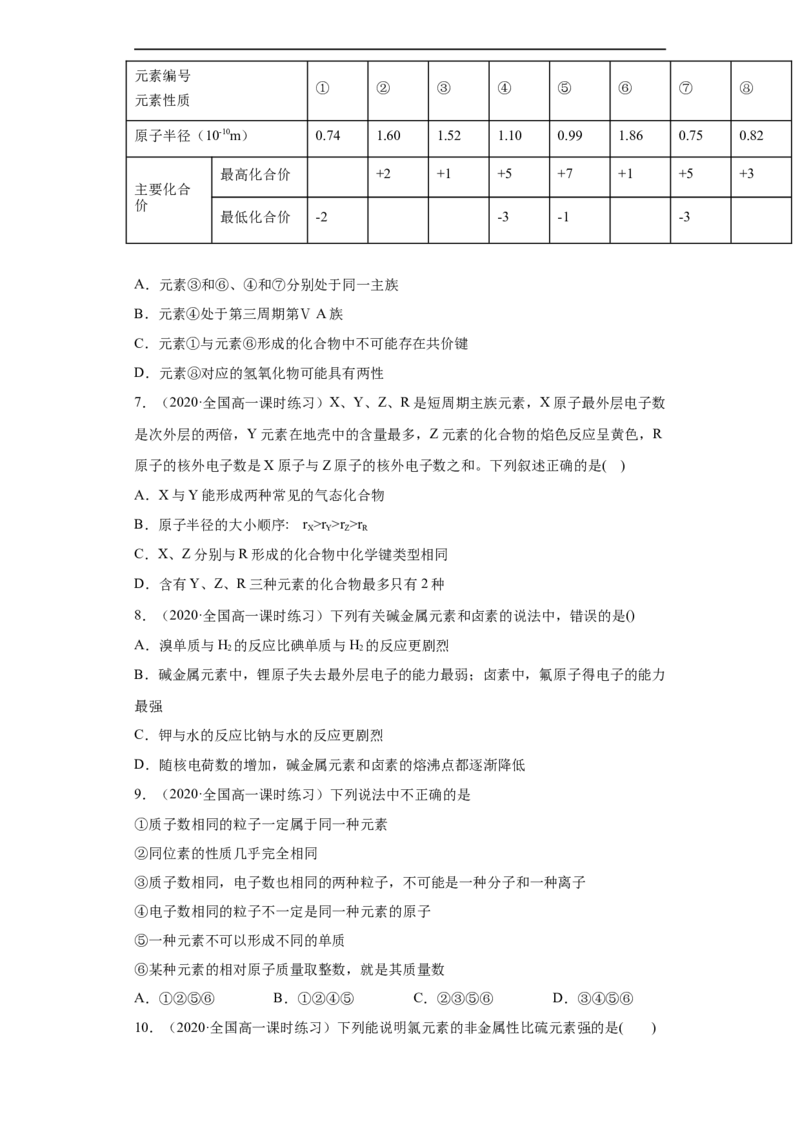
6.(2020·全国高一课时练习)根据下表中有关短周期元素性质的数据,判断下列说
法不正确的是( )元素编号
① ② ③ ④ ⑤ ⑥ ⑦ ⑧
元素性质
原子半径(10-10m) 0.74 1.60 1.52 1.10 0.99 1.86 0.75 0.82
最高化合价 +2 +1 +5 +7 +1 +5 +3
主要化合
价
最低化合价 -2 -3 -1 -3
A.元素③和⑥、④和⑦分别处于同一主族
B.元素④处于第三周期第ⅤA族
C.元素①与元素⑥形成的化合物中不可能存在共价键
D.元素⑧对应的氢氧化物可能具有两性
7.(2020·全国高一课时练习)X、Y、Z、R是短周期主族元素,X原子最外层电子数
是次外层的两倍,Y元素在地壳中的含量最多,Z元素的化合物的焰色反应呈黄色,R
原子的核外电子数是X原子与Z原子的核外电子数之和。下列叙述正确的是( )
A.X与Y能形成两种常见的气态化合物
B.原子半径的大小顺序: r >r >r >r
X Y Z R
C.X、Z分别与R形成的化合物中化学键类型相同
D.含有Y、Z、R三种元素的化合物最多只有2种
8.(2020·全国高一课时练习)下列有关碱金属元素和卤素的说法中,错误的是()
A.溴单质与H 的反应比碘单质与H 的反应更剧烈
2 2
B.碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子的能力
最强
C.钾与水的反应比钠与水的反应更剧烈
D.随核电荷数的增加,碱金属元素和卤素的熔沸点都逐渐降低
9.(2020·全国高一课时练习)下列说法中不正确的是
①质子数相同的粒子一定属于同一种元素
②同位素的性质几乎完全相同
③质子数相同,电子数也相同的两种粒子,不可能是一种分子和一种离子
④电子数相同的粒子不一定是同一种元素的原子
⑤一种元素不可以形成不同的单质
⑥某种元素的相对原子质量取整数,就是其质量数
A.①②⑤⑥ B.①②④⑤ C.②③⑤⑥ D.③④⑤⑥
10.(2020·全国高一课时练习)下列能说明氯元素的非金属性比硫元素强的是( )①HCl比 稳定
② 的还原性比 的强
③ 能与 反应生成S
④HCl的溶解度比 的大
⑤ 与Fe反应生成 ,S与Fe反应生成FeS
⑥HC的酸性比 的强
A.①②③⑤ B.①②④⑤ C.②③⑤⑥ D.①②③④⑤⑥
11.(2020·全国高一课时练习)下列说法正确的是( )。
A.离子键就是阴阳离子间的静电引力
B.所有金属元素与所有非金属元素间都能形成离子键
C.钠原子与氯原子结合成氯化钠后体系能量降低
D.在离子化合物CaCl 中,两个氯离子间也存在离子键
2
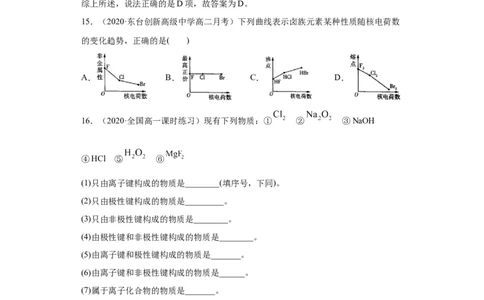
12.(2020·全国高一课时练习)几种短周期元素的原子半径及主要化合价如表所示:
元素符号 X Y Z R T
原子半径/nm 0.160 0.089 0.102 0.143 0.074
主要化合价 +2 +2 -2、+4、+6 +3 -2
根据表中信息,判断以下说法正确的是( )
A.单质与稀硫酸反应的速率大小:
B.X、R的最高价氧化物对应水化物均能溶于NaOH 溶液
C.元素最高价氧化物对应的水化物的碱性:
D.相同条件下,气态氢化物的稳定性:
13.(2020·全国高一课时练习)下列各数值表示有关元素的原子序数,其所表示的各
原子组中能以离子键相互结合成稳定化合物的是( )
A.6与16 B.11与17 C.14与8 D.10与19
14.(2020·全国高一课时练习)X、Y、Z、W是四种常见的短周期主族元素,其原子
半径随原子序数的变化如图所示。已知Y、Z两种元素的单质是空气的主要成分,W
原子的最外层电子数与Ne原子的最外层电子数相差1。下列说法正确的是( )A.Y、Z、W处于同一周期
B.Y、Z、W与X形成的化合物中均含有氢键
C.X、W可形成化学式为XW的离子化合物
D.简单离子半径:
综上所述,说法正确的是D项,故答案为D。
15.(2020·东台创新高级中学高二月考)下列曲线表示卤族元素某种性质随核电荷数
的变化趋势,正确的是( )
A. B. C. D.
16.(2020·全国高一课时练习)现有下列物质:① ② ③NaOH
④HCl ⑤ ⑥
(1)只由离子键构成的物质是________(填序号,下同)。
(2)只由极性键构成的物质是_________。
(3)只由非极性键构成的物质是________。
(4)由极性键和非极性键构成的物质是________。
(5)由离子键和极性键构成的物质是_______。
(6)由离子键和非极性键构成的物质是______。
(7)属于离子化合物的物质是_______。
(8)属于共价化合物的物质是_______。
17.(2020·全国高一课时练习)a、b、c、d、e、f、g为七种由短周期元素构成的粒
子,它们都具有10个电子,其结构特点如下:
粒子 a b c d e f g
原子核数 单核 单核 双核 多核 单核 多核 多核
所带电荷 0 +1 -1 0 +2 +1 0
其中b的离子半径大于e的离子半径;d是由四原子构成的分子;c和f在一定条件下
可形成两个共价型g分子。试写出:(1)用化学符号表示下列四种微粒:①c___;②d__;③f__;④g__。
(2)画出a微粒的结构示意图__。
(3)b与e相应元素的最高价氧化物对应水化物的碱性强弱为__>__(用化学式表示)。
(4)g与一种含有非极性键双核18电子分子反应的化学方程式为__,上述反应中,断裂
的化学键类型是__,形成的化学键类型是__。
18.(2020·全国高一课时练习)元素周期表与元素周期律在化学学习研究中有很重要
的作用。如表所示是五种元素的相关信息,W、X都位于第三周期。
元素 信息
Q 地壳中含量最高
W 最高化合价为+7
X 最高价氧化物对应的水化物在第三周期中碱性最强
Y 焰色试验(透过蓝色钴玻璃)火焰呈紫色
Z 原子结构示意图为
(1)Q在元素周期表中的位置是________。
(2)W的最高价氧化物对应的水化物的化学式是_________。
(3)X单质与水反应的离子方程式是__________。
(4)金属性 ,用原子结构解释原因:_________,失电子能力 ,金属性
。
(5)下列对于Z及其化合物的推断正确的是________(填字母)。
A.Z的最低负化合价与W的最低负化合价相同
B.Z的氢化物的稳定性弱于W的氢化物的稳定性
C.Z的单质的氧化性强于W的单质的氧化性
19.(2020·全国高一课时练习)Ⅰ.A、B、C、D四种元素,原子序数依次增大,A
原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元
素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上
的电子数之和。
(1)B为_______,D的最高价氧化物对应的水化物是______,简单离子半径大小
B_______(填“>”“<”或“=”)C。
(2)写出A、B的化合物与E反应的化学方程式:_______。
(3)A、B两元素形成的化合物属于______(填“离子”或“共价”)化合物。
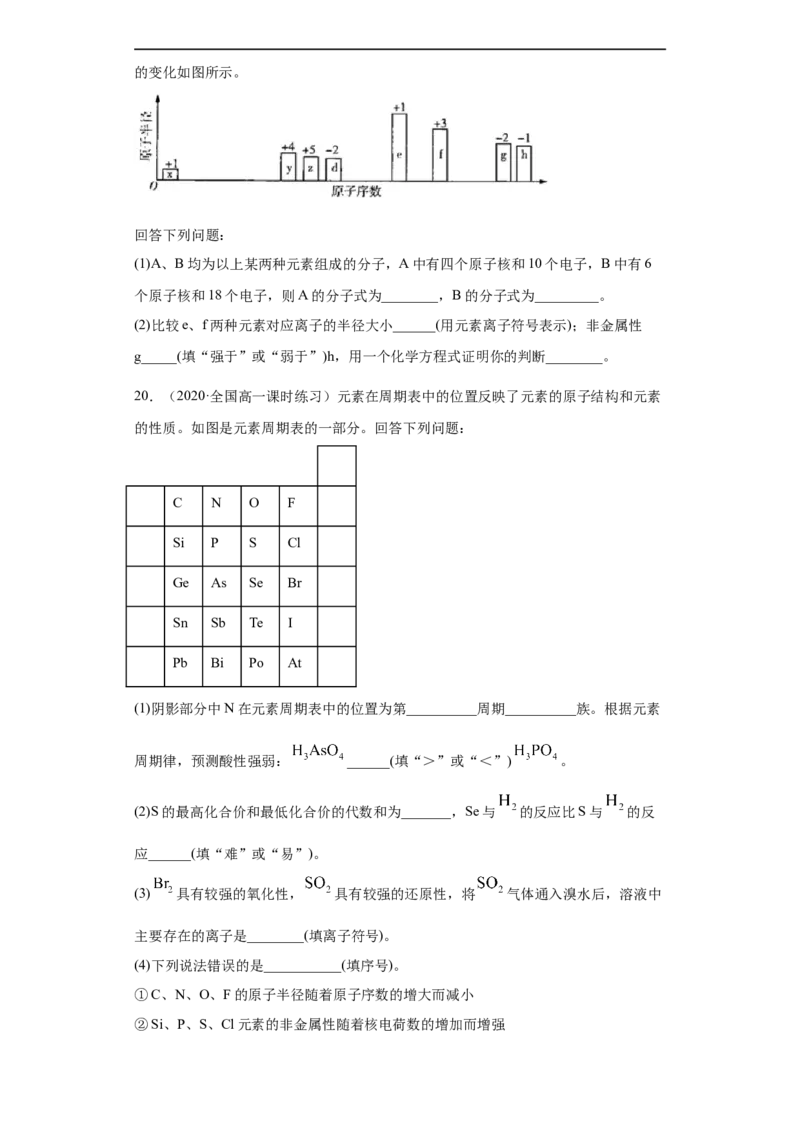
Ⅱ.随原子序数的递增,八种短周期元素原子半径的相对大小、最高正价或最低负价的变化如图所示。
回答下列问题:
(1)A、B均为以上某两种元素组成的分子,A中有四个原子核和10个电子,B中有6
个原子核和18个电子,则A的分子式为________,B的分子式为_________。
(2)比较e、f两种元素对应离子的半径大小______(用元素离子符号表示);非金属性
g_____(填“强于”或“弱于”)h,用一个化学方程式证明你的判断________。
20.(2020·全国高一课时练习)元素在周期表中的位置反映了元素的原子结构和元素
的性质。如图是元素周期表的一部分。回答下列问题:
C N O F
Si P S Cl
Ge As Se Br
Sn Sb Te I
Pb Bi Po At
(1)阴影部分中N在元素周期表中的位置为第__________周期__________族。根据元素
周期律,预测酸性强弱: ______(填“>”或“<”) 。
(2)S的最高化合价和最低化合价的代数和为_______,Se与 的反应比S与 的反
应______(填“难”或“易”)。
(3) 具有较强的氧化性, 具有较强的还原性,将 气体通入溴水后,溶液中
主要存在的离子是________(填离子符号)。
(4)下列说法错误的是___________(填序号)。
①C、N、O、F的原子半径随着原子序数的增大而减小
②Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强③由元素周期律可直接推断出酸性:
④HF、HCl、HBr、HI的稳定性逐渐减弱