文档内容
微专题 12 铝三角及其转化关系
1.Al3+、Al(OH) 、AlO之间的转化关系
3
实现上述各步转化的离子方程式:
(1)①Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
②Al3++3AlO+6HO===4Al(OH) ↓
2 3
③Al3++3OH-===Al(OH) ↓
3
(2)Al(OH) +3H+===Al3++3HO
3 2
(3)Al3++4OH-===AlO+2HO
2
(4)AlO+4H+===Al3++2HO
2
(5)①AlO+CO+2HO===Al(OH) ↓+HCO ②AlO+H++HO===Al(OH) ↓
2 2 3 2 3
(6)Al(OH) +OH-===AlO+2HO
3 2
2.与Al(OH) 沉淀生成有关的图象分析
3
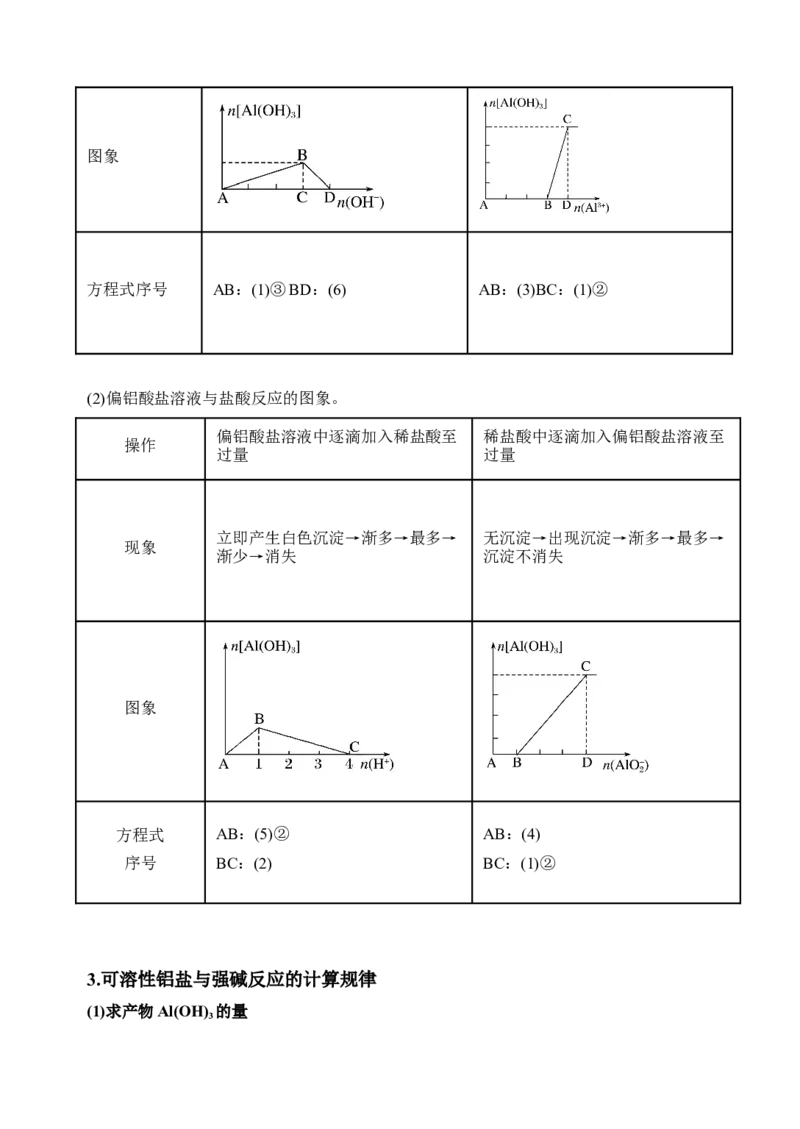
(1)可溶性铝盐溶液与NaOH溶液反应的图象(从上述转化关系中选择符合图象变化的离子
方程式,下同)。
可溶性铝盐溶液中逐滴加入NaOH NaOH溶液中逐滴加入可溶性铝盐
操作
溶液至过量 溶液至过量
立即产生白色沉淀→渐多→最多→ 无沉淀(有但即溶)→出现沉淀→渐
现象
渐少→消失 多→最多→沉淀不消失图象
方程式序号 AB:(1)③BD:(6) AB:(3)BC:(1)②
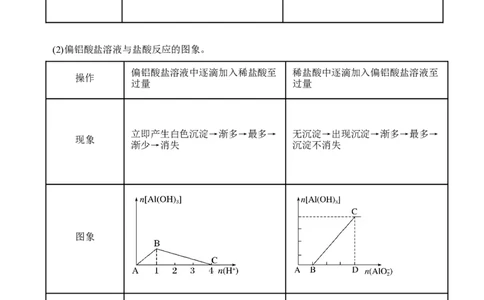
(2)偏铝酸盐溶液与盐酸反应的图象。
偏铝酸盐溶液中逐滴加入稀盐酸至 稀盐酸中逐滴加入偏铝酸盐溶液至
操作
过量 过量
立即产生白色沉淀→渐多→最多→ 无沉淀→出现沉淀→渐多→最多→
现象
渐少→消失 沉淀不消失
图象
方程式 AB:(5)② AB:(4)
序号 BC:(2) BC:(1)②
3.可溶性铝盐与强碱反应的计算规律
(1)求产物Al(OH) 的量
3①当n(OH-)≤3n(Al3+)时,n[Al(OH) ]=n(OH-);
3
②当3n(Al3+)<n(OH-)<4n(Al3+)时,n[Al(OH) ]=
3
4n(Al3+)-n(OH-);
③当n(OH-)≥4n(Al3+)时,n[Al(OH) ]=0,无沉淀。
3
(2)求反应物碱的量
①若碱不足(Al3+未完全沉淀),n(OH-)=3n[Al(OH) ];
3
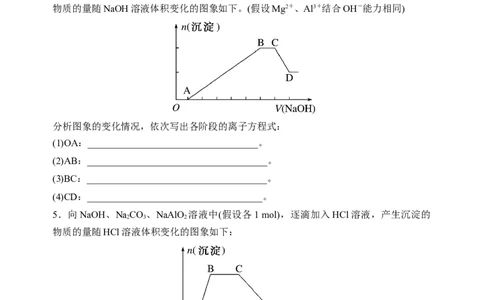
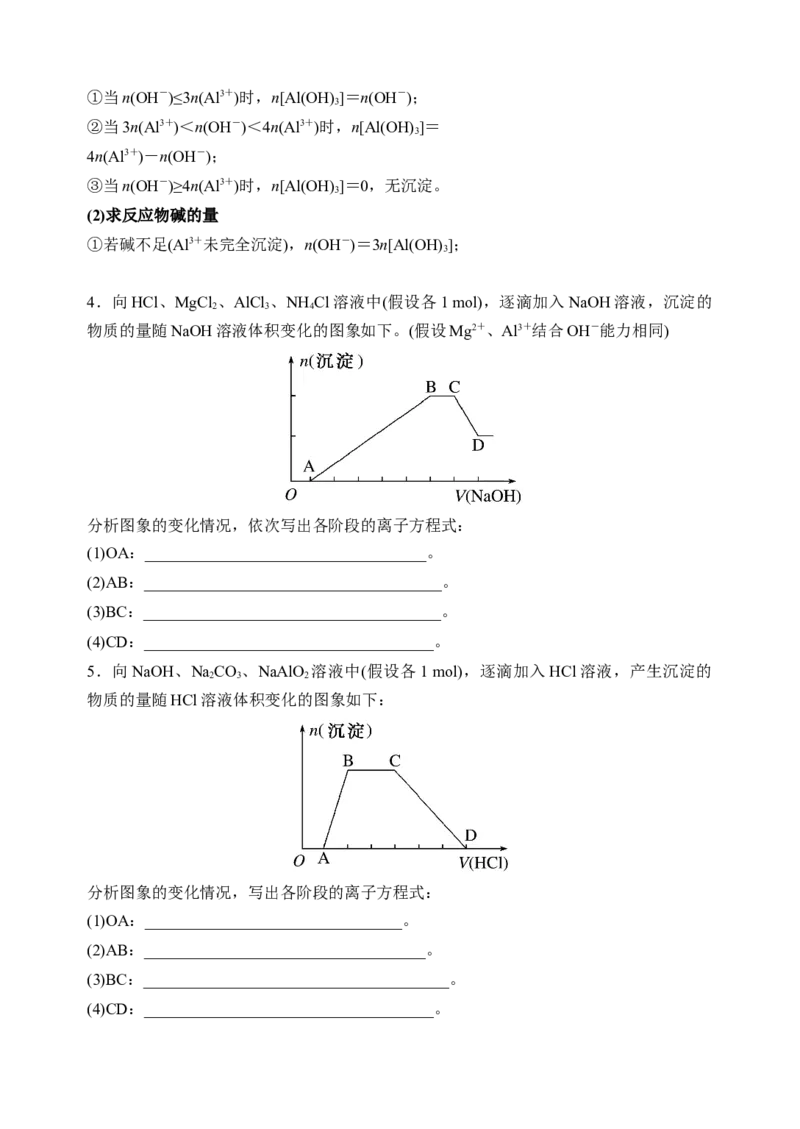
4.向HCl、MgCl 、AlCl 、NH Cl溶液中(假设各1 mol),逐滴加入NaOH溶液,沉淀的
2 3 4
物质的量随NaOH溶液体积变化的图象如下。(假设Mg2+、Al3+结合OH-能力相同)
分析图象的变化情况,依次写出各阶段的离子方程式:
(1)OA:___________________________________。
(2)AB:_____________________________________。
(3)BC:_____________________________________。
(4)CD:____________________________________。
5.向NaOH、NaCO 、NaAlO 溶液中(假设各1 mol),逐滴加入HCl溶液,产生沉淀的
2 3 2
物质的量随HCl溶液体积变化的图象如下:
分析图象的变化情况,写出各阶段的离子方程式:
(1)OA:________________________________。
(2)AB:___________________________________。
(3)BC:______________________________________。
(4)CD:____________________________________。6.与Al3+、AlO有关的离子反应的一般规律
(1)当溶液中有多种离子时,要考虑离子之间的反应顺序,如向含有 H+、NH、Mg2+、Al3
+的混合溶液中逐滴加入NaOH溶液,OH-先与H+反应,再与Mg2+、Al3+反应生成沉淀,
再与NH反应,最后才溶解Al(OH) 沉淀。
3
(2)AlO与HCO的反应不属于水解相互促进的反应,而是HCO电离出的H+与AlO发生反
应:AlO+HCO+HO===Al(OH) ↓+CO。
2 3
【典例精析】
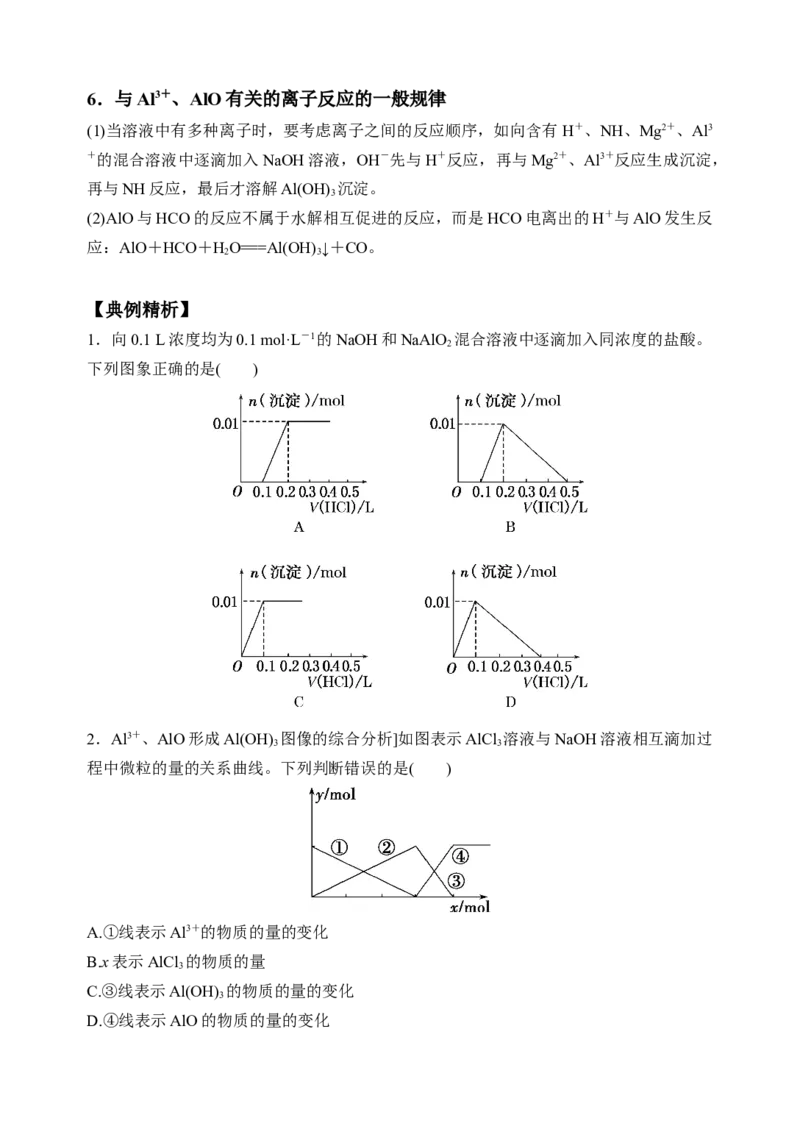
1.向0.1 L浓度均为0.1 mol·L-1的NaOH和NaAlO 混合溶液中逐滴加入同浓度的盐酸。
2
下列图象正确的是( )
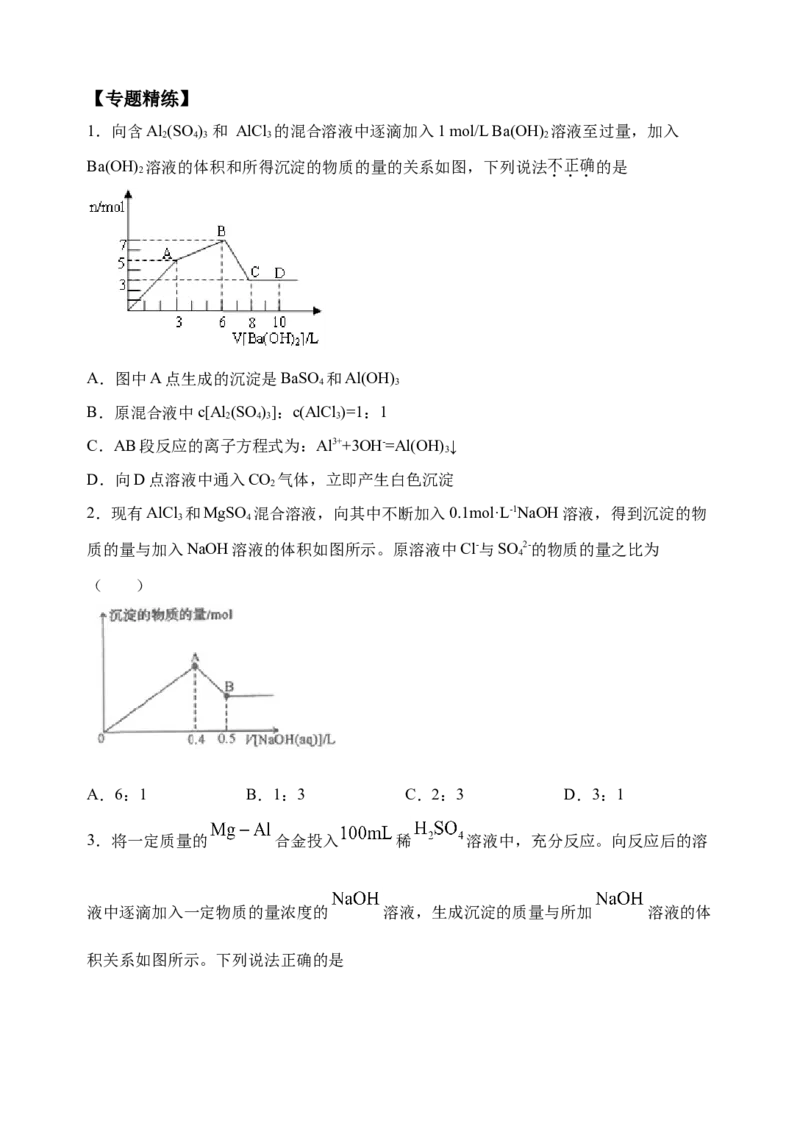
2.Al3+、AlO形成Al(OH) 图像的综合分析]如图表示AlCl 溶液与NaOH溶液相互滴加过
3 3
程中微粒的量的关系曲线。下列判断错误的是( )
A.①线表示Al3+的物质的量的变化
B.x表示AlCl 的物质的量
3
C.③线表示Al(OH) 的物质的量的变化
3
D.④线表示AlO的物质的量的变化【专题精练】
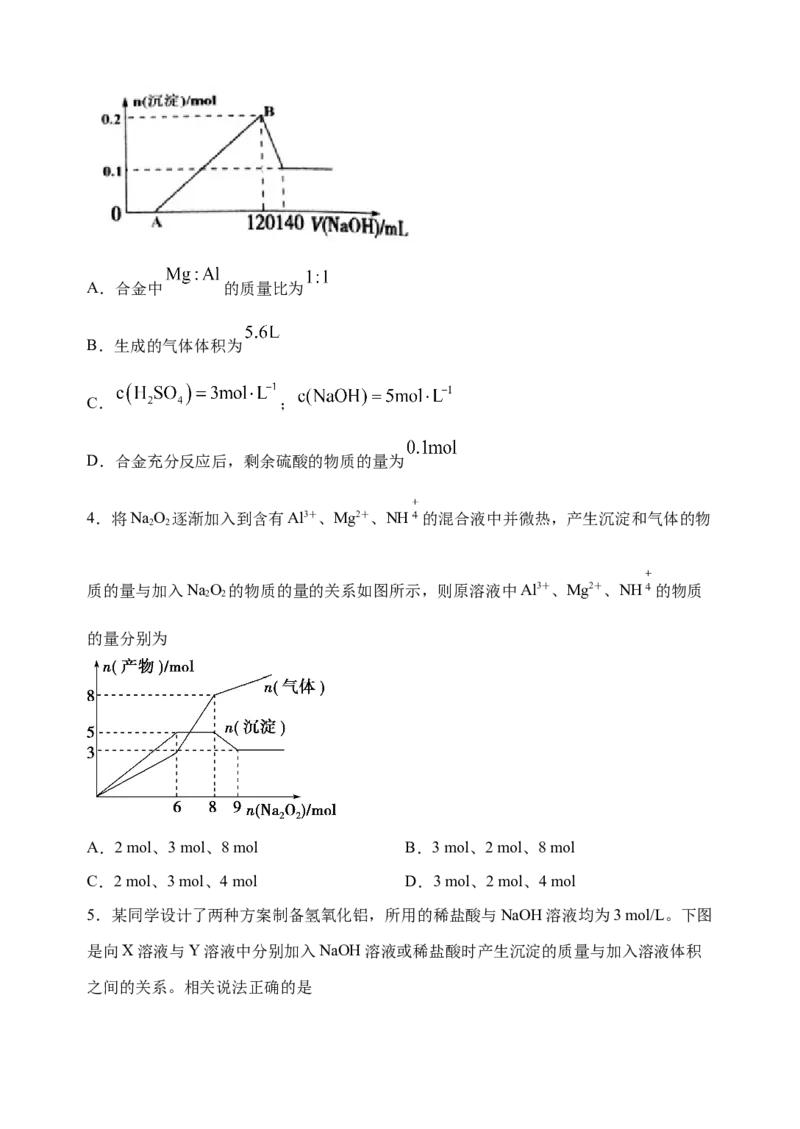
1.向含Al (SO ) 和 AlCl 的混合溶液中逐滴加入1 mol/L Ba(OH) 溶液至过量,加入
2 4 3 3 2
Ba(OH) 溶液的体积和所得沉淀的物质的量的关系如图,下列说法不正确的是
2
A.图中A点生成的沉淀是BaSO 和Al(OH)
4 3
B.原混合液中c[Al (SO )]:c(AlCl )=1:1
2 4 3 3
C.AB段反应的离子方程式为:Al3++3OH-=Al(OH) ↓
3
D.向D点溶液中通入CO 气体,立即产生白色沉淀
2
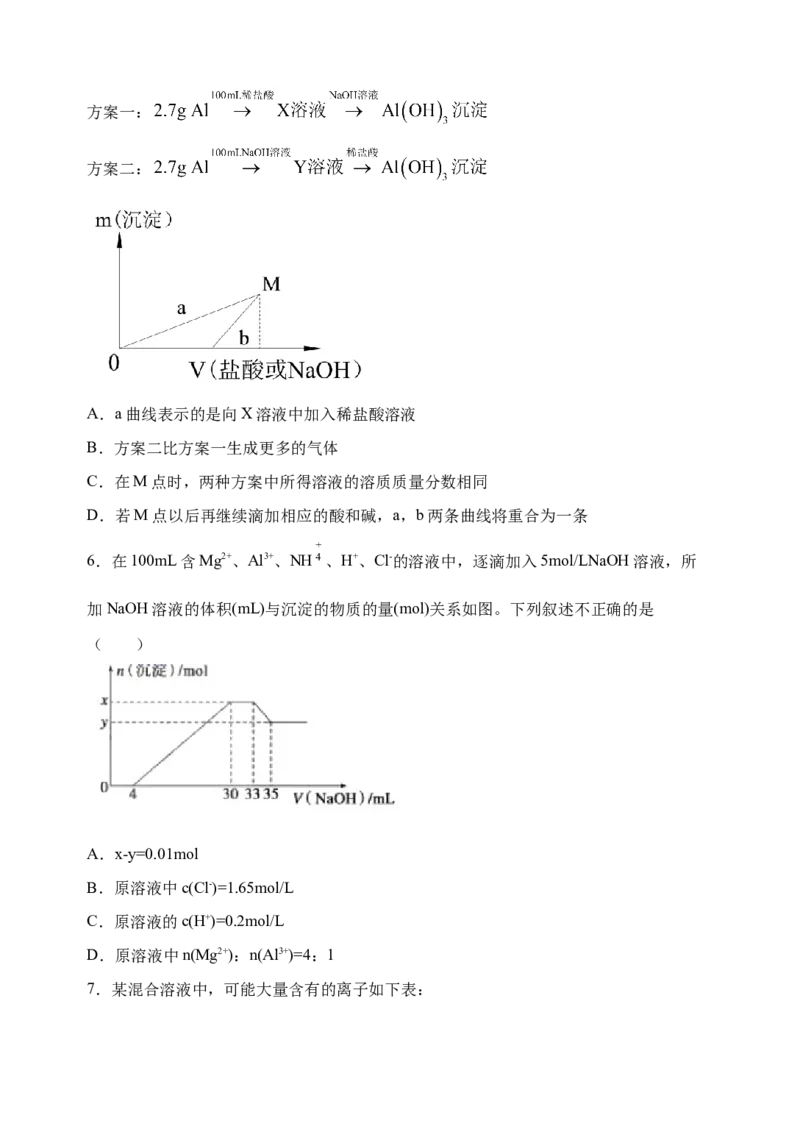
2.现有AlCl 和MgSO 混合溶液,向其中不断加入0.1mol·L-1NaOH溶液,得到沉淀的物
3 4
质的量与加入NaOH溶液的体积如图所示。原溶液中Cl-与SO 2-的物质的量之比为
4
( )
A.6:1 B.1:3 C.2:3 D.3:1
3.将一定质量的 合金投入 稀 溶液中,充分反应。向反应后的溶
液中逐滴加入一定物质的量浓度的 溶液,生成沉淀的质量与所加 溶液的体
积关系如图所示。下列说法正确的是A.合金中 的质量比为
B.生成的气体体积为
C. ;
D.合金充分反应后,剩余硫酸的物质的量为
4.将NaO 逐渐加入到含有Al3+、Mg2+、NH 的混合液中并微热,产生沉淀和气体的物
2 2
质的量与加入NaO 的物质的量的关系如图所示,则原溶液中Al3+、Mg2+、NH 的物质
2 2
的量分别为
A.2 mol、3 mol、8 mol B.3 mol、2 mol、8 mol
C.2 mol、3 mol、4 mol D.3 mol、2 mol、4 mol
5.某同学设计了两种方案制备氢氧化铝,所用的稀盐酸与NaOH溶液均为3 mol/L。下图
是向X溶液与Y溶液中分别加入NaOH溶液或稀盐酸时产生沉淀的质量与加入溶液体积
之间的关系。相关说法正确的是方案一:
方案二:
A.a曲线表示的是向X溶液中加入稀盐酸溶液
B.方案二比方案一生成更多的气体
C.在M点时,两种方案中所得溶液的溶质质量分数相同
D.若M点以后再继续滴加相应的酸和碱,a,b两条曲线将重合为一条
6.在100mL含Mg2+、Al3+、NH 、H+、Cl-的溶液中,逐滴加入5mol/LNaOH溶液,所
加NaOH溶液的体积(mL)与沉淀的物质的量(mol)关系如图。下列叙述不正确的是
( )
A.x-y=0.01mol
B.原溶液中c(Cl-)=1.65mol/L
C.原溶液的c(H+)=0.2mol/L
D.原溶液中n(Mg2+):n(Al3+)=4:1
7.某混合溶液中,可能大量含有的离子如下表:阳离子 H+、K+、Al3+、 、Mg2+
阴离子 OH−、 、 、
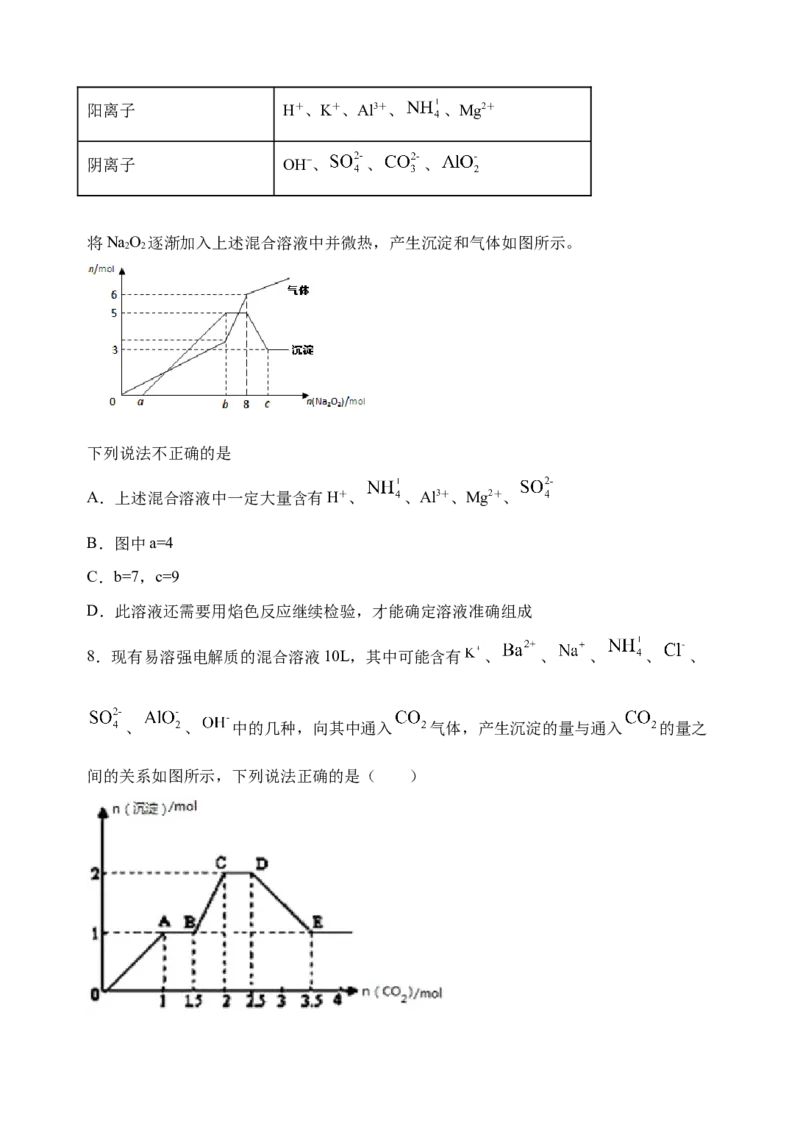
将NaO 逐渐加入上述混合溶液中并微热,产生沉淀和气体如图所示。
2 2
下列说法不正确的是
A.上述混合溶液中一定大量含有H+、 、Al3+、Mg2+、
B.图中a=4
C.b=7,c=9
D.此溶液还需要用焰色反应继续检验,才能确定溶液准确组成
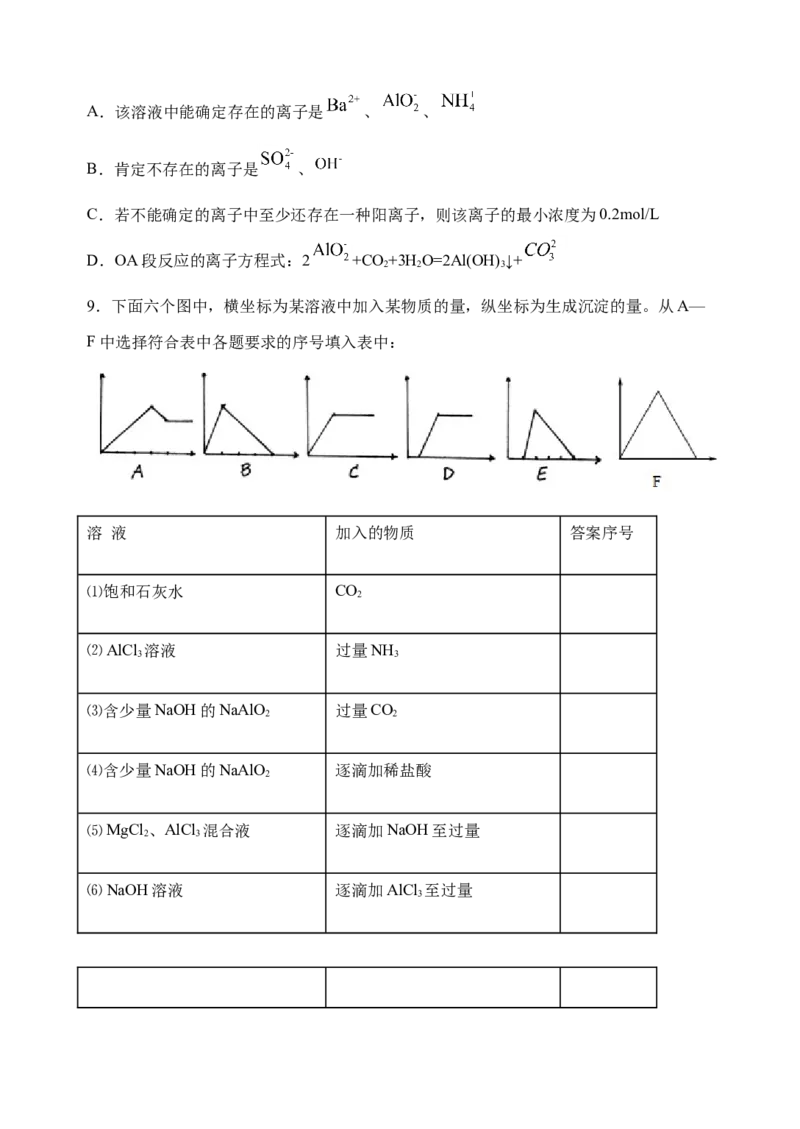
8.现有易溶强电解质的混合溶液10L,其中可能含有 、 、 、 、 、
、 、 中的几种,向其中通入 气体,产生沉淀的量与通入 的量之
间的关系如图所示,下列说法正确的是( )A.该溶液中能确定存在的离子是 、 、
B.肯定不存在的离子是 、
C.若不能确定的离子中至少还存在一种阳离子,则该离子的最小浓度为0.2mol/L
D.OA段反应的离子方程式:2 +CO +3H O=2Al(OH) ↓+
2 2 3
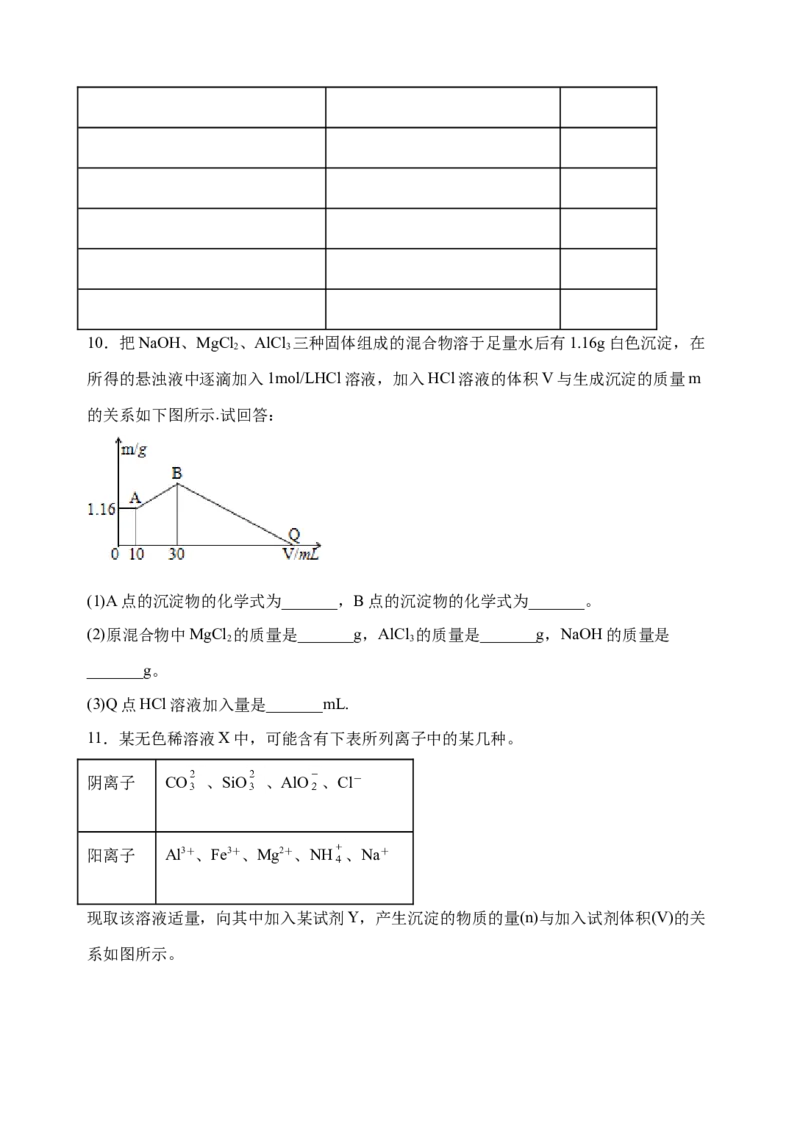
9.下面六个图中,横坐标为某溶液中加入某物质的量,纵坐标为生成沉淀的量。从A—
F中选择符合表中各题要求的序号填入表中:
溶 液 加入的物质 答案序号
⑴饱和石灰水 CO
2
⑵AlCl 溶液 过量NH
3 3
⑶含少量NaOH的NaAlO 过量CO
2 2
⑷含少量NaOH的NaAlO 逐滴加稀盐酸
2
⑸MgCl 、AlCl 混合液 逐滴加NaOH至过量
2 3
⑹NaOH溶液 逐滴加AlCl 至过量
310.把NaOH、MgCl 、AlCl 三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在
2 3
所得的悬浊液中逐滴加入1mol/LHCl溶液,加入HCl溶液的体积V与生成沉淀的质量m
的关系如下图所示.试回答:
(1)A点的沉淀物的化学式为_______,B点的沉淀物的化学式为_______。
(2)原混合物中MgCl 的质量是_______g,AlCl 的质量是_______g,NaOH的质量是
2 3
_______g。
(3)Q点HCl溶液加入量是_______mL.
11.某无色稀溶液X中,可能含有下表所列离子中的某几种。
阴离子 CO 、SiO 、AlO 、Cl-
阳离子 Al3+、Fe3+、Mg2+、NH 、Na+
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关
系如图所示。(1)若Y是盐酸,则oa段转化为沉淀的离子(指来源于X溶液的,下同)是
________________,ab段发生反应的离子是________,bc段发生反应的离子方程式为
__________。
(2)若Y是NaOH溶液,则X中一定含有的阳离子是_____________,其物质的量之比为
_________,ab段反应的离子方程式为____________。
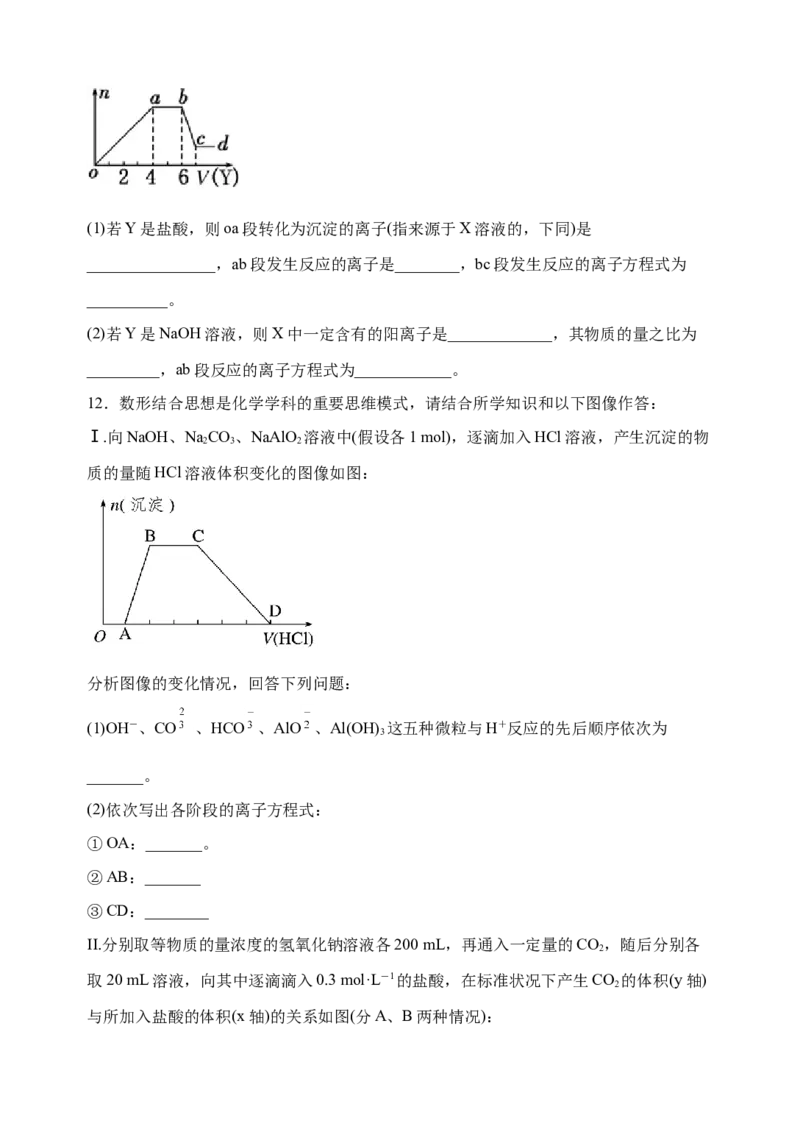
12.数形结合思想是化学学科的重要思维模式,请结合所学知识和以下图像作答:
Ⅰ.向NaOH、NaCO、NaAlO 溶液中(假设各1 mol),逐滴加入HCl溶液,产生沉淀的物
2 3 2
质的量随HCl溶液体积变化的图像如图:
分析图像的变化情况,回答下列问题:
(1)OH-、CO 、HCO 、AlO 、Al(OH) 这五种微粒与H+反应的先后顺序依次为
3
_______。
(2)依次写出各阶段的离子方程式:
①OA:_______。
②AB:_______
③CD:________
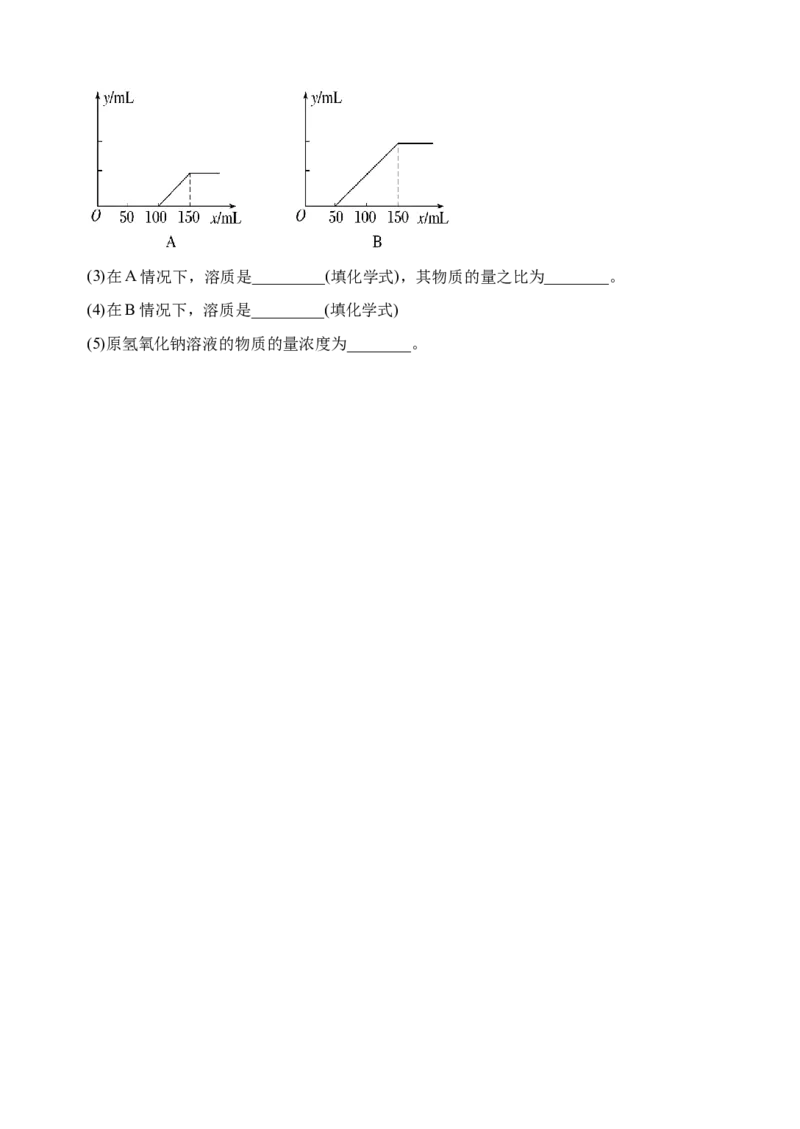
II.分别取等物质的量浓度的氢氧化钠溶液各200 mL,再通入一定量的CO,随后分别各
2
取20 mL溶液,向其中逐滴滴入0.3 mol·L-1的盐酸,在标准状况下产生CO 的体积(y轴)
2
与所加入盐酸的体积(x轴)的关系如图(分A、B两种情况):(3)在A情况下,溶质是_________(填化学式),其物质的量之比为________。
(4)在B情况下,溶质是_________(填化学式)
(5)原氢氧化钠溶液的物质的量浓度为________。